9.3 溶液的浓度 课件 (共21张PPT内嵌视频)2023-2024学年人教版化学九年级下册
文档属性
| 名称 | 9.3 溶液的浓度 课件 (共21张PPT内嵌视频)2023-2024学年人教版化学九年级下册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 11.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-04 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
课题3 溶液的浓度
死海中含有高浓度的盐分,为一般海水的8.6倍,致使水中没有生物存活,甚至连死海沿岸的陆地上也很少有除水草外的生物。
死海的中盐浓度怎样定量表示呢?
1.能说出溶质质量分数的概念和表示的含义。
2.能区分溶质质量分数和溶解度。
3.能掌握溶液稀释、浓缩的方法。
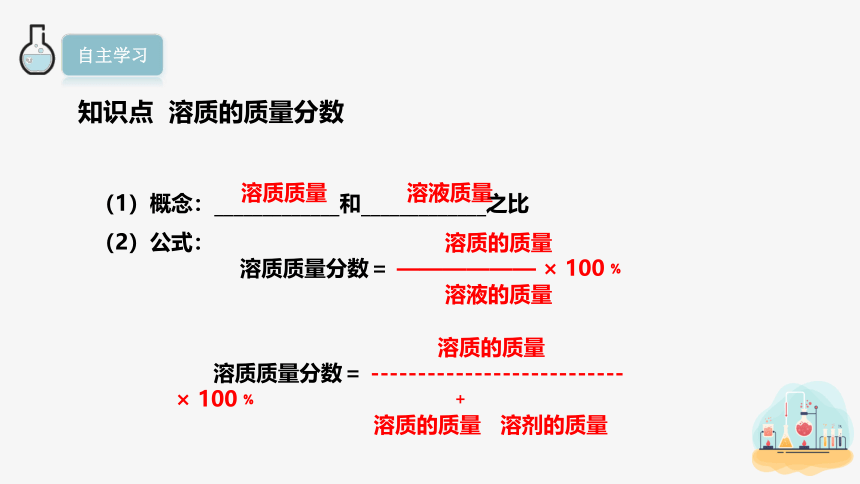
知识点 溶质的质量分数
(1)概念:_____________和_____________之比
(2)公式:
溶质的质量
溶质质量分数= —————— × 100﹪
溶液的质量
溶质质量
溶液质量
溶质的质量
溶质质量分数= --------------------------- × 100﹪
溶质的质量 溶剂的质量
+
探究一、比较溶液的浓稀
【实验1】
在室温下,向三个小烧杯中各加入20 mL水,然后分别加入0.1 g、0.5 g、2 g无水硫酸铜,振荡,使硫酸铜全部溶解,比较三种硫酸铜溶液的颜色。在这三种溶液中,哪种最浓?哪种溶液最稀?你判断的依据是什么?
【视频】三种浓稀不同的硫酸铜溶液
烧杯编号 溶液颜色比较 溶剂质量/g 溶质质量/g 溶液质量/g
1
2
3
结论 对于有色溶液来说,__________________
浅蓝
蓝色
深蓝
20
20
20
0.1
0.5
2
20.1
20.5
22
颜色越深,浓度越大
溶剂质量相同时,溶质质量越大,溶质质量分数越大。
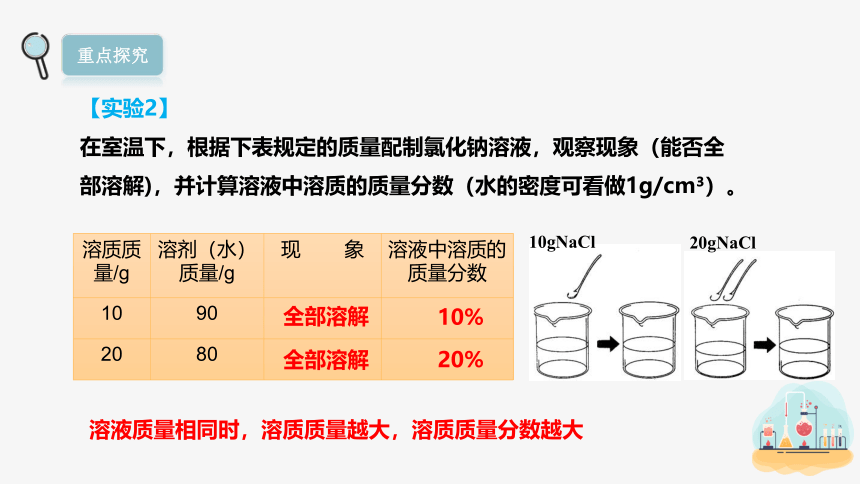
【实验2】
在室温下,根据下表规定的质量配制氯化钠溶液,观察现象(能否全部溶解),并计算溶液中溶质的质量分数(水的密度可看做1g/cm )。
10gNaCl
20gNaCl
溶质质量/g 溶剂(水)质量/g 现 象 溶液中溶质的质量分数
10 90
20 80
10%
20%
全部溶解
全部溶解
溶液质量相同时,溶质质量越大,溶质质量分数越大
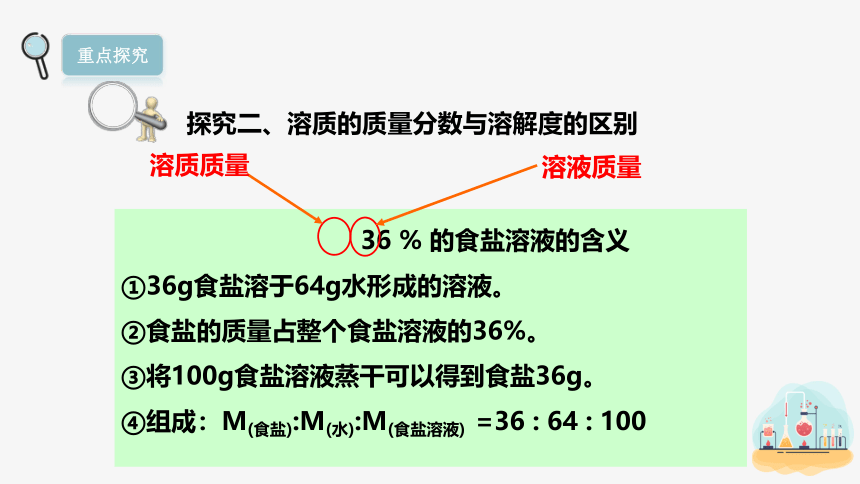
36 % 的食盐溶液的含义
①36g食盐溶于64g水形成的溶液。
②食盐的质量占整个食盐溶液的36%。
③将100g食盐溶液蒸干可以得到食盐36g。
④组成:M(食盐):M(水):M(食盐溶液) =36 : 64 : 100
溶质质量
溶液质量
探究二、溶质的质量分数与溶解度的区别
“20℃时,氯化钠固体的溶解度为36.0g”,其含义是什么?
在20℃时,100g水中溶解36.0g氯化钠固体,溶液达到饱和。
在20℃时,100g水中最多可溶解36.0g氯化钠固体。
已知20oC时,氯化钠的溶解度是36g。有人说“20oC时氯化钠饱和溶液中溶质的质量分数为36%。”这种说法对吗?为什么?
温度 溶质的质量 溶剂的质量 溶液的质量
20℃
36g
100g
100g+36g
溶质的质量分数为=36g/(100g+36g)=26.5%≠36%
T0C时饱和溶液的溶质质量分数 =
溶解度(g)
100g+溶解度(g)
某温度下某物质的溶解度为ag,则同温下它的饱和溶液中溶质质量分数_____a%(填大于,小于或等于)。
小于
讨论:20oC时,某同学配制的硝酸钾溶液的溶质质量分数为25%,请判断他的说法是否正确?(提示:20oC时,硝酸钾的溶解度为31.6g)
说法错误,硝酸钾饱和溶液的溶质的质量分数为
=31.6g/(100g+31.6g)≈24%<25%,20oC时配制硝酸钾溶质质量分数最大为24%,不可能为25%。
溶解度与溶质质量分数的比较
区别 溶解度 溶质的质量分数
概念
表示意义
条件
状态
单位
一定温度时,100g溶剂中最多溶解溶质的质量
任意溶液中,溶质质量与溶液质量之比
某物质溶解能力的大小
任一溶液的浓度大小
一定温度
不定温度
饱和状态
可饱和,可不饱和
g
无单位
1.现有100g质量分数为30%的硝酸钠溶液,若要把它的质量分数稀释为20%,你有方法实现吗?
(1)加入50水
(2)加入100g质量分数为10%的硝酸钠溶液
探究三、溶液的稀释、浓缩
1.计算原理在溶液稀释与浓缩的过程中,溶质的质量不会发生变化。
2.溶液稀释的方法与计算公式
(1)加水稀释:A为浓溶液质量,a%为浓溶液溶质的质量分数;B为稀释后溶液质量,b%表示稀释后溶质质量分数;M水表示加入水的质量。
A·a%=B·b%或A·a%=(A+M水)·b%
(2)加入稀溶液稀释浓溶液:A为浓溶液质量,a%为浓溶液溶质的质量分数;B为稀溶液质量,b%表示稀溶液溶质质量分数;c%代表混合后所得溶液的溶质质量分数。A·a%+B·b%=(A+B)·c%
稀释规律
2.现有100g质量分数为10%的硝酸钠溶液,若要把它的质量分数变为20%,有人觉得增加10g硝酸钠即可,你觉得是否正确,说说你的方法?
(1)蒸发掉50g水
(2)加入12.5g硝酸钠
(3)加入100g质量分数为30%的硝酸钠溶液
不正确
1.下列氯化钠溶液,其溶质的质量分数不等于15%的是( )
A.100 g水中溶解15 g氯化钠
B.氯化钠与水按15∶85的质量比形成的溶液
C.100 g 溶液中含15 g氯化钠
D.30 g氯化钠溶解于170 g水中所形成的溶液
A
2.在10%的硫酸铜溶液中,溶质、溶剂、溶液的质量之比为( )
A、溶质:溶剂=1:10 B、溶质:溶液=1:10
C、溶剂:溶液=9:11 D、溶质:溶液=1:11
B
3.现有100g质量分数为10%的硝酸钠溶液,若要把它的质量分数变为20%,可采用的方法有( )
A.蒸发掉溶剂质量的一半
B.蒸发掉50 g溶剂
C.加入10 g硝酸钠
D.加入20 g硝酸钠
B
4.现有某温度下的硝酸钾溶液35 g,若将其蒸干,得到7 g硝酸钾,则该溶液中溶质的质量分数为________。
(1)若将上述溶液取出2 mL,则剩余溶液的溶质质量分数为
________。
(2)若往上述溶液中加入21 g水,所得溶液的溶质质量分数
为_______。
(3)若往上述溶液中加入3 g硝酸钾,搅拌后完全溶解,所得
溶液的溶质质量分数为________。
(4)若往上述溶液中加入45 g 12%的硝酸钾溶液,所得溶液
的溶质质量分数为________。
20%
12.5%
26.3%
15.5%
20%
一、溶质的质量分数
1、概念:溶质质量与溶液质量之比。
2、计算公式:
溶质的质量分数
溶质质量
溶液质量
100%
溶质质量
溶质质量+溶剂质量
100%
t℃时,某物质的溶解度为Sg,则t℃,该物质饱和溶液中
溶质的质量分数
Sg
Sg +100g
100%
二、溶液稀释、浓缩的方法
课题3 溶液的浓度
死海中含有高浓度的盐分,为一般海水的8.6倍,致使水中没有生物存活,甚至连死海沿岸的陆地上也很少有除水草外的生物。
死海的中盐浓度怎样定量表示呢?
1.能说出溶质质量分数的概念和表示的含义。
2.能区分溶质质量分数和溶解度。
3.能掌握溶液稀释、浓缩的方法。
知识点 溶质的质量分数
(1)概念:_____________和_____________之比
(2)公式:
溶质的质量
溶质质量分数= —————— × 100﹪
溶液的质量
溶质质量
溶液质量
溶质的质量
溶质质量分数= --------------------------- × 100﹪
溶质的质量 溶剂的质量
+
探究一、比较溶液的浓稀
【实验1】
在室温下,向三个小烧杯中各加入20 mL水,然后分别加入0.1 g、0.5 g、2 g无水硫酸铜,振荡,使硫酸铜全部溶解,比较三种硫酸铜溶液的颜色。在这三种溶液中,哪种最浓?哪种溶液最稀?你判断的依据是什么?
【视频】三种浓稀不同的硫酸铜溶液
烧杯编号 溶液颜色比较 溶剂质量/g 溶质质量/g 溶液质量/g
1
2
3
结论 对于有色溶液来说,__________________
浅蓝
蓝色
深蓝
20
20
20
0.1
0.5
2
20.1
20.5
22
颜色越深,浓度越大
溶剂质量相同时,溶质质量越大,溶质质量分数越大。
【实验2】
在室温下,根据下表规定的质量配制氯化钠溶液,观察现象(能否全部溶解),并计算溶液中溶质的质量分数(水的密度可看做1g/cm )。
10gNaCl
20gNaCl
溶质质量/g 溶剂(水)质量/g 现 象 溶液中溶质的质量分数
10 90
20 80
10%
20%
全部溶解
全部溶解
溶液质量相同时,溶质质量越大,溶质质量分数越大
36 % 的食盐溶液的含义
①36g食盐溶于64g水形成的溶液。
②食盐的质量占整个食盐溶液的36%。
③将100g食盐溶液蒸干可以得到食盐36g。
④组成:M(食盐):M(水):M(食盐溶液) =36 : 64 : 100
溶质质量
溶液质量
探究二、溶质的质量分数与溶解度的区别
“20℃时,氯化钠固体的溶解度为36.0g”,其含义是什么?
在20℃时,100g水中溶解36.0g氯化钠固体,溶液达到饱和。
在20℃时,100g水中最多可溶解36.0g氯化钠固体。
已知20oC时,氯化钠的溶解度是36g。有人说“20oC时氯化钠饱和溶液中溶质的质量分数为36%。”这种说法对吗?为什么?
温度 溶质的质量 溶剂的质量 溶液的质量
20℃
36g
100g
100g+36g
溶质的质量分数为=36g/(100g+36g)=26.5%≠36%
T0C时饱和溶液的溶质质量分数 =
溶解度(g)
100g+溶解度(g)
某温度下某物质的溶解度为ag,则同温下它的饱和溶液中溶质质量分数_____a%(填大于,小于或等于)。
小于
讨论:20oC时,某同学配制的硝酸钾溶液的溶质质量分数为25%,请判断他的说法是否正确?(提示:20oC时,硝酸钾的溶解度为31.6g)
说法错误,硝酸钾饱和溶液的溶质的质量分数为
=31.6g/(100g+31.6g)≈24%<25%,20oC时配制硝酸钾溶质质量分数最大为24%,不可能为25%。
溶解度与溶质质量分数的比较
区别 溶解度 溶质的质量分数
概念
表示意义
条件
状态
单位
一定温度时,100g溶剂中最多溶解溶质的质量
任意溶液中,溶质质量与溶液质量之比
某物质溶解能力的大小
任一溶液的浓度大小
一定温度
不定温度
饱和状态
可饱和,可不饱和
g
无单位
1.现有100g质量分数为30%的硝酸钠溶液,若要把它的质量分数稀释为20%,你有方法实现吗?
(1)加入50水
(2)加入100g质量分数为10%的硝酸钠溶液
探究三、溶液的稀释、浓缩
1.计算原理在溶液稀释与浓缩的过程中,溶质的质量不会发生变化。
2.溶液稀释的方法与计算公式
(1)加水稀释:A为浓溶液质量,a%为浓溶液溶质的质量分数;B为稀释后溶液质量,b%表示稀释后溶质质量分数;M水表示加入水的质量。
A·a%=B·b%或A·a%=(A+M水)·b%
(2)加入稀溶液稀释浓溶液:A为浓溶液质量,a%为浓溶液溶质的质量分数;B为稀溶液质量,b%表示稀溶液溶质质量分数;c%代表混合后所得溶液的溶质质量分数。A·a%+B·b%=(A+B)·c%
稀释规律
2.现有100g质量分数为10%的硝酸钠溶液,若要把它的质量分数变为20%,有人觉得增加10g硝酸钠即可,你觉得是否正确,说说你的方法?
(1)蒸发掉50g水
(2)加入12.5g硝酸钠
(3)加入100g质量分数为30%的硝酸钠溶液
不正确
1.下列氯化钠溶液,其溶质的质量分数不等于15%的是( )
A.100 g水中溶解15 g氯化钠
B.氯化钠与水按15∶85的质量比形成的溶液
C.100 g 溶液中含15 g氯化钠
D.30 g氯化钠溶解于170 g水中所形成的溶液
A
2.在10%的硫酸铜溶液中,溶质、溶剂、溶液的质量之比为( )
A、溶质:溶剂=1:10 B、溶质:溶液=1:10
C、溶剂:溶液=9:11 D、溶质:溶液=1:11
B
3.现有100g质量分数为10%的硝酸钠溶液,若要把它的质量分数变为20%,可采用的方法有( )
A.蒸发掉溶剂质量的一半
B.蒸发掉50 g溶剂
C.加入10 g硝酸钠
D.加入20 g硝酸钠
B
4.现有某温度下的硝酸钾溶液35 g,若将其蒸干,得到7 g硝酸钾,则该溶液中溶质的质量分数为________。
(1)若将上述溶液取出2 mL,则剩余溶液的溶质质量分数为
________。
(2)若往上述溶液中加入21 g水,所得溶液的溶质质量分数
为_______。
(3)若往上述溶液中加入3 g硝酸钾,搅拌后完全溶解,所得
溶液的溶质质量分数为________。
(4)若往上述溶液中加入45 g 12%的硝酸钾溶液,所得溶液
的溶质质量分数为________。
20%
12.5%
26.3%
15.5%
20%
一、溶质的质量分数
1、概念:溶质质量与溶液质量之比。
2、计算公式:
溶质的质量分数
溶质质量
溶液质量
100%
溶质质量
溶质质量+溶剂质量
100%
t℃时,某物质的溶解度为Sg,则t℃,该物质饱和溶液中
溶质的质量分数
Sg
Sg +100g
100%
二、溶液稀释、浓缩的方法
同课章节目录
