人教版化学九年级下册第十单元 酸和碱学情评估试题(含答案)
文档属性
| 名称 | 人教版化学九年级下册第十单元 酸和碱学情评估试题(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 235.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-05 00:00:00 | ||
图片预览



文档简介
第十单元学情评估
可能用到的相对原子质量:H:1 O:16 Na:23 S:32
一、选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.NaOH可用于造纸和印染工业,NaOH属于( )
A.单质 B.酸
C.碱 D.盐
2.紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素,花青素遇酸性溶液或碱性溶液的变色情况跟石蕊溶液类似。在凉拌紫甘蓝丝时,观察到菜丝变成红色,加入的调味品可能是( )
A.食盐 B.味精
C.食醋 D.香油
3.被黄蜂叮咬后会感到非常疼痛,这是因为黄蜂分泌物中含有一种碱性物质。当被黄蜂叮咬后,可在患处涂抹( )
A.牙膏液(pH=8~9) B.肥皂水(pH=9~10)
C.苏打水(pH=11~12) D.白醋(pH=2~3)
4.下列图示的实验操作,正确的是( )
5.下列实验现象描述不正确的是( )
A.向氢氧化钠溶液中滴加紫色石蕊溶液,溶液变红
B.将二氧化碳通入澄清石灰水中,澄清石灰水变浑浊
C.打开盛有浓盐酸的试剂瓶,瓶口出现白雾
D.向盛有氧化铜的试管中滴加稀盐酸,黑色粉末溶解,溶液呈蓝色
6.下列有关物质的性质与用途对应正确的是( )
A.氢氧化钠具有碱性,可用于改良酸性土壤
B.酸碱指示剂遇酸、碱性溶液变色,可用于测定溶液的酸碱性
C.盐酸具有挥发性,可用于除铁锈
D.浓硫酸具有腐蚀性,可用作干燥剂
7.下列溶液敞口放置在空气中,不考虑水分蒸发,一段时间后溶液总质量变小的是( )
A.氢氧化钠溶液 B.澄清石灰水
C.浓硫酸 D.生理盐水
8.锥形瓶内盛有气体X,胶头滴管内盛有Y,若挤压胶头滴管使液体滴入瓶中,振荡,一会儿可见小气球鼓起。关于X、Y的推断不可能的是( )
INCLUDEPICTURE"24-16.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-16.tif" \* MERGEFORMATINET (第8题)
选项物质 A B C D
X HCl SO2 CO CO2
Y Ca(OH)2溶液 NaOH溶液 KOH溶液 NaOH溶液
9.科学探究中常用到推理的方法。根据下列实验事实推出的结论正确的是( )
选项 实验事实 实验结论
A 某溶液使酚酞溶液变红 该溶液一定是NaOH溶液
B 某物质可以导电 该物质一定是金属单质
C 常温下,测定某溶液的pH=3 该溶液一定呈酸性
D 向某固体中滴加稀盐酸,产生气泡 该固体一定是金属单质
10.某兴趣小组利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中的变化情况,记录得到图2和图3。则下列说法中不正确的是( )
INCLUDEPICTURE"初排J10-1.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\初排J10-1.tif" \* MERGEFORMATINET (第10题)
A.图1的仪器A中盛装的是稀盐酸
B.将图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加
D.图3中e→f的变化趋势可说明该反应是放热反应
二、非选择题:本题共6小题,共70分。
11.(6分)福建是茶叶的生产地之一,有着浓厚的茶文化。喝茶能提神解乏、兴奋消倦,其原因是茶叶中的咖啡碱能使人体中枢神经产生兴奋作用。茶树适宜生长在pH为4.5~6.5的土壤中。
(1)茶树适宜生长在________(填“酸性”“碱性”或“中性”)土壤中。
(2)茶农想测定茶园土壤的酸碱性强弱程度,他会选用____(填字母,下同)。
A.石蕊溶液 B.酚酞溶液 C.pH试纸
(3)茶农通过测定知道土壤pH约为3,请你帮他选取改良土壤的物质:________。
A.熟石灰 B.稀硫酸
12.(19分)某化学兴趣小组开展的氢氧化钠性质系列探究活动如图1所示:
INCLUDEPICTURE"24-17.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-17.tif" \* MERGEFORMATINET (第12题图1)
回答下列问题:
(1)实验①观察到氢氧化钠表面变________。
(2)实验②观察到溶液变成________色,实验③观察到溶液变成________色。由此得出:碱溶液能使指示剂变色。
(3)实验④:
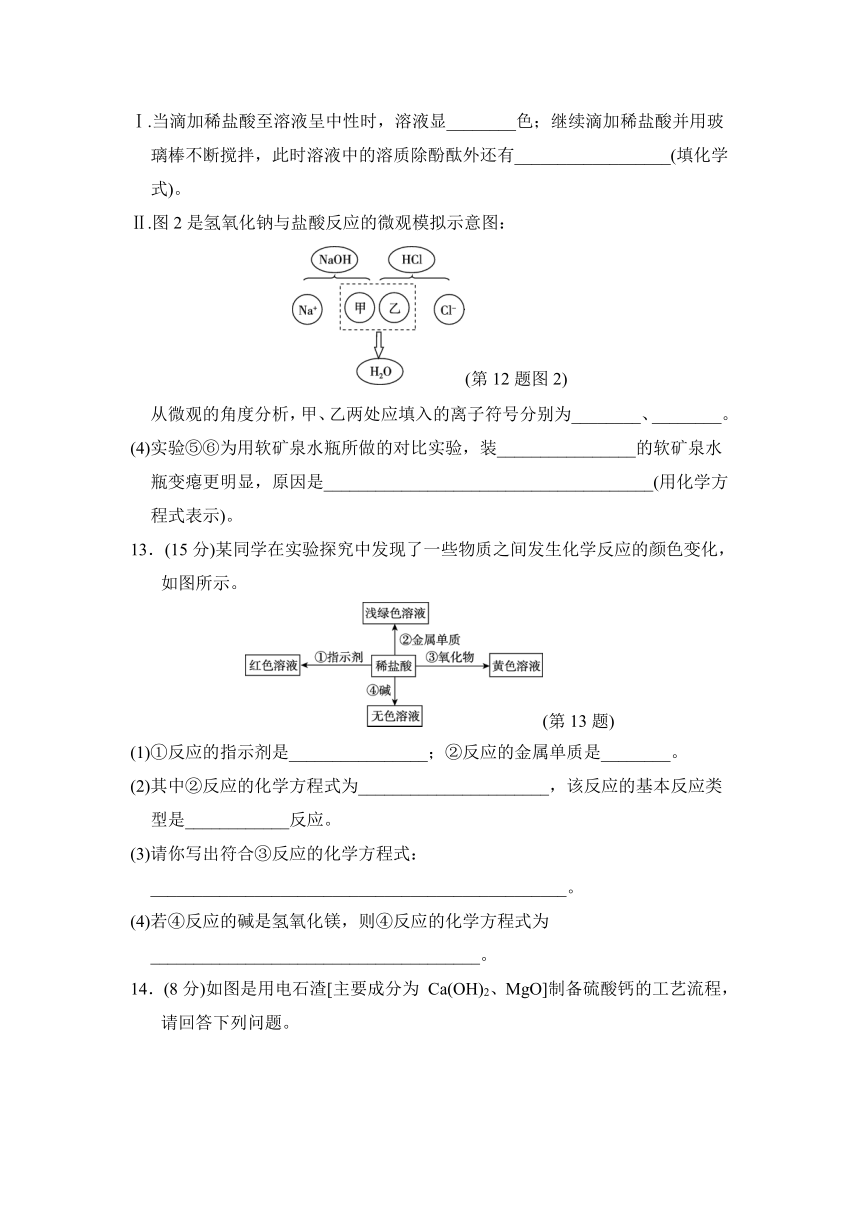
Ⅰ.当滴加稀盐酸至溶液呈中性时,溶液显________色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有__________________(填化学式)。
Ⅱ.图2是氢氧化钠与盐酸反应的微观模拟示意图:
INCLUDEPICTURE"24-18.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-18.tif" \* MERGEFORMATINET (第12题图2)
从微观的角度分析,甲、乙两处应填入的离子符号分别为________、________。
(4)实验⑤⑥为用软矿泉水瓶所做的对比实验,装________________的软矿泉水瓶变瘪更明显,原因是______________________________________(用化学方程式表示)。
13.(15分)某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
INCLUDEPICTURE"24-19.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-19.tif" \* MERGEFORMATINET (第13题)
(1)①反应的指示剂是________________;②反应的金属单质是________。
(2)其中②反应的化学方程式为______________________,该反应的基本反应类型是____________反应。
(3)请你写出符合③反应的化学方程式:________________________________________________。
(4)若④反应的碱是氢氧化镁,则④反应的化学方程式为______________________________________。
14.(8分)如图是用电石渣[主要成分为 Ca(OH)2、MgO]制备硫酸钙的工艺流程,请回答下列问题。
INCLUDEPICTURE"24-20.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-20.tif" \* MERGEFORMATINET (第14题)
已知:MgO 难溶于水;MgSO4易溶于水;CaSO4微溶于水。
(1)电石渣粉碎的目的是________________________________________________________________。
(2)反应器中发生的反应主要有__________________________________________(任写一个)。
(3)请简单叙述实验室稀释浓硫酸的方法:__________________________________________。
(4)实验室过滤液体时,如果过滤后液体依然浑浊,其原因可能是____________(任写一个)。
15.(12分)化学兴趣小组针对“酸碱中和反应”进行如下科学探究实验。
已知:稀硫酸与氢氧化钡的反应为H2SO4+Ba(OH)2===BaSO4↓+2H2O,且硫酸钡(BaSO4)是一种难溶于水的白色固体。
(1)验证酸与碱能发生反应。
如图1,在烧杯中加入约5 mL稀氢氧化钡溶液,用胶头滴管慢慢滴入10%的稀硫酸,并不断搅拌溶液,在不增加其他药品的条件下,如何判断氢氧化钡是否反应完全?方法是_______________________________________________________________。
INCLUDEPICTURE"初排J10-8.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\初排J10-8.tif" \* MERGEFORMATINET (第15题图1)
(2)探究中和反应过程的pH变化。利用pH传感器绘制出如图2曲线。
INCLUDEPICTURE"初排J10-9.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\初排J10-9.tif" \* MERGEFORMATINET (第15题图2)
取a、b、c三点状态时的物质,过滤,所得滤液呈中性的是______(填“a”“b”或“c”),c点所得滤液pH________(填“大于”“小于”或“等于”)原稀硫酸。
(3)探究酸与碱反应过程中溶液导电能力的变化。
【查阅资料】氢氧化钡溶液中含有Ba2+和OH-,稀硫酸中含有H+和SO42-。溶液的导电能力与单位体积溶液中离子的数目有关。
【猜想与假设】
氢氧化钡与稀硫酸恰好反应时溶液电导率为零。
【设计实验】
利用电导率传感器测定实验数据,绘制曲线如图3。
INCLUDEPICTURE"初排J10-10.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\初排J10-10.tif" \* MERGEFORMATINET (第15题图3)
【解释与结论】根据电导率曲线图可知,猜想不正确,可能原因是________________________(写出一点)。控制其他条件不变,溶液导电能力与单位体积溶液中离子数目的关系是________________________________________________________________。
【拓展与延伸】实验结束后,针对废液,可以用熟石灰中和处理过量的稀硫酸,该反应是利用中和反应原理,请再举一例中和反应在生活中的积极应用: ________________________________________________________________。
16.(10分)学习小组用已知浓度的氢氧化钠溶液测定某硫酸溶液的浓度。取该硫酸溶液20 g,滴加10%的氢氧化钠溶液,恰好完全反应时,共消耗氢氧化钠溶液40 g。计算:(提示:H2SO4+2NaOH===Na2SO4+2H2O)
(1)消耗的NaOH溶液中溶质的质量为________g。
(2)该硫酸溶液的溶质质量分数。
答案
一、1.C 2.C 3.D 4.D 5.A 6.B 7.B 8.C 9.C
10.C 点拨:A.溶液pH由大于7逐渐减小到pH小于7,说明是把稀盐酸加入氢氧化钠溶液中,图1的仪器A中盛装的是稀盐酸,正确;B.图2中d点所示溶液中溶质是氯化钠和过量的氯化氢,加热蒸干过程中氯化氢挥发掉,所得固体为氯化钠,氯化钠是纯净物,正确;C.图2中c→d过程中只是加入过量的稀盐酸,溶液中NaCl的质量不变,不正确;D.图3中e→f的变化趋势为温度升高,可说明该反应是放热反应,正确。故选C。
二、11.(1)酸性 (2)C (3)A
12.(1)潮湿 (2)蓝;红 (3)无;NaCl和HCl;OH-;H+
(4)氢氧化钠溶液;2NaOH+CO2===Na2CO3+H2O
13.(1)紫色石蕊溶液;铁(或Fe)
(2)Fe+2HCl===FeCl2+H2↑;置换
(3)Fe2O3+6HCl===2FeCl3+3H2O
(4)2HCl+Mg(OH)2===MgCl2+2H2O
14.(1)增大反应物接触面积,加快反应速率(合理即可)
(2)Ca(OH)2+H2SO4===CaSO4+2H2O(或MgO+H2SO4===MgSO4+H2O)
(3)将浓硫酸沿烧杯内壁缓慢倒入水中,边加边搅拌
(4)滤纸破损(合理即可)
15.(1)过滤,取澄清液体,再滴入少量稀硫酸,若无沉淀生成,则证明反应完全 (2)b;大于
(3)【解释与结论】硫酸钡有少量溶解在水中;单位体积溶液中离子数目越多,溶液导电能力越强
【拓展与延伸】治疗胃酸过多(或改良酸性土壤)
16.(1)4
(2)解:设20 g硫酸溶液中的溶质质量为x。
H2SO4+2NaOH===Na2SO4+2H2O
98 80
x 4 g
= x=4.9 g
该硫酸溶液的溶质质量分数为×100%=24.5%
答:该硫酸溶液的溶质质量分数为24.5%。
可能用到的相对原子质量:H:1 O:16 Na:23 S:32
一、选择题:本题共10小题,每小题3分,共30分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.NaOH可用于造纸和印染工业,NaOH属于( )
A.单质 B.酸
C.碱 D.盐
2.紫甘蓝是大众爱吃的蔬菜,含有丰富的花青素,花青素遇酸性溶液或碱性溶液的变色情况跟石蕊溶液类似。在凉拌紫甘蓝丝时,观察到菜丝变成红色,加入的调味品可能是( )
A.食盐 B.味精
C.食醋 D.香油
3.被黄蜂叮咬后会感到非常疼痛,这是因为黄蜂分泌物中含有一种碱性物质。当被黄蜂叮咬后,可在患处涂抹( )
A.牙膏液(pH=8~9) B.肥皂水(pH=9~10)
C.苏打水(pH=11~12) D.白醋(pH=2~3)
4.下列图示的实验操作,正确的是( )
5.下列实验现象描述不正确的是( )
A.向氢氧化钠溶液中滴加紫色石蕊溶液,溶液变红
B.将二氧化碳通入澄清石灰水中,澄清石灰水变浑浊
C.打开盛有浓盐酸的试剂瓶,瓶口出现白雾
D.向盛有氧化铜的试管中滴加稀盐酸,黑色粉末溶解,溶液呈蓝色
6.下列有关物质的性质与用途对应正确的是( )
A.氢氧化钠具有碱性,可用于改良酸性土壤
B.酸碱指示剂遇酸、碱性溶液变色,可用于测定溶液的酸碱性
C.盐酸具有挥发性,可用于除铁锈
D.浓硫酸具有腐蚀性,可用作干燥剂
7.下列溶液敞口放置在空气中,不考虑水分蒸发,一段时间后溶液总质量变小的是( )
A.氢氧化钠溶液 B.澄清石灰水
C.浓硫酸 D.生理盐水
8.锥形瓶内盛有气体X,胶头滴管内盛有Y,若挤压胶头滴管使液体滴入瓶中,振荡,一会儿可见小气球鼓起。关于X、Y的推断不可能的是( )
INCLUDEPICTURE"24-16.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-16.tif" \* MERGEFORMATINET (第8题)
选项物质 A B C D
X HCl SO2 CO CO2
Y Ca(OH)2溶液 NaOH溶液 KOH溶液 NaOH溶液
9.科学探究中常用到推理的方法。根据下列实验事实推出的结论正确的是( )
选项 实验事实 实验结论
A 某溶液使酚酞溶液变红 该溶液一定是NaOH溶液
B 某物质可以导电 该物质一定是金属单质
C 常温下,测定某溶液的pH=3 该溶液一定呈酸性
D 向某固体中滴加稀盐酸,产生气泡 该固体一定是金属单质
10.某兴趣小组利用图1装置研究稀盐酸与氢氧化钠溶液反应的过程,并用pH和温度传感器测量反应过程中的变化情况,记录得到图2和图3。则下列说法中不正确的是( )
INCLUDEPICTURE"初排J10-1.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\初排J10-1.tif" \* MERGEFORMATINET (第10题)
A.图1的仪器A中盛装的是稀盐酸
B.将图2中d点所示溶液加热蒸干所得固体为纯净物
C.图2中c→d所示溶液中NaCl的质量不断增加
D.图3中e→f的变化趋势可说明该反应是放热反应
二、非选择题:本题共6小题,共70分。
11.(6分)福建是茶叶的生产地之一,有着浓厚的茶文化。喝茶能提神解乏、兴奋消倦,其原因是茶叶中的咖啡碱能使人体中枢神经产生兴奋作用。茶树适宜生长在pH为4.5~6.5的土壤中。
(1)茶树适宜生长在________(填“酸性”“碱性”或“中性”)土壤中。
(2)茶农想测定茶园土壤的酸碱性强弱程度,他会选用____(填字母,下同)。
A.石蕊溶液 B.酚酞溶液 C.pH试纸
(3)茶农通过测定知道土壤pH约为3,请你帮他选取改良土壤的物质:________。
A.熟石灰 B.稀硫酸
12.(19分)某化学兴趣小组开展的氢氧化钠性质系列探究活动如图1所示:
INCLUDEPICTURE"24-17.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-17.tif" \* MERGEFORMATINET (第12题图1)
回答下列问题:
(1)实验①观察到氢氧化钠表面变________。
(2)实验②观察到溶液变成________色,实验③观察到溶液变成________色。由此得出:碱溶液能使指示剂变色。
(3)实验④:
Ⅰ.当滴加稀盐酸至溶液呈中性时,溶液显________色;继续滴加稀盐酸并用玻璃棒不断搅拌,此时溶液中的溶质除酚酞外还有__________________(填化学式)。
Ⅱ.图2是氢氧化钠与盐酸反应的微观模拟示意图:
INCLUDEPICTURE"24-18.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-18.tif" \* MERGEFORMATINET (第12题图2)
从微观的角度分析,甲、乙两处应填入的离子符号分别为________、________。
(4)实验⑤⑥为用软矿泉水瓶所做的对比实验,装________________的软矿泉水瓶变瘪更明显,原因是______________________________________(用化学方程式表示)。
13.(15分)某同学在实验探究中发现了一些物质之间发生化学反应的颜色变化,如图所示。
INCLUDEPICTURE"24-19.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-19.tif" \* MERGEFORMATINET (第13题)
(1)①反应的指示剂是________________;②反应的金属单质是________。
(2)其中②反应的化学方程式为______________________,该反应的基本反应类型是____________反应。
(3)请你写出符合③反应的化学方程式:________________________________________________。
(4)若④反应的碱是氢氧化镁,则④反应的化学方程式为______________________________________。
14.(8分)如图是用电石渣[主要成分为 Ca(OH)2、MgO]制备硫酸钙的工艺流程,请回答下列问题。
INCLUDEPICTURE"24-20.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\24-20.tif" \* MERGEFORMATINET (第14题)
已知:MgO 难溶于水;MgSO4易溶于水;CaSO4微溶于水。
(1)电石渣粉碎的目的是________________________________________________________________。
(2)反应器中发生的反应主要有__________________________________________(任写一个)。
(3)请简单叙述实验室稀释浓硫酸的方法:__________________________________________。
(4)实验室过滤液体时,如果过滤后液体依然浑浊,其原因可能是____________(任写一个)。
15.(12分)化学兴趣小组针对“酸碱中和反应”进行如下科学探究实验。
已知:稀硫酸与氢氧化钡的反应为H2SO4+Ba(OH)2===BaSO4↓+2H2O,且硫酸钡(BaSO4)是一种难溶于水的白色固体。
(1)验证酸与碱能发生反应。
如图1,在烧杯中加入约5 mL稀氢氧化钡溶液,用胶头滴管慢慢滴入10%的稀硫酸,并不断搅拌溶液,在不增加其他药品的条件下,如何判断氢氧化钡是否反应完全?方法是_______________________________________________________________。
INCLUDEPICTURE"初排J10-8.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\初排J10-8.tif" \* MERGEFORMATINET (第15题图1)
(2)探究中和反应过程的pH变化。利用pH传感器绘制出如图2曲线。
INCLUDEPICTURE"初排J10-9.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\初排J10-9.tif" \* MERGEFORMATINET (第15题图2)
取a、b、c三点状态时的物质,过滤,所得滤液呈中性的是______(填“a”“b”或“c”),c点所得滤液pH________(填“大于”“小于”或“等于”)原稀硫酸。
(3)探究酸与碱反应过程中溶液导电能力的变化。
【查阅资料】氢氧化钡溶液中含有Ba2+和OH-,稀硫酸中含有H+和SO42-。溶液的导电能力与单位体积溶液中离子的数目有关。
【猜想与假设】
氢氧化钡与稀硫酸恰好反应时溶液电导率为零。
【设计实验】
利用电导率传感器测定实验数据,绘制曲线如图3。
INCLUDEPICTURE"初排J10-10.tif" INCLUDEPICTURE "E:\\24春\\9化下R福建专用夹卷\\初排J10-10.tif" \* MERGEFORMATINET (第15题图3)
【解释与结论】根据电导率曲线图可知,猜想不正确,可能原因是________________________(写出一点)。控制其他条件不变,溶液导电能力与单位体积溶液中离子数目的关系是________________________________________________________________。
【拓展与延伸】实验结束后,针对废液,可以用熟石灰中和处理过量的稀硫酸,该反应是利用中和反应原理,请再举一例中和反应在生活中的积极应用: ________________________________________________________________。
16.(10分)学习小组用已知浓度的氢氧化钠溶液测定某硫酸溶液的浓度。取该硫酸溶液20 g,滴加10%的氢氧化钠溶液,恰好完全反应时,共消耗氢氧化钠溶液40 g。计算:(提示:H2SO4+2NaOH===Na2SO4+2H2O)
(1)消耗的NaOH溶液中溶质的质量为________g。
(2)该硫酸溶液的溶质质量分数。
答案
一、1.C 2.C 3.D 4.D 5.A 6.B 7.B 8.C 9.C
10.C 点拨:A.溶液pH由大于7逐渐减小到pH小于7,说明是把稀盐酸加入氢氧化钠溶液中,图1的仪器A中盛装的是稀盐酸,正确;B.图2中d点所示溶液中溶质是氯化钠和过量的氯化氢,加热蒸干过程中氯化氢挥发掉,所得固体为氯化钠,氯化钠是纯净物,正确;C.图2中c→d过程中只是加入过量的稀盐酸,溶液中NaCl的质量不变,不正确;D.图3中e→f的变化趋势为温度升高,可说明该反应是放热反应,正确。故选C。
二、11.(1)酸性 (2)C (3)A
12.(1)潮湿 (2)蓝;红 (3)无;NaCl和HCl;OH-;H+
(4)氢氧化钠溶液;2NaOH+CO2===Na2CO3+H2O
13.(1)紫色石蕊溶液;铁(或Fe)
(2)Fe+2HCl===FeCl2+H2↑;置换
(3)Fe2O3+6HCl===2FeCl3+3H2O
(4)2HCl+Mg(OH)2===MgCl2+2H2O
14.(1)增大反应物接触面积,加快反应速率(合理即可)
(2)Ca(OH)2+H2SO4===CaSO4+2H2O(或MgO+H2SO4===MgSO4+H2O)
(3)将浓硫酸沿烧杯内壁缓慢倒入水中,边加边搅拌
(4)滤纸破损(合理即可)
15.(1)过滤,取澄清液体,再滴入少量稀硫酸,若无沉淀生成,则证明反应完全 (2)b;大于
(3)【解释与结论】硫酸钡有少量溶解在水中;单位体积溶液中离子数目越多,溶液导电能力越强
【拓展与延伸】治疗胃酸过多(或改良酸性土壤)
16.(1)4
(2)解:设20 g硫酸溶液中的溶质质量为x。
H2SO4+2NaOH===Na2SO4+2H2O
98 80
x 4 g
= x=4.9 g
该硫酸溶液的溶质质量分数为×100%=24.5%
答:该硫酸溶液的溶质质量分数为24.5%。
同课章节目录
