8.1.自然资源的开发利用 基础检测题(含解析)2023-2024学年高一下学期化学人教版(2019)必修第二册
文档属性
| 名称 | 8.1.自然资源的开发利用 基础检测题(含解析)2023-2024学年高一下学期化学人教版(2019)必修第二册 |  | |
| 格式 | docx | ||
| 文件大小 | 1.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-06 12:26:54 | ||
图片预览



文档简介
8.1.自然资源的开发利用基础检测题-2023-2024学年高一下学期化学人教版(2019)必修第二册
一、单选题
1.人类最早使用的合金是
A.铜合金 B.铁合金 C.铝合金 D.镁合金
2.合金具有许多优良的物理、化学或机械性能。下列物质中,不属于合金的是
A.硬铝 B.不锈钢 C.生铁 D.铝
3.中国历史文化悠久,流传下许多精美文物。下列有关文物的描述错误的是
A.商周青铜器的主要成分是金属材料 B.秦兵马俑的主要成分是高分子材料
C.唐代丝绸的主要成分是蛋白质 D.宋代陶瓷的主要成分是无机非金属材料
4.新材料的发展充分体现了“中国技术”“中国制造”和“中国力量”。下列说法错误的是
A.蛟龙号潜水器用到了钛合金,22号钛元素属于过渡元素
B.港珠澳大桥用到的合金材料,具有强度大、密度小、耐腐蚀等性能
C.国产大飞机C919使用的“现代工业骨骼”碳纤维是一种新型有机高分子材料
D.“华为麒麟980”手机中芯片的主要成分是硅单质
5.石油在常压下分馏,得到的主要产品是
A.汽油、煤油、柴油、重油 B.煤油、柴油、重油、渣油
C.柴油、重油、石蜡、润滑油 D.凡士林、石蜡、沥青、石油焦
6.影响金属冶炼方法的主要因素是
A.金属的活动性大小
B.金属在地壳中的含量多少
C.金属的化合价高低
D.金属的导电性强弱
7.下列物质不属于合金的是( )
A.不锈钢 B.高碳钢
C.金刚石 D.白铜
8.北京冬奥会备受世界瞩目。下列说法错误的是
A.冰壶主材料花岗岩属于无机非金属材料
B.火炬“飞扬”使用的碳纤维属于有机高分子材料
C.冬奥会“同心”金属奖牌属于合金材料
D.短道速滑服使用的超高分子量聚乙烯属于有机高分子材料
9.下列说法不正确的是
A.碳酸钠和碳酸氢钠的溶液均显碱性,可用作食用碱或工业用碱
B.硬铝具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料
C.将Cl2通入澄清石灰水中制得以Ca(ClO)2为有效成分的漂白粉
D.储氢合金是一类能够吸收氢气, 并与氢气结合成金属氢化物的材料
10.下列有关金属的用途与相应性质不对应的是
A.用金做饰物是因为金的化学性质稳定、不褪色
B.用钨做白炽灯灯丝是因为其熔点高、导电性好
C.用镁合金做汽车部件是因为镁的密度小,化学性质活泼
D.用铝做包装用的铝箔是因为其延展性好,表面有钝化膜
11.当航天飞机返回地球进入大气层时,由于空气的剧烈摩擦,航天飞机尖端的温度超过1000℃。为防止高温将其烧毁,科学家给航天飞机相应部位设计安装了可靠的保护层.制作保护层的材料可能为( )
A.合成塑料 B.新型陶瓷 C.镁铝合金 D.不锈钢
12.工业生产中常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物——合金。这是制取合金的常用方法之一、根据下表数据判断,不宜用上述方法制取合金的是
金属 Na Cu Al Fe
熔点(℃) 97.5 1 083 660 1 535
沸点(℃) 883 2 595 2 200 3 000
其中不能形成合金的是
A.Cu与Al B.Fe与Na C.Fe与Cu D.Al与Na
13.关于卤素单质以及形成的负离子,下列说法正确的是
A.氯气有毒,氯离子也有毒 B.液溴在棕色瓶中水封密封保存
C.碘离子遇淀粉变蓝 D.海水中富含液溴
14.下列说法正确的是( )
A.石油是混合物,汽油是纯净物
B.沸点:汽油>煤油>柴油>润滑油
C.直馏汽油和裂化汽油成分完全相同
D.石油的分馏是物理变化,而裂化和裂解属于化学变化
15.悠久的历史孕育了丰富的民间艺术文化瑰宝。下列文物器具的材质主要为合金的是
选项 A B C D
文物器具
名称 端石琴式砚 馆陶黑陶 木雕罗汉像 信宜铜盉
A.A B.B C.C D.D
16.下列叙述错误的是
A.硬铝的密度小,强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料
B.常温下可用铁或铝制容器盛装浓硫酸
C.过氧化钠可用于呼吸面具的氧气的来源之一
D.氯气有毒,所以不能用于制造农药、染料和药品等
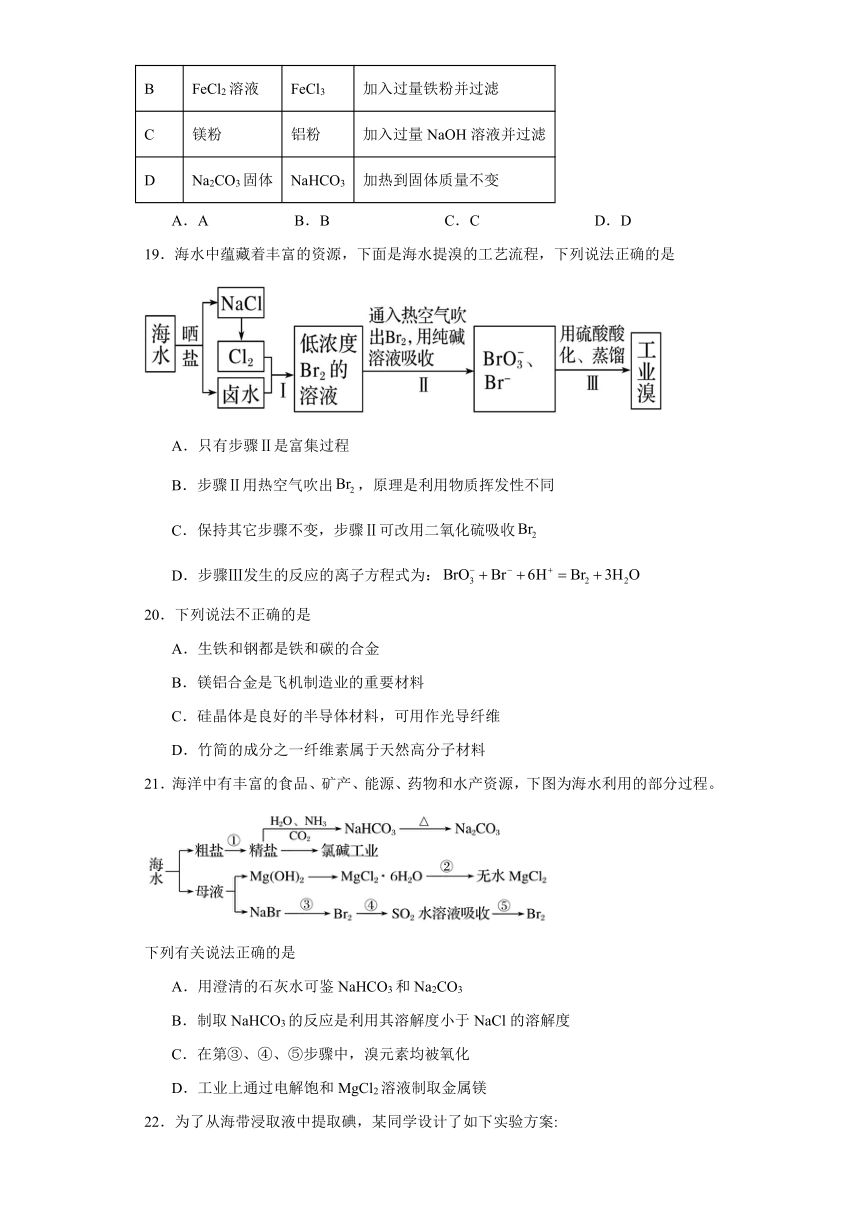
17.“空气吹出法”海水提溴的工艺流程如下:
下列说法中,不正确的是
A.实验室保存溴通常加少量水
B.海水提溴发生的反应均为氧化还原反应
C.经过吸收塔后,溴元素得到了富集
D.蒸馏塔中只发生了物理变化
18.下列除杂试剂或方法不正确的是选项
选项 被提纯物质 杂质 除杂试剂或方法
A Fe2O3 Al2O3 加入过量盐酸并过滤
B FeCl2溶液 FeCl3 加入过量铁粉并过滤
C 镁粉 铝粉 加入过量NaOH溶液并过滤
D Na2CO3固体 NaHCO3 加热到固体质量不变
A.A B.B C.C D.D
19.海水中蕴藏着丰富的资源,下面是海水提溴的工艺流程,下列说法正确的是
A.只有步骤Ⅱ是富集过程
B.步骤Ⅱ用热空气吹出,原理是利用物质挥发性不同
C.保持其它步骤不变,步骤Ⅱ可改用二氧化硫吸收
D.步骤Ⅲ发生的反应的离子方程式为:
20.下列说法不正确的是
A.生铁和钢都是铁和碳的合金
B.镁铝合金是飞机制造业的重要材料
C.硅晶体是良好的半导体材料,可用作光导纤维
D.竹简的成分之一纤维素属于天然高分子材料
21.海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
下列有关说法正确的是
A.用澄清的石灰水可鉴NaHCO3和Na2CO3
B.制取NaHCO3的反应是利用其溶解度小于NaCl的溶解度
C.在第③、④、⑤步骤中,溴元素均被氧化
D.工业上通过电解饱和MgCl2溶液制取金属镁
22.为了从海带浸取液中提取碘,某同学设计了如下实验方案:
下列说法不正确的是
A.上述实验方案中采用了反萃取法
B.②中有机溶剂a可为CCl4
C.③中发生反应的化学方程式:3I2+6NaOH=5NaI+NaIO3+3H2O
D.操作Z的名称是加热
23.溴主要以形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程示意如下。
下列说法不正确的是
A.将海水酸化的目的是避免后续流程中造成的损耗
B.中具有脱氯作用的离子仅为
C.溶液失去脱氯作用后,补加或加入铁粉,脱氯作用恢复
D.用溶液吸收溴,歧化为和。再用酸化歧化后的溶液得到,其离子方程式为
24.下列说法中正确的是
A.我国古代的技术应用中,粮食酿酒的工作原理不涉及化学反应
B.铁、铝、铜是制造潜艇必不可少的重要金属材料,三者均能导电,均为电解质
C.氯化钠在通电的情况下电离产生自由移动的离子
D.按制作文物的主要材料分类,青铜亚长牛尊属于金属文物
25.加碘盐中碘可能有两种存在形式KI或,某兴趣小组设计如图实验检验某品牌加碘盐中碘的存在形式。提供试剂:维生素C、过氧化氢溶液
下列说法错误的是
A.反应中加入稀硫酸可提高氧化剂的氧化能力
B.加碘盐中可同时添加和KI
C.若X为过氧化氢溶液,观察到溶液变蓝,则加碘盐中碘存在形式为KI
D.若X为维生素C,观察到溶液变蓝,则加碘盐中碘存在形式为
二、填空题
26.如图是我国古代和现代冶金的两张图片,那么人类使用金属的年代先后顺序与金属的活动性有什么关系 ?
27.请将下列物质的转化或分离方法的序号填在横线上(每一项只填写一种方法)。
①分馏 ②液化 ③气化 ④裂化 ⑤裂解 ⑥干馏 ⑦蒸馏
(1)把煤转化为焦炉气、煤焦油和焦炭等。
(2)从原油中分离出汽油、煤油、柴油等。
(3)将重油转化为汽油。
28.溴和碘的化合物在生产和生活中有广泛的用途.
(1)市场销售的某种食用精制盐中含碘酸钾。
①碘酸钾与碘化钾在酸性条件下发生如下反应,配平该反应的化学方程式:
( ) +( )KI+( ) =( ) +( ) +( )
②上述反应生成的I2可用四氯化碳检验,现象为 。
向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
Na2SO3稀溶液与I2反应的离子方程式是 。
(2)海水提溴过程中溴元素的变化如下:
①过程I,海水显碱性,调其pH<3.5后,再通入氯气,调节海水pH可提高C12的利用率,用平衡原理解释其原因是 。
②过程II,用热空气将溴赶出,再用浓Na2CO3溶液吸收。完成并配平下列方程式。
( ) +( ) =( ) +( ) +( )
③过程III,用硫酸酸化可得Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是 。
④NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入 2.6molNaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
则原溶液中NaI的物质的量为 mol.
试卷第1页,共3页
参考答案:
1.A
【详解】由于铜的活动性比较弱,以单质形成存在的比较多,所以人类历史上使用最早的合金是铜合金。故A符合题意,BCD不符合题意。
答案选A。
2.D
【详解】A.硬铝是铝、铜、镁、锰、硅等形成的铝合金,故A不符合题意;
B.不锈钢是铁与镍和铬形成的铁合金,故B不符合题意;
C.生铁是铁含有碳的铁合金,故C不符合题意;
D.铝是纯净的单质,不属于合金,故D符合题意;
故选D。
3.B
【详解】A.青铜器属于合金,为金属材料,故A正确;
B.秦兵马俑的主要成分是硅酸盐,属于传统无机非金属材料,故B错误;
C.丝绸的主要成分是蛋白质,故C正确;
D.陶瓷的主要成分是硅酸盐,属于无机非金属材料,故D正确;
故选:B。
4.C
【详解】A.22号钛元素位于第四周期ⅣB族,属于过渡元素,A项正确;
B.港珠澳大桥用到的合金材料,必须具有强度大、密度小、耐腐蚀等特性才能抵御恶劣环境及海水的侵蚀,B项正确;
C.碳纤维主要成分是碳单质,属于无机物,C项错误;
D.硅晶体是良好的半导体材料,常用于制作收集芯片,D项正确;
综上所述答案为C。
5.A
【详解】石油常压分馏产物:液化石油气、汽油、煤油、柴油、重油,故A满足,将重质油品进行减压蒸馏等处理,以得到渣油和燃料油等,B不满足;减压分馏过程的产物:重柴油、润滑油、凡士林、石蜡、沥青,故C、D不满足;
故选A。
6.A
【详解】不同的金属应选用不同的冶炼方法,金属的冶炼方法是根据金属的活动性强弱确定,与金属在地壳中的含量、化合价及金属的导电性没有关系,答案选A。
【点晴】注意根据金属的活动性强弱选择合适的冶炼方法,金属的活动性强弱和金属阳离子得电子能力之间有关系,一般来说,活泼金属用电解法,较活泼金属用热还原法,不活泼金属如Hg、Ag等用热分解法冶炼。
7.C
【详解】合金是一种金属与另一种或几种金属或非金属经过混合熔化,冷却凝固后得到的具有金属性质的固体产物。不锈钢、高碳钢、白铜等均属于合金,金刚石是碳的一种单质,不是合金,答案选C。
8.B
【详解】A.花岗岩的主要成分是石英、云母、长石等矿物,属于无机非金属材料,A正确;
B.碳纤维指的是含碳量在90%以上的高强度高模量纤维,属于无机非金属材料,B错误;
C.金属奖牌属于合金材料,C正确;
D.聚乙烯属于有机高分子材料,D正确;
故答案选B。
9.C
【详解】A.用pH试纸测定碳酸钠和碳酸氢钠的溶液均显碱性,碳酸氢钠可用作发酵粉和食品膨松剂,碳酸钠用于化工生产和除油污,故A正确;
B.硬铝是铝合金,具有硬度大、密度小,较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料,故B正确;
C.工业上将Cl2通入石灰乳中制得以CaClO)2为有效成分的漂白粉,故C错误;
D.一些合金能够大量吸收氢气,一定条件下与氢气结合成金属氢化物,又能放出氢气,这类金属材料叫做储氢合金,故D正确;
答案选C。
10.C
【详解】A.用金做饰物是因为金化学性质稳定,不褪色,A正确;
B.钨熔点高、导电性好,所以用作灯丝,B正确;
C.用镁合金做汽车部件是因为合金的密度小,强度高,与镁的化学性质活泼没有关系,C错误;
D.用铝做包装用的铝箔是因为其延展性好,且铝表面易被氧化为一层致密的钝化膜,D正确;
故选C。
11.B
【分析】航天飞机尖端的温度超过1000℃.为防止高温将其烧毁,则材料应为耐高温、不易导热的材料。
【详解】A.塑料的熔点很小,所以不能耐高温,A错误;
B.新型陶瓷耐高温熔点较高,所以能耐高温,可作保护层,B正确;
C.镁铝合金的熔点较低,C错误;
D.不锈钢为耐空气、蒸汽、水等弱腐蚀介质或具有不锈性的钢种,导热性能好,不适宜作保护层材料,D错误;
答案为B。
12.B
【详解】A.从表中数据可以看出,Cu的熔点低于Al的沸点,二者可以相互熔合而制成合金,A不符合题意;
B.Fe的熔点为1 535℃,而Na的沸点为883℃,则Fe的熔点高于Na的沸点,也就是Fe未熔化Na就已经汽化,二者不可能熔合成合金,B符合题意;
C.Fe的熔点低于Cu的沸点,二者可以熔合成合金,C不符合题意;
D.Al的熔点低于Na的沸点,二者可熔合成合金,D不符合题意;
故选B。
13.B
【详解】A.不同微粒的性质不同,氯气有毒,但氯离子没有毒,如NaCl是一种常用的调味剂,A错误;
B.液溴易挥发且溴蒸气有毒,故液溴在棕色瓶中水封密封保存,B正确;
C.I2遇到淀粉变蓝是其特性,但碘离子遇淀粉不变蓝,C错误;
D.Br2是活泼的非金属单质,化学性质活泼,故在海水中富含溴离子,不含液溴,D错误;
故答案为:B。
14.D
【详解】A.石油是混合物,汽油是多种烷烃(C5~C8)的混合物,故A错误;
B.烃分子中碳原子数越多沸点越高,沸点:汽油<煤油<柴油<润滑油,故B错误;
C.直馏汽油中不含烯烃,而裂化汽油中含有烯烃,两者组成上不完全相同,故C错误;
D.石油的分馏没有生成新物质,属于物理变化,而裂化和裂解有新物质生成,属于化学变化,故D正确;
选D。
15.D
【详解】由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质为合金,
A.砚的成分为无机盐,含碳酸钙,不是合金,故A不选;
B.馆陶黑陶材料为陶瓷,成分为硅酸盐,不是合金,故B不选;
C.木雕罗汉像,木材成分为纤维素,不是合金,故C不选;
D.信宜铜盉为铜合金,故D选;
故选:D。
16.D
【详解】A.硬铝是铝合金,其密度小,强度高,具有较强的抗腐蚀能力,可用于制造飞机和宇宙飞船等,A正确;
B.常温下,浓硫酸能使铁和铝钝化,所以常温下可用铁或铝制容器盛装浓硫酸,B正确;
C.过氧化钠能与二氧化碳和水反应,产生氧气,故过氧化钠可用于呼吸面具的氧气的来源之一,C正确;
D.氯气有毒,不用作食品工业,但是可用于制造农药、染料和药品等,D错误;
故选D。
17.D
【分析】根据流程分析可知,将氯气通入含有Br-的浓缩、酸化后的海水,发生反应2Br-+Cl2=2Cl-+Br2,经吹出塔后进入吸收塔,通入SO2,发生反应Br2+SO2+2H2O=2HBr+H2SO4,HBr进入蒸馏塔再与Cl2发生反应:2Br-+Cl2=2Cl-+Br2,经冷凝、精馏后得到Br2,据此分析解答。
【详解】A.溴易挥发,加水液封可以减少挥发损失,A正确;
B.海水提溴的过程中,均存在元素化合价的变化,均为氧化还原反应,B正确;
C.经过吸收塔后,所得溶液中的Br-浓度远大于进入吹出塔之前的海水中的Br-浓度,因此溴元素得到了富集,C正确;
D.蒸馏塔中发生了化学反应为:2Br-+Cl2=2Cl-+Br2,D错误;
答案选D。
18.A
【详解】A.氧化铝和氧化铁都能和盐酸反应,不能除杂,故A错误;
B.氯化铁和铁反应生成氯化亚铁,故可以除杂,故B正确;
C.铝和氢氧化钠反应生成偏铝酸钠和氢气,镁不与氢氧化钠反应,故可以除杂,故C正确;
D.碳酸氢钠固体加热分解,而碳酸钠固体加热不分解,故可以除杂,故D正确;
故选A。
19.B
【分析】海水通过晒盐分为NaCl和卤水,电解NaCl溶液制取Cl2,卤水中含有溴离子,通入Cl2,氯气将溴离子氧化成溴单质,通入热空气吹出溴,用纯碱溶液吸收溴单质,生成NaBr和NaBrO3,最后加入硫酸酸化,酸性条件下Br-、、H+反应生成溴单质。
【详解】A.步骤Ⅱ和步骤Ⅲ都是富集溴的过程,A错误;
B.步骤Ⅱ用热空气吹出溴,利用了溴易挥发而其他物质不易挥发的特性,B正确;
C.若其他步骤不变,步骤Ⅱ改为用SO2吸收溴,则两者反应生成硫酸根离子和溴离子,此时加入硫酸酸化蒸馏,无法得到单质溴,C错误;
D.步骤Ⅲ中Br-、、H+反应生成溴单质,离子方程式为+5Br-+6H+=3Br2+3H2O,D错误;
故答案选B。
20.C
【详解】A.生铁和钢都是铁和碳的合金,故A正确;
B.镁铝合金密度小、硬度大,是飞机制造业的重要材料,故B正确;
C.硅晶体是良好的半导体材料,可用作计算机芯片、太阳能电池,故C错误;
D.纤维素属于天然高分子材料,故D正确;
选C。
21.B
【详解】A.NaHCO3和Na2CO3都与澄清石灰水反应生成沉淀,不能鉴别,应用氯化钙溶液鉴别,选项A错误;
B.NaHCO3受热分解生成Na2CO3,所以Na2CO3的热稳定性大于NaHCO3,选项B正确;
C.第③、⑤步骤中,溴元素均被氧化,但④步骤,其被还原,选项C错误;
D.工业上通过电解熔融MgCl2制取金属镁,选项D错误。
答案选B。
【点睛】本题重点考查了化学与资源综合利用、环境保护等方面的知识,开发利用金属矿物和海水资源是新课程标准教材中的必修内容,在高考命题上也有所体现.金属矿物中的铁矿石、铝土矿相关内容,海水资源相关的海水提溴、海水提镁都是高考命题的热点,同学们应给予重视.只在掌握好相关的物理、化学性质以及基本实验技能就能顺利解答。
22.D
【分析】海带浸取液中碘元素以I-形式存在,H2O2具有强氧化性,反应①发生2I-+H2O2+2H+=I2+2H2O,I2易溶于有机溶剂,反应②萃取分液,得到含I2的有机溶液,然后加入NaOH溶液,发生3I2+6NaOH=5NaI+NaIO3+3H2O,NaI和NaIO3易溶于水,根据流程图,CCl4难溶于水,且密度大于水,下层溶液为CCl4,上层溶液为NaI和NaIO3,上层溶液加入H2SO4发生5I-+IO3-+6H+=3H2O+3I2,然后采用过滤的方法获得I2,据此分析;
【详解】A. 根据上述分析,I-先转化成I2,利用I2易溶于有机溶剂,进行萃取,得到I2的有机溶液,然后再获得I2的悬浊液,该实验方案中采用了反萃取法,故A说法正确;
B. 根据上述分析,有机溶剂a为CCl4,故B说法正确;
C. I2与NaOH反应发生歧化反应,其反应方程式为3I2+6NaOH=5NaI+NaIO3+3H2O,故C说法正确;
D. 含I2饿悬浊液获得I2固体,操作应是过滤,故D说法错误;
答案为D。
23.B
【分析】根据工艺流程分析将将海水酸化的目的是避免后续流程中造成的损耗,通入将氧化生成,利用热空气将溴蒸气吹出,再用脱氯,然后用溶液吸收溴,再酸化得到,据分析答题。
【详解】A.将海水酸化的目的是避免后续流程中造成的损耗,A正确;
B.中具有脱氯作用的离子不仅有,还有B错误;
C.溶液失去脱氯作用后,补加或加入铁粉,脱氯作用恢复,C正确;
D.用溶液吸收溴,歧化为和。再用酸化歧化后的溶液得到,其离子方程式为:,D正确;
故选B。
24.D
【详解】A.粮食酿酒中有乙醇等新物质生成,涉及化学反应,A错误;
B.铁、铝、铜都是单质,不属于电解质,B错误;
C.氯化钠在通电的情况下不能导电,无法电离产生自由移动的离子,C错误;
D.青铜亚长牛尊为青铜器,由铜、铅、锡等金属组成,属于金属文物,D正确;
故答案选D。
25.B
【详解】A.酸性条件下氧化剂的氧化能力增强,反应中加入稀硫酸可提高氧化剂的氧化能力,故A正确;
B.在酸性条件下发生如下反应:,故碘盐中不可同时添加KIO3和KI,故B错误;
C.X为过氧化氢溶液,过氧化氢具有强氧化性,与KI反应生成I2,观察到溶液变蓝,则加碘盐中碘存在形式为KI,故C正确;
D.维生素C具有还原性,KIO3具有氧化性,两者反应能生成I2,观察到溶液变蓝,则加碘盐中碘存在形式为,故D正确;
故选:B。
26.金属冶炼方法的选择取决于金属在自然界中的存在状态和金属的活泼性。金属越活泼,冶炼时所需条件要求越高,在人类历史上出现的相对晚一些。金属越不活泼,冶炼的方法越简单,人们使用的时间越早,所以有青铜、铁器等时代的发展历程。
【详解】金属冶炼方法的选择取决于金属在自然界中的存在状态和金属的活泼性。金属越活泼,冶炼时所需条件要求越高,在人类历史上出现的相对晚一些。金属越不活泼,冶炼的方法越简单,人们使用的时间越早,所以有青铜、铁器等时代的发展历程。故答案为:金属冶炼方法的选择取决于金属在自然界中的存在状态和金属的活泼性。金属越活泼,冶炼时所需条件要求越高,在人类历史上出现的相对晚一些。金属越不活泼,冶炼的方法越简单,人们使用的时间越早,所以有青铜、铁器等时代的发展历程。
27.(1)⑥
(2)①
(3)④
【详解】(1)把煤隔绝空气加强热,得焦炉气、煤焦油和焦炭等过程属于煤的干馏,故答案为⑥;
(2)根据原油中各组分沸点不同,从原油中分离出汽油、煤油、柴油等方法是分馏,故答案为①;
(3)将由长碳链组成的重油转化为短碳链组成的汽油的过程为裂化,故答案为④。
28.(1) 1 5 3 3 3 3 下层溶液显紫色 I2+SO+H2O=2I-+SO+2H+
(2) 通入Cl2发生歧化反应;Cl2+H2O H++Cl-+HClO,增大c(H+),平衡逆向移动,抑制Cl2与水的反应 3 3 1 3 5NaBr 盐酸有还原性,与溴酸根反应 3
【详解】(1)①KIO3中I元素的化合价由+5价降低为0,KIO3为氧化剂,KI中I元素的化合价由-1价升高为0,KI为还原剂,由得失电子守恒及质量守恒定律可知,反应的化学方程式为:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O。
②向溶液中加入四氯化碳,四氯化碳密度比水大在下层,将碘从水中萃取出来,下层溶液显紫色;Na2SO3稀溶液具有还原性,被氧化为硫酸钠,I2具有氧化性,被还原为I-,依据得失电子守恒、电荷守恒和原子守恒,反应的离子方程式为:I2+SO+H2O=2I-+SO+2H+。
(2)①通入氯气后发生反应:Cl2+H2O Cl-+H++HClO,增大c(H+),平衡逆向移动,抑制Cl2与水反应,因此调节海水pH可提高Cl2的利用率。
②溴元素化合价由0价升高到+5价,由0价降低到-1价,依据得失电子守恒和原子守恒可知,反应的化学方程式为:3Br2+3Na2CO3=NaBrO3+3CO2+5NaBr。
③相同条件下,若用盐酸酸化,由于溴酸根离子具有氧化性,氯离子具有还原性,两者发生氧化还原反应,导致一部分溴反应掉,则所得溴的质量减少。
④2.6molNaBrO3反应生成溴单质时转移的电子数为2.6×5=13mol,生成碘为0.5mol,转移的电子为1mol,则生成碘酸根离子转移的电子数为12mol,生成碘酸根离子的物质的量为2mol,根据碘原子守恒,则原溶液中NaI的物质的量为2mol+1mol=3mol
一、单选题
1.人类最早使用的合金是
A.铜合金 B.铁合金 C.铝合金 D.镁合金
2.合金具有许多优良的物理、化学或机械性能。下列物质中,不属于合金的是
A.硬铝 B.不锈钢 C.生铁 D.铝
3.中国历史文化悠久,流传下许多精美文物。下列有关文物的描述错误的是
A.商周青铜器的主要成分是金属材料 B.秦兵马俑的主要成分是高分子材料
C.唐代丝绸的主要成分是蛋白质 D.宋代陶瓷的主要成分是无机非金属材料
4.新材料的发展充分体现了“中国技术”“中国制造”和“中国力量”。下列说法错误的是
A.蛟龙号潜水器用到了钛合金,22号钛元素属于过渡元素
B.港珠澳大桥用到的合金材料,具有强度大、密度小、耐腐蚀等性能
C.国产大飞机C919使用的“现代工业骨骼”碳纤维是一种新型有机高分子材料
D.“华为麒麟980”手机中芯片的主要成分是硅单质
5.石油在常压下分馏,得到的主要产品是
A.汽油、煤油、柴油、重油 B.煤油、柴油、重油、渣油
C.柴油、重油、石蜡、润滑油 D.凡士林、石蜡、沥青、石油焦
6.影响金属冶炼方法的主要因素是
A.金属的活动性大小
B.金属在地壳中的含量多少
C.金属的化合价高低
D.金属的导电性强弱
7.下列物质不属于合金的是( )
A.不锈钢 B.高碳钢
C.金刚石 D.白铜
8.北京冬奥会备受世界瞩目。下列说法错误的是
A.冰壶主材料花岗岩属于无机非金属材料
B.火炬“飞扬”使用的碳纤维属于有机高分子材料
C.冬奥会“同心”金属奖牌属于合金材料
D.短道速滑服使用的超高分子量聚乙烯属于有机高分子材料
9.下列说法不正确的是
A.碳酸钠和碳酸氢钠的溶液均显碱性,可用作食用碱或工业用碱
B.硬铝具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料
C.将Cl2通入澄清石灰水中制得以Ca(ClO)2为有效成分的漂白粉
D.储氢合金是一类能够吸收氢气, 并与氢气结合成金属氢化物的材料
10.下列有关金属的用途与相应性质不对应的是
A.用金做饰物是因为金的化学性质稳定、不褪色
B.用钨做白炽灯灯丝是因为其熔点高、导电性好
C.用镁合金做汽车部件是因为镁的密度小,化学性质活泼
D.用铝做包装用的铝箔是因为其延展性好,表面有钝化膜
11.当航天飞机返回地球进入大气层时,由于空气的剧烈摩擦,航天飞机尖端的温度超过1000℃。为防止高温将其烧毁,科学家给航天飞机相应部位设计安装了可靠的保护层.制作保护层的材料可能为( )
A.合成塑料 B.新型陶瓷 C.镁铝合金 D.不锈钢
12.工业生产中常将两种或多种金属(或金属与非金属)在同一容器中加热使其熔合,冷凝后得到具有金属特性的熔合物——合金。这是制取合金的常用方法之一、根据下表数据判断,不宜用上述方法制取合金的是
金属 Na Cu Al Fe
熔点(℃) 97.5 1 083 660 1 535
沸点(℃) 883 2 595 2 200 3 000
其中不能形成合金的是
A.Cu与Al B.Fe与Na C.Fe与Cu D.Al与Na
13.关于卤素单质以及形成的负离子,下列说法正确的是
A.氯气有毒,氯离子也有毒 B.液溴在棕色瓶中水封密封保存
C.碘离子遇淀粉变蓝 D.海水中富含液溴
14.下列说法正确的是( )
A.石油是混合物,汽油是纯净物
B.沸点:汽油>煤油>柴油>润滑油
C.直馏汽油和裂化汽油成分完全相同
D.石油的分馏是物理变化,而裂化和裂解属于化学变化
15.悠久的历史孕育了丰富的民间艺术文化瑰宝。下列文物器具的材质主要为合金的是
选项 A B C D
文物器具
名称 端石琴式砚 馆陶黑陶 木雕罗汉像 信宜铜盉
A.A B.B C.C D.D
16.下列叙述错误的是
A.硬铝的密度小,强度高,具有较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料
B.常温下可用铁或铝制容器盛装浓硫酸
C.过氧化钠可用于呼吸面具的氧气的来源之一
D.氯气有毒,所以不能用于制造农药、染料和药品等
17.“空气吹出法”海水提溴的工艺流程如下:
下列说法中,不正确的是
A.实验室保存溴通常加少量水
B.海水提溴发生的反应均为氧化还原反应
C.经过吸收塔后,溴元素得到了富集
D.蒸馏塔中只发生了物理变化
18.下列除杂试剂或方法不正确的是选项
选项 被提纯物质 杂质 除杂试剂或方法
A Fe2O3 Al2O3 加入过量盐酸并过滤
B FeCl2溶液 FeCl3 加入过量铁粉并过滤
C 镁粉 铝粉 加入过量NaOH溶液并过滤
D Na2CO3固体 NaHCO3 加热到固体质量不变
A.A B.B C.C D.D
19.海水中蕴藏着丰富的资源,下面是海水提溴的工艺流程,下列说法正确的是
A.只有步骤Ⅱ是富集过程
B.步骤Ⅱ用热空气吹出,原理是利用物质挥发性不同
C.保持其它步骤不变,步骤Ⅱ可改用二氧化硫吸收
D.步骤Ⅲ发生的反应的离子方程式为:
20.下列说法不正确的是
A.生铁和钢都是铁和碳的合金
B.镁铝合金是飞机制造业的重要材料
C.硅晶体是良好的半导体材料,可用作光导纤维
D.竹简的成分之一纤维素属于天然高分子材料
21.海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
下列有关说法正确的是
A.用澄清的石灰水可鉴NaHCO3和Na2CO3
B.制取NaHCO3的反应是利用其溶解度小于NaCl的溶解度
C.在第③、④、⑤步骤中,溴元素均被氧化
D.工业上通过电解饱和MgCl2溶液制取金属镁
22.为了从海带浸取液中提取碘,某同学设计了如下实验方案:
下列说法不正确的是
A.上述实验方案中采用了反萃取法
B.②中有机溶剂a可为CCl4
C.③中发生反应的化学方程式:3I2+6NaOH=5NaI+NaIO3+3H2O
D.操作Z的名称是加热
23.溴主要以形式存在于海水(呈弱碱性)中,利用空气吹出法从海水中提溴,工艺流程示意如下。
下列说法不正确的是
A.将海水酸化的目的是避免后续流程中造成的损耗
B.中具有脱氯作用的离子仅为
C.溶液失去脱氯作用后,补加或加入铁粉,脱氯作用恢复
D.用溶液吸收溴,歧化为和。再用酸化歧化后的溶液得到,其离子方程式为
24.下列说法中正确的是
A.我国古代的技术应用中,粮食酿酒的工作原理不涉及化学反应
B.铁、铝、铜是制造潜艇必不可少的重要金属材料,三者均能导电,均为电解质
C.氯化钠在通电的情况下电离产生自由移动的离子
D.按制作文物的主要材料分类,青铜亚长牛尊属于金属文物
25.加碘盐中碘可能有两种存在形式KI或,某兴趣小组设计如图实验检验某品牌加碘盐中碘的存在形式。提供试剂:维生素C、过氧化氢溶液
下列说法错误的是
A.反应中加入稀硫酸可提高氧化剂的氧化能力
B.加碘盐中可同时添加和KI
C.若X为过氧化氢溶液,观察到溶液变蓝,则加碘盐中碘存在形式为KI
D.若X为维生素C,观察到溶液变蓝,则加碘盐中碘存在形式为
二、填空题
26.如图是我国古代和现代冶金的两张图片,那么人类使用金属的年代先后顺序与金属的活动性有什么关系 ?
27.请将下列物质的转化或分离方法的序号填在横线上(每一项只填写一种方法)。
①分馏 ②液化 ③气化 ④裂化 ⑤裂解 ⑥干馏 ⑦蒸馏
(1)把煤转化为焦炉气、煤焦油和焦炭等。
(2)从原油中分离出汽油、煤油、柴油等。
(3)将重油转化为汽油。
28.溴和碘的化合物在生产和生活中有广泛的用途.
(1)市场销售的某种食用精制盐中含碘酸钾。
①碘酸钾与碘化钾在酸性条件下发生如下反应,配平该反应的化学方程式:
( ) +( )KI+( ) =( ) +( ) +( )
②上述反应生成的I2可用四氯化碳检验,现象为 。
向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
Na2SO3稀溶液与I2反应的离子方程式是 。
(2)海水提溴过程中溴元素的变化如下:
①过程I,海水显碱性,调其pH<3.5后,再通入氯气,调节海水pH可提高C12的利用率,用平衡原理解释其原因是 。
②过程II,用热空气将溴赶出,再用浓Na2CO3溶液吸收。完成并配平下列方程式。
( ) +( ) =( ) +( ) +( )
③过程III,用硫酸酸化可得Br2和Na2SO4的混合溶液。相同条件下,若用盐酸酸化,则所得溴的质量减少,原因是 。
④NaBrO3是一种分析试剂。向硫酸酸化的NaI溶液中逐滴加入NaBrO3溶液,当加入 2.6molNaBrO3时,测得反应后溶液中溴和碘的存在形式及物质的量分别为:
则原溶液中NaI的物质的量为 mol.
试卷第1页,共3页
参考答案:
1.A
【详解】由于铜的活动性比较弱,以单质形成存在的比较多,所以人类历史上使用最早的合金是铜合金。故A符合题意,BCD不符合题意。
答案选A。
2.D
【详解】A.硬铝是铝、铜、镁、锰、硅等形成的铝合金,故A不符合题意;
B.不锈钢是铁与镍和铬形成的铁合金,故B不符合题意;
C.生铁是铁含有碳的铁合金,故C不符合题意;
D.铝是纯净的单质,不属于合金,故D符合题意;
故选D。
3.B
【详解】A.青铜器属于合金,为金属材料,故A正确;
B.秦兵马俑的主要成分是硅酸盐,属于传统无机非金属材料,故B错误;
C.丝绸的主要成分是蛋白质,故C正确;
D.陶瓷的主要成分是硅酸盐,属于无机非金属材料,故D正确;
故选:B。
4.C
【详解】A.22号钛元素位于第四周期ⅣB族,属于过渡元素,A项正确;
B.港珠澳大桥用到的合金材料,必须具有强度大、密度小、耐腐蚀等特性才能抵御恶劣环境及海水的侵蚀,B项正确;
C.碳纤维主要成分是碳单质,属于无机物,C项错误;
D.硅晶体是良好的半导体材料,常用于制作收集芯片,D项正确;
综上所述答案为C。
5.A
【详解】石油常压分馏产物:液化石油气、汽油、煤油、柴油、重油,故A满足,将重质油品进行减压蒸馏等处理,以得到渣油和燃料油等,B不满足;减压分馏过程的产物:重柴油、润滑油、凡士林、石蜡、沥青,故C、D不满足;
故选A。
6.A
【详解】不同的金属应选用不同的冶炼方法,金属的冶炼方法是根据金属的活动性强弱确定,与金属在地壳中的含量、化合价及金属的导电性没有关系,答案选A。
【点晴】注意根据金属的活动性强弱选择合适的冶炼方法,金属的活动性强弱和金属阳离子得电子能力之间有关系,一般来说,活泼金属用电解法,较活泼金属用热还原法,不活泼金属如Hg、Ag等用热分解法冶炼。
7.C
【详解】合金是一种金属与另一种或几种金属或非金属经过混合熔化,冷却凝固后得到的具有金属性质的固体产物。不锈钢、高碳钢、白铜等均属于合金,金刚石是碳的一种单质,不是合金,答案选C。
8.B
【详解】A.花岗岩的主要成分是石英、云母、长石等矿物,属于无机非金属材料,A正确;
B.碳纤维指的是含碳量在90%以上的高强度高模量纤维,属于无机非金属材料,B错误;
C.金属奖牌属于合金材料,C正确;
D.聚乙烯属于有机高分子材料,D正确;
故答案选B。
9.C
【详解】A.用pH试纸测定碳酸钠和碳酸氢钠的溶液均显碱性,碳酸氢钠可用作发酵粉和食品膨松剂,碳酸钠用于化工生产和除油污,故A正确;
B.硬铝是铝合金,具有硬度大、密度小,较强的抗腐蚀能力,是制造飞机和宇宙飞船的理想材料,故B正确;
C.工业上将Cl2通入石灰乳中制得以CaClO)2为有效成分的漂白粉,故C错误;
D.一些合金能够大量吸收氢气,一定条件下与氢气结合成金属氢化物,又能放出氢气,这类金属材料叫做储氢合金,故D正确;
答案选C。
10.C
【详解】A.用金做饰物是因为金化学性质稳定,不褪色,A正确;
B.钨熔点高、导电性好,所以用作灯丝,B正确;
C.用镁合金做汽车部件是因为合金的密度小,强度高,与镁的化学性质活泼没有关系,C错误;
D.用铝做包装用的铝箔是因为其延展性好,且铝表面易被氧化为一层致密的钝化膜,D正确;
故选C。
11.B
【分析】航天飞机尖端的温度超过1000℃.为防止高温将其烧毁,则材料应为耐高温、不易导热的材料。
【详解】A.塑料的熔点很小,所以不能耐高温,A错误;
B.新型陶瓷耐高温熔点较高,所以能耐高温,可作保护层,B正确;
C.镁铝合金的熔点较低,C错误;
D.不锈钢为耐空气、蒸汽、水等弱腐蚀介质或具有不锈性的钢种,导热性能好,不适宜作保护层材料,D错误;
答案为B。
12.B
【详解】A.从表中数据可以看出,Cu的熔点低于Al的沸点,二者可以相互熔合而制成合金,A不符合题意;
B.Fe的熔点为1 535℃,而Na的沸点为883℃,则Fe的熔点高于Na的沸点,也就是Fe未熔化Na就已经汽化,二者不可能熔合成合金,B符合题意;
C.Fe的熔点低于Cu的沸点,二者可以熔合成合金,C不符合题意;
D.Al的熔点低于Na的沸点,二者可熔合成合金,D不符合题意;
故选B。
13.B
【详解】A.不同微粒的性质不同,氯气有毒,但氯离子没有毒,如NaCl是一种常用的调味剂,A错误;
B.液溴易挥发且溴蒸气有毒,故液溴在棕色瓶中水封密封保存,B正确;
C.I2遇到淀粉变蓝是其特性,但碘离子遇淀粉不变蓝,C错误;
D.Br2是活泼的非金属单质,化学性质活泼,故在海水中富含溴离子,不含液溴,D错误;
故答案为:B。
14.D
【详解】A.石油是混合物,汽油是多种烷烃(C5~C8)的混合物,故A错误;
B.烃分子中碳原子数越多沸点越高,沸点:汽油<煤油<柴油<润滑油,故B错误;
C.直馏汽油中不含烯烃,而裂化汽油中含有烯烃,两者组成上不完全相同,故C错误;
D.石油的分馏没有生成新物质,属于物理变化,而裂化和裂解有新物质生成,属于化学变化,故D正确;
选D。
15.D
【详解】由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质为合金,
A.砚的成分为无机盐,含碳酸钙,不是合金,故A不选;
B.馆陶黑陶材料为陶瓷,成分为硅酸盐,不是合金,故B不选;
C.木雕罗汉像,木材成分为纤维素,不是合金,故C不选;
D.信宜铜盉为铜合金,故D选;
故选:D。
16.D
【详解】A.硬铝是铝合金,其密度小,强度高,具有较强的抗腐蚀能力,可用于制造飞机和宇宙飞船等,A正确;
B.常温下,浓硫酸能使铁和铝钝化,所以常温下可用铁或铝制容器盛装浓硫酸,B正确;
C.过氧化钠能与二氧化碳和水反应,产生氧气,故过氧化钠可用于呼吸面具的氧气的来源之一,C正确;
D.氯气有毒,不用作食品工业,但是可用于制造农药、染料和药品等,D错误;
故选D。
17.D
【分析】根据流程分析可知,将氯气通入含有Br-的浓缩、酸化后的海水,发生反应2Br-+Cl2=2Cl-+Br2,经吹出塔后进入吸收塔,通入SO2,发生反应Br2+SO2+2H2O=2HBr+H2SO4,HBr进入蒸馏塔再与Cl2发生反应:2Br-+Cl2=2Cl-+Br2,经冷凝、精馏后得到Br2,据此分析解答。
【详解】A.溴易挥发,加水液封可以减少挥发损失,A正确;
B.海水提溴的过程中,均存在元素化合价的变化,均为氧化还原反应,B正确;
C.经过吸收塔后,所得溶液中的Br-浓度远大于进入吹出塔之前的海水中的Br-浓度,因此溴元素得到了富集,C正确;
D.蒸馏塔中发生了化学反应为:2Br-+Cl2=2Cl-+Br2,D错误;
答案选D。
18.A
【详解】A.氧化铝和氧化铁都能和盐酸反应,不能除杂,故A错误;
B.氯化铁和铁反应生成氯化亚铁,故可以除杂,故B正确;
C.铝和氢氧化钠反应生成偏铝酸钠和氢气,镁不与氢氧化钠反应,故可以除杂,故C正确;
D.碳酸氢钠固体加热分解,而碳酸钠固体加热不分解,故可以除杂,故D正确;
故选A。
19.B
【分析】海水通过晒盐分为NaCl和卤水,电解NaCl溶液制取Cl2,卤水中含有溴离子,通入Cl2,氯气将溴离子氧化成溴单质,通入热空气吹出溴,用纯碱溶液吸收溴单质,生成NaBr和NaBrO3,最后加入硫酸酸化,酸性条件下Br-、、H+反应生成溴单质。
【详解】A.步骤Ⅱ和步骤Ⅲ都是富集溴的过程,A错误;
B.步骤Ⅱ用热空气吹出溴,利用了溴易挥发而其他物质不易挥发的特性,B正确;
C.若其他步骤不变,步骤Ⅱ改为用SO2吸收溴,则两者反应生成硫酸根离子和溴离子,此时加入硫酸酸化蒸馏,无法得到单质溴,C错误;
D.步骤Ⅲ中Br-、、H+反应生成溴单质,离子方程式为+5Br-+6H+=3Br2+3H2O,D错误;
故答案选B。
20.C
【详解】A.生铁和钢都是铁和碳的合金,故A正确;
B.镁铝合金密度小、硬度大,是飞机制造业的重要材料,故B正确;
C.硅晶体是良好的半导体材料,可用作计算机芯片、太阳能电池,故C错误;
D.纤维素属于天然高分子材料,故D正确;
选C。
21.B
【详解】A.NaHCO3和Na2CO3都与澄清石灰水反应生成沉淀,不能鉴别,应用氯化钙溶液鉴别,选项A错误;
B.NaHCO3受热分解生成Na2CO3,所以Na2CO3的热稳定性大于NaHCO3,选项B正确;
C.第③、⑤步骤中,溴元素均被氧化,但④步骤,其被还原,选项C错误;
D.工业上通过电解熔融MgCl2制取金属镁,选项D错误。
答案选B。
【点睛】本题重点考查了化学与资源综合利用、环境保护等方面的知识,开发利用金属矿物和海水资源是新课程标准教材中的必修内容,在高考命题上也有所体现.金属矿物中的铁矿石、铝土矿相关内容,海水资源相关的海水提溴、海水提镁都是高考命题的热点,同学们应给予重视.只在掌握好相关的物理、化学性质以及基本实验技能就能顺利解答。
22.D
【分析】海带浸取液中碘元素以I-形式存在,H2O2具有强氧化性,反应①发生2I-+H2O2+2H+=I2+2H2O,I2易溶于有机溶剂,反应②萃取分液,得到含I2的有机溶液,然后加入NaOH溶液,发生3I2+6NaOH=5NaI+NaIO3+3H2O,NaI和NaIO3易溶于水,根据流程图,CCl4难溶于水,且密度大于水,下层溶液为CCl4,上层溶液为NaI和NaIO3,上层溶液加入H2SO4发生5I-+IO3-+6H+=3H2O+3I2,然后采用过滤的方法获得I2,据此分析;
【详解】A. 根据上述分析,I-先转化成I2,利用I2易溶于有机溶剂,进行萃取,得到I2的有机溶液,然后再获得I2的悬浊液,该实验方案中采用了反萃取法,故A说法正确;
B. 根据上述分析,有机溶剂a为CCl4,故B说法正确;
C. I2与NaOH反应发生歧化反应,其反应方程式为3I2+6NaOH=5NaI+NaIO3+3H2O,故C说法正确;
D. 含I2饿悬浊液获得I2固体,操作应是过滤,故D说法错误;
答案为D。
23.B
【分析】根据工艺流程分析将将海水酸化的目的是避免后续流程中造成的损耗,通入将氧化生成,利用热空气将溴蒸气吹出,再用脱氯,然后用溶液吸收溴,再酸化得到,据分析答题。
【详解】A.将海水酸化的目的是避免后续流程中造成的损耗,A正确;
B.中具有脱氯作用的离子不仅有,还有B错误;
C.溶液失去脱氯作用后,补加或加入铁粉,脱氯作用恢复,C正确;
D.用溶液吸收溴,歧化为和。再用酸化歧化后的溶液得到,其离子方程式为:,D正确;
故选B。
24.D
【详解】A.粮食酿酒中有乙醇等新物质生成,涉及化学反应,A错误;
B.铁、铝、铜都是单质,不属于电解质,B错误;
C.氯化钠在通电的情况下不能导电,无法电离产生自由移动的离子,C错误;
D.青铜亚长牛尊为青铜器,由铜、铅、锡等金属组成,属于金属文物,D正确;
故答案选D。
25.B
【详解】A.酸性条件下氧化剂的氧化能力增强,反应中加入稀硫酸可提高氧化剂的氧化能力,故A正确;
B.在酸性条件下发生如下反应:,故碘盐中不可同时添加KIO3和KI,故B错误;
C.X为过氧化氢溶液,过氧化氢具有强氧化性,与KI反应生成I2,观察到溶液变蓝,则加碘盐中碘存在形式为KI,故C正确;
D.维生素C具有还原性,KIO3具有氧化性,两者反应能生成I2,观察到溶液变蓝,则加碘盐中碘存在形式为,故D正确;
故选:B。
26.金属冶炼方法的选择取决于金属在自然界中的存在状态和金属的活泼性。金属越活泼,冶炼时所需条件要求越高,在人类历史上出现的相对晚一些。金属越不活泼,冶炼的方法越简单,人们使用的时间越早,所以有青铜、铁器等时代的发展历程。
【详解】金属冶炼方法的选择取决于金属在自然界中的存在状态和金属的活泼性。金属越活泼,冶炼时所需条件要求越高,在人类历史上出现的相对晚一些。金属越不活泼,冶炼的方法越简单,人们使用的时间越早,所以有青铜、铁器等时代的发展历程。故答案为:金属冶炼方法的选择取决于金属在自然界中的存在状态和金属的活泼性。金属越活泼,冶炼时所需条件要求越高,在人类历史上出现的相对晚一些。金属越不活泼,冶炼的方法越简单,人们使用的时间越早,所以有青铜、铁器等时代的发展历程。
27.(1)⑥
(2)①
(3)④
【详解】(1)把煤隔绝空气加强热,得焦炉气、煤焦油和焦炭等过程属于煤的干馏,故答案为⑥;
(2)根据原油中各组分沸点不同,从原油中分离出汽油、煤油、柴油等方法是分馏,故答案为①;
(3)将由长碳链组成的重油转化为短碳链组成的汽油的过程为裂化,故答案为④。
28.(1) 1 5 3 3 3 3 下层溶液显紫色 I2+SO+H2O=2I-+SO+2H+
(2) 通入Cl2发生歧化反应;Cl2+H2O H++Cl-+HClO,增大c(H+),平衡逆向移动,抑制Cl2与水的反应 3 3 1 3 5NaBr 盐酸有还原性,与溴酸根反应 3
【详解】(1)①KIO3中I元素的化合价由+5价降低为0,KIO3为氧化剂,KI中I元素的化合价由-1价升高为0,KI为还原剂,由得失电子守恒及质量守恒定律可知,反应的化学方程式为:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O。
②向溶液中加入四氯化碳,四氯化碳密度比水大在下层,将碘从水中萃取出来,下层溶液显紫色;Na2SO3稀溶液具有还原性,被氧化为硫酸钠,I2具有氧化性,被还原为I-,依据得失电子守恒、电荷守恒和原子守恒,反应的离子方程式为:I2+SO+H2O=2I-+SO+2H+。
(2)①通入氯气后发生反应:Cl2+H2O Cl-+H++HClO,增大c(H+),平衡逆向移动,抑制Cl2与水反应,因此调节海水pH可提高Cl2的利用率。
②溴元素化合价由0价升高到+5价,由0价降低到-1价,依据得失电子守恒和原子守恒可知,反应的化学方程式为:3Br2+3Na2CO3=NaBrO3+3CO2+5NaBr。
③相同条件下,若用盐酸酸化,由于溴酸根离子具有氧化性,氯离子具有还原性,两者发生氧化还原反应,导致一部分溴反应掉,则所得溴的质量减少。
④2.6molNaBrO3反应生成溴单质时转移的电子数为2.6×5=13mol,生成碘为0.5mol,转移的电子为1mol,则生成碘酸根离子转移的电子数为12mol,生成碘酸根离子的物质的量为2mol,根据碘原子守恒,则原溶液中NaI的物质的量为2mol+1mol=3mol
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
