2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 期末评估题(含答案)
文档属性
| 名称 | 2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 期末评估题(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 331.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-07 21:22:02 | ||
图片预览



文档简介
2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 期末评估题(含答案)
鲁教版第五单元 定量研究化学反应
一、选择题。(16题)
1、在化学方程式:C2H8N2 + 2N2O4 = 3X + 2CO2 + 4H2O中,X 的化学式为( )
A. N2 B. H2 C. O2 D. CO
2、植物光合作用可表示为CO2+H2O 淀粉+O2,下列有关说法中正确的是( )
A.淀粉中一定含有C、H两种元素
B.淀粉中一定只含有C、H两种元素
C.淀粉中可能有三种以上的元素
D.淀粉可能是一种单质或一种化合物
3、现取2.3g某有机物在空气中完全燃烧,生成4.4g二氧化碳和2.7g水。对该物质的组成有下列推断:①一定含碳氢元素 ②一定不含氧元素 ③可能含氧元素 ④一定含氧元素 ⑤分子中C、H的原子个数比为2∶5 ⑥分子中C、H、O的元素质量比为12∶3∶8。其中正确的是( )
A.①③⑤ B.①④⑥ C.①②⑤ D.①④⑤
4、在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7:8,当2.8gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )
A.9.6g B.8.8g C.6.8g D.4.4g
5、阻燃剂氢氧化铝受热分解时吸收热量,同时生成耐高温的氧化铝和水蒸气,起到防火作用.下列关于该阻燃剂防火原因的叙述中错误的是( )
A. 反应吸热,降低了可燃物的着火点
B. 生成氧化铝覆盖在可燃物表面,隔绝空气
C. 生成大量水蒸气,降低可燃物周围氧气浓度
D. 反应能够降低温度,可燃物不易达到着火点
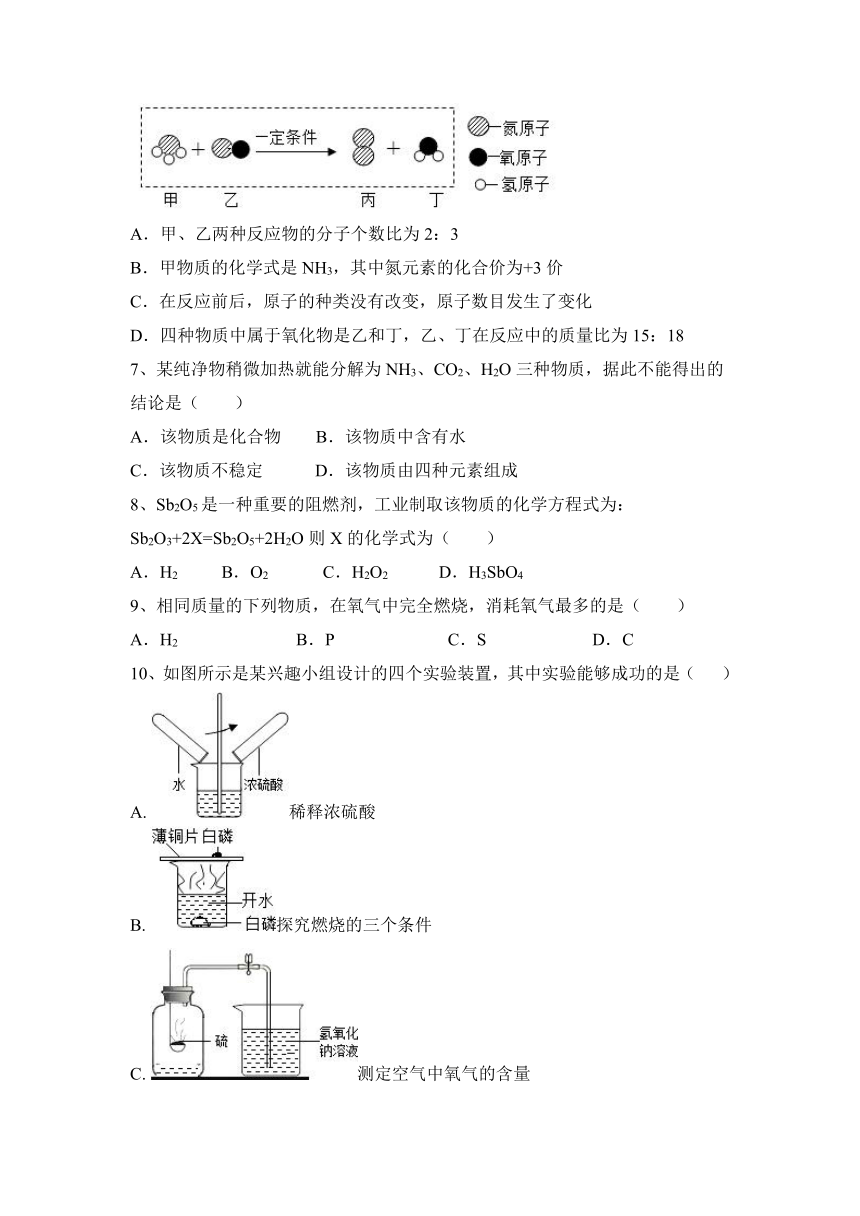
6、科学研究发现,在一定条件下,甲、乙两种气体混合发生反应(微观示意图如图)。该反应产物无污染可用于汽车尾气处理。下列说法正确的是( )
A.甲、乙两种反应物的分子个数比为2:3
B.甲物质的化学式是NH3,其中氮元素的化合价为+3价
C.在反应前后,原子的种类没有改变,原子数目发生了变化
D.四种物质中属于氧化物是乙和丁,乙、丁在反应中的质量比为15:18
7、某纯净物稍微加热就能分解为NH3、CO2、H2O三种物质,据此不能得出的结论是( )
A.该物质是化合物 B.该物质中含有水
C.该物质不稳定 D.该物质由四种元素组成
8、Sb2O5是一种重要的阻燃剂,工业制取该物质的化学方程式为:Sb2O3+2X=Sb2O5+2H2O则X的化学式为( )
A.H2 B.O2 C.H2O2 D.H3SbO4
9、相同质量的下列物质,在氧气中完全燃烧,消耗氧气最多的是( )
A.H2 B.P C.S D.C
10、如图所示是某兴趣小组设计的四个实验装置,其中实验能够成功的是( )
A. 稀释浓硫酸
B. 探究燃烧的三个条件
C. 测定空气中氧气的含量
D. 验证质量守恒定律
11、推理是学习化学的一种重要方法,以下推理正确的是( )
A.化学变化伴随着能量变化,所以有能量变化的一定是化学变化
B.蜡烛在空气中燃烧后质量减轻,所以不符合质量守恒定律
C.同种元素有相同的核电荷数,所以核电荷数相同的微粒一定属于同种元素
D.化合物由多种元素组成,因此由多种元素组成的纯净物一定是化合物
12、下列现象能用质量守恒定律解释的是
A.蜡烛燃烧时慢慢变短
B.10 g食盐完全溶解于90g水中,得到100g食盐水
C.打开酒精的瓶盖一段时间,酒精质量变小
D.2体积的氢气加压后变成1体积
13、二氧化碳和氢气可在一定条件下反应,生产一种重要的化工原料甲醇,化学方程式为。下列有关该反应的说法错误的是( )
A.为 CO2的利用创造了一种新途径
B.属于化合反应
C.反应前后分子数发生了改变
D.钌-膦络合物的质量在反应前后没有改变
14、加热15.8g高锰酸钾,当产生1.6g氧气时,固体剩余物的成分是( )
A.K2MnO4和MnO2 B.KMnO4、K2MnO4和MnO2
C.KMnO4和MnO2 D.KMnO4和K2MnO4
15、某同学用下图所示装置探究可燃物燃烧的条件,得到以下实验事实:①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧。能证明可燃物必须达到一定温度(着火点)才能燃烧的实验事实是( )
A. ①② B. ②④ C. ①④ D. ③④
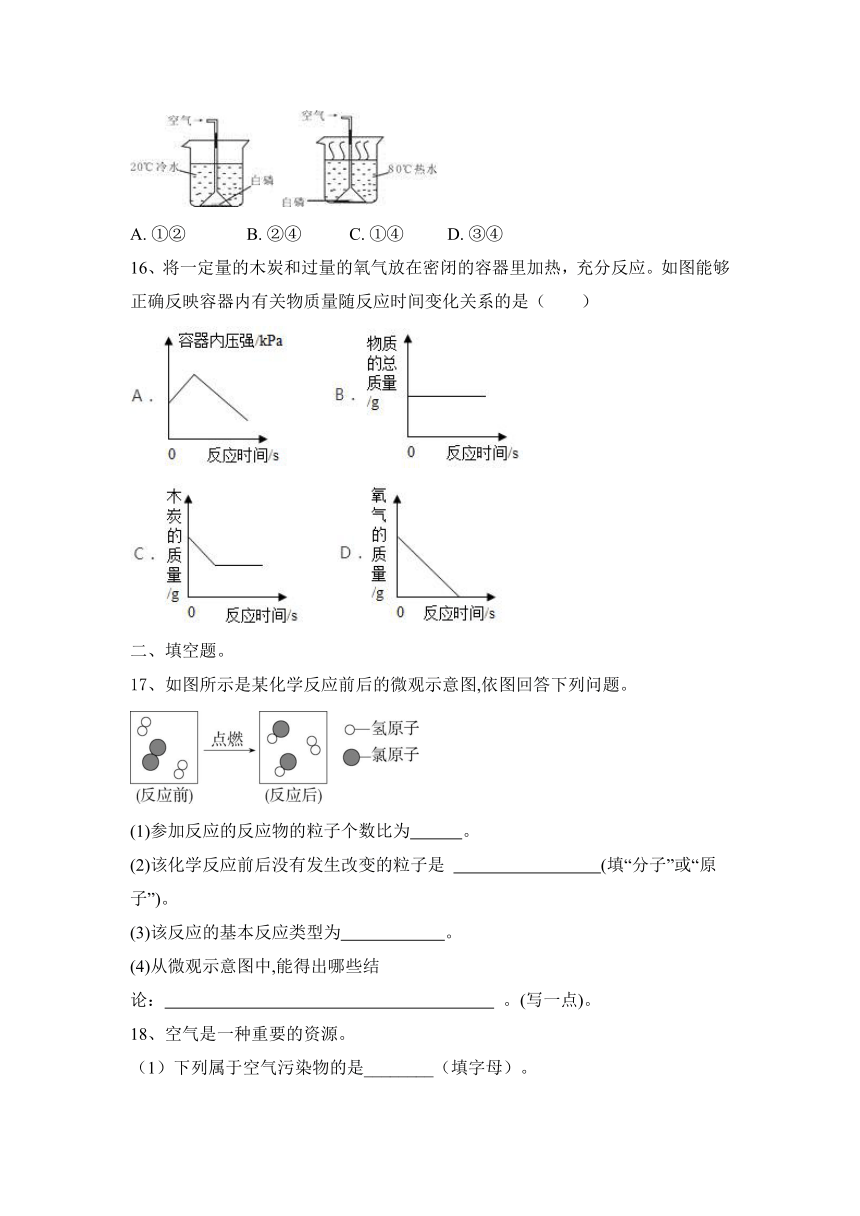
16、将一定量的木炭和过量的氧气放在密闭的容器里加热,充分反应。如图能够正确反映容器内有关物质量随反应时间变化关系的是( )
二、填空题。
17、如图所示是某化学反应前后的微观示意图,依图回答下列问题。
(1)参加反应的反应物的粒子个数比为 。
(2)该化学反应前后没有发生改变的粒子是 (填“分子”或“原子”)。
(3)该反应的基本反应类型为 。
(4)从微观示意图中,能得出哪些结论: 。(写一点)。
18、空气是一种重要的资源。
(1)下列属于空气污染物的是________(填字母)。
A 臭氧 B 二氧化氮C PM2.5D PM10
(2)氢气是清洁能源,写出氢气燃烧的化学方程式_____________________。
(3)食品包装中充氮气可以防腐,是由于氮气_____________________。
(4)同温同压下,气体的体积比等于分子个数比。若空气中其他成分忽略不计,如图可表示空气微观模型的是________(填字母)。
19、根据下列装置图,回答有关问题。
(1)写出装置图中标号仪器的名称。a_______;b_______。
(2)实验室用过氧化氢溶液制取氧气可选择的发生装置是___ (填字母),此反应的化学方程式__ 。
(3)若使用高锰酸钾制取氧气,可选用的装置组合是_____(填字母)。
(4)选用D装置收集氧气的原因是_____ 。
(5)加热15.8g高锰酸钾,完全反应后,理论上可以得到____氧气?
20、化学与生产、生活有着密切的联系,请用所学的化学知识回答下列问题:
(1)“共享单车”已走进城市的大街小巷,符合“低碳出行”理念,“低碳”指的是较低的 气体排放,“共享单车”采用铝合金作支架,铝合金属于 (填“纯净物”或“混合物”)。
(2)运动员剧烈运动后感到肌肉酸痛,放松一段时间后慢慢消失的原因是血液中的乳酸(C3H6O3)与吸入的氧气反应:C3H6O3+3O2=3CO2+3R,则R的化学式为 ,新能源公交车环保,节能,大大方便了市民的出行,氢能是未来最理想的能源,从环保角度分析,氢能最突出的优点是 。氢氧燃料电池是一种将 能转化为 能的装置。
21、写出符合要求的化学方程式:
(1)铁在氧气中燃烧: ;
(2)加热高锰酸钾固体制氧气: ;
(3)电解水的方程式: 。
三、综合应用题。
22、质量守恒定律是一条重要规律。请利用该规律的相关知识回答下列问题。
(1)蜡烛在空气中燃烧时生成二氧化碳和水。由此判断蜡烛中一定含有的元素是________(填元素符号),判断的依据是________ (用微粒的观点解释)。
(2)某同学取一根洁净的铜丝,称量其质量为m1 g,将此铜丝加热(提示:生成氧化铜)并冷却后再次称量,其质量为m2g,则m1________m2(填“>”、“<”或“=”),产生这一结果的原因是________ 。
(3)在密闭容器中放入X、Y、Z、W四种物质并使其发生反应,测得有关数据如下表。关于此反应的认识正确的是________(填字母序号)。
物质 X Y Z W
反应前的质量(g) 2 1 16 16
一段时间后的质量(g) 17 m 6 11
A.m=1
B.该反应为分解反应
C.X与Z的化学计量数之比是3:2
D.若该反应充分进行,反应后W仍有剩余
四、实验题。
23、如图是初中化学中的一些重要实验。
(1)图1实验中,能证明可燃物燃烧跟温度有关的实验现象是:
。
(2)通过图2中A、B对比说明燃烧需要的条件是 。
(3)切割白磷时,应在水下进行。其原因是 。
五、计算题。
24、化学兴趣小组的同学们要测定某过氧化氢溶液的溶质质量分数。他们称取50.0 g过氧化氢溶液放入盛有2.0 g二氧化锰的烧杯(烧杯质量为76.0 g)中。待完全反应后,称量反应后物质连同烧杯的质量为126.4 g(氧气逸出带出的水分忽略不计)。请计算回答。
(1)反应后产生氧气的质量是 g。
(2)该过氧化氢溶液的溶质质量分数是多少 (写出计算过程)
2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 期末评估题(含答案)
鲁教版第五单元 定量研究化学反应
一、选择题。(16题)
1、在化学方程式:C2H8N2 + 2N2O4 = 3X + 2CO2 + 4H2O中,X 的化学式为( )
A. N2 B. H2 C. O2 D. CO
【答案】A
2、植物光合作用可表示为CO2+H2O 淀粉+O2,下列有关说法中正确的是( )
A.淀粉中一定含有C、H两种元素
B.淀粉中一定只含有C、H两种元素
C.淀粉中可能有三种以上的元素
D.淀粉可能是一种单质或一种化合物
【答案】A
3、现取2.3g某有机物在空气中完全燃烧,生成4.4g二氧化碳和2.7g水。对该物质的组成有下列推断:①一定含碳氢元素 ②一定不含氧元素 ③可能含氧元素 ④一定含氧元素 ⑤分子中C、H的原子个数比为2∶5 ⑥分子中C、H、O的元素质量比为12∶3∶8。其中正确的是( )
A.①③⑤ B.①④⑥ C.①②⑤ D.①④⑤
【答案】B
4、在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7:8,当2.8gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )
A.9.6g B.8.8g C.6.8g D.4.4g
【答案】B
5、阻燃剂氢氧化铝受热分解时吸收热量,同时生成耐高温的氧化铝和水蒸气,起到防火作用.下列关于该阻燃剂防火原因的叙述中错误的是( )
A. 反应吸热,降低了可燃物的着火点
B. 生成氧化铝覆盖在可燃物表面,隔绝空气
C. 生成大量水蒸气,降低可燃物周围氧气浓度
D. 反应能够降低温度,可燃物不易达到着火点
【答案】A
6、科学研究发现,在一定条件下,甲、乙两种气体混合发生反应(微观示意图如图)。该反应产物无污染可用于汽车尾气处理。下列说法正确的是( )
A.甲、乙两种反应物的分子个数比为2:3
B.甲物质的化学式是NH3,其中氮元素的化合价为+3价
C.在反应前后,原子的种类没有改变,原子数目发生了变化
D.四种物质中属于氧化物是乙和丁,乙、丁在反应中的质量比为15:18
【答案】A
7、某纯净物稍微加热就能分解为NH3、CO2、H2O三种物质,据此不能得出的结论是( )
A.该物质是化合物 B.该物质中含有水
C.该物质不稳定 D.该物质由四种元素组成
【答案】B
8、Sb2O5是一种重要的阻燃剂,工业制取该物质的化学方程式为:Sb2O3+2X=Sb2O5+2H2O则X的化学式为( )
A.H2 B.O2 C.H2O2 D.H3SbO4
【答案】C
9、相同质量的下列物质,在氧气中完全燃烧,消耗氧气最多的是( )
A.H2 B.P C.S D.C
【答案】A
10、如图所示是某兴趣小组设计的四个实验装置,其中实验能够成功的是( )
A. 稀释浓硫酸
B. 探究燃烧的三个条件
C. 测定空气中氧气的含量
D. 验证质量守恒定律
【答案】C
11、推理是学习化学的一种重要方法,以下推理正确的是( )
A.化学变化伴随着能量变化,所以有能量变化的一定是化学变化
B.蜡烛在空气中燃烧后质量减轻,所以不符合质量守恒定律
C.同种元素有相同的核电荷数,所以核电荷数相同的微粒一定属于同种元素
D.化合物由多种元素组成,因此由多种元素组成的纯净物一定是化合物
【答案】D
12、下列现象能用质量守恒定律解释的是
A.蜡烛燃烧时慢慢变短
B.10 g食盐完全溶解于90g水中,得到100g食盐水
C.打开酒精的瓶盖一段时间,酒精质量变小
D.2体积的氢气加压后变成1体积
【答案】A
13、二氧化碳和氢气可在一定条件下反应,生产一种重要的化工原料甲醇,化学方程式为。下列有关该反应的说法错误的是( )
A.为 CO2的利用创造了一种新途径
B.属于化合反应
C.反应前后分子数发生了改变
D.钌-膦络合物的质量在反应前后没有改变
【答案】B
14、加热15.8g高锰酸钾,当产生1.6g氧气时,固体剩余物的成分是( )
A.K2MnO4和MnO2 B.KMnO4、K2MnO4和MnO2
C.KMnO4和MnO2 D.KMnO4和K2MnO4
【答案】A
15、某同学用下图所示装置探究可燃物燃烧的条件,得到以下实验事实:①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧。能证明可燃物必须达到一定温度(着火点)才能燃烧的实验事实是( )
A. ①② B. ②④ C. ①④ D. ③④
【答案】B
16、将一定量的木炭和过量的氧气放在密闭的容器里加热,充分反应。如图能够正确反映容器内有关物质量随反应时间变化关系的是( )
【答案】B
二、填空题。
17、如图所示是某化学反应前后的微观示意图,依图回答下列问题。
(1)参加反应的反应物的粒子个数比为 。
(2)该化学反应前后没有发生改变的粒子是 (填“分子”或“原子”)。
(3)该反应的基本反应类型为 。
(4)从微观示意图中,能得出哪些结论: 。(写一点)。
【答案】(1)1∶1 (2)原子 (3)化合反应
(4)在化学反应中,分子可分,原子不可再分(合理即可)
18、空气是一种重要的资源。
(1)下列属于空气污染物的是________(填字母)。
A 臭氧 B 二氧化氮C PM2.5D PM10
(2)氢气是清洁能源,写出氢气燃烧的化学方程式_____________________。
(3)食品包装中充氮气可以防腐,是由于氮气_____________________。
(4)同温同压下,气体的体积比等于分子个数比。若空气中其他成分忽略不计,如图可表示空气微观模型的是________(填字母)。
【答案】ABCD 2H2 + O22H2O 化学性质不活泼 C
19、根据下列装置图,回答有关问题。
(1)写出装置图中标号仪器的名称。a_______;b_______。
(2)实验室用过氧化氢溶液制取氧气可选择的发生装置是___ (填字母),此反应的化学方程式__ 。
(3)若使用高锰酸钾制取氧气,可选用的装置组合是_____(填字母)。
(4)选用D装置收集氧气的原因是_____ 。
(5)加热15.8g高锰酸钾,完全反应后,理论上可以得到____氧气?
【答案】(1)试管 集气瓶 B (2)
(3)AC或AD (4)氧气不易溶于水 (5)1.6g
20、化学与生产、生活有着密切的联系,请用所学的化学知识回答下列问题:
(1)“共享单车”已走进城市的大街小巷,符合“低碳出行”理念,“低碳”指的是较低的 气体排放,“共享单车”采用铝合金作支架,铝合金属于 (填“纯净物”或“混合物”)。
(2)运动员剧烈运动后感到肌肉酸痛,放松一段时间后慢慢消失的原因是血液中的乳酸(C3H6O3)与吸入的氧气反应:C3H6O3+3O2=3CO2+3R,则R的化学式为 ,新能源公交车环保,节能,大大方便了市民的出行,氢能是未来最理想的能源,从环保角度分析,氢能最突出的优点是 。氢氧燃料电池是一种将 能转化为 能的装置。
【答案】二氧化碳;混合物;H2O;不污染环境;化学;电
21、写出符合要求的化学方程式:
(1)铁在氧气中燃烧: ;
(2)加热高锰酸钾固体制氧气: ;
(3)电解水的方程式: 。
【答案】(1)3Fe+2O2Fe3O4;
(2)2KMnO4K2MnO4+MnO2+O2↑;
(3)2H2O2H2↑+O2↑。
三、综合应用题。
22、质量守恒定律是一条重要规律。请利用该规律的相关知识回答下列问题。
(1)蜡烛在空气中燃烧时生成二氧化碳和水。由此判断蜡烛中一定含有的元素是________(填元素符号),判断的依据是________ (用微粒的观点解释)。
(2)某同学取一根洁净的铜丝,称量其质量为m1 g,将此铜丝加热(提示:生成氧化铜)并冷却后再次称量,其质量为m2g,则m1________m2(填“>”、“<”或“=”),产生这一结果的原因是________ 。
(3)在密闭容器中放入X、Y、Z、W四种物质并使其发生反应,测得有关数据如下表。关于此反应的认识正确的是________(填字母序号)。
物质 X Y Z W
反应前的质量(g) 2 1 16 16
一段时间后的质量(g) 17 m 6 11
A.m=1
B.该反应为分解反应
C.X与Z的化学计量数之比是3:2
D.若该反应充分进行,反应后W仍有剩余
【答案】(1)C、H ;反应前后原子的种类不变
(2)< ;m1中没有包含参加反应的氧气的质量 (3)A D
四、实验题。
23、如图是初中化学中的一些重要实验。
(1)图1实验中,能证明可燃物燃烧跟温度有关的实验现象是:
。
(2)通过图2中A、B对比说明燃烧需要的条件是 。
(3)切割白磷时,应在水下进行。其原因是 。
【答案】(1)铜片上的白磷燃烧,红磷不燃烧;
(2)燃烧需要氧气(或空气);
(3)防止在空气中切割时白磷自燃。
五、计算题。
24、化学兴趣小组的同学们要测定某过氧化氢溶液的溶质质量分数。他们称取50.0 g过氧化氢溶液放入盛有2.0 g二氧化锰的烧杯(烧杯质量为76.0 g)中。待完全反应后,称量反应后物质连同烧杯的质量为126.4 g(氧气逸出带出的水分忽略不计)。请计算回答。
(1)反应后产生氧气的质量是 g。
(2)该过氧化氢溶液的溶质质量分数是多少 (写出计算过程)
【答案】(1)1.6
(2)解:设生成1.6 g氧气需要过氧化氢的质量为x。
2H2O2 2H2+O2↑
68 32
x 1.6 g
= 解得x=3.4 g
该过氧化氢溶液的溶质质量分数为×100%=6.8%
答:该过氧化氢溶液的溶质质量分数为6.8%。
鲁教版第五单元 定量研究化学反应
一、选择题。(16题)
1、在化学方程式:C2H8N2 + 2N2O4 = 3X + 2CO2 + 4H2O中,X 的化学式为( )
A. N2 B. H2 C. O2 D. CO
2、植物光合作用可表示为CO2+H2O 淀粉+O2,下列有关说法中正确的是( )
A.淀粉中一定含有C、H两种元素
B.淀粉中一定只含有C、H两种元素
C.淀粉中可能有三种以上的元素
D.淀粉可能是一种单质或一种化合物
3、现取2.3g某有机物在空气中完全燃烧,生成4.4g二氧化碳和2.7g水。对该物质的组成有下列推断:①一定含碳氢元素 ②一定不含氧元素 ③可能含氧元素 ④一定含氧元素 ⑤分子中C、H的原子个数比为2∶5 ⑥分子中C、H、O的元素质量比为12∶3∶8。其中正确的是( )
A.①③⑤ B.①④⑥ C.①②⑤ D.①④⑤
4、在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7:8,当2.8gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )
A.9.6g B.8.8g C.6.8g D.4.4g
5、阻燃剂氢氧化铝受热分解时吸收热量,同时生成耐高温的氧化铝和水蒸气,起到防火作用.下列关于该阻燃剂防火原因的叙述中错误的是( )
A. 反应吸热,降低了可燃物的着火点
B. 生成氧化铝覆盖在可燃物表面,隔绝空气
C. 生成大量水蒸气,降低可燃物周围氧气浓度
D. 反应能够降低温度,可燃物不易达到着火点
6、科学研究发现,在一定条件下,甲、乙两种气体混合发生反应(微观示意图如图)。该反应产物无污染可用于汽车尾气处理。下列说法正确的是( )
A.甲、乙两种反应物的分子个数比为2:3
B.甲物质的化学式是NH3,其中氮元素的化合价为+3价
C.在反应前后,原子的种类没有改变,原子数目发生了变化
D.四种物质中属于氧化物是乙和丁,乙、丁在反应中的质量比为15:18
7、某纯净物稍微加热就能分解为NH3、CO2、H2O三种物质,据此不能得出的结论是( )
A.该物质是化合物 B.该物质中含有水
C.该物质不稳定 D.该物质由四种元素组成
8、Sb2O5是一种重要的阻燃剂,工业制取该物质的化学方程式为:Sb2O3+2X=Sb2O5+2H2O则X的化学式为( )
A.H2 B.O2 C.H2O2 D.H3SbO4
9、相同质量的下列物质,在氧气中完全燃烧,消耗氧气最多的是( )
A.H2 B.P C.S D.C
10、如图所示是某兴趣小组设计的四个实验装置,其中实验能够成功的是( )
A. 稀释浓硫酸
B. 探究燃烧的三个条件
C. 测定空气中氧气的含量
D. 验证质量守恒定律
11、推理是学习化学的一种重要方法,以下推理正确的是( )
A.化学变化伴随着能量变化,所以有能量变化的一定是化学变化
B.蜡烛在空气中燃烧后质量减轻,所以不符合质量守恒定律
C.同种元素有相同的核电荷数,所以核电荷数相同的微粒一定属于同种元素
D.化合物由多种元素组成,因此由多种元素组成的纯净物一定是化合物
12、下列现象能用质量守恒定律解释的是
A.蜡烛燃烧时慢慢变短
B.10 g食盐完全溶解于90g水中,得到100g食盐水
C.打开酒精的瓶盖一段时间,酒精质量变小
D.2体积的氢气加压后变成1体积
13、二氧化碳和氢气可在一定条件下反应,生产一种重要的化工原料甲醇,化学方程式为。下列有关该反应的说法错误的是( )
A.为 CO2的利用创造了一种新途径
B.属于化合反应
C.反应前后分子数发生了改变
D.钌-膦络合物的质量在反应前后没有改变
14、加热15.8g高锰酸钾,当产生1.6g氧气时,固体剩余物的成分是( )
A.K2MnO4和MnO2 B.KMnO4、K2MnO4和MnO2
C.KMnO4和MnO2 D.KMnO4和K2MnO4
15、某同学用下图所示装置探究可燃物燃烧的条件,得到以下实验事实:①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧。能证明可燃物必须达到一定温度(着火点)才能燃烧的实验事实是( )
A. ①② B. ②④ C. ①④ D. ③④
16、将一定量的木炭和过量的氧气放在密闭的容器里加热,充分反应。如图能够正确反映容器内有关物质量随反应时间变化关系的是( )
二、填空题。
17、如图所示是某化学反应前后的微观示意图,依图回答下列问题。
(1)参加反应的反应物的粒子个数比为 。
(2)该化学反应前后没有发生改变的粒子是 (填“分子”或“原子”)。
(3)该反应的基本反应类型为 。
(4)从微观示意图中,能得出哪些结论: 。(写一点)。
18、空气是一种重要的资源。
(1)下列属于空气污染物的是________(填字母)。
A 臭氧 B 二氧化氮C PM2.5D PM10
(2)氢气是清洁能源,写出氢气燃烧的化学方程式_____________________。
(3)食品包装中充氮气可以防腐,是由于氮气_____________________。
(4)同温同压下,气体的体积比等于分子个数比。若空气中其他成分忽略不计,如图可表示空气微观模型的是________(填字母)。
19、根据下列装置图,回答有关问题。
(1)写出装置图中标号仪器的名称。a_______;b_______。
(2)实验室用过氧化氢溶液制取氧气可选择的发生装置是___ (填字母),此反应的化学方程式__ 。
(3)若使用高锰酸钾制取氧气,可选用的装置组合是_____(填字母)。
(4)选用D装置收集氧气的原因是_____ 。
(5)加热15.8g高锰酸钾,完全反应后,理论上可以得到____氧气?
20、化学与生产、生活有着密切的联系,请用所学的化学知识回答下列问题:
(1)“共享单车”已走进城市的大街小巷,符合“低碳出行”理念,“低碳”指的是较低的 气体排放,“共享单车”采用铝合金作支架,铝合金属于 (填“纯净物”或“混合物”)。
(2)运动员剧烈运动后感到肌肉酸痛,放松一段时间后慢慢消失的原因是血液中的乳酸(C3H6O3)与吸入的氧气反应:C3H6O3+3O2=3CO2+3R,则R的化学式为 ,新能源公交车环保,节能,大大方便了市民的出行,氢能是未来最理想的能源,从环保角度分析,氢能最突出的优点是 。氢氧燃料电池是一种将 能转化为 能的装置。
21、写出符合要求的化学方程式:
(1)铁在氧气中燃烧: ;
(2)加热高锰酸钾固体制氧气: ;
(3)电解水的方程式: 。
三、综合应用题。
22、质量守恒定律是一条重要规律。请利用该规律的相关知识回答下列问题。
(1)蜡烛在空气中燃烧时生成二氧化碳和水。由此判断蜡烛中一定含有的元素是________(填元素符号),判断的依据是________ (用微粒的观点解释)。
(2)某同学取一根洁净的铜丝,称量其质量为m1 g,将此铜丝加热(提示:生成氧化铜)并冷却后再次称量,其质量为m2g,则m1________m2(填“>”、“<”或“=”),产生这一结果的原因是________ 。
(3)在密闭容器中放入X、Y、Z、W四种物质并使其发生反应,测得有关数据如下表。关于此反应的认识正确的是________(填字母序号)。
物质 X Y Z W
反应前的质量(g) 2 1 16 16
一段时间后的质量(g) 17 m 6 11
A.m=1
B.该反应为分解反应
C.X与Z的化学计量数之比是3:2
D.若该反应充分进行,反应后W仍有剩余
四、实验题。
23、如图是初中化学中的一些重要实验。
(1)图1实验中,能证明可燃物燃烧跟温度有关的实验现象是:
。
(2)通过图2中A、B对比说明燃烧需要的条件是 。
(3)切割白磷时,应在水下进行。其原因是 。
五、计算题。
24、化学兴趣小组的同学们要测定某过氧化氢溶液的溶质质量分数。他们称取50.0 g过氧化氢溶液放入盛有2.0 g二氧化锰的烧杯(烧杯质量为76.0 g)中。待完全反应后,称量反应后物质连同烧杯的质量为126.4 g(氧气逸出带出的水分忽略不计)。请计算回答。
(1)反应后产生氧气的质量是 g。
(2)该过氧化氢溶液的溶质质量分数是多少 (写出计算过程)
2023—2024学年鲁教版化学九年级上册第五单元 定量研究化学反应 期末评估题(含答案)
鲁教版第五单元 定量研究化学反应
一、选择题。(16题)
1、在化学方程式:C2H8N2 + 2N2O4 = 3X + 2CO2 + 4H2O中,X 的化学式为( )
A. N2 B. H2 C. O2 D. CO
【答案】A
2、植物光合作用可表示为CO2+H2O 淀粉+O2,下列有关说法中正确的是( )
A.淀粉中一定含有C、H两种元素
B.淀粉中一定只含有C、H两种元素
C.淀粉中可能有三种以上的元素
D.淀粉可能是一种单质或一种化合物
【答案】A
3、现取2.3g某有机物在空气中完全燃烧,生成4.4g二氧化碳和2.7g水。对该物质的组成有下列推断:①一定含碳氢元素 ②一定不含氧元素 ③可能含氧元素 ④一定含氧元素 ⑤分子中C、H的原子个数比为2∶5 ⑥分子中C、H、O的元素质量比为12∶3∶8。其中正确的是( )
A.①③⑤ B.①④⑥ C.①②⑤ D.①④⑤
【答案】B
4、在反应A+3B=2C+3D中,已知A和B的相对分子质量之比为7:8,当2.8gA与一定量B恰好完全反应后,生成3.6gD,则C的质量为( )
A.9.6g B.8.8g C.6.8g D.4.4g
【答案】B
5、阻燃剂氢氧化铝受热分解时吸收热量,同时生成耐高温的氧化铝和水蒸气,起到防火作用.下列关于该阻燃剂防火原因的叙述中错误的是( )
A. 反应吸热,降低了可燃物的着火点
B. 生成氧化铝覆盖在可燃物表面,隔绝空气
C. 生成大量水蒸气,降低可燃物周围氧气浓度
D. 反应能够降低温度,可燃物不易达到着火点
【答案】A
6、科学研究发现,在一定条件下,甲、乙两种气体混合发生反应(微观示意图如图)。该反应产物无污染可用于汽车尾气处理。下列说法正确的是( )
A.甲、乙两种反应物的分子个数比为2:3
B.甲物质的化学式是NH3,其中氮元素的化合价为+3价
C.在反应前后,原子的种类没有改变,原子数目发生了变化
D.四种物质中属于氧化物是乙和丁,乙、丁在反应中的质量比为15:18
【答案】A
7、某纯净物稍微加热就能分解为NH3、CO2、H2O三种物质,据此不能得出的结论是( )
A.该物质是化合物 B.该物质中含有水
C.该物质不稳定 D.该物质由四种元素组成
【答案】B
8、Sb2O5是一种重要的阻燃剂,工业制取该物质的化学方程式为:Sb2O3+2X=Sb2O5+2H2O则X的化学式为( )
A.H2 B.O2 C.H2O2 D.H3SbO4
【答案】C
9、相同质量的下列物质,在氧气中完全燃烧,消耗氧气最多的是( )
A.H2 B.P C.S D.C
【答案】A
10、如图所示是某兴趣小组设计的四个实验装置,其中实验能够成功的是( )
A. 稀释浓硫酸
B. 探究燃烧的三个条件
C. 测定空气中氧气的含量
D. 验证质量守恒定律
【答案】C
11、推理是学习化学的一种重要方法,以下推理正确的是( )
A.化学变化伴随着能量变化,所以有能量变化的一定是化学变化
B.蜡烛在空气中燃烧后质量减轻,所以不符合质量守恒定律
C.同种元素有相同的核电荷数,所以核电荷数相同的微粒一定属于同种元素
D.化合物由多种元素组成,因此由多种元素组成的纯净物一定是化合物
【答案】D
12、下列现象能用质量守恒定律解释的是
A.蜡烛燃烧时慢慢变短
B.10 g食盐完全溶解于90g水中,得到100g食盐水
C.打开酒精的瓶盖一段时间,酒精质量变小
D.2体积的氢气加压后变成1体积
【答案】A
13、二氧化碳和氢气可在一定条件下反应,生产一种重要的化工原料甲醇,化学方程式为。下列有关该反应的说法错误的是( )
A.为 CO2的利用创造了一种新途径
B.属于化合反应
C.反应前后分子数发生了改变
D.钌-膦络合物的质量在反应前后没有改变
【答案】B
14、加热15.8g高锰酸钾,当产生1.6g氧气时,固体剩余物的成分是( )
A.K2MnO4和MnO2 B.KMnO4、K2MnO4和MnO2
C.KMnO4和MnO2 D.KMnO4和K2MnO4
【答案】A
15、某同学用下图所示装置探究可燃物燃烧的条件,得到以下实验事实:①不通空气时,冷水中的白磷不燃烧;②通空气时,冷水中的白磷不燃烧;③不通空气时,热水中的白磷不燃烧;④通空气时,热水中的白磷燃烧。能证明可燃物必须达到一定温度(着火点)才能燃烧的实验事实是( )
A. ①② B. ②④ C. ①④ D. ③④
【答案】B
16、将一定量的木炭和过量的氧气放在密闭的容器里加热,充分反应。如图能够正确反映容器内有关物质量随反应时间变化关系的是( )
【答案】B
二、填空题。
17、如图所示是某化学反应前后的微观示意图,依图回答下列问题。
(1)参加反应的反应物的粒子个数比为 。
(2)该化学反应前后没有发生改变的粒子是 (填“分子”或“原子”)。
(3)该反应的基本反应类型为 。
(4)从微观示意图中,能得出哪些结论: 。(写一点)。
【答案】(1)1∶1 (2)原子 (3)化合反应
(4)在化学反应中,分子可分,原子不可再分(合理即可)
18、空气是一种重要的资源。
(1)下列属于空气污染物的是________(填字母)。
A 臭氧 B 二氧化氮C PM2.5D PM10
(2)氢气是清洁能源,写出氢气燃烧的化学方程式_____________________。
(3)食品包装中充氮气可以防腐,是由于氮气_____________________。
(4)同温同压下,气体的体积比等于分子个数比。若空气中其他成分忽略不计,如图可表示空气微观模型的是________(填字母)。
【答案】ABCD 2H2 + O22H2O 化学性质不活泼 C
19、根据下列装置图,回答有关问题。
(1)写出装置图中标号仪器的名称。a_______;b_______。
(2)实验室用过氧化氢溶液制取氧气可选择的发生装置是___ (填字母),此反应的化学方程式__ 。
(3)若使用高锰酸钾制取氧气,可选用的装置组合是_____(填字母)。
(4)选用D装置收集氧气的原因是_____ 。
(5)加热15.8g高锰酸钾,完全反应后,理论上可以得到____氧气?
【答案】(1)试管 集气瓶 B (2)
(3)AC或AD (4)氧气不易溶于水 (5)1.6g
20、化学与生产、生活有着密切的联系,请用所学的化学知识回答下列问题:
(1)“共享单车”已走进城市的大街小巷,符合“低碳出行”理念,“低碳”指的是较低的 气体排放,“共享单车”采用铝合金作支架,铝合金属于 (填“纯净物”或“混合物”)。
(2)运动员剧烈运动后感到肌肉酸痛,放松一段时间后慢慢消失的原因是血液中的乳酸(C3H6O3)与吸入的氧气反应:C3H6O3+3O2=3CO2+3R,则R的化学式为 ,新能源公交车环保,节能,大大方便了市民的出行,氢能是未来最理想的能源,从环保角度分析,氢能最突出的优点是 。氢氧燃料电池是一种将 能转化为 能的装置。
【答案】二氧化碳;混合物;H2O;不污染环境;化学;电
21、写出符合要求的化学方程式:
(1)铁在氧气中燃烧: ;
(2)加热高锰酸钾固体制氧气: ;
(3)电解水的方程式: 。
【答案】(1)3Fe+2O2Fe3O4;
(2)2KMnO4K2MnO4+MnO2+O2↑;
(3)2H2O2H2↑+O2↑。
三、综合应用题。
22、质量守恒定律是一条重要规律。请利用该规律的相关知识回答下列问题。
(1)蜡烛在空气中燃烧时生成二氧化碳和水。由此判断蜡烛中一定含有的元素是________(填元素符号),判断的依据是________ (用微粒的观点解释)。
(2)某同学取一根洁净的铜丝,称量其质量为m1 g,将此铜丝加热(提示:生成氧化铜)并冷却后再次称量,其质量为m2g,则m1________m2(填“>”、“<”或“=”),产生这一结果的原因是________ 。
(3)在密闭容器中放入X、Y、Z、W四种物质并使其发生反应,测得有关数据如下表。关于此反应的认识正确的是________(填字母序号)。
物质 X Y Z W
反应前的质量(g) 2 1 16 16
一段时间后的质量(g) 17 m 6 11
A.m=1
B.该反应为分解反应
C.X与Z的化学计量数之比是3:2
D.若该反应充分进行,反应后W仍有剩余
【答案】(1)C、H ;反应前后原子的种类不变
(2)< ;m1中没有包含参加反应的氧气的质量 (3)A D
四、实验题。
23、如图是初中化学中的一些重要实验。
(1)图1实验中,能证明可燃物燃烧跟温度有关的实验现象是:
。
(2)通过图2中A、B对比说明燃烧需要的条件是 。
(3)切割白磷时,应在水下进行。其原因是 。
【答案】(1)铜片上的白磷燃烧,红磷不燃烧;
(2)燃烧需要氧气(或空气);
(3)防止在空气中切割时白磷自燃。
五、计算题。
24、化学兴趣小组的同学们要测定某过氧化氢溶液的溶质质量分数。他们称取50.0 g过氧化氢溶液放入盛有2.0 g二氧化锰的烧杯(烧杯质量为76.0 g)中。待完全反应后,称量反应后物质连同烧杯的质量为126.4 g(氧气逸出带出的水分忽略不计)。请计算回答。
(1)反应后产生氧气的质量是 g。
(2)该过氧化氢溶液的溶质质量分数是多少 (写出计算过程)
【答案】(1)1.6
(2)解:设生成1.6 g氧气需要过氧化氢的质量为x。
2H2O2 2H2+O2↑
68 32
x 1.6 g
= 解得x=3.4 g
该过氧化氢溶液的溶质质量分数为×100%=6.8%
答:该过氧化氢溶液的溶质质量分数为6.8%。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
