天津市滨海新区田家炳中学2023-2024学年高三上学期期中考试化学试题(含答案)
文档属性
| 名称 | 天津市滨海新区田家炳中学2023-2024学年高三上学期期中考试化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 573.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-08 23:29:29 | ||
图片预览



文档简介
滨海新区田家炳中学2023-2024-1高三年级期中考试
化学试卷
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分,考试时间60分钟。考试结束后,上交答题卡。
以下数据可供解题时参考:
相对原子质量:H∶1 N∶14 C∶12 O∶16 Na∶23 Cl∶35.5 Fe∶56
第Ⅰ卷(选择题,共36分)
一、选择题(本题共18个小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符合题目要求的。)
1.下列说法不正确的是( )
A.硅酸钠是一种难溶于水的硅酸盐 B.镁在空气中燃烧可生成氧化镁和氮化镁
C.钠与水反应生成氢氧化钠和氢气 D.常温下,铝遇浓硝酸或浓硫酸时会发生钝化
2.化学与生活密切相关。下列叙述正确的是( )
A.漂白粉与盐酸可混合使用以提高消毒效果 B.温室气体是形成酸雨的主要物质
C.棉花、麻和蚕丝均为碳水化合物 D.干冰可用在舞台上制造“云雾”
3.下列有关物质的性质与用途不具有对应关系的是( )
A.铁粉能与反应,可用作食品保存的吸氧剂
B.纳米能与酸反应,可用作铁磁性材料
C.具有氧化性,可用于腐蚀印刷电路板上的Cu
D.聚合硫酸铁能水解并形成胶休,可用于净水
4.氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然固氮、人工固氮都是将转化为
B.侯氏制碱法以、、、NaCl为原料制备和
C.工业上通过催化氧化等反应过程生产
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
5.下列有关物质性质及应用的说法正确的是( )
A.过量的铜与浓硝酸反应可生成NO
B.Fe在中的燃烧产物可用于制红色涂料
C.Li在空气中燃烧生成
D.、都能使酸性高锰酸钾溶液褪色,前者表现出还原性,后者表现出漂白性
6.在火星上工作的美国“勇气号”“机遇号”探测车的一个重要任务就是收集有关及其硫酸盐的信息,用以证明火星上存在或曾经存在过水。以下叙述正确的是( )
A.与互为同素异形体
B.制备Al用电解法,制备Fe、Cu可用还原法
C.将通入溶液中至饱和,有沉淀产生
D.检验从火星上带回来的红色物质是否是的操作步骤:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液
7.实验室用和浓盐酸反应生成后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
A. B.
C. D.
8.宏观辨识与微观探析是化学学科核心素养之一。下列物质实验对应的反应方程式书写正确的是( )
A.放入水中:
B.水蒸气通过灼热铁粉:
C.铜丝插入热的浓硫酸中:
D.实验室用铜与浓硝酸制二氧化氮:
9.下列各组离子在给定溶液中能大量共存的是( )
A.在0.1氨水中:、、、
B.在0.1氯化钠溶液中:、、、
C.在0.1醋酸溶液中:、、、
D.在0.1硝酸银溶液中:、、、
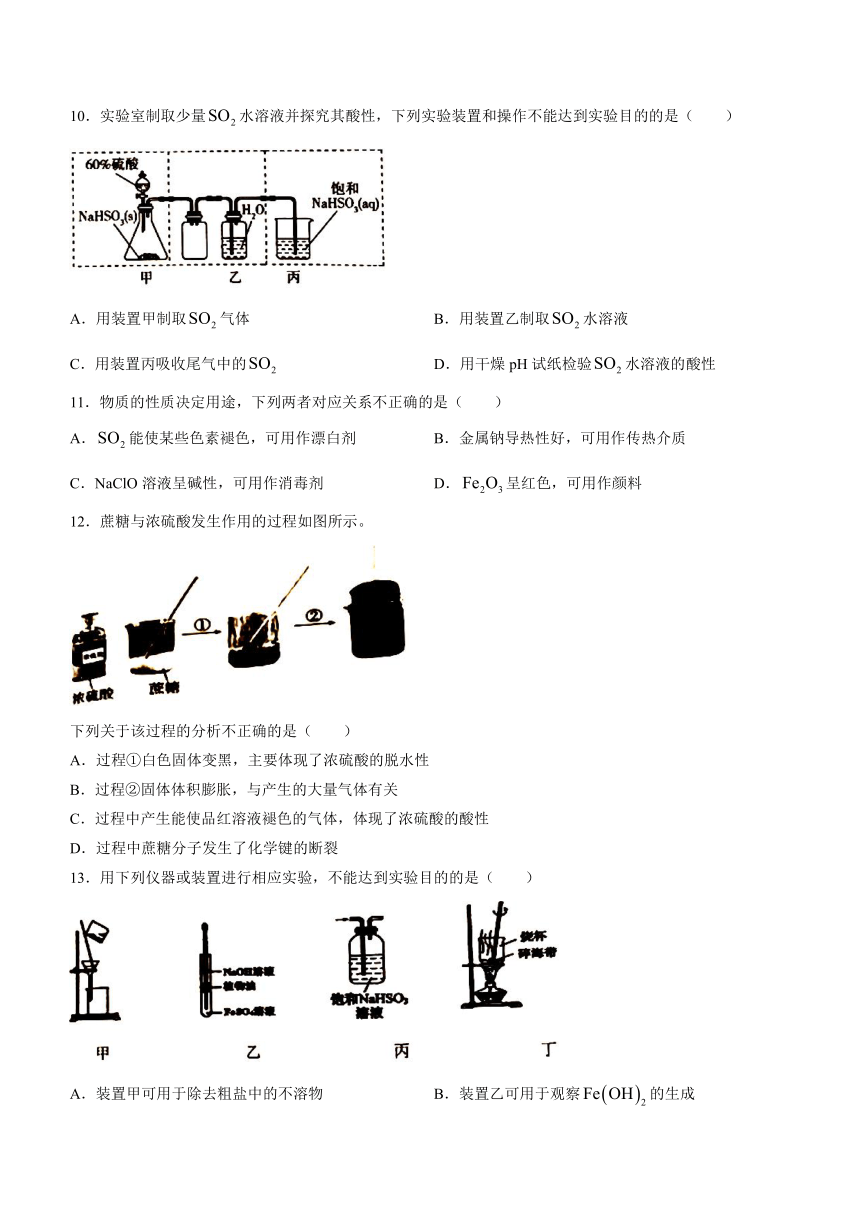
10.实验室制取少量水溶液并探究其酸性,下列实验装置和操作不能达到实验目的的是( )
A.用装置甲制取气体 B.用装置乙制取水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验水溶液的酸性
11.物质的性质决定用途,下列两者对应关系不正确的是( )
A.能使某些色素褪色,可用作漂白剂 B.金属钠导热性好,可用作传热介质
C.NaClO溶液呈碱性,可用作消毒剂 D.呈红色,可用作颜料
12.蔗糖与浓硫酸发生作用的过程如图所示。
下列关于该过程的分析不正确的是( )
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂
13.用下列仪器或装置进行相应实验,不能达到实验目的的是( )
A.装置甲可用于除去粗盐中的不溶物 B.装置乙可用于观察的生成
C.装置丙可用于除去中的HCl D.装置丁可用于灼烧碎海带
14.下列离子方程式书写正确的是( )
A.溶于氢碘酸:
B.溶液中加入氨水:
C.漂白粉溶液除废气中的:
D.Al粉溶于过量NaOH溶液:
15.氯化铁是一种重要的盐,下列说法不正确的是( )
A.氯化铁属于弱电解质 B.氯化铁溶液能导电
C.氯化铁可由铁与氯气反应制得 D.氯化铁溶液可制备氢氧化铁胶体
16.物质的性质决定用途,下列两者对应关系不正确的是( )
A.过氧化钠能与二氧化碳反应生成氧气,可作潜水艇中的供氧剂
B.氧化钙易吸水,可用作干燥剂
C.维生素C具有还原性,可用作食品抗氧化剂
D.铝有强还原性,可用于制作门窗框架
17.为阿伏加德罗常数的值,下列说法错误的是( )
A.1.4g CO和的混合气体中原子数目为0.1
B.100mL 12mol/L的浓盐酸与足量反应生成的分子数为0.3
C.相同条件下,23g Na和78g 分别与足量水反应生成的气体体积相同
D.100g质量分数为46%的乙醇溶液中含有氢原子数为12
18.合成氨及氨氧化制硝酸的流程如图所示,下列说法错误的是( )
A.从氨分离器中分离出氨,主要利用了其易液化的性质
B.氧化炉中发生反应的化学方程式为
C.向吸收塔中通入空气的主要作用是提高氮元素的利用率
D.酸雨和光化学烟雾的形成均与氮氧化物有关
第Ⅱ卷(非选择题,共46分)
二、非选择题
19.(14分)
物质集合M中含有常见物质、、Al、、Fe、、Na,这些物质按照以下方法进行分类后如图所示,请按照要求回答问题。
(1)B组物质中属于非电解质的物质为 ,其中水溶液显碱性的原因用方程式表示为
。
(2)C组物质中能与冷水反应生成还原性气体的化学方程式为 。
(3)D组物质的共同点是常温下在 中会发生钝化。
(4)请写D组中能与氢氧化钠溶液反应的离子方程式 。
(5)请写出F组中的酸性氧化物与硫化氢反应的化学方程式: 。
(6)将E组中的两种物质混合,混合物中金属原子与氧原子的物质的量之比为3∶4,这两种物质的物质的量之比 ∶ = ∶ (等号前填写物质的化学式,等号后填数字)
20.(16分)
氮及其化合物在工农业生产和生活中有着重要作用。有资料显示过量的氨气和氯气在常温下可合成(岩脑砂的主要成分),某实验小组对该反应进行探究,并对岩脑砂进行元素测定,回答下列问题:
(1)的制备:
①利用装置B制取实验所需的氯气,写出该反应的化学方程式 。
②装置C的名称为 。
③为了使氨气和氯气在D中充分混合(提示:氨气从e口进,氯气从f口进,二者形成逆向流动,更有利于两者的充分混合),请确定上述装置的合理连接顺序:
→ → →ef←h←g← ← ← (用小写字母和箭头表示,箭头方向与气流方向一致)。
④该实验装置除了D处导管易堵塞外,还存在的不足之处是 。
⑤验证岩脑砂中所含的操作为
。
(2)岩脑砂中元素的定量测定:准确称取a g岩脑砂,与足量的氧化铜混合加热,发生的反应为,利用下列装置测定岩脑砂中氮元素和氯元素的质量之比(夹持装置省略)。
①装置H中盛装的试剂是 (填试剂名称)。
②已知装置J中也装有碱石灰,其目的是 。
③若装置I增重b g,利用装置K测得气体体积为V L(已知常温常压下气体摩尔体积为24.5),则岩脑砂中 (用含b、V的代数式表示,不必化简)。
21.(16分)
无水常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和杂质)为原料制备无水(s)。
已知:氯化亚砜()熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和 。
(2)为避免引入新的杂质,试剂B可以选用 (填编号)。
A.溶液 B.水 C.水 D.溶液
(3)操作②是蒸发结晶,加热的同时通入HCl(g)的目的是 。
(4)取少量D晶体,溶于水并滴加KSCN溶液,现象是 。
(5)反应D→E的化学方程式为 。
(6)由D转化成E的过程中可能产生少量亚铁盐,写出一种可能的还原剂 ,并设计实验验证是该还原剂将还原的 。
参考答案
1-18
ADBAA/BDDCC/CCDAA/DBB
答案:
19.每个空2分,共14分
(1)①.、 ②.
(2)
(3)浓硝酸或浓硫酸
(4)
(5)
(6)
20.(16分)均为2分。
(1)①M
②(球形)干燥管
③a→d→c、j←i←b(顿号前后各一分,共2分)
④无尾气处理装置
⑤取少量岩脑砂于试管中,加少量蒸馏水溶解,再加入适量浓NaOH溶液并加热,若产生使湿润的红色石蕊试纸变蓝的气体,则含有。
(2)①浓硫酸
②防止装置K中的水蒸气进入装置I,影响实验结果
③
21.每个空2分,共16分
(1)漏斗
(2)BD
(3)防止水解
(4)溶液变为血红色
(5)
(6)
先加盐酸酸化,再加溶液,产生白色沉淀,则是将还原
化学试卷
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分,共100分,考试时间60分钟。考试结束后,上交答题卡。
以下数据可供解题时参考:
相对原子质量:H∶1 N∶14 C∶12 O∶16 Na∶23 Cl∶35.5 Fe∶56
第Ⅰ卷(选择题,共36分)
一、选择题(本题共18个小题,每小题3分,共54分。在每小题给出的四个选项中,只有一项是符合题目要求的。)
1.下列说法不正确的是( )
A.硅酸钠是一种难溶于水的硅酸盐 B.镁在空气中燃烧可生成氧化镁和氮化镁
C.钠与水反应生成氢氧化钠和氢气 D.常温下,铝遇浓硝酸或浓硫酸时会发生钝化
2.化学与生活密切相关。下列叙述正确的是( )
A.漂白粉与盐酸可混合使用以提高消毒效果 B.温室气体是形成酸雨的主要物质
C.棉花、麻和蚕丝均为碳水化合物 D.干冰可用在舞台上制造“云雾”
3.下列有关物质的性质与用途不具有对应关系的是( )
A.铁粉能与反应,可用作食品保存的吸氧剂
B.纳米能与酸反应,可用作铁磁性材料
C.具有氧化性,可用于腐蚀印刷电路板上的Cu
D.聚合硫酸铁能水解并形成胶休,可用于净水
4.氮及其化合物的转化具有重要应用。下列说法不正确的是( )
A.自然固氮、人工固氮都是将转化为
B.侯氏制碱法以、、、NaCl为原料制备和
C.工业上通过催化氧化等反应过程生产
D.多种形态的氮及其化合物间的转化形成了自然界的“氮循环”
5.下列有关物质性质及应用的说法正确的是( )
A.过量的铜与浓硝酸反应可生成NO
B.Fe在中的燃烧产物可用于制红色涂料
C.Li在空气中燃烧生成
D.、都能使酸性高锰酸钾溶液褪色,前者表现出还原性,后者表现出漂白性
6.在火星上工作的美国“勇气号”“机遇号”探测车的一个重要任务就是收集有关及其硫酸盐的信息,用以证明火星上存在或曾经存在过水。以下叙述正确的是( )
A.与互为同素异形体
B.制备Al用电解法,制备Fe、Cu可用还原法
C.将通入溶液中至饱和,有沉淀产生
D.检验从火星上带回来的红色物质是否是的操作步骤:样品→粉碎→加水溶解→过滤→向滤液中滴加KSCN溶液
7.实验室用和浓盐酸反应生成后,按照净化、收集、性质检验及尾气处理的顺序进行实验。下列装置(“→”表示气流方向)不能达到实验目的的是( )
A. B.
C. D.
8.宏观辨识与微观探析是化学学科核心素养之一。下列物质实验对应的反应方程式书写正确的是( )
A.放入水中:
B.水蒸气通过灼热铁粉:
C.铜丝插入热的浓硫酸中:
D.实验室用铜与浓硝酸制二氧化氮:
9.下列各组离子在给定溶液中能大量共存的是( )
A.在0.1氨水中:、、、
B.在0.1氯化钠溶液中:、、、
C.在0.1醋酸溶液中:、、、
D.在0.1硝酸银溶液中:、、、
10.实验室制取少量水溶液并探究其酸性,下列实验装置和操作不能达到实验目的的是( )
A.用装置甲制取气体 B.用装置乙制取水溶液
C.用装置丙吸收尾气中的 D.用干燥pH试纸检验水溶液的酸性
11.物质的性质决定用途,下列两者对应关系不正确的是( )
A.能使某些色素褪色,可用作漂白剂 B.金属钠导热性好,可用作传热介质
C.NaClO溶液呈碱性,可用作消毒剂 D.呈红色,可用作颜料
12.蔗糖与浓硫酸发生作用的过程如图所示。
下列关于该过程的分析不正确的是( )
A.过程①白色固体变黑,主要体现了浓硫酸的脱水性
B.过程②固体体积膨胀,与产生的大量气体有关
C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性
D.过程中蔗糖分子发生了化学键的断裂
13.用下列仪器或装置进行相应实验,不能达到实验目的的是( )
A.装置甲可用于除去粗盐中的不溶物 B.装置乙可用于观察的生成
C.装置丙可用于除去中的HCl D.装置丁可用于灼烧碎海带
14.下列离子方程式书写正确的是( )
A.溶于氢碘酸:
B.溶液中加入氨水:
C.漂白粉溶液除废气中的:
D.Al粉溶于过量NaOH溶液:
15.氯化铁是一种重要的盐,下列说法不正确的是( )
A.氯化铁属于弱电解质 B.氯化铁溶液能导电
C.氯化铁可由铁与氯气反应制得 D.氯化铁溶液可制备氢氧化铁胶体
16.物质的性质决定用途,下列两者对应关系不正确的是( )
A.过氧化钠能与二氧化碳反应生成氧气,可作潜水艇中的供氧剂
B.氧化钙易吸水,可用作干燥剂
C.维生素C具有还原性,可用作食品抗氧化剂
D.铝有强还原性,可用于制作门窗框架
17.为阿伏加德罗常数的值,下列说法错误的是( )
A.1.4g CO和的混合气体中原子数目为0.1
B.100mL 12mol/L的浓盐酸与足量反应生成的分子数为0.3
C.相同条件下,23g Na和78g 分别与足量水反应生成的气体体积相同
D.100g质量分数为46%的乙醇溶液中含有氢原子数为12
18.合成氨及氨氧化制硝酸的流程如图所示,下列说法错误的是( )
A.从氨分离器中分离出氨,主要利用了其易液化的性质
B.氧化炉中发生反应的化学方程式为
C.向吸收塔中通入空气的主要作用是提高氮元素的利用率
D.酸雨和光化学烟雾的形成均与氮氧化物有关
第Ⅱ卷(非选择题,共46分)
二、非选择题
19.(14分)
物质集合M中含有常见物质、、Al、、Fe、、Na,这些物质按照以下方法进行分类后如图所示,请按照要求回答问题。
(1)B组物质中属于非电解质的物质为 ,其中水溶液显碱性的原因用方程式表示为
。
(2)C组物质中能与冷水反应生成还原性气体的化学方程式为 。
(3)D组物质的共同点是常温下在 中会发生钝化。
(4)请写D组中能与氢氧化钠溶液反应的离子方程式 。
(5)请写出F组中的酸性氧化物与硫化氢反应的化学方程式: 。
(6)将E组中的两种物质混合,混合物中金属原子与氧原子的物质的量之比为3∶4,这两种物质的物质的量之比 ∶ = ∶ (等号前填写物质的化学式,等号后填数字)
20.(16分)
氮及其化合物在工农业生产和生活中有着重要作用。有资料显示过量的氨气和氯气在常温下可合成(岩脑砂的主要成分),某实验小组对该反应进行探究,并对岩脑砂进行元素测定,回答下列问题:
(1)的制备:
①利用装置B制取实验所需的氯气,写出该反应的化学方程式 。
②装置C的名称为 。
③为了使氨气和氯气在D中充分混合(提示:氨气从e口进,氯气从f口进,二者形成逆向流动,更有利于两者的充分混合),请确定上述装置的合理连接顺序:
→ → →ef←h←g← ← ← (用小写字母和箭头表示,箭头方向与气流方向一致)。
④该实验装置除了D处导管易堵塞外,还存在的不足之处是 。
⑤验证岩脑砂中所含的操作为
。
(2)岩脑砂中元素的定量测定:准确称取a g岩脑砂,与足量的氧化铜混合加热,发生的反应为,利用下列装置测定岩脑砂中氮元素和氯元素的质量之比(夹持装置省略)。
①装置H中盛装的试剂是 (填试剂名称)。
②已知装置J中也装有碱石灰,其目的是 。
③若装置I增重b g,利用装置K测得气体体积为V L(已知常温常压下气体摩尔体积为24.5),则岩脑砂中 (用含b、V的代数式表示,不必化简)。
21.(16分)
无水常作为芳烃氯代反应的催化剂。某研究小组设计了如下流程,以废铁屑(含有少量碳和杂质)为原料制备无水(s)。
已知:氯化亚砜()熔点-101℃,沸点76℃,易水解。
回答问题:
(1)操作①是过滤,用到的玻璃仪器有烧杯、玻璃棒和 。
(2)为避免引入新的杂质,试剂B可以选用 (填编号)。
A.溶液 B.水 C.水 D.溶液
(3)操作②是蒸发结晶,加热的同时通入HCl(g)的目的是 。
(4)取少量D晶体,溶于水并滴加KSCN溶液,现象是 。
(5)反应D→E的化学方程式为 。
(6)由D转化成E的过程中可能产生少量亚铁盐,写出一种可能的还原剂 ,并设计实验验证是该还原剂将还原的 。
参考答案
1-18
ADBAA/BDDCC/CCDAA/DBB
答案:
19.每个空2分,共14分
(1)①.、 ②.
(2)
(3)浓硝酸或浓硫酸
(4)
(5)
(6)
20.(16分)均为2分。
(1)①M
②(球形)干燥管
③a→d→c、j←i←b(顿号前后各一分,共2分)
④无尾气处理装置
⑤取少量岩脑砂于试管中,加少量蒸馏水溶解,再加入适量浓NaOH溶液并加热,若产生使湿润的红色石蕊试纸变蓝的气体,则含有。
(2)①浓硫酸
②防止装置K中的水蒸气进入装置I,影响实验结果
③
21.每个空2分,共16分
(1)漏斗
(2)BD
(3)防止水解
(4)溶液变为血红色
(5)
(6)
先加盐酸酸化,再加溶液,产生白色沉淀,则是将还原
同课章节目录
