天津市滨海新区重点中学2023-2024学年高二上学期期中考试化学试题(含答案)
文档属性
| 名称 | 天津市滨海新区重点中学2023-2024学年高二上学期期中考试化学试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 629.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-08 23:12:46 | ||
图片预览



文档简介
天津市滨海新区重点中学2022-2023-2高二年级期中考试
化学试卷
一、单选题(每个2分,共28题,共56分)
1.下列有关晶体常识的叙述错误的是( )
A.水晶属于晶体,有固定的熔点,而玻璃无固定的熔点,属于非晶体
B.当单一波长的X-射线通过晶体时可以看到明显的分立的斑点或者谱线
C.晶体都具有自范性。自范性是晶体的本质属性
D.晶体都具有规则的几何外形,而非晶体都不具有规则的几何外形
2.下列说法正确的是( )
A.若把分子写成分子,违背了共价键的饱和性
B.s轨道和p轨道重叠可以形成键
C.所有共价键都具有方向性
D.冰融化时分子中的共价键发生断裂
3.下列性质中,能充分说明某晶体一定是离子晶体的是( )
A.熔点很高 B.能溶于水,且水溶液能导电
C.固态时不导电而熔化时能导电 D.有固定熔点且晶态时表现各向异性
4.下列晶体分类正确的一组是( )
晶体类型 离子晶体 共价晶体 分子晶体
A KOH Ne P
B HCl 乙醇
C 晶体硅 甲苯
D 晶体硅 石墨
A.A B.B C.C D.D
5.二氧化碳经常用来灭火,但金属镁能够在二氧化碳中燃烧:,下列关于该反应中涉及物质的说法错误的是( )
A.Mg属于金属晶体
B.干冰中一个分子周围有4个紧邻的分子
C.Mg0熔点高,可以用作耐高温材料
D.金刚石和石墨互为同素异形体,二者C的杂化方式和晶体类型都不同
6.分子式为的芳香烃,其可能的结构有(不考虑立体异构)( )
A.3 B.5 C.4 D.6
7.下列对有关事实的解释正确的是( )
选项 事实 解释
A 的热稳定性比强 分子间能形成氢键
B 基态比稳定 基态价电子排布式为,是半充满的稳定结构
C 石墨能够导电 石墨是离子晶体
D 与分子的空间构型不同 它们中心原子杂化轨道类型不同
A.A B.B C.C D.D
8.下列说法正确的是( )
A.HF、HCl、HBr、HI的熔、沸点依次升高 B.、都是含有极性键的非极性分子
C.、、都是直线形分子 D.在水中的溶解性:戊醇>乙二醇>乙醇
9.以下关于萃取、分液操作的叙述中,正确的是( )
A.把混合液体转移至分液漏斗,塞上玻璃塞,如图用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开活塞
10.金刚砂(SiC)是重要的工业制品,可由反应制得:。SiC的晶体结构与金刚石类似,如图所示。下列说法错误的是( )
A.Si属于p区元素,在SiC中的化合价为+4价
B.X可与氧气反应生成Y,Y分子的中心原子杂化方式为sp杂化
C.金刚石熔点比SiC晶体熔点高
D.Si位于第四周期ⅣA族
11.火药制备是我国古代闻名的化学工艺,原理为,下列说法正确的是( )
A.的电子式:
B.和都是非极性分子
C.的结构示意图:
D.基态O原子核外电子轨道表达式:
12.甲烷晶体的晶胞结构如下图,下列有关说法不正确的是( )
A.甲烷在常温下呈气态,说明甲烷晶体属于分子晶体
B.晶体中1个分子有12个紧邻的甲烷分子
C.晶体熔化时需克服共价键
D.可燃冰()是在低温高压下形成的晶体
13.下列有机化合物按碳的骨架进行分类,其中与其他三种有机化合物属于不同类别的是( )
A. B. C. D.
14.下列物质中都含有“”,其中一种有别于其他三种,该物质是( )
A. B. C. D.
15.下列有机化合物中不属于烃的衍生物的是( )
A. B. C. D.
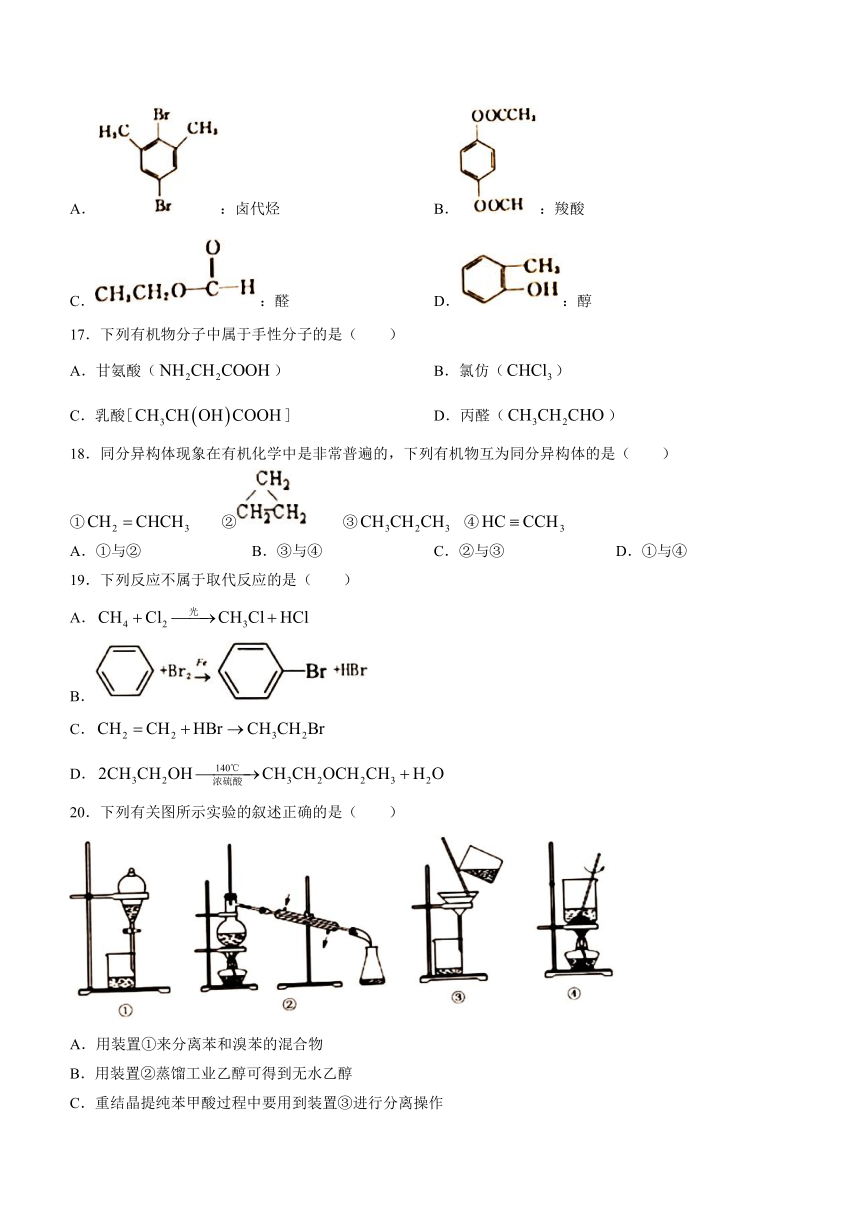
16.下列关于物质的分类中正确的是( )
A.:卤代烃 B.:羧酸
C.:醛 D.:醇
17.下列有机物分子中属于手性分子的是( )
A.甘氨酸() B.氯仿()
C.乳酸[] D.丙醛()
18.同分异构体现象在有机化学中是非常普遍的,下列有机物互为同分异构体的是( )
① ② ③ ④
A.①与② B.③与④ C.②与③ D.①与④
19.下列反应不属于取代反应的是( )
A.
B.
C.
D.
20.下列有关图所示实验的叙述正确的是( )
A.用装置①来分离苯和溴苯的混合物
B.用装置②蒸馏工业乙醇可得到无水乙醇
C.重结晶提纯苯甲酸过程中要用到装置③进行分离操作
D.装置④为蒸发结晶装置,实验者用玻璃棒不断搅拌溶液,以促进液体挥发,烧杯底部垫上石棉网,能让容器受热更加均匀
21.下列说法不正确的是( )
A.乙烯通入溴的四氯化碳溶液中,因发生加成反应而使溶液褪色
B.甲烷和氯气的混合气体在光照条件下反应,生成纯净的
C.丙烯()中的三个碳原子在同一个平面上
D.苯分子的六个碳原子具有平面正六边形结构
22.根据乙烯的性质可以推测丙烯()的性质,下列说法错误的是( )
A.丙烯能使酸性高锰酸钾溶液褪色 B.与HCl在一定条件下能加成,并只得到一种产物
C.丙烯能在空气中燃烧,产生黑烟 D.聚丙烯的结构可以表示为
23.下列有机物的命名正确的是( )
A.3,3-二甲基丁烷 B.3,3-二甲基-2-乙基戊烷
C.3-甲基丁烷 D.2,2-二甲基丙烷
24.下列关于有机化合物的说法错误的是( )
A.正己烷和2,2-二甲基丁烷互为同系物
B.中共平面的原子数目最多为15个
C.正丁烷的沸点比异丁烷的高,乙醇的沸点比二甲醚的高
D.甲苯能使酸性高锰酸钾溶液褪色,而烷烃则不能,说明苯环活化了甲基
25.下列烯烃有顺反异构体的是( )
A.乙烯 B.丙烯 C.2-甲基-1-丙烯 D.2-戊烯
26.下列表示不正确的是( )
A.乙烯的结构式: B.乙烷的结构简式:
C.2-甲基丁烷的键线式: D.甲基的电子式:
27.乙基环己烷()的一氯代物(不考虑立体异构)有( )
A.3种 B.4种 C.5种 D.6种
28.下列有关石墨晶体的说法正确的是( )
A.由于石墨晶体导电,所以它是金属晶体 B.由于石墨的熔点很高,所以它是原子晶体
C.由于石墨质软,所以它是分子晶体 D.石墨晶体是一种混合晶体
二、综合题(共44分)
29.回答下面问题(每空2分,共8分)
(1)和分子构型都为V形,中心原子的杂化形式都是 。
(2)和是同一主族元素的最高正价氧化物,常温下为气体,为高熔点固体。请分析原因: 。
(3)石墨的片层结构如图所示,试回答:
片层中平均每个正六边形含有 个碳原子。
(4)的化学名称为 。
30.回答下列问题:(每空2分,共6分)
(1)分子的空间结构为平面三角形,则分子为 (填“极性”或“非极性”)分子,其分子中的共价键类型为 键(填“极性”或“非极性”)。
(2)的熔点比 (填“高”“低”或“无法确定”)。
31.回答下列问题:(每空2分,共8分)
(1)基态核外电子排布式为 。
(2)C、N、O元素的第一电离能由大到小的顺序为 。
(3)1mol 中含有键的数目为 。
(4)的晶胞结构如图所示,其中的配位数是 。
32.某芳香烃A的质谱图如图所示:
回答下列问题:(每空2分,共12分)
(1)A的名称为 。
(2)A分子的核磁共振氢谱有 组峰,峰面积之比为 。
(3)A分子中最多有 个原子共平面。
(4)已知9.2g A在足量中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重 g、
g。
33.下图中A、B、C分别是三种有机物的结构模型:
A. B. C.
请回答下列问题:(前两个每空1分,后面每空2分,共10分)
(1)A、B两种模型分别是有机物的 模型和 模型。
(2)A及其同系物的分子式符合通式 (用n表示)。当n= 时,烷烃开始出现同分异构体。
(3)A、B、C三种有机物中,所有原子均共面的是 (填化学名称)。
(4)有机物C具有的结构或性质是 (填字母)。
a.是碳碳双键和碳碳单键交替的结构 b.有毒、不溶于水、密度比水小
c.能使酸性溶液褪色 d.一定条件下能与氢气或氧气反应
高二化学期中考试答案
D A C C B C B B D D
B C C D D A C A C C
B B D A D B D D
29.(每空2分,共8分)
答案:
(1)杂化
(2)(为分子晶体,为共价晶体,共价键的强度大于分子间作用力)
(3)2
(4)邻氟甲苯或2-氟甲苯
30.(每空1分,共6分)
(1)非极性 极性
(2)低
31.(每空2分,共8分)
(1)[Ar]或
(2)N>O>C
(3)8(或)
(4)4
32.(每空2分,共12分)
(1)甲苯
(2)4 1∶2∶2∶3
(3)13
(4)7.2 30.8
33.(前两个每空1分,后面每空2分,共10分)
(1)球棍 空间充填
(2)(n≥1) 4
(3)乙烯、苯
(4)bd
化学试卷
一、单选题(每个2分,共28题,共56分)
1.下列有关晶体常识的叙述错误的是( )
A.水晶属于晶体,有固定的熔点,而玻璃无固定的熔点,属于非晶体
B.当单一波长的X-射线通过晶体时可以看到明显的分立的斑点或者谱线
C.晶体都具有自范性。自范性是晶体的本质属性
D.晶体都具有规则的几何外形,而非晶体都不具有规则的几何外形
2.下列说法正确的是( )
A.若把分子写成分子,违背了共价键的饱和性
B.s轨道和p轨道重叠可以形成键
C.所有共价键都具有方向性
D.冰融化时分子中的共价键发生断裂
3.下列性质中,能充分说明某晶体一定是离子晶体的是( )
A.熔点很高 B.能溶于水,且水溶液能导电
C.固态时不导电而熔化时能导电 D.有固定熔点且晶态时表现各向异性
4.下列晶体分类正确的一组是( )
晶体类型 离子晶体 共价晶体 分子晶体
A KOH Ne P
B HCl 乙醇
C 晶体硅 甲苯
D 晶体硅 石墨
A.A B.B C.C D.D
5.二氧化碳经常用来灭火,但金属镁能够在二氧化碳中燃烧:,下列关于该反应中涉及物质的说法错误的是( )
A.Mg属于金属晶体
B.干冰中一个分子周围有4个紧邻的分子
C.Mg0熔点高,可以用作耐高温材料
D.金刚石和石墨互为同素异形体,二者C的杂化方式和晶体类型都不同
6.分子式为的芳香烃,其可能的结构有(不考虑立体异构)( )
A.3 B.5 C.4 D.6
7.下列对有关事实的解释正确的是( )
选项 事实 解释
A 的热稳定性比强 分子间能形成氢键
B 基态比稳定 基态价电子排布式为,是半充满的稳定结构
C 石墨能够导电 石墨是离子晶体
D 与分子的空间构型不同 它们中心原子杂化轨道类型不同
A.A B.B C.C D.D
8.下列说法正确的是( )
A.HF、HCl、HBr、HI的熔、沸点依次升高 B.、都是含有极性键的非极性分子
C.、、都是直线形分子 D.在水中的溶解性:戊醇>乙二醇>乙醇
9.以下关于萃取、分液操作的叙述中,正确的是( )
A.把混合液体转移至分液漏斗,塞上玻璃塞,如图用力振荡
B.振荡几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振荡并放气后,手持分液漏斗静置待液体分层
D.分液时,需先将上口玻璃塞打开或玻璃塞上的凹槽对准漏斗口上的小孔,再打开活塞
10.金刚砂(SiC)是重要的工业制品,可由反应制得:。SiC的晶体结构与金刚石类似,如图所示。下列说法错误的是( )
A.Si属于p区元素,在SiC中的化合价为+4价
B.X可与氧气反应生成Y,Y分子的中心原子杂化方式为sp杂化
C.金刚石熔点比SiC晶体熔点高
D.Si位于第四周期ⅣA族
11.火药制备是我国古代闻名的化学工艺,原理为,下列说法正确的是( )
A.的电子式:
B.和都是非极性分子
C.的结构示意图:
D.基态O原子核外电子轨道表达式:
12.甲烷晶体的晶胞结构如下图,下列有关说法不正确的是( )
A.甲烷在常温下呈气态,说明甲烷晶体属于分子晶体
B.晶体中1个分子有12个紧邻的甲烷分子
C.晶体熔化时需克服共价键
D.可燃冰()是在低温高压下形成的晶体
13.下列有机化合物按碳的骨架进行分类,其中与其他三种有机化合物属于不同类别的是( )
A. B. C. D.
14.下列物质中都含有“”,其中一种有别于其他三种,该物质是( )
A. B. C. D.
15.下列有机化合物中不属于烃的衍生物的是( )
A. B. C. D.
16.下列关于物质的分类中正确的是( )
A.:卤代烃 B.:羧酸
C.:醛 D.:醇
17.下列有机物分子中属于手性分子的是( )
A.甘氨酸() B.氯仿()
C.乳酸[] D.丙醛()
18.同分异构体现象在有机化学中是非常普遍的,下列有机物互为同分异构体的是( )
① ② ③ ④
A.①与② B.③与④ C.②与③ D.①与④
19.下列反应不属于取代反应的是( )
A.
B.
C.
D.
20.下列有关图所示实验的叙述正确的是( )
A.用装置①来分离苯和溴苯的混合物
B.用装置②蒸馏工业乙醇可得到无水乙醇
C.重结晶提纯苯甲酸过程中要用到装置③进行分离操作
D.装置④为蒸发结晶装置,实验者用玻璃棒不断搅拌溶液,以促进液体挥发,烧杯底部垫上石棉网,能让容器受热更加均匀
21.下列说法不正确的是( )
A.乙烯通入溴的四氯化碳溶液中,因发生加成反应而使溶液褪色
B.甲烷和氯气的混合气体在光照条件下反应,生成纯净的
C.丙烯()中的三个碳原子在同一个平面上
D.苯分子的六个碳原子具有平面正六边形结构
22.根据乙烯的性质可以推测丙烯()的性质,下列说法错误的是( )
A.丙烯能使酸性高锰酸钾溶液褪色 B.与HCl在一定条件下能加成,并只得到一种产物
C.丙烯能在空气中燃烧,产生黑烟 D.聚丙烯的结构可以表示为
23.下列有机物的命名正确的是( )
A.3,3-二甲基丁烷 B.3,3-二甲基-2-乙基戊烷
C.3-甲基丁烷 D.2,2-二甲基丙烷
24.下列关于有机化合物的说法错误的是( )
A.正己烷和2,2-二甲基丁烷互为同系物
B.中共平面的原子数目最多为15个
C.正丁烷的沸点比异丁烷的高,乙醇的沸点比二甲醚的高
D.甲苯能使酸性高锰酸钾溶液褪色,而烷烃则不能,说明苯环活化了甲基
25.下列烯烃有顺反异构体的是( )
A.乙烯 B.丙烯 C.2-甲基-1-丙烯 D.2-戊烯
26.下列表示不正确的是( )
A.乙烯的结构式: B.乙烷的结构简式:
C.2-甲基丁烷的键线式: D.甲基的电子式:
27.乙基环己烷()的一氯代物(不考虑立体异构)有( )
A.3种 B.4种 C.5种 D.6种
28.下列有关石墨晶体的说法正确的是( )
A.由于石墨晶体导电,所以它是金属晶体 B.由于石墨的熔点很高,所以它是原子晶体
C.由于石墨质软,所以它是分子晶体 D.石墨晶体是一种混合晶体
二、综合题(共44分)
29.回答下面问题(每空2分,共8分)
(1)和分子构型都为V形,中心原子的杂化形式都是 。
(2)和是同一主族元素的最高正价氧化物,常温下为气体,为高熔点固体。请分析原因: 。
(3)石墨的片层结构如图所示,试回答:
片层中平均每个正六边形含有 个碳原子。
(4)的化学名称为 。
30.回答下列问题:(每空2分,共6分)
(1)分子的空间结构为平面三角形,则分子为 (填“极性”或“非极性”)分子,其分子中的共价键类型为 键(填“极性”或“非极性”)。
(2)的熔点比 (填“高”“低”或“无法确定”)。
31.回答下列问题:(每空2分,共8分)
(1)基态核外电子排布式为 。
(2)C、N、O元素的第一电离能由大到小的顺序为 。
(3)1mol 中含有键的数目为 。
(4)的晶胞结构如图所示,其中的配位数是 。
32.某芳香烃A的质谱图如图所示:
回答下列问题:(每空2分,共12分)
(1)A的名称为 。
(2)A分子的核磁共振氢谱有 组峰,峰面积之比为 。
(3)A分子中最多有 个原子共平面。
(4)已知9.2g A在足量中充分燃烧,混合气体依次通过足量的浓硫酸和碱石灰,分别增重 g、
g。
33.下图中A、B、C分别是三种有机物的结构模型:
A. B. C.
请回答下列问题:(前两个每空1分,后面每空2分,共10分)
(1)A、B两种模型分别是有机物的 模型和 模型。
(2)A及其同系物的分子式符合通式 (用n表示)。当n= 时,烷烃开始出现同分异构体。
(3)A、B、C三种有机物中,所有原子均共面的是 (填化学名称)。
(4)有机物C具有的结构或性质是 (填字母)。
a.是碳碳双键和碳碳单键交替的结构 b.有毒、不溶于水、密度比水小
c.能使酸性溶液褪色 d.一定条件下能与氢气或氧气反应
高二化学期中考试答案
D A C C B C B B D D
B C C D D A C A C C
B B D A D B D D
29.(每空2分,共8分)
答案:
(1)杂化
(2)(为分子晶体,为共价晶体,共价键的强度大于分子间作用力)
(3)2
(4)邻氟甲苯或2-氟甲苯
30.(每空1分,共6分)
(1)非极性 极性
(2)低
31.(每空2分,共8分)
(1)[Ar]或
(2)N>O>C
(3)8(或)
(4)4
32.(每空2分,共12分)
(1)甲苯
(2)4 1∶2∶2∶3
(3)13
(4)7.2 30.8
33.(前两个每空1分,后面每空2分,共10分)
(1)球棍 空间充填
(2)(n≥1) 4
(3)乙烯、苯
(4)bd
同课章节目录
