福建省三明市五校2023-2024学年高一上学期期中联考化学试题(含答案)
文档属性
| 名称 | 福建省三明市五校2023-2024学年高一上学期期中联考化学试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 593.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-10 08:19:02 | ||
图片预览



文档简介
三明市五校2023-2024学年高一上学期期中联考
化学试卷
(考试时间:90分钟 满分:100分)
参考的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Fe-56 Cu-64
一、选择题(每小题只有一个正确选项,每小题3分,共48分)
1.化学与生活生产密切相关,下列说法错误的是( )
A.“卤水点豆腐,一物降一物”,该过程发生胶体的聚沉
B.“凡石灰,经火焚炼为用”,这里的石灰是
C.“青蒿一握,以水二升渍,绞取汁”,受此启发屠呦呦利用乙醚提取青蒿素
D.能与碱反应,所以可用作焙制糕点的膨松剂
2.晋代葛洪的《食肉方》去除黑痣的药方中记载:“取白炭灰(熟石灰),获灰(草木灰),等分,煎令如膏……,并可与去黑子”。对于能除去黑痣的物质的说法正确的是( )
A.是 B.有强腐蚀性
C.只有溶于水才能电离 D.是
3.2019年诺贝尔化学奖颁给几位在锂离子电池研发领域做出贡献的科学家,锂单质化学性质与钠类似,活泼性比钠略弱。它的密度为,将绿豆大的锂投入水中,下列实验现象合理的有( )
①锂沉入水中 ②锂浮在水面上
③水中有大量气泡 ④反应后在水中加入几滴石蕊试液,溶液变红
⑤反应比钠剧烈 ⑥锂四处游动
A.②③⑥ B.①③⑥ C.②③⑤ D.②④⑤⑥
4.已知两瓶气体,分别是和,可以区别它们的方法或试剂是( )
①观察颜色 ②打开瓶盖看有无白雾
③硝酸银溶液 ④湿润的红色石蕊试纸
⑤湿润的蓝色石蕊试纸
A.①③④ B.①②④ C.①②④⑤ D.①②⑤
5.下列物质分类组合正确的是( )
选项 混合物 酸性氧化物 碱性氧化物 盐
A 漂白粉
B 碱石灰
C
D 冰水混合物
6.新型冠状病毒(冠状病毒粒子直径约60~220nm)主要传播途径有飞沫传播、接触传播和气溶胶传播。下列有关说法不正确的是( )
A.气溶胶的分散剂为气体
B.利用丁达尔效应可检测气溶胶中的冠状病毒
C.用含氯消毒剂如84消毒液、等可杀灭新冠病毒
D.用“人工肾”进行血液透析救治危重新冠肺炎患者,利用了胶体的性质
7.设为阿伏加德罗常数的值,下列叙述正确的是( )
A.中所含离子数为
B.中含有的质子数为
C.将的溶液制成胶体后,其中含有氢氧化铁胶粒数为
D.常温常压下,与的混和气体中含有的原子数目为
8.一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入,右边充入和的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同)。右侧与分子数之比为( )
A.1:3 B.3:1 C.1:2 D.2:1
9.把和混合物6.56g溶于水制成溶液,测得溶液中的浓度为。向该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量为( )
A.2.925g B.5.85g C.6.56g D.无法确定
10.下列溶液中和与的溶液中和分别相等的是( )
A.的溶液 B.的的溶液
C.的溶液 D.的溶液
11.下列反应的离子方程式正确的是( )
A.氯气与水反应:
B.往溶液中通入少量:
C.向沸水中滴加饱和溶液制备胶体:
D.溶液中加入过量的溶液:
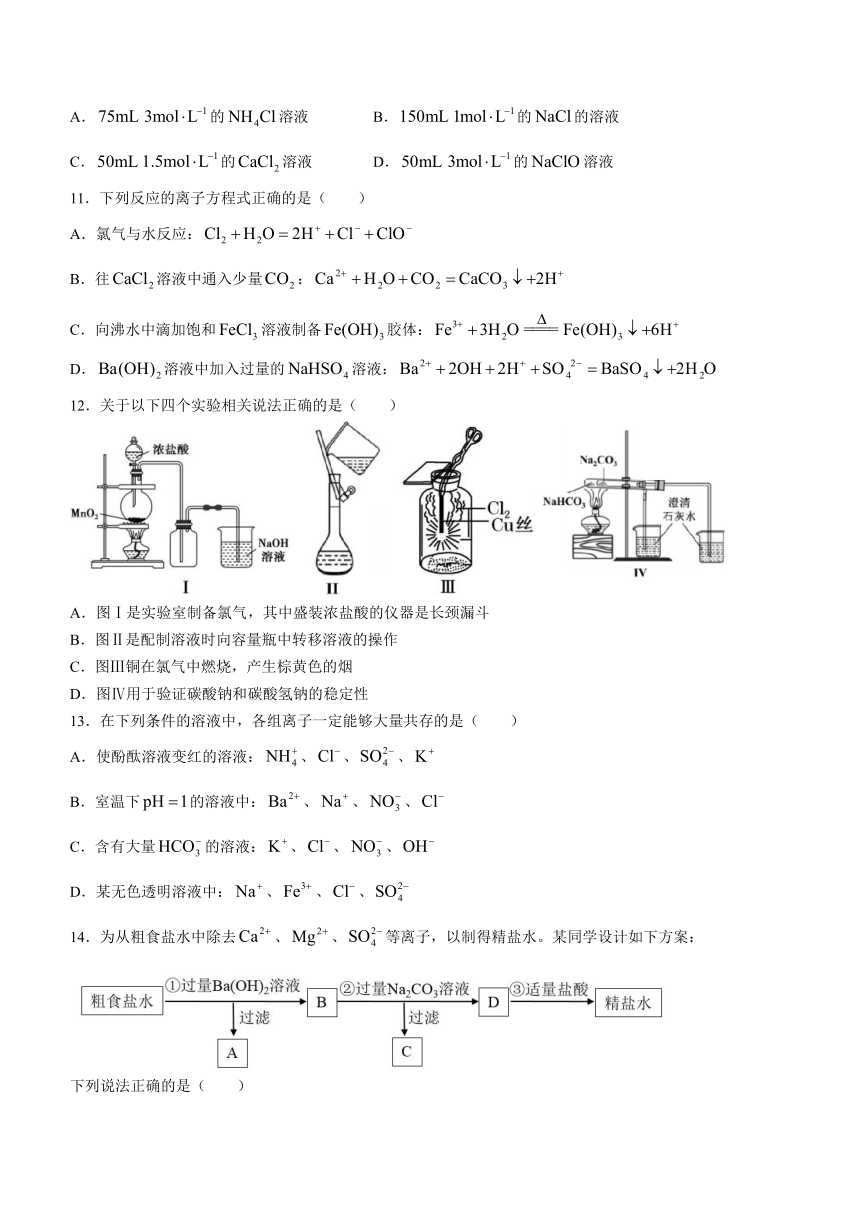
12.关于以下四个实验相关说法正确的是( )
A.图Ⅰ是实验室制备氯气,其中盛装浓盐酸的仪器是长颈漏斗
B.图Ⅱ是配制溶液时向容量瓶中转移溶液的操作
C.图Ⅲ铜在氯气中燃烧,产生棕黄色的烟
D.图Ⅳ用于验证碳酸钠和碳酸氢钠的稳定性
13.在下列条件的溶液中,各组离子一定能够大量共存的是( )
A.使酚酞溶液变红的溶液:、、、
B.室温下的溶液中:、、、
C.含有大量的溶液:、、、
D.某无色透明溶液中:、、、
14.为从粗食盐水中除去、、等离子,以制得精盐水。某同学设计如下方案:
下列说法正确的是( )
A.A中主要有和,也可能有一些
B.②中加入过量溶液的主要目的是为了除去、
C.D中只有、、这三种离子
D.③中发生的反应只有
15.某无色、澄清溶液中可能含有①②③④⑤⑥、⑦中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下,下列结论正确的是( )
步骤 操作 现象
Ⅰ 用紫色石蕊试液检验 溶液变红
Ⅱ 向溶液中滴加溶液和稀盐酸 有白色沉淀生成
Ⅲ 将Ⅱ中所得混合物过滤,向滤液中加入溶液和稀 有白色沉淀生成
A.肯定含有的离子是③⑥ B.该实验无法确定是否含有②
C.肯定没有的离子是⑥⑦ D.可能含有的离子是①③
16.相对分子质量为的气态化合物VL(标准状况)溶于水中,得到溶液的质量分数为,密度为,物质的量浓度为。下列说法正确的是( )
A.溶液的质量分数可表示为
B.物质的量浓度c可表示为
C.溶液密度可表示为
D.相对分子质量可表示为
二、填空题(本题含4小题,共52分)
17.(12分)回答下列问题:
素材Ⅰ.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:。结合素材回答问题(1)~(3):
(1)该反应中的摩尔质量是________。
(2)28g铁粉中含有的Fe原子数是_______。
(3)若28g铁粉完全反应,析出Cu单质的物质的量为_______。
素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是:。结合素材回答问题(4)~(5):
(4)在相同条件下体积相同的和两种气体含有的原子数之比为_______。
(5)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的的体积是_______。
素材Ⅲ.向空气中排放会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
离子
浓度() 0.06 0.08 0.02 0.04 a
(6)该雨水中氢离子的浓度________。
18.(14分)阅读下列科普短文并填空。
燃料电池具有能量转化率高、对环境友好等特点。燃料电池在工作时,从负极连续通入①氢气或②等燃料,从正极连续通入③氧气,二者在电池内部(含有④或⑤等物质的溶液)发生反应生成⑥、⑦或⑧溶液,同时产生电能。
(1)在上述短文标有序号的物质中,能导电的是________(填序号,下同);属于强电解质的是________;属于非电解质的是________。
(2)过量⑦通入⑤的溶液或⑧中均能生成同种物质,该物质与④的溶液反应的离子方程式为________。
(3)将⑤的溶液逐滴加入同浓度④的溶液中,此过程溶液的电导率变化曲线为下图中的_____(填“Ⅰ”或“Ⅱ”),________mL。
(4)将甲烷燃料电池产生的气体⑦,体积为11.2L(标准状况下)通入2L⑤的溶液中生成正盐,该溶液⑤的物质的量浓度为________。
19.(12分)84消毒液是杀菌性强、杀菌范围广的产品,以次氯酸钠为主要成分。
Ⅰ.(1)工业上制取84消毒液的离子方程式是________________________________________。
Ⅱ.84消毒液有效氯是指单位体积消毒液含与消毒能力相当的氯气的质量(消毒能力与氯气相当),一般市售84消毒液有效氯为。
(2)某兴趣小组通过实验测得某品牌84消毒液有效氯为,假设有效氯都来自次氯酸钠,则该消毒液中的物质的量浓度为________。
(3)将该品牌消毒液准确稀释成有效氯为的稀溶液,用于餐具消毒。
①实验中需要的玻璃仪器除量筒、胶头滴管、烧杯外还要________;
②下列操作会导致有效氯偏低的是________(填字母序号);
A.容量瓶用蒸馏水洗涤后未干燥 B.用量筒量取84消毒液时仰视读数
C.移液时有少量液体溅出 D.加水定容时仰视刻度线
Ⅲ.该小组继续探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售84消毒液稀释至100倍,测得稀释后溶液的;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计);
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
烧杯 溶液的pH 现象
a 10 10min后,红纸基本不褪色
b 7 10min后,红纸颜色变浅
c 4 10min后,红纸基本褪色
和物质的量分数(a)随溶液pH变化的关系如图所示:
(4)①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色________。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是________。
20.(14分)X、Y、Z、W四种化合物均由1-18号元素组成,其中X含有四种元素,X、Y、Z均含钠元素,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物,产物及反应条件已略去),回答下列问题:
(1)①X生成Z的化学方程式________。
②X溶于水的发生电离的方程式________________________________。
③向Z的水溶液中通入的离子方程式________________________________。
(2)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中两种化合物分别放在装置Ⅰ、装置Ⅱ,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
①装置Ⅱ中物质的化学式是________。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,所需仪器装置是________(从上图中选择必要装置,填写编号)。
(3)向Z溶液中通入氯气,可制得生产和生活中某种消毒液的主要成分,同时有X和氯化钠生成,该反应的化学方程式是________。
(4)为测定X和Z混合物中Z的质量分数,某课外小组取ag混合物充分加热,质量减少bg,则混合物中Z的质量分数是________(用含a、b的代数式表示)。
三明市五校2023-2024学年高一上学期期中联考
化学答案
一、选择题(每小题3分,共48分)
1-5 DBACA 6-10 BDBAC 11-15 DCBAD 16.A
17.(12分,每空2分)
(1)
(2)
(3)
(4)3:2
(5)22.4L
(6)0.12
18.(14分,每空2分)
(1)①.⑥⑧ ②.④⑤ ③.②⑦
(2)
(3)①.Ⅱ ②.20
(4)0.5
19.(12分,每空2分)
(1)
(2)
(3)①.玻璃棒、500mL容量瓶 ②.CD
(4)①.越慢
②.b烧杯中溶液的pH大于c烧杯中溶液的pH,的浓度较小,反应较慢,褪色较慢
20.(14分,每空2分)
(1)①.
②.
③.
(2)①. ②.Ⅰ、Ⅳ、Ⅴ
(3)
(4)
化学试卷
(考试时间:90分钟 满分:100分)
参考的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Fe-56 Cu-64
一、选择题(每小题只有一个正确选项,每小题3分,共48分)
1.化学与生活生产密切相关,下列说法错误的是( )
A.“卤水点豆腐,一物降一物”,该过程发生胶体的聚沉
B.“凡石灰,经火焚炼为用”,这里的石灰是
C.“青蒿一握,以水二升渍,绞取汁”,受此启发屠呦呦利用乙醚提取青蒿素
D.能与碱反应,所以可用作焙制糕点的膨松剂
2.晋代葛洪的《食肉方》去除黑痣的药方中记载:“取白炭灰(熟石灰),获灰(草木灰),等分,煎令如膏……,并可与去黑子”。对于能除去黑痣的物质的说法正确的是( )
A.是 B.有强腐蚀性
C.只有溶于水才能电离 D.是
3.2019年诺贝尔化学奖颁给几位在锂离子电池研发领域做出贡献的科学家,锂单质化学性质与钠类似,活泼性比钠略弱。它的密度为,将绿豆大的锂投入水中,下列实验现象合理的有( )
①锂沉入水中 ②锂浮在水面上
③水中有大量气泡 ④反应后在水中加入几滴石蕊试液,溶液变红
⑤反应比钠剧烈 ⑥锂四处游动
A.②③⑥ B.①③⑥ C.②③⑤ D.②④⑤⑥
4.已知两瓶气体,分别是和,可以区别它们的方法或试剂是( )
①观察颜色 ②打开瓶盖看有无白雾
③硝酸银溶液 ④湿润的红色石蕊试纸
⑤湿润的蓝色石蕊试纸
A.①③④ B.①②④ C.①②④⑤ D.①②⑤
5.下列物质分类组合正确的是( )
选项 混合物 酸性氧化物 碱性氧化物 盐
A 漂白粉
B 碱石灰
C
D 冰水混合物
6.新型冠状病毒(冠状病毒粒子直径约60~220nm)主要传播途径有飞沫传播、接触传播和气溶胶传播。下列有关说法不正确的是( )
A.气溶胶的分散剂为气体
B.利用丁达尔效应可检测气溶胶中的冠状病毒
C.用含氯消毒剂如84消毒液、等可杀灭新冠病毒
D.用“人工肾”进行血液透析救治危重新冠肺炎患者,利用了胶体的性质
7.设为阿伏加德罗常数的值,下列叙述正确的是( )
A.中所含离子数为
B.中含有的质子数为
C.将的溶液制成胶体后,其中含有氢氧化铁胶粒数为
D.常温常压下,与的混和气体中含有的原子数目为
8.一个密闭容器,中间有一可自由滑动的隔板(厚度可忽略)将容器分成两部分,当左边充入,右边充入和的混合气体共8g时,隔板处于如图位置(左、右两侧温度相同)。右侧与分子数之比为( )
A.1:3 B.3:1 C.1:2 D.2:1
9.把和混合物6.56g溶于水制成溶液,测得溶液中的浓度为。向该溶液中加入一定量盐酸恰好完全反应,将溶液蒸干后,所得固体质量为( )
A.2.925g B.5.85g C.6.56g D.无法确定
10.下列溶液中和与的溶液中和分别相等的是( )
A.的溶液 B.的的溶液
C.的溶液 D.的溶液
11.下列反应的离子方程式正确的是( )
A.氯气与水反应:
B.往溶液中通入少量:
C.向沸水中滴加饱和溶液制备胶体:
D.溶液中加入过量的溶液:
12.关于以下四个实验相关说法正确的是( )
A.图Ⅰ是实验室制备氯气,其中盛装浓盐酸的仪器是长颈漏斗
B.图Ⅱ是配制溶液时向容量瓶中转移溶液的操作
C.图Ⅲ铜在氯气中燃烧,产生棕黄色的烟
D.图Ⅳ用于验证碳酸钠和碳酸氢钠的稳定性
13.在下列条件的溶液中,各组离子一定能够大量共存的是( )
A.使酚酞溶液变红的溶液:、、、
B.室温下的溶液中:、、、
C.含有大量的溶液:、、、
D.某无色透明溶液中:、、、
14.为从粗食盐水中除去、、等离子,以制得精盐水。某同学设计如下方案:
下列说法正确的是( )
A.A中主要有和,也可能有一些
B.②中加入过量溶液的主要目的是为了除去、
C.D中只有、、这三种离子
D.③中发生的反应只有
15.某无色、澄清溶液中可能含有①②③④⑤⑥、⑦中的若干种,依次进行下列实验,且每步所加试剂均过量,观察到的现象如下,下列结论正确的是( )
步骤 操作 现象
Ⅰ 用紫色石蕊试液检验 溶液变红
Ⅱ 向溶液中滴加溶液和稀盐酸 有白色沉淀生成
Ⅲ 将Ⅱ中所得混合物过滤,向滤液中加入溶液和稀 有白色沉淀生成
A.肯定含有的离子是③⑥ B.该实验无法确定是否含有②
C.肯定没有的离子是⑥⑦ D.可能含有的离子是①③
16.相对分子质量为的气态化合物VL(标准状况)溶于水中,得到溶液的质量分数为,密度为,物质的量浓度为。下列说法正确的是( )
A.溶液的质量分数可表示为
B.物质的量浓度c可表示为
C.溶液密度可表示为
D.相对分子质量可表示为
二、填空题(本题含4小题,共52分)
17.(12分)回答下列问题:
素材Ⅰ.“熬胆矾铁釜,久之亦化为铜”涉及到的化学反应为:。结合素材回答问题(1)~(3):
(1)该反应中的摩尔质量是________。
(2)28g铁粉中含有的Fe原子数是_______。
(3)若28g铁粉完全反应,析出Cu单质的物质的量为_______。
素材Ⅱ.宋代《洗冤集录》中记载有“银针探毒”,其原理是:。结合素材回答问题(4)~(5):
(4)在相同条件下体积相同的和两种气体含有的原子数之比为_______。
(5)在0℃、101kPa条件下,11.2L氧气完全反应,消耗的的体积是_______。
素材Ⅲ.向空气中排放会造成酸雨,检测出某地雨水中的离子组成和浓度如下表所示:
离子
浓度() 0.06 0.08 0.02 0.04 a
(6)该雨水中氢离子的浓度________。
18.(14分)阅读下列科普短文并填空。
燃料电池具有能量转化率高、对环境友好等特点。燃料电池在工作时,从负极连续通入①氢气或②等燃料,从正极连续通入③氧气,二者在电池内部(含有④或⑤等物质的溶液)发生反应生成⑥、⑦或⑧溶液,同时产生电能。
(1)在上述短文标有序号的物质中,能导电的是________(填序号,下同);属于强电解质的是________;属于非电解质的是________。
(2)过量⑦通入⑤的溶液或⑧中均能生成同种物质,该物质与④的溶液反应的离子方程式为________。
(3)将⑤的溶液逐滴加入同浓度④的溶液中,此过程溶液的电导率变化曲线为下图中的_____(填“Ⅰ”或“Ⅱ”),________mL。
(4)将甲烷燃料电池产生的气体⑦,体积为11.2L(标准状况下)通入2L⑤的溶液中生成正盐,该溶液⑤的物质的量浓度为________。
19.(12分)84消毒液是杀菌性强、杀菌范围广的产品,以次氯酸钠为主要成分。
Ⅰ.(1)工业上制取84消毒液的离子方程式是________________________________________。
Ⅱ.84消毒液有效氯是指单位体积消毒液含与消毒能力相当的氯气的质量(消毒能力与氯气相当),一般市售84消毒液有效氯为。
(2)某兴趣小组通过实验测得某品牌84消毒液有效氯为,假设有效氯都来自次氯酸钠,则该消毒液中的物质的量浓度为________。
(3)将该品牌消毒液准确稀释成有效氯为的稀溶液,用于餐具消毒。
①实验中需要的玻璃仪器除量筒、胶头滴管、烧杯外还要________;
②下列操作会导致有效氯偏低的是________(填字母序号);
A.容量瓶用蒸馏水洗涤后未干燥 B.用量筒量取84消毒液时仰视读数
C.移液时有少量液体溅出 D.加水定容时仰视刻度线
Ⅲ.该小组继续探究84消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5mL市售84消毒液稀释至100倍,测得稀释后溶液的;
步骤2:将稀释后溶液各20mL分别加入3个洁净的小烧杯中;
步骤3:用溶液将3个烧杯内溶液的pH分别调至10、7和4(溶液体积变化忽略不计);
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
烧杯 溶液的pH 现象
a 10 10min后,红纸基本不褪色
b 7 10min后,红纸颜色变浅
c 4 10min后,红纸基本褪色
和物质的量分数(a)随溶液pH变化的关系如图所示:
(4)①由实验现象可获得结论:溶液的pH在4~10范围内,pH越大,红纸褪色________。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是________。
20.(14分)X、Y、Z、W四种化合物均由1-18号元素组成,其中X含有四种元素,X、Y、Z均含钠元素,W为无色无味气体。这四种化合物具有下列转化关系(部分反应物,产物及反应条件已略去),回答下列问题:
(1)①X生成Z的化学方程式________。
②X溶于水的发生电离的方程式________________________________。
③向Z的水溶液中通入的离子方程式________________________________。
(2)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中两种化合物分别放在装置Ⅰ、装置Ⅱ,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
①装置Ⅱ中物质的化学式是________。
②用X含有的四种元素中的两种组成的某化合物,在催化剂存在下制备并收集纯净干燥的装置Ⅴ中气体,所需仪器装置是________(从上图中选择必要装置,填写编号)。
(3)向Z溶液中通入氯气,可制得生产和生活中某种消毒液的主要成分,同时有X和氯化钠生成,该反应的化学方程式是________。
(4)为测定X和Z混合物中Z的质量分数,某课外小组取ag混合物充分加热,质量减少bg,则混合物中Z的质量分数是________(用含a、b的代数式表示)。
三明市五校2023-2024学年高一上学期期中联考
化学答案
一、选择题(每小题3分,共48分)
1-5 DBACA 6-10 BDBAC 11-15 DCBAD 16.A
17.(12分,每空2分)
(1)
(2)
(3)
(4)3:2
(5)22.4L
(6)0.12
18.(14分,每空2分)
(1)①.⑥⑧ ②.④⑤ ③.②⑦
(2)
(3)①.Ⅱ ②.20
(4)0.5
19.(12分,每空2分)
(1)
(2)
(3)①.玻璃棒、500mL容量瓶 ②.CD
(4)①.越慢
②.b烧杯中溶液的pH大于c烧杯中溶液的pH,的浓度较小,反应较慢,褪色较慢
20.(14分,每空2分)
(1)①.
②.
③.
(2)①. ②.Ⅰ、Ⅳ、Ⅴ
(3)
(4)
同课章节目录
