10.1常见的酸和碱基础练习 (含解析)人教版初中化学九年级下册
文档属性
| 名称 | 10.1常见的酸和碱基础练习 (含解析)人教版初中化学九年级下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 175.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-11 00:00:00 | ||
图片预览





文档简介
10.1常见的酸和碱基础练习
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.下列除杂所选用的试剂中,正确的是
物质 所含杂质 除杂试剂
A 铁粉 铜粉 稀盐酸
B CO CO2 浓H2SO4
C CO2 CO 灼热的CuO
D FeSO4溶液 CuSO4溶液 加入锌后过滤
A.A B.B C.C D.D
2.下列鉴别物质的试剂,不正确的是
序号 待鉴别的物质 鉴别试剂
A 蒸馏水与过氧化氢溶液 二氧化锰
B 硝酸铵与食盐固体 水
C 稀盐酸与氯化钠溶液 酚酞溶液
D 一氧化碳与二氧化碳气体 澄清的石灰水
A.A B.B C.C D.D
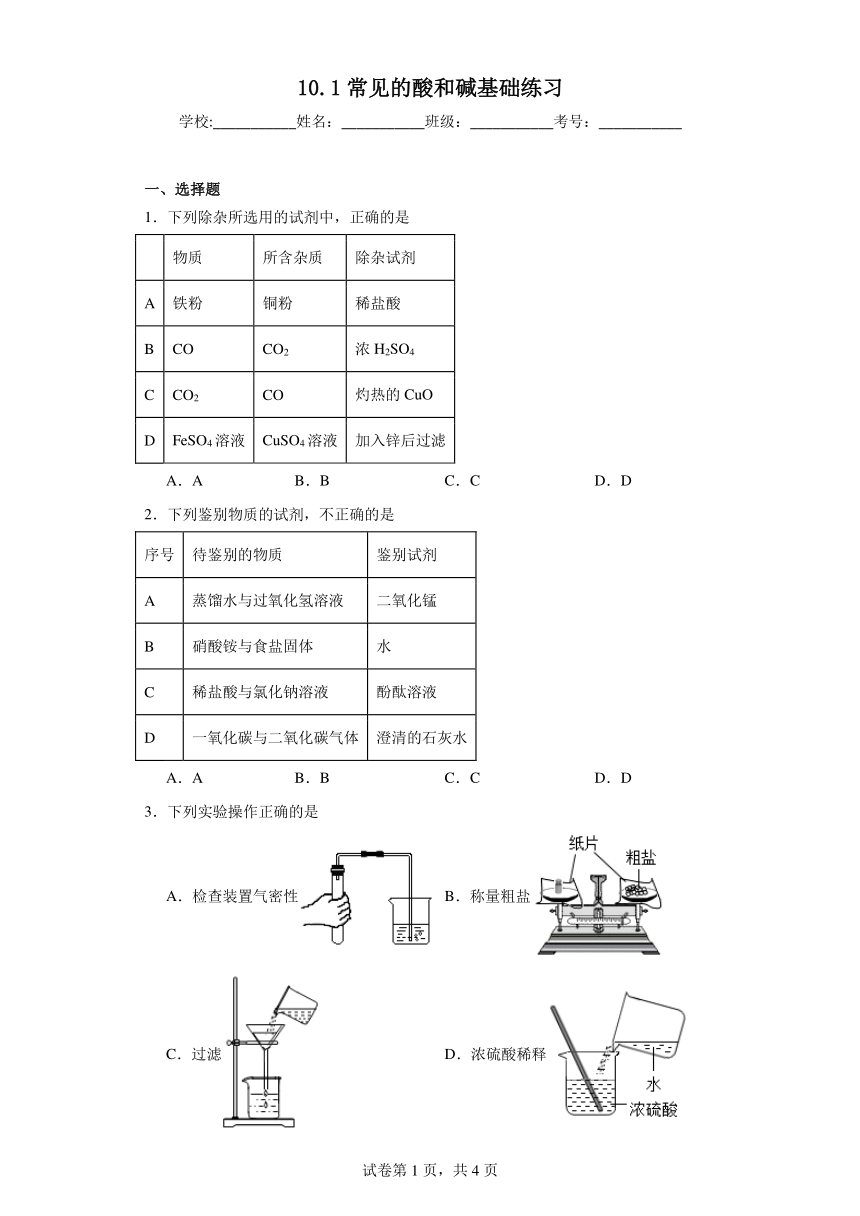
3.下列实验操作正确的是
A.检查装置气密性 B.称量粗盐
C.过滤 D.浓硫酸稀释
4.如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是①稀盐酸和石灰石;②稀硫酸和锌;③水和生石灰;④水和氯化钠。
A.①②③④ B.①②③
C.①②④ D.②③④
5.下列由于发生化学反应而使溶液质量变大的是( )
A.浓盐酸 B.浓硫酸 C.澄清石灰水 D.氢氧化钠溶液
6.常温分别将1克下列固体与99克水充分反应混和,所得溶液的溶质质量分数由小到大的顺序是:①CuSO4·5H2O;②Na2O;③KNO3;④CaO
A.①②③④ B.④③②① C.④①③② D.①③②④
7.下列实验操作中,正确的是
A.干燥气体 B.倾倒液体
C.稀释浓硫酸 D.取用固体
8.下列各组实验方法能达到实验目的的是
选项 实验目的 实验操作
A 除去氧化铜中混有的炭粉 在氧气流中充分加热混合物
B 验证质量守恒定律 碳酸钠和稀盐酸在敞口容器中反应
C 探究锌、铁、铜的金属活动性顺序 将铜丝、铁丝分别插入硫酸锌溶液中
D 除去氧化钙中混有的少量碳酸钙 加水溶解、过滤、洗涤、干燥
A.A B.B C.C D.D
9.下列各组中的气体,既可用浓H2SO4干燥,又可以用碱石灰干燥的一组是
A.H2、O2、SO2 B.CO、H2、CH4 C.O2、HCl、CH4 D.CO、CH4、NH3
10.下列对实验意外事故的处理错误的是
A.若不慎将燃着的酒精灯碰倒,洒出的酒精在桌上燃烧,应立刻用湿抹布扑盖
B.若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液
C.若不慎将腐蚀性药液溅入眼睛,要先用手揉眼睛,再立即用水冲洗
D.若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液
二、判断题
11.NaOH和Ca(OH)2化学性质相似,因为在水中解离出的阴离子都是OH﹣( )
12.用无色酚酞溶液可以区分开澄清石灰水和食盐溶液( )
13.向紫色石蕊溶液中通入CO2,溶液变红,说明CO2呈酸性( )
14.浓硫酸可用于干燥二氧化碳,所以浓盐酸也可用于干燥二氧化碳( )
15.因为NaOH能使无色酚酞变红,所以Cu(OH)2也能使无色酚酞变红( )
三、综合应用题
16.小匡在实验室做酸碱盐的性质实验时发现,一瓶标注氢氧化钠溶液的试剂瓶是敞口放置的。为了检验这瓶氢氧化钠溶液是否变质,小匡与同组的小胡同学共同探究:
他们依据所学的化学知识,对这瓶溶液的成分作了如下猜想:
猜想一:可能是NaOH溶液:
猜想二:可能是Na2CO3溶液:
猜想三:可能是NaOH和Na2CO3的混合溶液。
【查阅资料得知】:Na2CO3溶液能使酚酞溶液变红,CaC12溶液、BaC12溶液呈中性、氢氧化钡溶液呈碱性。
【实验验证及结论】
小匡同学取适量的该溶液,加入过量氢氧化钡溶液,充分反应后静置,观察到有白色沉淀产生,静置,向上层清液中滴加酚酞溶液,溶液变红,得出猜想三成立。
(1)小胡同学认为小匡同学的实验不能得出相应的结论,理由是 。
(2)请你在小匡同学实验的基础上,设计出能够验证猜想三成立的实验方案 。
17.煤燃烧生成的SO2污染环境,某工厂采用烟气脱硫工艺消除SO2,并将其转化为化工原料CaSO4,实现“变废为宝”,反应为。
(1)吸收二氧化硫的反应前后有化合价发生变化的元素是 (填元素符号)。
(2)SO2大量排放产生的环境问题是 。
(3)CaO,俗称生石灰。不仅可以用于燃煤脱硫,还可以用来作干燥剂,用生石灰作干燥剂的原理是 。(用化学方程式表示)
(4)根据化学方程式计算,若煤厂要处理16吨二氧化硫,至少需要加入生石灰的质量是多少?
18.水和溶液在生产、生活中具有广泛的用途。
(1)实验室稀释浓硫酸的正确操作顺序是 (填字母),并用玻璃棒不断搅拌。
a.将水沿器壁缓慢注入浓硫酸中 b.将浓硫酸沿器壁缓慢注入水中
(2)甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。
①t2℃时,甲物质的溶解度是 g。
②t2℃时,将质量相等的甲、乙的饱和溶液分别降温到t1℃,得到的两种溶液中溶质的质量分数相比,甲 乙(填“大于”、“小于”或“等于”)。
(3)实验室稀释浓硫酸。
①将50mL溶质质量分数为98%的浓H2SO4,加水稀释为质量分数为24.5%的稀H2SO4.已知所用溶质质量分数为98%的浓H2SO4密度为1.98g/cm3;水的密度为1g/cm3,则需加水的体积是 mL(计算结果保留一位小数)。
②取40g溶质质量分数为24.5%的稀H2SO4和足量的锌,完全反应后,生成氢气的质量是 ?(利用化学方程式进行计算,并在答题卡上写出完整计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】A、铁粉能与稀盐酸反应生成氯化亚铁和氢气,铜不与稀盐酸反应,反而会把原物质除去,不符合除杂原则,故A不符合题意;
B、二氧化碳不能与浓硫酸反应,不能除去杂质,不符合除杂原则,故B不符合题意;
C、CO能与灼热的氧化铜反应生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故C符合题意;
D、锌与FeSO4和CuSO4均能发生反应,不符合除杂原则,故D不符合题意。
故选C。
2.C
【详解】A、鉴别蒸馏水与过氧化氢溶液,加入二氧化锰,有气泡产生是过氧化氢溶液,无现象的是蒸馏水,可以鉴别开来,该选项不符合题意;
B、鉴别硝酸铵与食盐固体,加水,温度会降低的为硝酸铵,温度不变的是食盐固体,可以鉴别开来,该选项不符合题意;
C、无色酚酞溶液遇碱(碱性)溶液变红,而稀盐酸显酸性,氯化钠溶液显中性,都不能使无色酚酞溶液变红,故无法鉴别开来,该选项符合题意;
D、鉴别一氧化碳与二氧化碳气体,因为二氧化能使澄清的石灰水变浑浊,故可用澄清的石灰水鉴别一氧化碳与二氧化碳气体,该选项不符合题意。
故选C。
3.A
【详解】A、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气,图中所示操作正确;
B、托盘天平的使用要遵循“左物右码”的原则,图中所示砝码与药品位置放反了,图中所示操作错误;
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,且漏斗下端没有紧靠在烧杯内壁上,图中所示操作错误;
D、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时的扩散,一定不能把水注入浓硫酸中,图中所示操作错误。
故选A。
4.B
【分析】注射器中的活塞向右移动,是瓶内压强变大,可能是反应生成气体,也可能是反应放热或溶解放热。
【详解】①稀盐酸和石灰石反应生成二氧化碳气体,使得瓶内压强变大,导致注射器中的活塞向右移动;②稀硫酸和锌反应生成气体,瓶内气体增多,使得瓶内压强变大,导致注射器中的活塞向右移动;③水和生石灰反应放热,瓶内温度升高,使得瓶内压强变大,导致注射器中的活塞向右移动;④氯化钠溶于水温度变化不明显,瓶内压强无明显变化,注射器中的活塞不会发生移动。故选B。
5.D
【详解】A、浓盐酸具有挥发性,露置在空气中会使其质量减少,故选项错误。
B、浓硫酸具有吸水性,放置在空气中会吸收空气中的水分,使其质量增加,但发生的是物理变化,故选项错误。
C、澄清石灰水与空气中的二氧化碳发生化学反应,生成碳酸钙沉淀,导致溶液质量减小,故选项错误。
D、氢氧化钠溶液敞口露置在空气中,能与空气中的二氧化碳发生化学反应生成碳酸钠和水,发生了化学变化导致溶液质量增加,故选项正确。
故选:D。
【点睛】掌握常见的酸碱盐的物理性质与化学性质、在空气中的质量变化等是正确解答此类题的关键。
6.C
【详解】根据①CuSO4·5H2O溶于水后,会失去结晶水,则最终得到的溶质硫酸铜质量小于1g;②Na2O会与水反应生成氢氧化钠,则形成的溶液中溶质是氢氧化钠,根据质量守恒定律,氢氧化钠的质量大于氧化钠的质量即大于1g;③KNO3溶于水溶质即硝酸钾1g;④CaO会与水反应生成氢氧化钙,但氢氧化钙属于微溶物,因此溶解的氢氧化钙质量在这四种物质中最少;故所得的溶液中溶质质量分数有小到大的顺序是④CaO<①CuSO4·5H2O<③KNO3<②Na2O,故选:C
7.B
【详解】A、气体从长导管进气能接触到浓硫酸,除去气体中的水蒸气,A错误;
B、倾倒液体要注意瓶塞倒放、标签冲向手心、试剂瓶口紧贴容器口,B正确;
C、稀释浓硫酸要将浓硫酸沿烧杯内壁缓缓倒入水中,并用玻璃棒不断搅拌,C错误;
D、取用固体药品要用药匙,不能直接用手碰药品,D错误。
故选:B。
8.A
【详解】A、在氧气流中加热混合物,碳能和氧气反应生成二氧化碳气体,从而把氧化铜中的碳粉除去,选项正确;
B、装置是敞口的装置,碳酸钠和稀盐酸反应产生的二氧化碳从烧杯中逸出,总质量减少,不能验证质量守恒定律,选项错误;
C、将铁和铜分别加入到硫酸锌的溶液中,由于铁、铜不能置换出溶液中的锌,能得出锌的活动性大于铁、铜,但不能比较铁、铜的活动性,选项错误;
D、加水溶解,碳酸钙不溶于水,氧化钙和水反应会变成氢氧化钙,将原物质除去,不符合除杂原则,选项错误。
故选A。
9.B
【详解】A、SO2能和碱反应,所以只能用浓硫酸干燥;H2、O2是中性气体,所以既能用浓硫酸又能用碱石灰干燥,故选项错误;
B、CO、H2、CH4都是中性气体,所以既能用浓硫酸又能用碱石灰干燥,故选项正确;
C、HCl能和碱反应,所以只能用浓硫酸干燥;O2、CH4是中性气体,所以既能用浓硫酸又能用碱石灰干燥,故选项错误;
D、NH3能与浓硫酸反应,所以只能用碱石灰干燥;CO、CH4是中性气体,所以既能用浓硫酸又能用碱石灰干燥,故选项错误。
故选B。
10.C
【详解】A、若不慎将燃着的酒精灯碰倒,洒出的酒精在桌上燃烧,应立刻用湿抹布扑盖,既可降低温度,还能隔绝氧气,从而达到灭火的目的,正确;
B、若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液,利用中和反应将粘在皮肤上的烧碱溶液反应掉,正确;
C、若不慎将腐蚀性药液溅入眼睛,要先立即用水冲洗,再不断眨眼睛,错误;
D、若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液,正确;
故选C。
11.正确
【详解】NaOH和Ca(OH)2都属于碱,化学性质相似,因为在水中解离出的阴离子都是OH﹣,正确。
12.正确
【详解】澄清石灰水溶液显碱性,能使酚酞实验变红色;食盐溶液不能酚酞试液变色,能区别;正确。
13.错误
【详解】向紫色石蕊溶液中通入CO2,二氧化碳与水反应生成碳酸,碳酸使紫色石蕊试液变红,不能说明CO2呈酸性,故错误。
14.错误
【详解】浓硫酸具有吸水性且不与二氧化碳反应,所以可以用于干燥二氧化碳,但浓盐酸具有极强的挥发性,不能用于干燥二氧化碳,故此题判断为错误。
15.错误
【详解】氢氧化钠溶液成碱性,能使酚酞试剂变红色,但是氢氧化铜不溶于水,不能形成碱性溶液,不能使无色酚酞变红,故该说法错误。
16.(1)氢氧化钡和碳酸钠溶液反应生成了氢氧化钠,同时加入的氢氧化钡溶液过量,都会干扰原物质中氢氧化钠的检验
(2)将小匡同学实验中的氢氧化钡溶液换为氯化钡溶液,若滴加酚酞后溶液仍变红,则猜想三成立,若溶液未变红,则猜想二成立(合理即可)
【详解】(1)氢氧化钡和碳酸钠溶液反应生成了氢氧化钠,同时加入的氢氧化钡溶液过量,都能使酚酞变红,都会干扰原物质中氢氧化钠的检验,无法确定原物质中是否含有氢氧化钠;
(2)将小匡同学实验中的氢氧化钡溶液换为氯化钡溶液,加入过量氯化钡溶液后,产生白色沉淀,再取上层清液,滴加几滴酚酞溶液,若滴加酚酞后溶液仍变红,则猜想三成立,若溶液未变红,则猜想二成立(合理即可)。
17.(1)S、O
(2)形成酸雨
(3)
(4)解:设至少需要加入生石灰的质量为x
答:至少需要加入生石灰的质量是14t。
【详解】(1)吸收二氧化硫的反应中,二氧化硫中硫元素的化合价从+4变成+6,氧元素的化合价从0变成-2,则有化合价变化的元素是S、O,故填:S、O;
(2)煤中硫燃烧产生的SO2大量排放到空气中会产生的环境问题是形成酸雨,故填:形成酸雨;
(3)石灰作干燥剂是生石灰能与空气中的水反应生成氢氧化钙,方程式为:
(4)见答案。
18.(1)b
(2) 80 等于
(3) 297.0 溶液中H2SO4的质量=40g×24.5%=9.8g
解:设生成氢气的质量为,
解得
答:生成氢气的质量为0.2g。
【详解】(1)稀释浓硫酸时,将浓硫酸沿器壁缓慢注入水中,并用玻璃棒不断搅拌,故填:b;
(2)①由图可知,t2℃时,甲物质的溶解度是80g,故填:80;
②t2℃时,将质量相等的甲、乙的饱和溶液分别降温到t1℃,甲、乙的溶解度都减小,溶液仍为饱和溶液,甲、乙的溶解度相等,根据饱和溶液溶质质量分数公式,可知两种溶液的溶质质量分数相同,故填:相等;
(3)①溶液稀释前后溶质的质量不变,50mL溶质质量分数为98%的浓H2SO4溶液的质量=50mL×1.98g/cm3=99g,
解:设加入水的质量为,
解得
需加水的体积=,故填:297.0
②见答案。
答案第1页,共2页
答案第1页,共2页
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.下列除杂所选用的试剂中,正确的是
物质 所含杂质 除杂试剂
A 铁粉 铜粉 稀盐酸
B CO CO2 浓H2SO4
C CO2 CO 灼热的CuO
D FeSO4溶液 CuSO4溶液 加入锌后过滤
A.A B.B C.C D.D
2.下列鉴别物质的试剂,不正确的是
序号 待鉴别的物质 鉴别试剂
A 蒸馏水与过氧化氢溶液 二氧化锰
B 硝酸铵与食盐固体 水
C 稀盐酸与氯化钠溶液 酚酞溶液
D 一氧化碳与二氧化碳气体 澄清的石灰水
A.A B.B C.C D.D
3.下列实验操作正确的是
A.检查装置气密性 B.称量粗盐
C.过滤 D.浓硫酸稀释
4.如图所示装置气密性良好、要使注射器中的活塞向右移动,使用的液体M和固体N可能是①稀盐酸和石灰石;②稀硫酸和锌;③水和生石灰;④水和氯化钠。
A.①②③④ B.①②③
C.①②④ D.②③④
5.下列由于发生化学反应而使溶液质量变大的是( )
A.浓盐酸 B.浓硫酸 C.澄清石灰水 D.氢氧化钠溶液
6.常温分别将1克下列固体与99克水充分反应混和,所得溶液的溶质质量分数由小到大的顺序是:①CuSO4·5H2O;②Na2O;③KNO3;④CaO
A.①②③④ B.④③②① C.④①③② D.①③②④
7.下列实验操作中,正确的是
A.干燥气体 B.倾倒液体
C.稀释浓硫酸 D.取用固体
8.下列各组实验方法能达到实验目的的是
选项 实验目的 实验操作
A 除去氧化铜中混有的炭粉 在氧气流中充分加热混合物
B 验证质量守恒定律 碳酸钠和稀盐酸在敞口容器中反应
C 探究锌、铁、铜的金属活动性顺序 将铜丝、铁丝分别插入硫酸锌溶液中
D 除去氧化钙中混有的少量碳酸钙 加水溶解、过滤、洗涤、干燥
A.A B.B C.C D.D
9.下列各组中的气体,既可用浓H2SO4干燥,又可以用碱石灰干燥的一组是
A.H2、O2、SO2 B.CO、H2、CH4 C.O2、HCl、CH4 D.CO、CH4、NH3
10.下列对实验意外事故的处理错误的是
A.若不慎将燃着的酒精灯碰倒,洒出的酒精在桌上燃烧,应立刻用湿抹布扑盖
B.若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液
C.若不慎将腐蚀性药液溅入眼睛,要先用手揉眼睛,再立即用水冲洗
D.若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液
二、判断题
11.NaOH和Ca(OH)2化学性质相似,因为在水中解离出的阴离子都是OH﹣( )
12.用无色酚酞溶液可以区分开澄清石灰水和食盐溶液( )
13.向紫色石蕊溶液中通入CO2,溶液变红,说明CO2呈酸性( )
14.浓硫酸可用于干燥二氧化碳,所以浓盐酸也可用于干燥二氧化碳( )
15.因为NaOH能使无色酚酞变红,所以Cu(OH)2也能使无色酚酞变红( )
三、综合应用题
16.小匡在实验室做酸碱盐的性质实验时发现,一瓶标注氢氧化钠溶液的试剂瓶是敞口放置的。为了检验这瓶氢氧化钠溶液是否变质,小匡与同组的小胡同学共同探究:
他们依据所学的化学知识,对这瓶溶液的成分作了如下猜想:
猜想一:可能是NaOH溶液:
猜想二:可能是Na2CO3溶液:
猜想三:可能是NaOH和Na2CO3的混合溶液。
【查阅资料得知】:Na2CO3溶液能使酚酞溶液变红,CaC12溶液、BaC12溶液呈中性、氢氧化钡溶液呈碱性。
【实验验证及结论】
小匡同学取适量的该溶液,加入过量氢氧化钡溶液,充分反应后静置,观察到有白色沉淀产生,静置,向上层清液中滴加酚酞溶液,溶液变红,得出猜想三成立。
(1)小胡同学认为小匡同学的实验不能得出相应的结论,理由是 。
(2)请你在小匡同学实验的基础上,设计出能够验证猜想三成立的实验方案 。
17.煤燃烧生成的SO2污染环境,某工厂采用烟气脱硫工艺消除SO2,并将其转化为化工原料CaSO4,实现“变废为宝”,反应为。
(1)吸收二氧化硫的反应前后有化合价发生变化的元素是 (填元素符号)。
(2)SO2大量排放产生的环境问题是 。
(3)CaO,俗称生石灰。不仅可以用于燃煤脱硫,还可以用来作干燥剂,用生石灰作干燥剂的原理是 。(用化学方程式表示)
(4)根据化学方程式计算,若煤厂要处理16吨二氧化硫,至少需要加入生石灰的质量是多少?
18.水和溶液在生产、生活中具有广泛的用途。
(1)实验室稀释浓硫酸的正确操作顺序是 (填字母),并用玻璃棒不断搅拌。
a.将水沿器壁缓慢注入浓硫酸中 b.将浓硫酸沿器壁缓慢注入水中
(2)甲、乙两种不含结晶水的固体物质的溶解度曲线如图所示。
①t2℃时,甲物质的溶解度是 g。
②t2℃时,将质量相等的甲、乙的饱和溶液分别降温到t1℃,得到的两种溶液中溶质的质量分数相比,甲 乙(填“大于”、“小于”或“等于”)。
(3)实验室稀释浓硫酸。
①将50mL溶质质量分数为98%的浓H2SO4,加水稀释为质量分数为24.5%的稀H2SO4.已知所用溶质质量分数为98%的浓H2SO4密度为1.98g/cm3;水的密度为1g/cm3,则需加水的体积是 mL(计算结果保留一位小数)。
②取40g溶质质量分数为24.5%的稀H2SO4和足量的锌,完全反应后,生成氢气的质量是 ?(利用化学方程式进行计算,并在答题卡上写出完整计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
【详解】A、铁粉能与稀盐酸反应生成氯化亚铁和氢气,铜不与稀盐酸反应,反而会把原物质除去,不符合除杂原则,故A不符合题意;
B、二氧化碳不能与浓硫酸反应,不能除去杂质,不符合除杂原则,故B不符合题意;
C、CO能与灼热的氧化铜反应生成铜和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,故C符合题意;
D、锌与FeSO4和CuSO4均能发生反应,不符合除杂原则,故D不符合题意。
故选C。
2.C
【详解】A、鉴别蒸馏水与过氧化氢溶液,加入二氧化锰,有气泡产生是过氧化氢溶液,无现象的是蒸馏水,可以鉴别开来,该选项不符合题意;
B、鉴别硝酸铵与食盐固体,加水,温度会降低的为硝酸铵,温度不变的是食盐固体,可以鉴别开来,该选项不符合题意;
C、无色酚酞溶液遇碱(碱性)溶液变红,而稀盐酸显酸性,氯化钠溶液显中性,都不能使无色酚酞溶液变红,故无法鉴别开来,该选项符合题意;
D、鉴别一氧化碳与二氧化碳气体,因为二氧化能使澄清的石灰水变浑浊,故可用澄清的石灰水鉴别一氧化碳与二氧化碳气体,该选项不符合题意。
故选C。
3.A
【详解】A、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气,图中所示操作正确;
B、托盘天平的使用要遵循“左物右码”的原则,图中所示砝码与药品位置放反了,图中所示操作错误;
C、过滤液体时,要注意“一贴、二低、三靠”的原则,图中缺少玻璃棒引流,且漏斗下端没有紧靠在烧杯内壁上,图中所示操作错误;
D、稀释浓硫酸时,要把浓硫酸缓缓地沿器壁注入水中,同时用玻璃棒不断搅拌,以使热量及时的扩散,一定不能把水注入浓硫酸中,图中所示操作错误。
故选A。
4.B
【分析】注射器中的活塞向右移动,是瓶内压强变大,可能是反应生成气体,也可能是反应放热或溶解放热。
【详解】①稀盐酸和石灰石反应生成二氧化碳气体,使得瓶内压强变大,导致注射器中的活塞向右移动;②稀硫酸和锌反应生成气体,瓶内气体增多,使得瓶内压强变大,导致注射器中的活塞向右移动;③水和生石灰反应放热,瓶内温度升高,使得瓶内压强变大,导致注射器中的活塞向右移动;④氯化钠溶于水温度变化不明显,瓶内压强无明显变化,注射器中的活塞不会发生移动。故选B。
5.D
【详解】A、浓盐酸具有挥发性,露置在空气中会使其质量减少,故选项错误。
B、浓硫酸具有吸水性,放置在空气中会吸收空气中的水分,使其质量增加,但发生的是物理变化,故选项错误。
C、澄清石灰水与空气中的二氧化碳发生化学反应,生成碳酸钙沉淀,导致溶液质量减小,故选项错误。
D、氢氧化钠溶液敞口露置在空气中,能与空气中的二氧化碳发生化学反应生成碳酸钠和水,发生了化学变化导致溶液质量增加,故选项正确。
故选:D。
【点睛】掌握常见的酸碱盐的物理性质与化学性质、在空气中的质量变化等是正确解答此类题的关键。
6.C
【详解】根据①CuSO4·5H2O溶于水后,会失去结晶水,则最终得到的溶质硫酸铜质量小于1g;②Na2O会与水反应生成氢氧化钠,则形成的溶液中溶质是氢氧化钠,根据质量守恒定律,氢氧化钠的质量大于氧化钠的质量即大于1g;③KNO3溶于水溶质即硝酸钾1g;④CaO会与水反应生成氢氧化钙,但氢氧化钙属于微溶物,因此溶解的氢氧化钙质量在这四种物质中最少;故所得的溶液中溶质质量分数有小到大的顺序是④CaO<①CuSO4·5H2O<③KNO3<②Na2O,故选:C
7.B
【详解】A、气体从长导管进气能接触到浓硫酸,除去气体中的水蒸气,A错误;
B、倾倒液体要注意瓶塞倒放、标签冲向手心、试剂瓶口紧贴容器口,B正确;
C、稀释浓硫酸要将浓硫酸沿烧杯内壁缓缓倒入水中,并用玻璃棒不断搅拌,C错误;
D、取用固体药品要用药匙,不能直接用手碰药品,D错误。
故选:B。
8.A
【详解】A、在氧气流中加热混合物,碳能和氧气反应生成二氧化碳气体,从而把氧化铜中的碳粉除去,选项正确;
B、装置是敞口的装置,碳酸钠和稀盐酸反应产生的二氧化碳从烧杯中逸出,总质量减少,不能验证质量守恒定律,选项错误;
C、将铁和铜分别加入到硫酸锌的溶液中,由于铁、铜不能置换出溶液中的锌,能得出锌的活动性大于铁、铜,但不能比较铁、铜的活动性,选项错误;
D、加水溶解,碳酸钙不溶于水,氧化钙和水反应会变成氢氧化钙,将原物质除去,不符合除杂原则,选项错误。
故选A。
9.B
【详解】A、SO2能和碱反应,所以只能用浓硫酸干燥;H2、O2是中性气体,所以既能用浓硫酸又能用碱石灰干燥,故选项错误;
B、CO、H2、CH4都是中性气体,所以既能用浓硫酸又能用碱石灰干燥,故选项正确;
C、HCl能和碱反应,所以只能用浓硫酸干燥;O2、CH4是中性气体,所以既能用浓硫酸又能用碱石灰干燥,故选项错误;
D、NH3能与浓硫酸反应,所以只能用碱石灰干燥;CO、CH4是中性气体,所以既能用浓硫酸又能用碱石灰干燥,故选项错误。
故选B。
10.C
【详解】A、若不慎将燃着的酒精灯碰倒,洒出的酒精在桌上燃烧,应立刻用湿抹布扑盖,既可降低温度,还能隔绝氧气,从而达到灭火的目的,正确;
B、若不慎将烧碱溶液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液,利用中和反应将粘在皮肤上的烧碱溶液反应掉,正确;
C、若不慎将腐蚀性药液溅入眼睛,要先立即用水冲洗,再不断眨眼睛,错误;
D、若不慎将浓硫酸沾到皮肤上,应立即用大量水冲洗,然后涂上3%~5%的碳酸氢钠溶液,正确;
故选C。
11.正确
【详解】NaOH和Ca(OH)2都属于碱,化学性质相似,因为在水中解离出的阴离子都是OH﹣,正确。
12.正确
【详解】澄清石灰水溶液显碱性,能使酚酞实验变红色;食盐溶液不能酚酞试液变色,能区别;正确。
13.错误
【详解】向紫色石蕊溶液中通入CO2,二氧化碳与水反应生成碳酸,碳酸使紫色石蕊试液变红,不能说明CO2呈酸性,故错误。
14.错误
【详解】浓硫酸具有吸水性且不与二氧化碳反应,所以可以用于干燥二氧化碳,但浓盐酸具有极强的挥发性,不能用于干燥二氧化碳,故此题判断为错误。
15.错误
【详解】氢氧化钠溶液成碱性,能使酚酞试剂变红色,但是氢氧化铜不溶于水,不能形成碱性溶液,不能使无色酚酞变红,故该说法错误。
16.(1)氢氧化钡和碳酸钠溶液反应生成了氢氧化钠,同时加入的氢氧化钡溶液过量,都会干扰原物质中氢氧化钠的检验
(2)将小匡同学实验中的氢氧化钡溶液换为氯化钡溶液,若滴加酚酞后溶液仍变红,则猜想三成立,若溶液未变红,则猜想二成立(合理即可)
【详解】(1)氢氧化钡和碳酸钠溶液反应生成了氢氧化钠,同时加入的氢氧化钡溶液过量,都能使酚酞变红,都会干扰原物质中氢氧化钠的检验,无法确定原物质中是否含有氢氧化钠;
(2)将小匡同学实验中的氢氧化钡溶液换为氯化钡溶液,加入过量氯化钡溶液后,产生白色沉淀,再取上层清液,滴加几滴酚酞溶液,若滴加酚酞后溶液仍变红,则猜想三成立,若溶液未变红,则猜想二成立(合理即可)。
17.(1)S、O
(2)形成酸雨
(3)
(4)解:设至少需要加入生石灰的质量为x
答:至少需要加入生石灰的质量是14t。
【详解】(1)吸收二氧化硫的反应中,二氧化硫中硫元素的化合价从+4变成+6,氧元素的化合价从0变成-2,则有化合价变化的元素是S、O,故填:S、O;
(2)煤中硫燃烧产生的SO2大量排放到空气中会产生的环境问题是形成酸雨,故填:形成酸雨;
(3)石灰作干燥剂是生石灰能与空气中的水反应生成氢氧化钙,方程式为:
(4)见答案。
18.(1)b
(2) 80 等于
(3) 297.0 溶液中H2SO4的质量=40g×24.5%=9.8g
解:设生成氢气的质量为,
解得
答:生成氢气的质量为0.2g。
【详解】(1)稀释浓硫酸时,将浓硫酸沿器壁缓慢注入水中,并用玻璃棒不断搅拌,故填:b;
(2)①由图可知,t2℃时,甲物质的溶解度是80g,故填:80;
②t2℃时,将质量相等的甲、乙的饱和溶液分别降温到t1℃,甲、乙的溶解度都减小,溶液仍为饱和溶液,甲、乙的溶解度相等,根据饱和溶液溶质质量分数公式,可知两种溶液的溶质质量分数相同,故填:相等;
(3)①溶液稀释前后溶质的质量不变,50mL溶质质量分数为98%的浓H2SO4溶液的质量=50mL×1.98g/cm3=99g,
解:设加入水的质量为,
解得
需加水的体积=,故填:297.0
②见答案。
答案第1页,共2页
答案第1页,共2页
同课章节目录
