专题四 电化学 主观题突破 电极反应式书写及电化学计算(共29张PPT)-2024年高考化学二轮复习
文档属性
| 名称 | 专题四 电化学 主观题突破 电极反应式书写及电化学计算(共29张PPT)-2024年高考化学二轮复习 |  | |
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-11 22:04:45 | ||
图片预览




文档简介
(共29张PPT)
电极反应式书写及电化学计算
主观题突破
真题演练
01
1
2
3
4
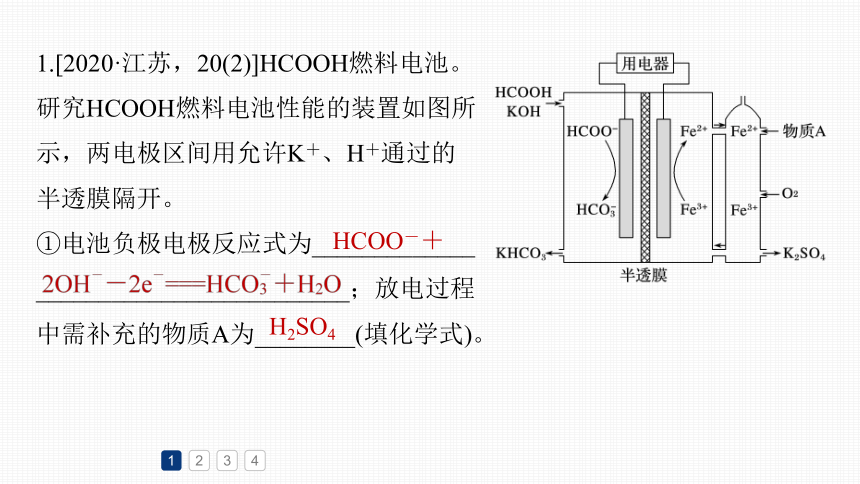
1.[2020·江苏,20(2)]HCOOH燃料电池。
研究HCOOH燃料电池性能的装置如图所
示,两电极区间用允许K+、H+通过的
半透膜隔开。
①电池负极电极反应式为_____________
_________________________;放电过程
中需补充的物质A为________(填化学式)。
HCOO-+
H2SO4
1
2
3
4
1
2
3
4
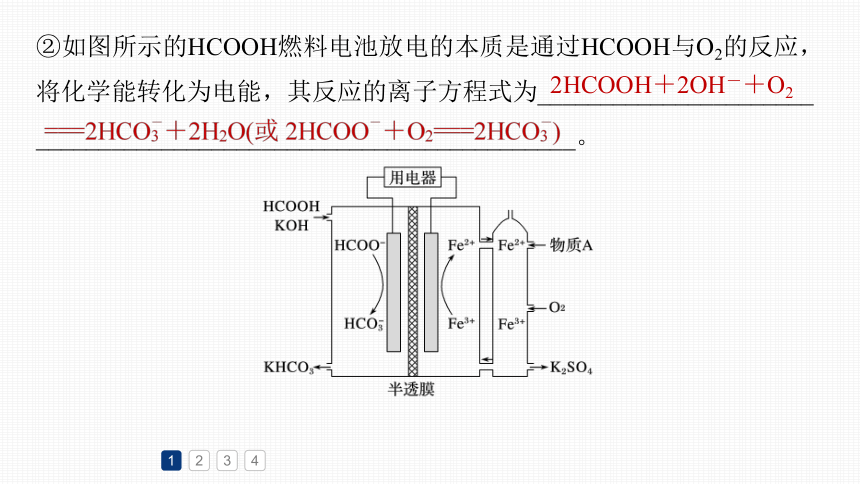
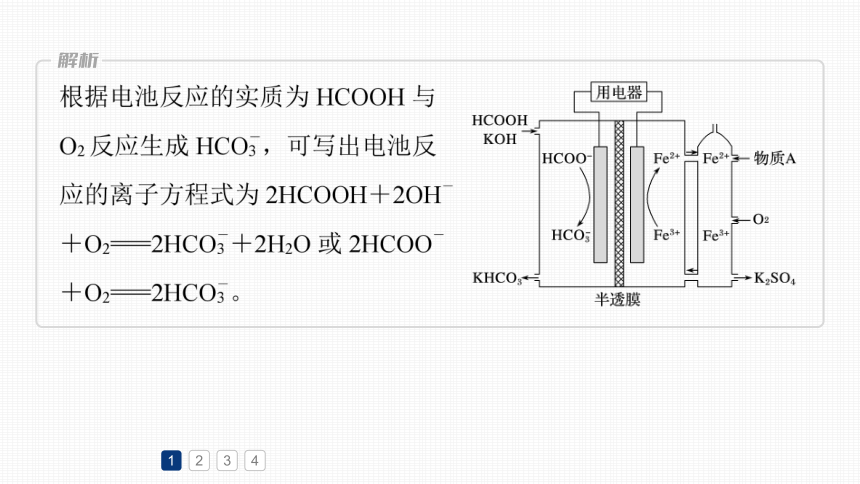
②如图所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为______________________
___________________________________________。
2HCOOH+2OH-+O2
1
2
3
4
1
2
3
4
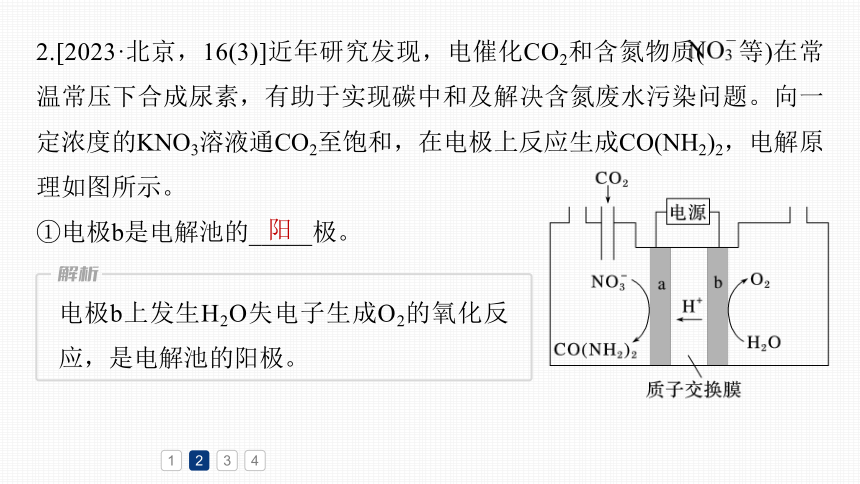
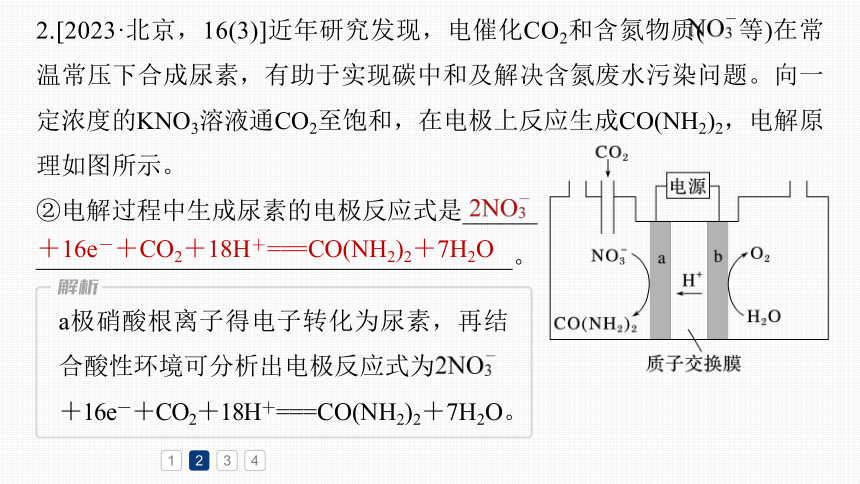
2.[2023·北京,16(3)]近年研究发现,电催化CO2和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示。
①电极b是电解池的_____极。
阳
电极b上发生H2O失电子生成O2的氧化反应,是电解池的阳极。
1
2
3
4
2.[2023·北京,16(3)]近年研究发现,电催化CO2和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示。
②电解过程中生成尿素的电极反应式是______
______________________________________。
+16e-+CO2+18H+===CO(NH2)2+7H2O
a极硝酸根离子得电子转化为尿素,再结合酸性环境可分析出电极反应式为
+16e-+CO2+18H+===CO(NH2)2+7H2O。
1
2
3
4
3.[2021·湖南,16(4)(5)]氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法Ⅱ.氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图
所示。
(4)电解过程中OH-的移动方向为__________(填“从左往右”或“从右往左”)。
从右往左
由图可知,通NH3的一极氮元素化合价升高,发生氧化反应,为电解池的阳极,则另一电极为阴极,电解过程中OH-移向阳极,则从右往左移动。
1
2
3
4
1
2
3
4
(5)阳极的电极反应式为_______________________
___________。
2NH3-6e-+6OH-===
N2+6H2O
阳极NH3失电子发生氧化反应生成N2,结合碱性条件,电极反应式为2NH3-6e-+6OH-===N2+6H2O。
1
2
3
4
4.[2021·山东,17(4)]利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应的化学方程式为4Na2CrO4+4H2O
2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在____(填“阴”或“阳”)极室制得,电解时通过膜的离子主要为_______。
阳
Na+
考向预测
02
1
2
3
4
5
6
1.(2023·江苏省百校高三下学期第三次联考)近年来,生物电催化技术运用微生物电解池实现了CO2的甲烷化,其工作原理如图所示。
(1)微生物电解池实现CO2甲烷化的阴极电极反应式为______________________________。
CO2+8H++8e-===CH4+2H2O
由图可知,CO2在阴极得电子生成CH4,根据得失电子守恒和电荷守恒配平电极反应式:CO2+8H++8e-===CH4+2H2O。
1
2
3
4
5
6
标准状况下112 m3 CH4的物质的量为 =5×103 mol,由
电极反应式CO2+8H++8e-===CH4+2H2O可知转移电子5×103 mol×
8=4×104 mol。
1
2
3
4
5
6
(2)如果处理有机物[(CH2O)n]产生标准状况下112 m3 CH4,则理论上导线中通过电子的物质的量为____________。
4×104 mol
标准状况下112 m3 CH4的物质的量为 =5×103 mol,由
电极反应式CO2+8H++8e-===CH4+2H2O可知转移电子5×103 mol×
8=4×104 mol。
1
2
3
4
5
6
2.(2023·海安高级中学高三下学期3月月考)含苯乙烯的废水会对环境造成严重的污染,可采用电解法进行处理,其工作原理如图(电解液是含苯乙烯和硫酸的废水,pH=6.2),已知:·OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。
若电路中通过10 mol电子,则有_____ g苯乙烯被羟基自由基完全氧化成CO2和H2O。
26
1
2
3
4
5
6
苯乙烯被羟基自由基完全氧化成CO2和H2O的关系式为
C8H8~8CO2~40e-
104 g 40 mol
m 10 mol,解得m=26 g。
1
2
3
4
5
6
3.(2023·海安高级中学高三下学期阶段考试)用电解法可将CO2转化为多种燃料,原理如图所示。
若阴极只生成CO、HCOOH、C2H4,且各产物的生成速率相同,则相同条件下,Pt电极上产生的O2与Cu电极上产生的C2H4的体积比为______。
4∶1
1
2
3
4
5
6
设阴极生成CO、HCOOH、C2H4的物质的量各为1 mol,则阴极共得到电子的物质的量为2 mol+2 mol+6 mol×2=16 mol,则相同条件下,Pt电极上OH-失电子产生的O2的物质的量为 =4 mol,相同条件下,Pt电极上产生的O2与Cu电极上产生的C2H4的体积比为4∶1。
1
2
3
4
5
6
4.(2023·海安高级中学高三下学期模拟)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示,若生成的乙烯和乙烷的物质的量之比为1∶1,则阳极的电极反应式为_______________________________________。
4CH4+3O2--6e-===C2H4+C2H6+3H2O
1
2
3
4
5
6
由图可知,电极B为电解池的阳极,甲烷在阳极失去电子与O2-发生氧化反应生成乙烯、乙烷和水,电极反应式为4CH4+3O2--6e-===C2H4+C2H6+3H2O。
1
2
3
4
5
6
5.(2023·淮阴中学高三下学期一模)含氮化合物(NOx、 等)是环境污染物,可用三维电极法消除其污染。
它是在传统的电解槽两电极之间填充粒状或碎
屑状材料,填充的粒子电极表面能带电,成为
新的一极(第三极)。如图为用三维电极法处理
氨氮废水的原理图,石墨板作为阴、阳极,自
制活性炭为填充材料,电解一定浓度的
(NH4)2SO4、NH4Cl与NaCl的酸性混合溶液来
进行模拟。
1
2
3
4
5
6
(1)该装置可以生成大量氧化性更强的·OH,
·OH去除 的离子方程式为____________
_____________________。
===N2↑+6H2O+2H+
1
2
3
4
5
6
(2)相比于传统的二维电极反应系统,三维电极的优点有______________
_________________________________________________________________________________。
率;能耗低,能降低运行成本;粒子电极表面会生成许多强氧化性物质,提高了氧化效率
提高了电流效
相比于传统的二维电极反应系统,三维电极的电极比表面积增大,提高了电流效率;三维电极能耗低,能降低运行成本,粒子电极表面会生成许多强氧化活性物质,提高了催化效率,没有电催化氧化对阳极的严格要求。
1
2
3
4
5
6
6.(2023·江苏省决胜新高考高三下学期大联考)电解氧化吸收法可以消除氮氧化物污染:其原理如图所示。从A口出来的物质是_______________。电解池阴极的电极反应式为_________________________________。
O2和较浓的硫酸
1
2
3
4
5
6
1
2
3
4
5
6
则阳极室的硫酸浓度会变大,故从A口中出来的物质是O2和较浓的硫酸;
本课结束
电极反应式书写及电化学计算
主观题突破
真题演练
01
1
2
3
4
1.[2020·江苏,20(2)]HCOOH燃料电池。
研究HCOOH燃料电池性能的装置如图所
示,两电极区间用允许K+、H+通过的
半透膜隔开。
①电池负极电极反应式为_____________
_________________________;放电过程
中需补充的物质A为________(填化学式)。
HCOO-+
H2SO4
1
2
3
4
1
2
3
4
②如图所示的HCOOH燃料电池放电的本质是通过HCOOH与O2的反应,将化学能转化为电能,其反应的离子方程式为______________________
___________________________________________。
2HCOOH+2OH-+O2
1
2
3
4
1
2
3
4
2.[2023·北京,16(3)]近年研究发现,电催化CO2和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示。
①电极b是电解池的_____极。
阳
电极b上发生H2O失电子生成O2的氧化反应,是电解池的阳极。
1
2
3
4
2.[2023·北京,16(3)]近年研究发现,电催化CO2和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含氮废水污染问题。向一定浓度的KNO3溶液通CO2至饱和,在电极上反应生成CO(NH2)2,电解原理如图所示。
②电解过程中生成尿素的电极反应式是______
______________________________________。
+16e-+CO2+18H+===CO(NH2)2+7H2O
a极硝酸根离子得电子转化为尿素,再结合酸性环境可分析出电极反应式为
+16e-+CO2+18H+===CO(NH2)2+7H2O。
1
2
3
4
3.[2021·湖南,16(4)(5)]氨气中氢含量高,是一种优良的小分子储氢载体,且安全、易储运,可通过下面两种方法由氨气得到氢气。
方法Ⅱ.氨电解法制氢气
利用电解原理,将氨转化为高纯氢气,其装置如图
所示。
(4)电解过程中OH-的移动方向为__________(填“从左往右”或“从右往左”)。
从右往左
由图可知,通NH3的一极氮元素化合价升高,发生氧化反应,为电解池的阳极,则另一电极为阴极,电解过程中OH-移向阳极,则从右往左移动。
1
2
3
4
1
2
3
4
(5)阳极的电极反应式为_______________________
___________。
2NH3-6e-+6OH-===
N2+6H2O
阳极NH3失电子发生氧化反应生成N2,结合碱性条件,电极反应式为2NH3-6e-+6OH-===N2+6H2O。
1
2
3
4
4.[2021·山东,17(4)]利用膜电解技术(装置如图所示),以Na2CrO4为主要原料制备Na2Cr2O7的总反应的化学方程式为4Na2CrO4+4H2O
2Na2Cr2O7+4NaOH+2H2↑+O2↑。则Na2Cr2O7在____(填“阴”或“阳”)极室制得,电解时通过膜的离子主要为_______。
阳
Na+
考向预测
02
1
2
3
4
5
6
1.(2023·江苏省百校高三下学期第三次联考)近年来,生物电催化技术运用微生物电解池实现了CO2的甲烷化,其工作原理如图所示。
(1)微生物电解池实现CO2甲烷化的阴极电极反应式为______________________________。
CO2+8H++8e-===CH4+2H2O
由图可知,CO2在阴极得电子生成CH4,根据得失电子守恒和电荷守恒配平电极反应式:CO2+8H++8e-===CH4+2H2O。
1
2
3
4
5
6
标准状况下112 m3 CH4的物质的量为 =5×103 mol,由
电极反应式CO2+8H++8e-===CH4+2H2O可知转移电子5×103 mol×
8=4×104 mol。
1
2
3
4
5
6
(2)如果处理有机物[(CH2O)n]产生标准状况下112 m3 CH4,则理论上导线中通过电子的物质的量为____________。
4×104 mol
标准状况下112 m3 CH4的物质的量为 =5×103 mol,由
电极反应式CO2+8H++8e-===CH4+2H2O可知转移电子5×103 mol×
8=4×104 mol。
1
2
3
4
5
6
2.(2023·海安高级中学高三下学期3月月考)含苯乙烯的废水会对环境造成严重的污染,可采用电解法进行处理,其工作原理如图(电解液是含苯乙烯和硫酸的废水,pH=6.2),已知:·OH(羟基自由基)具有很强的氧化性,可以将苯乙烯氧化成CO2和H2O。
若电路中通过10 mol电子,则有_____ g苯乙烯被羟基自由基完全氧化成CO2和H2O。
26
1
2
3
4
5
6
苯乙烯被羟基自由基完全氧化成CO2和H2O的关系式为
C8H8~8CO2~40e-
104 g 40 mol
m 10 mol,解得m=26 g。
1
2
3
4
5
6
3.(2023·海安高级中学高三下学期阶段考试)用电解法可将CO2转化为多种燃料,原理如图所示。
若阴极只生成CO、HCOOH、C2H4,且各产物的生成速率相同,则相同条件下,Pt电极上产生的O2与Cu电极上产生的C2H4的体积比为______。
4∶1
1
2
3
4
5
6
设阴极生成CO、HCOOH、C2H4的物质的量各为1 mol,则阴极共得到电子的物质的量为2 mol+2 mol+6 mol×2=16 mol,则相同条件下,Pt电极上OH-失电子产生的O2的物质的量为 =4 mol,相同条件下,Pt电极上产生的O2与Cu电极上产生的C2H4的体积比为4∶1。
1
2
3
4
5
6
4.(2023·海安高级中学高三下学期模拟)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如图所示,若生成的乙烯和乙烷的物质的量之比为1∶1,则阳极的电极反应式为_______________________________________。
4CH4+3O2--6e-===C2H4+C2H6+3H2O
1
2
3
4
5
6
由图可知,电极B为电解池的阳极,甲烷在阳极失去电子与O2-发生氧化反应生成乙烯、乙烷和水,电极反应式为4CH4+3O2--6e-===C2H4+C2H6+3H2O。
1
2
3
4
5
6
5.(2023·淮阴中学高三下学期一模)含氮化合物(NOx、 等)是环境污染物,可用三维电极法消除其污染。
它是在传统的电解槽两电极之间填充粒状或碎
屑状材料,填充的粒子电极表面能带电,成为
新的一极(第三极)。如图为用三维电极法处理
氨氮废水的原理图,石墨板作为阴、阳极,自
制活性炭为填充材料,电解一定浓度的
(NH4)2SO4、NH4Cl与NaCl的酸性混合溶液来
进行模拟。
1
2
3
4
5
6
(1)该装置可以生成大量氧化性更强的·OH,
·OH去除 的离子方程式为____________
_____________________。
===N2↑+6H2O+2H+
1
2
3
4
5
6
(2)相比于传统的二维电极反应系统,三维电极的优点有______________
_________________________________________________________________________________。
率;能耗低,能降低运行成本;粒子电极表面会生成许多强氧化性物质,提高了氧化效率
提高了电流效
相比于传统的二维电极反应系统,三维电极的电极比表面积增大,提高了电流效率;三维电极能耗低,能降低运行成本,粒子电极表面会生成许多强氧化活性物质,提高了催化效率,没有电催化氧化对阳极的严格要求。
1
2
3
4
5
6
6.(2023·江苏省决胜新高考高三下学期大联考)电解氧化吸收法可以消除氮氧化物污染:其原理如图所示。从A口出来的物质是_______________。电解池阴极的电极反应式为_________________________________。
O2和较浓的硫酸
1
2
3
4
5
6
1
2
3
4
5
6
则阳极室的硫酸浓度会变大,故从A口中出来的物质是O2和较浓的硫酸;
本课结束
同课章节目录
