第十一单元盐化肥 单元训练题-2023-2024学年九年级化学人教版下册(含答案)
文档属性
| 名称 | 第十一单元盐化肥 单元训练题-2023-2024学年九年级化学人教版下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 701.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-12 00:00:00 | ||
图片预览




文档简介
第十一单元 盐 化肥 单元训练题
一、选择题
1.哈尔滨市的标志性建筑有很多,按时间段划分,每个时间节点都会有一个代表性的建筑。如图的龙塔也是哈尔滨的标志性建筑。下列有关叙述正确的是
A.建筑中用到的室内大理石地面的主要成分是氧化钙
B.建设过程中更多使用的是纯金属,纯金属性能一定比合金好
C.塔周围的铁制围栏表面进行了刷漆处理,主要是为了美观
D.红色涂料中含有的氧化铁,不属于金属材料
2.“化学扑克接龙”是学习化学的一种游戏,扑克牌面标注物质的化学式。其游戏规则是:当上家出牌时,下家跟出的牌所标注的物质必须能与上家的发生反应。某局游戏中,从甲到戊五个人各有一张不同的牌,牌面分别标注了“CuSO4”、“H2SO4”、“NaOH”、“Zn”、“Fe2O3”。若甲的牌为“Fe2O3”,且按甲→乙→丙→丁→戊依次出牌时都能满足“接龙”规则,下列说法正确的有
①乙一定是硫酸 ②丙一定是氢氧化钠 ③丁一定是CuSO4 ④戊可以是Zn
A.1个 B.2个 C.3个 D.4个
3.如表设计方案合理的是
选项 实验目的 设计方案(主要操作)
A 鉴别化肥K2SO4和KNO3 分别加水溶解
B 检验溶液中是否含有 取样,加入足量的稀盐酸
C 探究温度对分子运动速率的影响 分别向等体积冷水和热水中放入等量品红
D 去除粗盐中泥沙 加水溶解、蒸发
A.A B.B C.C D.D
4.生态文明建设是关系中华民族永续发展的根本大计,“绿水青山就是金山银山”是建设生态文明的重要理念,下列做法不符合该理念的是
A.工业废水经过处理达标后排放 B.施用大量农药减少植物病虫害
C.使用太阳能路灯,既节能又环保 D.生活垃圾分类回收,实现垃圾资源化
5.下图是利用海水提取粗盐过程图,下列说法正确的是
A.a 为蒸发池
B.在 b 中可以得到氯化钠的饱和溶液
C.海水晒盐主要是利用蒸发结晶的方法得到粗盐晶体
D.析出晶体后的母液为氯化钠的不饱和溶液
6.下列转化能实现且可以通过一步反应实现的是:①H2O2→H2;②H2→H2O;③ H2O→O2;④S→SO3⑤Fe→Cu;⑥NaOH→Cu(OH)2
A.①②③④⑤⑥ B.②③④⑤⑥ C.②③⑤⑥ D.②④⑤⑥
7.从海水得到的粗盐,往往含有可溶性杂质(主要有CaCl2、MgCl2、Na2SO4)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活.粗盐提纯的部分流程如下:
其中,滤液一至滤液二之间需进行三步操作:
操作①:加入过量的碳酸钠溶液,除去滤液中的Ca2+
操作②:加入过量的X,除去滤液中的Mg2+
操作③:加入过量的氯化钡溶液,除去滤液中的
加入试剂的顺序不正确的为
A.①②③ B.③①② C.③②① D.②③①
8.有一包均匀混合的Na2CO3和NaHCO3的固体粉末,为了测定其组成,小董同学称取不同质量的粉末样品溶于水,然后分别滴加相同浓度的稀盐酸100g,充分反应后记录生成CO2的质量与所取的混合固体质量关系如图所示。已知,向该混合物溶液滴加稀盐酸时,发生的化学反应分两步进行。第一步反应:。第二步反应:。根据图中信息,下列说法不正确的是
A.样品中碳酸钠的质量分数为55.8%
B.a点时所得溶液中的溶质为NaCl、Na2CO3、NaHCO3
C.14.25g样品中含NaHCO3的质量为6.3g
D.当固体样品质量为4.75g时,所取样品与100g稀盐酸恰好完全反应
9.甲、乙、丙均为初中化学常见的物质,它们之间相互关系如图所示(图中“—”表示相连的物质能相互反应,“→”表示一种物质可一步转化成另一种物质)。由此得出以下结论:
①甲、乙、丙必须含同种元素。
②图中所示关系均可通过置换反应实现。
③甲若是碱,丙只能是盐。
④丙若是氧化物,甲可以是单质或氧化物。
⑤甲、乙、丙可以是同一类别的物质(物质类别是指单质、氧化物、酸、碱、盐)。
其中正确的结论有
A.4个 B.3个 C.2个 D.1个
10.向一定质量和的混合溶液中逐滴加入溶质质量分数为10.0%的溶液。反应过程中加入的溶液的质量与产生沉淀或气体的质量关系如图所示,说法正确的是
A.图中段表示生成沉淀的过程 B.b点溶液中溶质有2种
C.x值为106.0 D.c点溶液的
11.关于化学上的归类不正确的是
选项 归类 物质
A 缓慢氧化 铁生锈、人的呼吸、食物腐败
B 黑色固体 氧化铜、四氧化三铁、二氧化锰
C 可以直接加热的仪器 试管、烧杯、蒸发皿
D 受热易分解的物质 碳酸氢铵、铜绿、高锰酸钾
A.A B.B C.C D.D
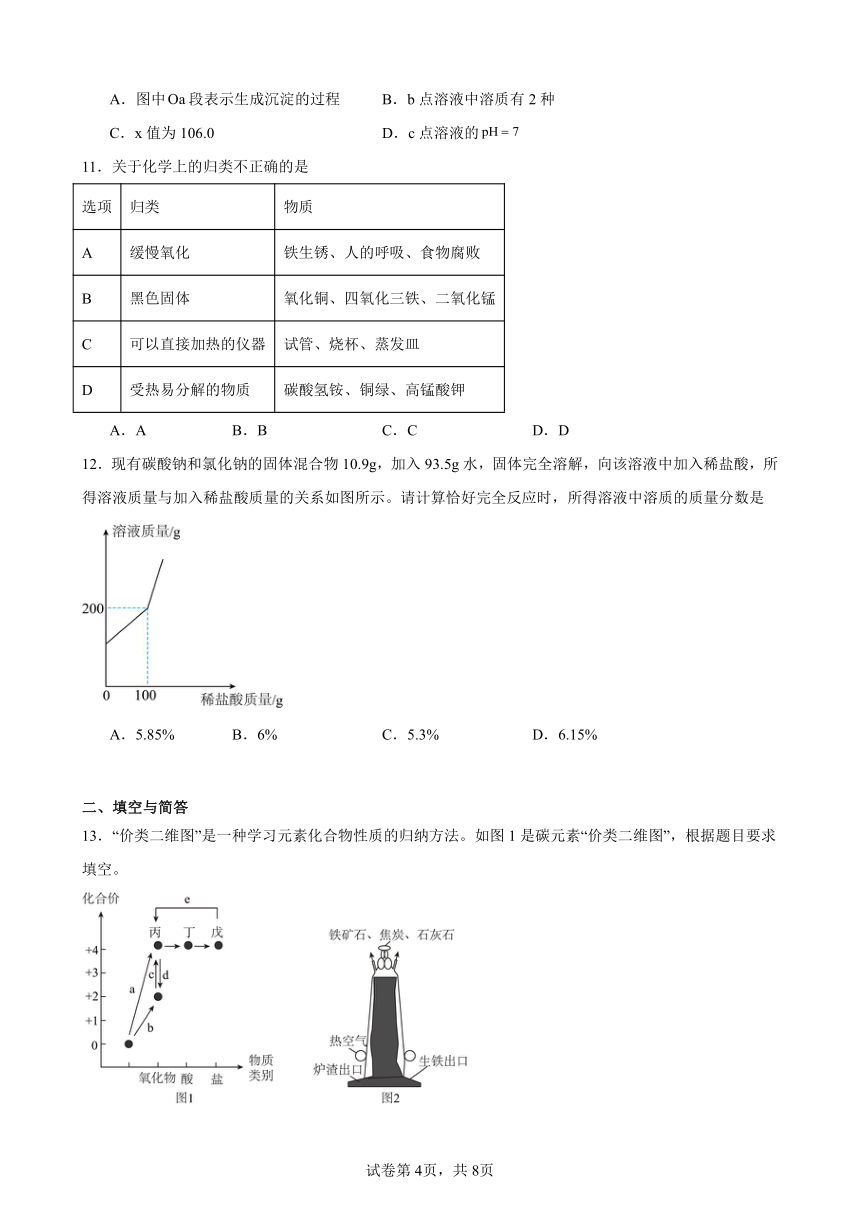
12.现有碳酸钠和氯化钠的固体混合物10.9g,加入93.5g水,固体完全溶解,向该溶液中加入稀盐酸,所得溶液质量与加入稀盐酸质量的关系如图所示。请计算恰好完全反应时,所得溶液中溶质的质量分数是
A.5.85% B.6% C.5.3% D.6.15%
二、填空与简答
13.“价类二维图”是一种学习元素化合物性质的归纳方法。如图1是碳元素“价类二维图”,根据题目要求填空。
(1)甲的物质类别是 。
(2)丁的化学式是 。
(3)图2炼铁高炉中,焦炭发生了反应:
①,该反应对应图1中的反应 。(填“a”或“b”)
②,该反应利用了碳的 性。
(4)炼铁高炉中,CO赤铁矿(主要成分是Fe2O3)反应生成铁,请写出反应的化学方程式: 。
(5)若戊是Na2CO3,可以与 反应转化为丙(反应e)。
14.“中国智慧”、“中国制造”誉满全球。首艘由我国自主建造的极地科学考察破冰船“雪龙2号”已于2019年上半年交付使用,执行我国极地考察任务。请回答相关问题。
(1)船体主要由钢板制成,钢板属于 (填“金属材料”或“合成材料”),船体表面涂有红色防护漆,其防锈原理是 。
(2)制造船舶所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出工业上用赤铁矿炼铁的化学方程式 。
(3)将一定质量的铁粉和铜粉的混合物加入到硝酸银和硝酸铝的混合溶液中,充分反应后过滤得到滤渣和滤液。往滤渣中滴加稀盐酸,无明显现象。则关于滤渣和滤液的说法正确的是 。
①滤渣中一定含有银和铜
②滤液中一定含有硝酸亚铁和硝酸铜
③滤渣中一定含有银
④滤液中滴加稀盐酸一定没有白色沉淀生成
⑤滤渣的质量一定比反应前铁粉和铜粉混合物的质量大
A.①③ B.③④⑤ C.③⑤ D.②④⑤
15.人类对氧化还原反应的认识过程中的三个阶段。
【阶段I】得失氧说:物质跟氧发生的反应叫氧化反应,含氧化合物中的氧被夺取的反应叫还原反应。
【阶段Ⅱ】化合价升降说:凡是出现元素化合价升降的化学反应都是氧化还原反应,化合价升高的反应叫氧化反应,化合价降低的反应叫还原反应。
【阶段Ⅲ】电子转移说:化合价升降的原因是电子的转移。凡有电子转移发生的化学反应都是氧化还原反应,失电子的反应叫氧化反应,得电子的反应叫还原反应。
(1)根据得失氧说,在 化学变化中,H2发生了 反应。
(2)电子转移是元素化合价改变的本质原因。 反应前后,化合价升高的元素是 ,说明该元素的原子得失电子情况为 。
(3)根据化合价升降说,化学反应的四种基本类型中,一定不属于氧化还原反应是 反应,写出该类型反应的一个化学方程式 。
(4)关于氧化还原反应的认识,下列理解错误的是______(填标号)。
A.氧化和还原是相互对立又辩证统一的关系
B.电子转移说是从微观视角来探析和建构氧化还原反应的概念
C.自然界中发生的氧化还原反应对人类的生活和生产都是有利的
16.酸、碱、盐在生产和生活中有着广泛的应用。
(1)氢氧化钙是一种生活中常见的碱,下列属于氢氧化钙用途的是_______(填标号)。
A.改良酸性土壤 B.配制波尔多液
C.治疗胃酸过多 D.刷墙、砌砖
(2)①碱溶液中都含有 (填离子符号),所以碱有一些相似的化学性质。
②如图所示,向稀氢氧化钠溶液中加入过量稀盐酸,充分反应后,所得溶液中溶质的成分为 (填化学式)。
(3)烧杯中盛有一定量的物质,向其中逐滴加入X溶液至过量,产生沉淀或气体的质量与加入的X溶液的质量关系如图所示。下列实验可用该图像表示的是 (填标号)。
选项 烧杯中盛放的物质 X溶液
A 表面锈蚀的铁制品 稀硫酸
B 氢氧化钠和氯化钡的混合溶液 稀硫酸
C 盐酸和氯化钙的混合溶液 硝酸银溶液
D 稀硫酸和硝酸铁的混合溶液 氢氧化钠溶液
(4)KNO3和NaCl的溶解度曲线如图所示,请回答下列问题:
①60℃时,向50g水中加入60gKNO3,充分溶解后,所得溶液的质量为 g。
②60℃时,分别将等质量的KNO3和NaC1的饱和溶液降温至20℃,所得溶液中溶剂质量大小关系为KNO3 NaCl(填“>”、“<”或“=”)。
③20℃时,KNO3的饱和溶液中溶质的质量分数为 (写出计算式即可)。
三、计算题
17.某化学兴趣小组的同学将一包氯化钠和碳酸钠的固体混合物,溶于75.1g水制成溶液,然后向其中加入溶质质量分数为10%的氯化钙溶液至恰好完全反应,生成沉淀10g,将滤液蒸干后得到固体25g。回答:
(1)写出上述反应的化学方程式 。
(2)试列出求解混合物中碳酸钠质量(x)的比例式 。
(3)原固体混合物中氯化钠的质量为 g。
(4)反应后所得滤液中溶质的质量分数为 。
(5)若配置10%的氯化钙溶液200g,需要向25%氯化钙溶液加水多少 g。
18.取氯化钙和盐酸的混合溶液 51.88g,逐滴滴加 10 .6%的碳酸钠溶液。所加入碳酸钠溶液的质量和混合溶液 pH变化关系如图所示 ,回答下列问题:
(1)BC段反应的化学方程式为 。
(2)D点所含有的物质 。
(3)计算充分反应至C点时所得溶液中溶质的质量分数(写出计算过程 ,计算结果精确至 0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.B
5.C
6.C
7.A
8.B
9.B
10.C
11.C
12.B
13.(1)单质
(2)H2CO3
(3) a 还原
(4)3
(5)稀盐酸
14.(1) 金属材料 隔绝水和氧气
(2)7
(3)C
15.(1)氧化
(2) Fe/铁元素 失去2个电子
(3) 复分解反应 NaOH+HCl=NaCl+H2O
(4)C
16.(1)ABD
(2) OH- NaCl、HCl
(3)AD
(4) 105 < ×100%
17.(1)
(2)
(3)13.3
(4)12.5%
(5)120
18.(1)
(2)氯化钠、碳酸钠
(3)解:设碳酸钠和盐酸反应生成的二氧化碳的质量为x,生成的氯化钠的质量为y;而碳酸钠和氯化钙反应生成的碳酸钙的质量为z,生成的氯化钠的质量为n。
解得:x=0.88g;y=2.34g
解得:z=1g;a=1.17g
C点时所得溶液中溶质的质量分数为 ≈4.4%
答:充分反应至C点时所得溶液中溶质的质量分数为4.4%。
答案第1页,共2页
答案第1页,共2页
一、选择题
1.哈尔滨市的标志性建筑有很多,按时间段划分,每个时间节点都会有一个代表性的建筑。如图的龙塔也是哈尔滨的标志性建筑。下列有关叙述正确的是
A.建筑中用到的室内大理石地面的主要成分是氧化钙
B.建设过程中更多使用的是纯金属,纯金属性能一定比合金好
C.塔周围的铁制围栏表面进行了刷漆处理,主要是为了美观
D.红色涂料中含有的氧化铁,不属于金属材料
2.“化学扑克接龙”是学习化学的一种游戏,扑克牌面标注物质的化学式。其游戏规则是:当上家出牌时,下家跟出的牌所标注的物质必须能与上家的发生反应。某局游戏中,从甲到戊五个人各有一张不同的牌,牌面分别标注了“CuSO4”、“H2SO4”、“NaOH”、“Zn”、“Fe2O3”。若甲的牌为“Fe2O3”,且按甲→乙→丙→丁→戊依次出牌时都能满足“接龙”规则,下列说法正确的有
①乙一定是硫酸 ②丙一定是氢氧化钠 ③丁一定是CuSO4 ④戊可以是Zn
A.1个 B.2个 C.3个 D.4个
3.如表设计方案合理的是
选项 实验目的 设计方案(主要操作)
A 鉴别化肥K2SO4和KNO3 分别加水溶解
B 检验溶液中是否含有 取样,加入足量的稀盐酸
C 探究温度对分子运动速率的影响 分别向等体积冷水和热水中放入等量品红
D 去除粗盐中泥沙 加水溶解、蒸发
A.A B.B C.C D.D
4.生态文明建设是关系中华民族永续发展的根本大计,“绿水青山就是金山银山”是建设生态文明的重要理念,下列做法不符合该理念的是
A.工业废水经过处理达标后排放 B.施用大量农药减少植物病虫害
C.使用太阳能路灯,既节能又环保 D.生活垃圾分类回收,实现垃圾资源化
5.下图是利用海水提取粗盐过程图,下列说法正确的是
A.a 为蒸发池
B.在 b 中可以得到氯化钠的饱和溶液
C.海水晒盐主要是利用蒸发结晶的方法得到粗盐晶体
D.析出晶体后的母液为氯化钠的不饱和溶液
6.下列转化能实现且可以通过一步反应实现的是:①H2O2→H2;②H2→H2O;③ H2O→O2;④S→SO3⑤Fe→Cu;⑥NaOH→Cu(OH)2
A.①②③④⑤⑥ B.②③④⑤⑥ C.②③⑤⑥ D.②④⑤⑥
7.从海水得到的粗盐,往往含有可溶性杂质(主要有CaCl2、MgCl2、Na2SO4)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活.粗盐提纯的部分流程如下:
其中,滤液一至滤液二之间需进行三步操作:
操作①:加入过量的碳酸钠溶液,除去滤液中的Ca2+
操作②:加入过量的X,除去滤液中的Mg2+
操作③:加入过量的氯化钡溶液,除去滤液中的
加入试剂的顺序不正确的为
A.①②③ B.③①② C.③②① D.②③①
8.有一包均匀混合的Na2CO3和NaHCO3的固体粉末,为了测定其组成,小董同学称取不同质量的粉末样品溶于水,然后分别滴加相同浓度的稀盐酸100g,充分反应后记录生成CO2的质量与所取的混合固体质量关系如图所示。已知,向该混合物溶液滴加稀盐酸时,发生的化学反应分两步进行。第一步反应:。第二步反应:。根据图中信息,下列说法不正确的是
A.样品中碳酸钠的质量分数为55.8%
B.a点时所得溶液中的溶质为NaCl、Na2CO3、NaHCO3
C.14.25g样品中含NaHCO3的质量为6.3g
D.当固体样品质量为4.75g时,所取样品与100g稀盐酸恰好完全反应
9.甲、乙、丙均为初中化学常见的物质,它们之间相互关系如图所示(图中“—”表示相连的物质能相互反应,“→”表示一种物质可一步转化成另一种物质)。由此得出以下结论:
①甲、乙、丙必须含同种元素。
②图中所示关系均可通过置换反应实现。
③甲若是碱,丙只能是盐。
④丙若是氧化物,甲可以是单质或氧化物。
⑤甲、乙、丙可以是同一类别的物质(物质类别是指单质、氧化物、酸、碱、盐)。
其中正确的结论有
A.4个 B.3个 C.2个 D.1个
10.向一定质量和的混合溶液中逐滴加入溶质质量分数为10.0%的溶液。反应过程中加入的溶液的质量与产生沉淀或气体的质量关系如图所示,说法正确的是
A.图中段表示生成沉淀的过程 B.b点溶液中溶质有2种
C.x值为106.0 D.c点溶液的
11.关于化学上的归类不正确的是
选项 归类 物质
A 缓慢氧化 铁生锈、人的呼吸、食物腐败
B 黑色固体 氧化铜、四氧化三铁、二氧化锰
C 可以直接加热的仪器 试管、烧杯、蒸发皿
D 受热易分解的物质 碳酸氢铵、铜绿、高锰酸钾
A.A B.B C.C D.D
12.现有碳酸钠和氯化钠的固体混合物10.9g,加入93.5g水,固体完全溶解,向该溶液中加入稀盐酸,所得溶液质量与加入稀盐酸质量的关系如图所示。请计算恰好完全反应时,所得溶液中溶质的质量分数是
A.5.85% B.6% C.5.3% D.6.15%
二、填空与简答
13.“价类二维图”是一种学习元素化合物性质的归纳方法。如图1是碳元素“价类二维图”,根据题目要求填空。
(1)甲的物质类别是 。
(2)丁的化学式是 。
(3)图2炼铁高炉中,焦炭发生了反应:
①,该反应对应图1中的反应 。(填“a”或“b”)
②,该反应利用了碳的 性。
(4)炼铁高炉中,CO赤铁矿(主要成分是Fe2O3)反应生成铁,请写出反应的化学方程式: 。
(5)若戊是Na2CO3,可以与 反应转化为丙(反应e)。
14.“中国智慧”、“中国制造”誉满全球。首艘由我国自主建造的极地科学考察破冰船“雪龙2号”已于2019年上半年交付使用,执行我国极地考察任务。请回答相关问题。
(1)船体主要由钢板制成,钢板属于 (填“金属材料”或“合成材料”),船体表面涂有红色防护漆,其防锈原理是 。
(2)制造船舶所需的大量钢铁是以铁矿石为主要原料冶炼而得。写出工业上用赤铁矿炼铁的化学方程式 。
(3)将一定质量的铁粉和铜粉的混合物加入到硝酸银和硝酸铝的混合溶液中,充分反应后过滤得到滤渣和滤液。往滤渣中滴加稀盐酸,无明显现象。则关于滤渣和滤液的说法正确的是 。
①滤渣中一定含有银和铜
②滤液中一定含有硝酸亚铁和硝酸铜
③滤渣中一定含有银
④滤液中滴加稀盐酸一定没有白色沉淀生成
⑤滤渣的质量一定比反应前铁粉和铜粉混合物的质量大
A.①③ B.③④⑤ C.③⑤ D.②④⑤
15.人类对氧化还原反应的认识过程中的三个阶段。
【阶段I】得失氧说:物质跟氧发生的反应叫氧化反应,含氧化合物中的氧被夺取的反应叫还原反应。
【阶段Ⅱ】化合价升降说:凡是出现元素化合价升降的化学反应都是氧化还原反应,化合价升高的反应叫氧化反应,化合价降低的反应叫还原反应。
【阶段Ⅲ】电子转移说:化合价升降的原因是电子的转移。凡有电子转移发生的化学反应都是氧化还原反应,失电子的反应叫氧化反应,得电子的反应叫还原反应。
(1)根据得失氧说,在 化学变化中,H2发生了 反应。
(2)电子转移是元素化合价改变的本质原因。 反应前后,化合价升高的元素是 ,说明该元素的原子得失电子情况为 。
(3)根据化合价升降说,化学反应的四种基本类型中,一定不属于氧化还原反应是 反应,写出该类型反应的一个化学方程式 。
(4)关于氧化还原反应的认识,下列理解错误的是______(填标号)。
A.氧化和还原是相互对立又辩证统一的关系
B.电子转移说是从微观视角来探析和建构氧化还原反应的概念
C.自然界中发生的氧化还原反应对人类的生活和生产都是有利的
16.酸、碱、盐在生产和生活中有着广泛的应用。
(1)氢氧化钙是一种生活中常见的碱,下列属于氢氧化钙用途的是_______(填标号)。
A.改良酸性土壤 B.配制波尔多液
C.治疗胃酸过多 D.刷墙、砌砖
(2)①碱溶液中都含有 (填离子符号),所以碱有一些相似的化学性质。
②如图所示,向稀氢氧化钠溶液中加入过量稀盐酸,充分反应后,所得溶液中溶质的成分为 (填化学式)。
(3)烧杯中盛有一定量的物质,向其中逐滴加入X溶液至过量,产生沉淀或气体的质量与加入的X溶液的质量关系如图所示。下列实验可用该图像表示的是 (填标号)。
选项 烧杯中盛放的物质 X溶液
A 表面锈蚀的铁制品 稀硫酸
B 氢氧化钠和氯化钡的混合溶液 稀硫酸
C 盐酸和氯化钙的混合溶液 硝酸银溶液
D 稀硫酸和硝酸铁的混合溶液 氢氧化钠溶液
(4)KNO3和NaCl的溶解度曲线如图所示,请回答下列问题:
①60℃时,向50g水中加入60gKNO3,充分溶解后,所得溶液的质量为 g。
②60℃时,分别将等质量的KNO3和NaC1的饱和溶液降温至20℃,所得溶液中溶剂质量大小关系为KNO3 NaCl(填“>”、“<”或“=”)。
③20℃时,KNO3的饱和溶液中溶质的质量分数为 (写出计算式即可)。
三、计算题
17.某化学兴趣小组的同学将一包氯化钠和碳酸钠的固体混合物,溶于75.1g水制成溶液,然后向其中加入溶质质量分数为10%的氯化钙溶液至恰好完全反应,生成沉淀10g,将滤液蒸干后得到固体25g。回答:
(1)写出上述反应的化学方程式 。
(2)试列出求解混合物中碳酸钠质量(x)的比例式 。
(3)原固体混合物中氯化钠的质量为 g。
(4)反应后所得滤液中溶质的质量分数为 。
(5)若配置10%的氯化钙溶液200g,需要向25%氯化钙溶液加水多少 g。
18.取氯化钙和盐酸的混合溶液 51.88g,逐滴滴加 10 .6%的碳酸钠溶液。所加入碳酸钠溶液的质量和混合溶液 pH变化关系如图所示 ,回答下列问题:
(1)BC段反应的化学方程式为 。
(2)D点所含有的物质 。
(3)计算充分反应至C点时所得溶液中溶质的质量分数(写出计算过程 ,计算结果精确至 0.1%)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.D
2.C
3.C
4.B
5.C
6.C
7.A
8.B
9.B
10.C
11.C
12.B
13.(1)单质
(2)H2CO3
(3) a 还原
(4)3
(5)稀盐酸
14.(1) 金属材料 隔绝水和氧气
(2)7
(3)C
15.(1)氧化
(2) Fe/铁元素 失去2个电子
(3) 复分解反应 NaOH+HCl=NaCl+H2O
(4)C
16.(1)ABD
(2) OH- NaCl、HCl
(3)AD
(4) 105 < ×100%
17.(1)
(2)
(3)13.3
(4)12.5%
(5)120
18.(1)
(2)氯化钠、碳酸钠
(3)解:设碳酸钠和盐酸反应生成的二氧化碳的质量为x,生成的氯化钠的质量为y;而碳酸钠和氯化钙反应生成的碳酸钙的质量为z,生成的氯化钠的质量为n。
解得:x=0.88g;y=2.34g
解得:z=1g;a=1.17g
C点时所得溶液中溶质的质量分数为 ≈4.4%
答:充分反应至C点时所得溶液中溶质的质量分数为4.4%。
答案第1页,共2页
答案第1页,共2页
同课章节目录
