5.1 课时3 不同价态含硫物质的转化 课件(共19张ppt) 2023-2024学年高一化学人教版(2019)必修2
文档属性
| 名称 | 5.1 课时3 不同价态含硫物质的转化 课件(共19张ppt) 2023-2024学年高一化学人教版(2019)必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 59.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-12 00:00:00 | ||
图片预览






文档简介
第五章 化工生产中的重要非金属原元素
第一节 硫及其化合物 课时3
视频
知道含不同价态硫元素的物质可以相互转化,并能设计实验进行探究或验证,增强对氧化还原反应的认识。
知识点一:自然界中硫的存在和转化
1.自然界中硫的存在
火山喷发附近
含硫矿物:FeS2、CuFeS2、NaSO4·10H2O、CaSO4·2H2O、S
有刺激性气味的气体弥漫空中:H2S、SO2等
从物质类别和化合价角度分类火山喷发所形成的物质。
物质类别
氧化物:SO2、SO3
FeS2、CuFeS2、NaSO4·10H2O、CaSO4·2H2O、S、H2S、SO2、SO3、H2SO3、H2SO4
酸:H2SO3、H2SO4
盐:FeS2、CuFeS2、
NaSO4·10H2O、CaSO4·2H2O
单质:S
化合价
-2价:CuFeS2
-1价:FeS2
0价:S
+4价:SO2、H2SO3
+6价:SO3、H2SO4、NaSO4·10H2O、CaSO4·2H2O
火山喷发时,自然界中的含硫物质发生了哪些变化?空气中刺鼻的气味是如何产生的?
2SO2 + O2 2SO3
SO2+H2O H2SO3
SO3+H2O=H2SO4
自然界中的含硫物质在一定条件下能够相互转化,如刺鼻的气味来自含硫物质在高温条件下被空气中的氧气氧化产生的二氧化硫。
实验室如何实现不同价态含硫物质的相互转化呢
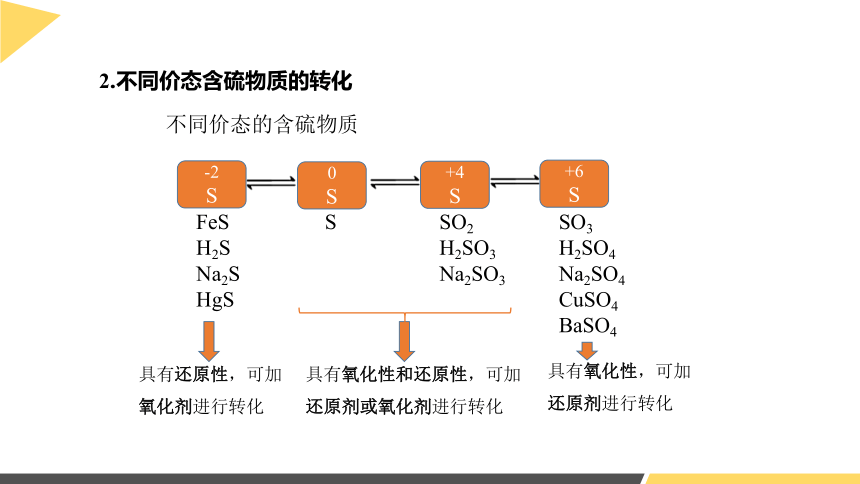
2.不同价态含硫物质的转化
不同价态的含硫物质
-2
S
0
S
+4
S
+6
S
FeS
H2S
Na2S
HgS
S
SO2
H2SO3
Na2SO3
SO3
H2SO4
Na2SO4
CuSO4
BaSO4
具有还原性,可加氧化剂进行转化
具有氧化性和还原性,可加还原剂或氧化剂进行转化
具有氧化性,可加还原剂进行转化
常见的氧化剂:O2、酸性KMnO4溶液、浓硫酸、氯水、H2O2等
常见的还原剂:金属单质、H2、H2S、C、SO2等
【设计方案】
{8A107856-5554-42FB-B03E-39F5DBC370BA}实验序号
价态变化
转化前的含硫物质
选择试剂
转化后的含硫物质
预期现象
1
0→-2
S
2
+6→+4
H2SO4
3
+4→0
SO2
4
-2→0
H2S
5
0→+4
S
6
+4→+6
H2SO3
Fe
FeS
生成黑色固体
Cu
SO2
产生刺激性气体,该气体能使品红溶液褪色
H2S
S
生成淡黄色固体
生成淡黄色固体
H2O2
S
空气
SO2
硫燃烧,发出淡蓝色火焰,产生刺激性气味的气体
氯水
H2SO4
反应后向其加入稀盐酸无明显现象,滴加氯化钡溶液,产生白色沉淀
【实施方案】
实验现象
混合物一端红热,直到整个混合物红热,结成黑色块状“FeS”
Fe + S FeS
║
?
硫单质与铁的反应
视频
实验1
0
-2
浓硫酸与铜片反应
实验现象
铜片溶解,表面有气泡产生;品红溶液褪色。
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
║
?
视频
实验2
+6
+4
实验现象
发出明亮的蓝紫色火焰,放出大量的热,生成一种
有刺激性气味的气体
S + O2 SO2
║
?
硫单质与氧气的反应
视频
实验5
0
+4
实验现象
加入氯水后,无明显现象,再加BaCl2溶液,有不溶于HCl溶液的白色沉淀生成,
Cl2+SO2+2H2O===H2SO4+2HCl
视频
实验6
+4
+6
二氧化硫水溶液与氯水的反应
酸
单质
盐
氧化物
+4
0
+6
硫元素化合价
物质类别
-2
氢化物
H2S
SO3
H2SO4
SO2
H2SO3
Na2SO4
Na2SO3
S
概括?整合
构建硫及其化合物之间的转化关系
2H2SO4(浓)+S===3SO2↑+2H2O
?
SO2+2H2S===3S↓+2H2O
S + O2===SO2
?
H2SO4+2NaOH===Na2SO4+2H2O
2Na2SO3+O2===2Na2SO4
B
1.下列转化不能一步实现的是( )
A.H2S→S B.S→SO3
C.H2SO4→SO2 D.Na2SO3→SO2
练一练
2.下列反应产生的气体,通入Na2SO3溶液不反应的是( )
A.Al与NaOH溶液 B.MnO2和浓盐酸共热
C.浓硝酸和铜片 D.铜片和浓硫酸共热
A
3.H2S是无色有恶臭味的有毒气体,空气中含0.1%的H2S就会迅速引起头痛、晕眩等症状,吸入大量H2S会造成昏迷或死亡。是一种神经毒剂。亦为窒息性和刺激性气体。其毒作用的主要靶器是中枢神经系统和呼吸系统,亦可伴有心脏等多器官损害,下列有关H2S的性质和用途说法不正确的是( )
A.硫化氢能被氧气、氯气、碘、溴等单质氧化成硫单质
B.将H2S通入Pb(NO3)2溶液得到黑色沉淀,再加双氧水,沉淀会转化为白色
C.将H2S气体通入CuSO4溶液中得到CuS沉淀,通入FeSO4溶液会产生FeS沉淀
D.H2S通入到FeCl3溶液中,溶液酸性增强
C
4.“价类”二维图是构建元素化合物知识网络的一种思维模型。如图是硫元素部分关系图。下列相关说法不正确的是( )
A.图中A点对应的物质既可以被氧化也能被还原
B.可以实现B→E→A→B物质循环
C.图中C和D两点对应的物质能互相反应生成硫单质
D.化学式为Na2S2O3的物质在图中对应点为F点,可表现出强氧化性
D
5.硫的价类二维图如图所示,用正确的化学用语表示。
(1)H2SO4的电离方程式为 。
(2)①的离子方程式为 。
(3)②的化学方程式为 。
(4)③的离子方程式为 。
(5)④的化学方程式为 。
H2SO4 = 2H++
SO42?
?
SO2+2H2S=3S↓+2H2O
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
H2SO3+2OH-= +2H2O
SO32?
?
SO2+Cl2+2H2O= +4H++2Cl-
SO42?
?
酸
单质
盐
氧化物
+4
0
+6
硫元素化合价
物质类别
-2
氢化物
H2S
SO3
H2SO4
SO2
H2SO3
Na2SO4
Na2SO3
S
第一节 硫及其化合物 课时3
视频
知道含不同价态硫元素的物质可以相互转化,并能设计实验进行探究或验证,增强对氧化还原反应的认识。
知识点一:自然界中硫的存在和转化
1.自然界中硫的存在
火山喷发附近
含硫矿物:FeS2、CuFeS2、NaSO4·10H2O、CaSO4·2H2O、S
有刺激性气味的气体弥漫空中:H2S、SO2等
从物质类别和化合价角度分类火山喷发所形成的物质。
物质类别
氧化物:SO2、SO3
FeS2、CuFeS2、NaSO4·10H2O、CaSO4·2H2O、S、H2S、SO2、SO3、H2SO3、H2SO4
酸:H2SO3、H2SO4
盐:FeS2、CuFeS2、
NaSO4·10H2O、CaSO4·2H2O
单质:S
化合价
-2价:CuFeS2
-1价:FeS2
0价:S
+4价:SO2、H2SO3
+6价:SO3、H2SO4、NaSO4·10H2O、CaSO4·2H2O
火山喷发时,自然界中的含硫物质发生了哪些变化?空气中刺鼻的气味是如何产生的?
2SO2 + O2 2SO3
SO2+H2O H2SO3
SO3+H2O=H2SO4
自然界中的含硫物质在一定条件下能够相互转化,如刺鼻的气味来自含硫物质在高温条件下被空气中的氧气氧化产生的二氧化硫。
实验室如何实现不同价态含硫物质的相互转化呢
2.不同价态含硫物质的转化
不同价态的含硫物质
-2
S
0
S
+4
S
+6
S
FeS
H2S
Na2S
HgS
S
SO2
H2SO3
Na2SO3
SO3
H2SO4
Na2SO4
CuSO4
BaSO4
具有还原性,可加氧化剂进行转化
具有氧化性和还原性,可加还原剂或氧化剂进行转化
具有氧化性,可加还原剂进行转化
常见的氧化剂:O2、酸性KMnO4溶液、浓硫酸、氯水、H2O2等
常见的还原剂:金属单质、H2、H2S、C、SO2等
【设计方案】
{8A107856-5554-42FB-B03E-39F5DBC370BA}实验序号
价态变化
转化前的含硫物质
选择试剂
转化后的含硫物质
预期现象
1
0→-2
S
2
+6→+4
H2SO4
3
+4→0
SO2
4
-2→0
H2S
5
0→+4
S
6
+4→+6
H2SO3
Fe
FeS
生成黑色固体
Cu
SO2
产生刺激性气体,该气体能使品红溶液褪色
H2S
S
生成淡黄色固体
生成淡黄色固体
H2O2
S
空气
SO2
硫燃烧,发出淡蓝色火焰,产生刺激性气味的气体
氯水
H2SO4
反应后向其加入稀盐酸无明显现象,滴加氯化钡溶液,产生白色沉淀
【实施方案】
实验现象
混合物一端红热,直到整个混合物红热,结成黑色块状“FeS”
Fe + S FeS
║
?
硫单质与铁的反应
视频
实验1
0
-2
浓硫酸与铜片反应
实验现象
铜片溶解,表面有气泡产生;品红溶液褪色。
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
║
?
视频
实验2
+6
+4
实验现象
发出明亮的蓝紫色火焰,放出大量的热,生成一种
有刺激性气味的气体
S + O2 SO2
║
?
硫单质与氧气的反应
视频
实验5
0
+4
实验现象
加入氯水后,无明显现象,再加BaCl2溶液,有不溶于HCl溶液的白色沉淀生成,
Cl2+SO2+2H2O===H2SO4+2HCl
视频
实验6
+4
+6
二氧化硫水溶液与氯水的反应
酸
单质
盐
氧化物
+4
0
+6
硫元素化合价
物质类别
-2
氢化物
H2S
SO3
H2SO4
SO2
H2SO3
Na2SO4
Na2SO3
S
概括?整合
构建硫及其化合物之间的转化关系
2H2SO4(浓)+S===3SO2↑+2H2O
?
SO2+2H2S===3S↓+2H2O
S + O2===SO2
?
H2SO4+2NaOH===Na2SO4+2H2O
2Na2SO3+O2===2Na2SO4
B
1.下列转化不能一步实现的是( )
A.H2S→S B.S→SO3
C.H2SO4→SO2 D.Na2SO3→SO2
练一练
2.下列反应产生的气体,通入Na2SO3溶液不反应的是( )
A.Al与NaOH溶液 B.MnO2和浓盐酸共热
C.浓硝酸和铜片 D.铜片和浓硫酸共热
A
3.H2S是无色有恶臭味的有毒气体,空气中含0.1%的H2S就会迅速引起头痛、晕眩等症状,吸入大量H2S会造成昏迷或死亡。是一种神经毒剂。亦为窒息性和刺激性气体。其毒作用的主要靶器是中枢神经系统和呼吸系统,亦可伴有心脏等多器官损害,下列有关H2S的性质和用途说法不正确的是( )
A.硫化氢能被氧气、氯气、碘、溴等单质氧化成硫单质
B.将H2S通入Pb(NO3)2溶液得到黑色沉淀,再加双氧水,沉淀会转化为白色
C.将H2S气体通入CuSO4溶液中得到CuS沉淀,通入FeSO4溶液会产生FeS沉淀
D.H2S通入到FeCl3溶液中,溶液酸性增强
C
4.“价类”二维图是构建元素化合物知识网络的一种思维模型。如图是硫元素部分关系图。下列相关说法不正确的是( )
A.图中A点对应的物质既可以被氧化也能被还原
B.可以实现B→E→A→B物质循环
C.图中C和D两点对应的物质能互相反应生成硫单质
D.化学式为Na2S2O3的物质在图中对应点为F点,可表现出强氧化性
D
5.硫的价类二维图如图所示,用正确的化学用语表示。
(1)H2SO4的电离方程式为 。
(2)①的离子方程式为 。
(3)②的化学方程式为 。
(4)③的离子方程式为 。
(5)④的化学方程式为 。
H2SO4 = 2H++
SO42?
?
SO2+2H2S=3S↓+2H2O
Cu+2H2SO4(浓) CuSO4+SO2↑+2H2O
H2SO3+2OH-= +2H2O
SO32?
?
SO2+Cl2+2H2O= +4H++2Cl-
SO42?
?
酸
单质
盐
氧化物
+4
0
+6
硫元素化合价
物质类别
-2
氢化物
H2S
SO3
H2SO4
SO2
H2SO3
Na2SO4
Na2SO3
S
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
