7.1 课时1 有机化合物中碳原子的成键特点 烷烃的结构 课件 (共25张ppt)2023-2024学年高一化学人教版(2019)必修2
文档属性
| 名称 | 7.1 课时1 有机化合物中碳原子的成键特点 烷烃的结构 课件 (共25张ppt)2023-2024学年高一化学人教版(2019)必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-12 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
①CO ②CH4 ③C2H5OH(乙醇) ④H2CO3
⑤CH3Cl ⑥C6H12O6(葡萄糖) ⑦KSCN ⑧NaHCO3 ⑨CO(NH2)2(尿素) ⑩C2H2
【判断】下列物质属于有机物的是_ ____________。
②③⑤⑥⑨⑩
【注意】并不是含有C的化合物就是有机物, 如CO2、碳酸、碳酸盐、 碳的金属化合物 ( CaC2)等是无机物。
1.定义: 大多数含有碳元素的化合物
组成元素:(1)一定含有碳元素
(2)也可能含有H、N、P、S、O、卤素等元素
有机化合物
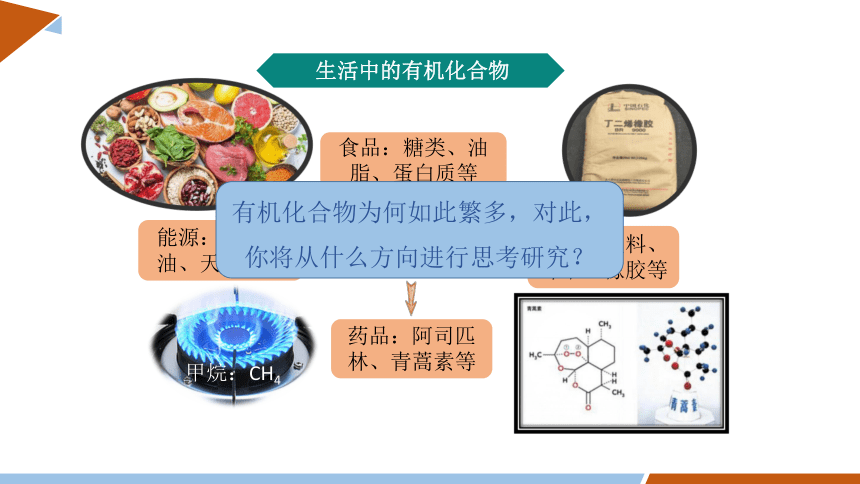
生活中的有机化合物
食品:糖类、油脂、蛋白质等
药品:阿司匹林、青蒿素等
有机化合物
能源:煤、石油、天然气等
材料:塑料、纤维、橡胶等
甲烷:CH4
有机化合物为何如此繁多,对此,你将从什么方向进行思考研究?
第七章 有机化合物
第一节 认识有机化合物 课时1
1.知道有机化合物中碳原子的成键特点。
2.通过模型拼接知道碳原子成键的多样性。
3.掌握烷烃的简单命名。
4.知道同系物和同分异构体的概念。
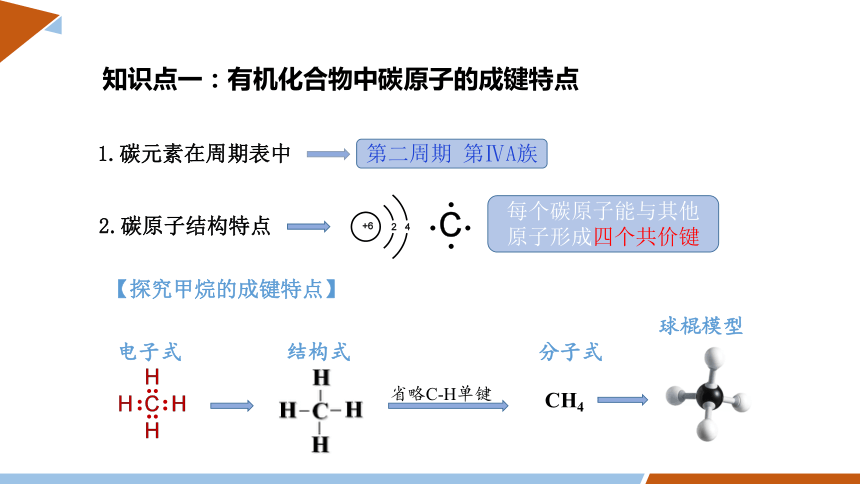
知识点一:有机化合物中碳原子的成键特点
2.碳原子结构特点
1.碳元素在周期表中
第二周期 第ⅣA族
每个碳原子能与其他原子形成四个共价键
电子式
结构式
省略C-H单键
分子式
CH4
球棍模型
【探究甲烷的成键特点】
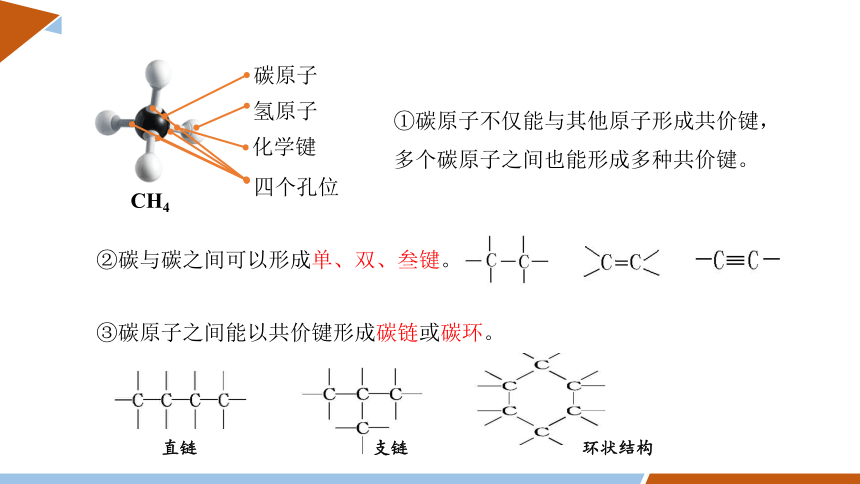
CH4
碳原子
氢原子
化学键
四个孔位
②碳与碳之间可以形成单、双、叁键。
③碳原子之间能以共价键形成碳链或碳环。
①碳原子不仅能与其他原子形成共价键,多个碳原子之间也能形成多种共价键。
直链
支链
环状结构
【思考与讨论】
下图是表示4个碳原子相互结合的方式。黑球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合。
(1)碳原子间所成的化学键全是碳碳单键的有_____________(填字母,下同),含有碳碳双键的有________,含有碳碳三键的有______。
C、D、E、F
A、B、J
G、H
(2)碳骨架为链状的有_______________________,为环状的有_______,含有支链的有________。
(3)以小球表示碳原子,小棍表示化学键,试画出3个碳原子相互结合的所有碳骨架的示意图: 。
A、B、C、D、G、H、J
E、F
C、E、J
(6)写出它们的分子式:
A:C4H8、B:C4H8、C:C4H10、D:C4H10、E:C4H8、F:C4H8、G:C4H6、H:C4H6、J:C4H8
(1)碳原子所成价键多:有机化合物中,碳原子最外层有4个单电子,可以形成4个共价键,比氮、氧、氢或卤素原子所成价键都要多。
(2)碳原子成键方式多样:含有多个碳原子的有机化合物,碳原子间成键方式较多,可以形成单键,也可以形成双键或三键。
(3)碳骨架多样:碳原子间所成骨架有多种,可以是直链,也可以成环,也可以带支链。
(4)成链原子及种类多而灵活:有机物分子中碳原子可以与一个或若干个碳原子成键,也可以和其他原子成键,数目不等。
【有机物种类繁多的原因】
知识点二:烷烃和烷烃的结构
1.甲烷的结构
分子结构示意图 球棍模型 空间充填模型
【实验数据表明】
①甲烷分子中的5个原子不在同一平面上;②正四面体的空间结构;③碳原子位于正四面体的中心,4个氢原子分别位于4个顶点;④分子中的4个C—H的长度和强度相同,相互之间的夹角相等。
结构式
2.烷烃的结构
【思考与讨论】请根据碳原子的成键规律和下表提供的信息,写出丁烷的结构式和乙烷、丙烷、丁烷的分子式。
有机化合物 乙烷 丙烷 丁烷
碳原子数 2 3 4
结构式
分子式
C2H6
C3H8
C4H10
结合上表信息,总结这类有机化合物的组成和分子结构特点?
a.只含有碳和氢两种元素
b.单键:碳原子之间都以_____结合。
c.饱和:碳原子剩余价键全部跟________结合。
d.结构:每个碳原子都与其他原子形成_______结构。
【结构特点】
单键
氢原子
四面体
只含有碳、氢两种元素的有机物。
+
=
烃
t
īng
q
火
àn
t īng
气
(1)烷烃的概念
分子中碳原子之间都以单键结合,碳原子剩余价键均与氢原子结合,使碳原子的化合价都达到饱和的有机物,也称饱和烃。
甲烷 甲基
乙烷 乙基
或 —C2H5
烃基:烃失去一个或几个氢原子所剩余的原子团。
【烃基的特点】呈电中性的原子团,含有未成键的单电子,不能独立存在。
(2)烷烃的简单命名
CH4
1个碳
甲烷
C2H6
2个碳
乙烷
C3H8
3个碳
丙烷
碳原子数 (n) 及表示
n≤10 1 2 3 4 5 6 7 8 9 10
甲烷 乙烷 丙烷 丁烷 戊烷 己烷 庚烷 辛烷 壬烷 癸烷
n>10 相应汉字数字+烷
(3)烷烃的通式和结构简式
有机化合物 乙烷 丙烷 丁烷
结构式
省略化学键
结构简式
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3CH3
CH3CH2CH3
CH3(CH2)2CH3
相差一个CH2原子团
相差一个CH2原子团
烷烃分子式的通式
CnH2n+2
用结构式表示碳原子较多的复杂有机物时,可以省略有机物中的某些单键(双键、三键和支链单键保留)。
(4)同系物
定义:结构相似,在分子组成上相差一个或若干个“CH2”原子团的物质互称为同系物。
①通式相同的同类物质;
②结构相似;
③分子式不同、组成上相差一个或若干CH2原子团。
构成同系物的特点
下列物质中属于同系物的是 。
②③④
比较大家写出的丁烷的结构式是否相同,思考产生这种现象的可能原因。
【思考与讨论】
CH3CH2CH2CH3
分子式相同,结构式不同---同分异构体
碳原子形成直链
碳原子带有支链
C4H10
(5)同分异构现象和同分异构体
①同分异构体现象:
化合物具有相同的分子式,但具有不同的结构现象,叫做同分异构体现象。
②同分异构体:
具有同分异构体现象的化合物互称为同分异构体。
同分异构体 分子式相同 相对分子质量必相同
不一定属于同一类物质
结构不同 原子或原子团的连接顺序不同
原子的空间排列不同
根据上面对同分异构体的介绍,写一写戊烷的同分异构体。
【思考】具有同分异构现象的烷烃如何命名
当碳原子数相同,而结构不同时,可用正、异、新表示不同烷烃
如:丁烷的两种分子的命名:
无支链时,CH3CH2CH2CH3称为 ;
有支链时, 称为 。
正丁烷
异丁烷
CH3-CH2-CH2-CH2-CH3
CH3-CH-CH2-CH3
CH3
正戊烷
异戊烷
CH3-C-CH3
新戊烷
CH3
CH3
戊烷的三种分子的命名
1. 在丙烷(C3H8)、正丁烷(C4H10)分子中,碳链是直线形状吗?
2. 每个碳原子与周围最近原子共同构成什么结构?
1.不是,是锯齿状结构,丙烷碳原子间结构为 ,正丁烷碳原子间结构为 。
2.每个碳原子与周围最近原子构成四面体结构。
【思考与讨论】
练一练
1.目前,人们在自然界中发现的物质和人工合成的物质已超过1亿种,其中绝大多数都是有机化合物,而且新的有机物仍在源源不断地被发现或被合成出来。下列有关碳元素形成的有机化合物种类繁多的原因叙述不正确的是( )
A.常温下碳原子的性质活泼,容易跟多种原子形成共价键
B.碳原子之间既可以形成稳定的单键,又可以形成双键和三键
C.碳原子可以跟碳原子或其他原子形成4根共价键
D.多个碳原子之间可以结合成碳链,也可以结合成碳环
A
2.键线式可以简明扼要的表示碳氢化合物, 这种键线式物质是( )
A.丁烷 B.异丁烷 C.异戊烷 D.新戊烷
3.主链含有五个碳原子的烷烃C7H16的结构共有( )
A.4种 B.5种 C.6种 D.7种
①(CH3)3CCH2CH2CH3 ②CH3CH2C(CH3)2CH2CH3
③CH3CH2CH(CH2CH3)CH2CH3 ④(CH3)2CHCH2CH(CH3)2
⑤(CCH3)2CHCH(CH3)CH2CH3
C
B
4.下列物质中,互为同系物的有 ,互为同分异构体的有 ,互为同素异形体的有 ,属于同位素的有 。
①正戊烷;②白磷;③ ;④ ;
⑤;⑥红磷;⑦。
①③/③④
①④
②⑥
⑤⑦
有机化合物
碳原子的成键特点
烷烃的结构
每个碳原子能与其他原子形成四个共价键
碳与碳之间可以形成单、双、叁键
碳原子之间能以共价键形成碳链或碳环
烷烃:分子中碳原子之间都以单键结合,碳原子剩余价键均与氢原子结合,使碳原子的化合价都达到饱和的有机物
烃基:烃失去一个或几个氢原子所剩余的原子团
烷烃的简单命名
烷烃的通式:CnH2n+2
同系物
同分异构体和同分异构现象
①CO ②CH4 ③C2H5OH(乙醇) ④H2CO3
⑤CH3Cl ⑥C6H12O6(葡萄糖) ⑦KSCN ⑧NaHCO3 ⑨CO(NH2)2(尿素) ⑩C2H2
【判断】下列物质属于有机物的是_ ____________。
②③⑤⑥⑨⑩
【注意】并不是含有C的化合物就是有机物, 如CO2、碳酸、碳酸盐、 碳的金属化合物 ( CaC2)等是无机物。
1.定义: 大多数含有碳元素的化合物
组成元素:(1)一定含有碳元素
(2)也可能含有H、N、P、S、O、卤素等元素
有机化合物
生活中的有机化合物
食品:糖类、油脂、蛋白质等
药品:阿司匹林、青蒿素等
有机化合物
能源:煤、石油、天然气等
材料:塑料、纤维、橡胶等
甲烷:CH4
有机化合物为何如此繁多,对此,你将从什么方向进行思考研究?
第七章 有机化合物
第一节 认识有机化合物 课时1
1.知道有机化合物中碳原子的成键特点。
2.通过模型拼接知道碳原子成键的多样性。
3.掌握烷烃的简单命名。
4.知道同系物和同分异构体的概念。
知识点一:有机化合物中碳原子的成键特点
2.碳原子结构特点
1.碳元素在周期表中
第二周期 第ⅣA族
每个碳原子能与其他原子形成四个共价键
电子式
结构式
省略C-H单键
分子式
CH4
球棍模型
【探究甲烷的成键特点】
CH4
碳原子
氢原子
化学键
四个孔位
②碳与碳之间可以形成单、双、叁键。
③碳原子之间能以共价键形成碳链或碳环。
①碳原子不仅能与其他原子形成共价键,多个碳原子之间也能形成多种共价键。
直链
支链
环状结构
【思考与讨论】
下图是表示4个碳原子相互结合的方式。黑球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢原子结合。
(1)碳原子间所成的化学键全是碳碳单键的有_____________(填字母,下同),含有碳碳双键的有________,含有碳碳三键的有______。
C、D、E、F
A、B、J
G、H
(2)碳骨架为链状的有_______________________,为环状的有_______,含有支链的有________。
(3)以小球表示碳原子,小棍表示化学键,试画出3个碳原子相互结合的所有碳骨架的示意图: 。
A、B、C、D、G、H、J
E、F
C、E、J
(6)写出它们的分子式:
A:C4H8、B:C4H8、C:C4H10、D:C4H10、E:C4H8、F:C4H8、G:C4H6、H:C4H6、J:C4H8
(1)碳原子所成价键多:有机化合物中,碳原子最外层有4个单电子,可以形成4个共价键,比氮、氧、氢或卤素原子所成价键都要多。
(2)碳原子成键方式多样:含有多个碳原子的有机化合物,碳原子间成键方式较多,可以形成单键,也可以形成双键或三键。
(3)碳骨架多样:碳原子间所成骨架有多种,可以是直链,也可以成环,也可以带支链。
(4)成链原子及种类多而灵活:有机物分子中碳原子可以与一个或若干个碳原子成键,也可以和其他原子成键,数目不等。
【有机物种类繁多的原因】
知识点二:烷烃和烷烃的结构
1.甲烷的结构
分子结构示意图 球棍模型 空间充填模型
【实验数据表明】
①甲烷分子中的5个原子不在同一平面上;②正四面体的空间结构;③碳原子位于正四面体的中心,4个氢原子分别位于4个顶点;④分子中的4个C—H的长度和强度相同,相互之间的夹角相等。
结构式
2.烷烃的结构
【思考与讨论】请根据碳原子的成键规律和下表提供的信息,写出丁烷的结构式和乙烷、丙烷、丁烷的分子式。
有机化合物 乙烷 丙烷 丁烷
碳原子数 2 3 4
结构式
分子式
C2H6
C3H8
C4H10
结合上表信息,总结这类有机化合物的组成和分子结构特点?
a.只含有碳和氢两种元素
b.单键:碳原子之间都以_____结合。
c.饱和:碳原子剩余价键全部跟________结合。
d.结构:每个碳原子都与其他原子形成_______结构。
【结构特点】
单键
氢原子
四面体
只含有碳、氢两种元素的有机物。
+
=
烃
t
īng
q
火
àn
t īng
气
(1)烷烃的概念
分子中碳原子之间都以单键结合,碳原子剩余价键均与氢原子结合,使碳原子的化合价都达到饱和的有机物,也称饱和烃。
甲烷 甲基
乙烷 乙基
或 —C2H5
烃基:烃失去一个或几个氢原子所剩余的原子团。
【烃基的特点】呈电中性的原子团,含有未成键的单电子,不能独立存在。
(2)烷烃的简单命名
CH4
1个碳
甲烷
C2H6
2个碳
乙烷
C3H8
3个碳
丙烷
碳原子数 (n) 及表示
n≤10 1 2 3 4 5 6 7 8 9 10
甲烷 乙烷 丙烷 丁烷 戊烷 己烷 庚烷 辛烷 壬烷 癸烷
n>10 相应汉字数字+烷
(3)烷烃的通式和结构简式
有机化合物 乙烷 丙烷 丁烷
结构式
省略化学键
结构简式
CH3CH3
CH3CH2CH3
CH3CH2CH2CH3
CH3CH3
CH3CH2CH3
CH3(CH2)2CH3
相差一个CH2原子团
相差一个CH2原子团
烷烃分子式的通式
CnH2n+2
用结构式表示碳原子较多的复杂有机物时,可以省略有机物中的某些单键(双键、三键和支链单键保留)。
(4)同系物
定义:结构相似,在分子组成上相差一个或若干个“CH2”原子团的物质互称为同系物。
①通式相同的同类物质;
②结构相似;
③分子式不同、组成上相差一个或若干CH2原子团。
构成同系物的特点
下列物质中属于同系物的是 。
②③④
比较大家写出的丁烷的结构式是否相同,思考产生这种现象的可能原因。
【思考与讨论】
CH3CH2CH2CH3
分子式相同,结构式不同---同分异构体
碳原子形成直链
碳原子带有支链
C4H10
(5)同分异构现象和同分异构体
①同分异构体现象:
化合物具有相同的分子式,但具有不同的结构现象,叫做同分异构体现象。
②同分异构体:
具有同分异构体现象的化合物互称为同分异构体。
同分异构体 分子式相同 相对分子质量必相同
不一定属于同一类物质
结构不同 原子或原子团的连接顺序不同
原子的空间排列不同
根据上面对同分异构体的介绍,写一写戊烷的同分异构体。
【思考】具有同分异构现象的烷烃如何命名
当碳原子数相同,而结构不同时,可用正、异、新表示不同烷烃
如:丁烷的两种分子的命名:
无支链时,CH3CH2CH2CH3称为 ;
有支链时, 称为 。
正丁烷
异丁烷
CH3-CH2-CH2-CH2-CH3
CH3-CH-CH2-CH3
CH3
正戊烷
异戊烷
CH3-C-CH3
新戊烷
CH3
CH3
戊烷的三种分子的命名
1. 在丙烷(C3H8)、正丁烷(C4H10)分子中,碳链是直线形状吗?
2. 每个碳原子与周围最近原子共同构成什么结构?
1.不是,是锯齿状结构,丙烷碳原子间结构为 ,正丁烷碳原子间结构为 。
2.每个碳原子与周围最近原子构成四面体结构。
【思考与讨论】
练一练
1.目前,人们在自然界中发现的物质和人工合成的物质已超过1亿种,其中绝大多数都是有机化合物,而且新的有机物仍在源源不断地被发现或被合成出来。下列有关碳元素形成的有机化合物种类繁多的原因叙述不正确的是( )
A.常温下碳原子的性质活泼,容易跟多种原子形成共价键
B.碳原子之间既可以形成稳定的单键,又可以形成双键和三键
C.碳原子可以跟碳原子或其他原子形成4根共价键
D.多个碳原子之间可以结合成碳链,也可以结合成碳环
A
2.键线式可以简明扼要的表示碳氢化合物, 这种键线式物质是( )
A.丁烷 B.异丁烷 C.异戊烷 D.新戊烷
3.主链含有五个碳原子的烷烃C7H16的结构共有( )
A.4种 B.5种 C.6种 D.7种
①(CH3)3CCH2CH2CH3 ②CH3CH2C(CH3)2CH2CH3
③CH3CH2CH(CH2CH3)CH2CH3 ④(CH3)2CHCH2CH(CH3)2
⑤(CCH3)2CHCH(CH3)CH2CH3
C
B
4.下列物质中,互为同系物的有 ,互为同分异构体的有 ,互为同素异形体的有 ,属于同位素的有 。
①正戊烷;②白磷;③ ;④ ;
⑤;⑥红磷;⑦。
①③/③④
①④
②⑥
⑤⑦
有机化合物
碳原子的成键特点
烷烃的结构
每个碳原子能与其他原子形成四个共价键
碳与碳之间可以形成单、双、叁键
碳原子之间能以共价键形成碳链或碳环
烷烃:分子中碳原子之间都以单键结合,碳原子剩余价键均与氢原子结合,使碳原子的化合价都达到饱和的有机物
烃基:烃失去一个或几个氢原子所剩余的原子团
烷烃的简单命名
烷烃的通式:CnH2n+2
同系物
同分异构体和同分异构现象
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
