6.1 课时1 化学反应与热能 课件(共26张ppt) 2023-2024学年高一化学人教版(2019)必修2
文档属性
| 名称 | 6.1 课时1 化学反应与热能 课件(共26张ppt) 2023-2024学年高一化学人教版(2019)必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 23.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-12 00:00:00 | ||
图片预览







文档简介
(共26张PPT)
700多年前,著名的意大利旅行家马克·波罗到过中国,看见中国人烧煤炼铁,这是他生平第一次看到煤做燃料,马克·波罗在他的游记里记载了这件新鲜事。书中写到,中国有一种黑色石头,能燃烧,着起火来像火柴一样,而且终夜不灭。现代科学可以这样解释,煤中含有大量的碳,燃烧时放出热能。
这种能量从何而来?
它与化学物质和化学反应有什么关系?
高温条件提供的热能在石灰石的分解中有什么作用?
第六章 化学反应与能量
第一节 化学反应与能量变化 课时1
化学变化的特征:
我们利用化学反应可以:
化学变化中除有新物质生成外,常伴随着放热、发光、变色、放出气体、生成沉淀等现象发生。
①制取新物质
②利用反应中产生的能量
1.通过实验,知道常见的放热反应和吸热反应,强化物质变化中伴随能量变化的观念。
2.能从反应物和生成物所具有的能量、化学键的断裂与形成两个角度解释化学反应中能量变化的主要原因。
3.知道节能的意义与方法。
知识点一:化学反应中存在热量变化
1.放热反应与吸热反应
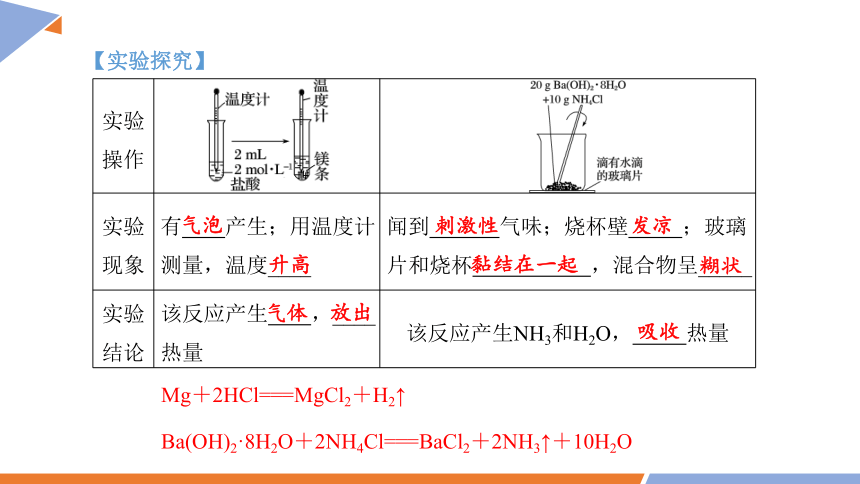
【实验6-1】
【实验6-2】
实验 操作
实验 现象 有 产生;用温度计测量,温度____ 闻到 气味;烧杯壁 ;玻璃片和烧杯 ,混合物呈_____
实验 结论 该反应产生 ,____ 热量 该反应产生NH3和H2O, 热量
气泡
升高
刺激性
发凉
黏结在一起
糊状
气体
放出
吸收
【实验探究】
Mg+2HCl===MgCl2+H2↑
Ba(OH)2·8H2O+2NH4Cl===BaCl2+2NH3↑+10H2O
【结论】
化学反应除了有新物质生成以外,还总会伴随着能量变化,通常主要表现为热能的变化,有的 热量,有的 热量。
放出
吸收
(1)概念
①放热反应:释放热量的化学反应。
②吸热反应:吸收热量的化学反应。
(1)硝酸铵固体溶于水,溶液的温度降低,该变化为吸热反应( )
(2)氢气燃烧,浓硫酸溶于水,都放出热量,这些变化都为放热反应( )
(3)化学反应既有物质变化,又有能量变化( )
(4)镁条在空气中燃烧是放热反应,反应过程中所释放的能量全部转化为热能( )
(5)吸热反应需要加热才能进行,放热反应都不需要加热就可以进行( )
判断正误
×
×
√
×
×
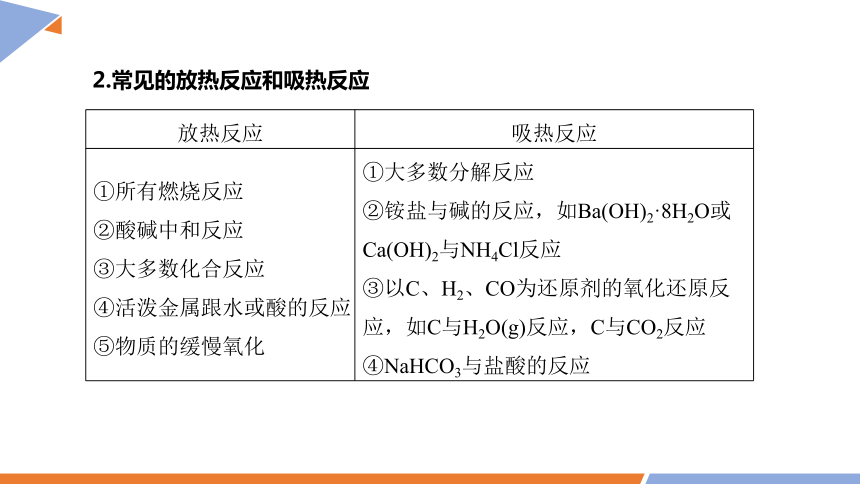
放热反应 吸热反应
①所有燃烧反应 ②酸碱中和反应 ③大多数化合反应 ④活泼金属跟水或酸的反应 ⑤物质的缓慢氧化 ①大多数分解反应
②铵盐与碱的反应,如Ba(OH)2·8H2O或Ca(OH)2与NH4Cl反应
③以C、H2、CO为还原剂的氧化还原反应,如C与H2O(g)反应,C与CO2反应
④NaHCO3与盐酸的反应
2.常见的放热反应和吸热反应
有关吸热反应和放热反应理解的三个“不一定”
(1)放热反应不一定容易发生,如合成氨反应需要在高温、高压和催化剂作用下才能发生;吸热反应不一定难发生,如Ba(OH)2·8H2O与NH4Cl的反应在常温下能发生。
(2)需要加热才能发生的反应不一定是吸热反应,如硫与铁的反应;吸热反应不一定需要加热,如Ba(OH)2·8H2O晶体和NH4Cl晶体的反应。
(3)放热过程不一定是放热反应,如NaOH固体的溶解和浓硫酸的稀释是放热过程,但不是放热反应;吸热过程不一定是吸热反应,如升华、蒸发等过程是吸热过程,但不是吸热反应。
归纳总结
氧化汞的分解
氧化汞分子
( HgO )
破裂成汞原子和氧原子
汞原子
(Hg)
氧分子
(O2)
加热
氧化汞
HgO
汞 + 氧气
Hg O2
加热
知识点二:化学反应中能量变化的原因
1.化学反应中能量变化的实质
宏观
微观
生成了新的物质,能量变化
旧化学键断裂、新化学键形成
吸收能量
放出能量
【微观探析】
(1)以H2+Cl2===2HCl反应为例探究化学反应中能量变化
①该反应过程中共吸收 kJ能量,共放出 kJ能量。
②该反应 (填“放出”或“吸收”) kJ热量,为 反应。
679
862
放出
183
放热
(2)化学反应中能量变化的实质原因
反
应
物
旧化学 键断裂
新化学 键形成
吸收能量
释放能量
生
成
物
决定
能
量
变
化
释放能量大于吸收能量:放热反应
吸收能量大于释放能量:吸热反应
一个化学反应是否为放热还是吸热取决于什么呢?
取决于所有断键吸收的总能量与所有形成新键放出的总能量的相对大小
2.化学反应中能量变化决定因素
放热反应 吸热反应
各种物质都具有能量。不同的物质不仅组成不同,结构不同,所具有的能量也不同。
化学能转化为热能
热能转化为化学能被生成物“储存”
知识点三:化学能与热能相互转化的应用
阅读课本p34-35页,回答下列问题。
1.现阶段人类获取热能的主要途径是: ;使用最多的常规能源是: ___ 。
2.化石燃料获取能量面临的问题
(1)储量有限,短期内不可再生。
(2)影响环境:煤、石油产品燃烧排放的 __ 等是大气污染物的主要来源。
物质的燃烧
化石燃料(煤、石油和天然气)
粉尘、SO2、NOx、CO
3.节能减排的措施
(1)燃料燃烧阶段提高燃料的燃烧效率。
(2)能量利用阶段提高能源的利用率。
(3)开发使用新能源,目前人们比较关注的新能源有_____ ____________
_ 等。
太阳能、风能、地热能、
海洋能和氢能
不同社会发展水平时期的人均耗能量
节能和寻找清洁的能源成为人类的必然选择
小明的爸爸是一名出租车司机,为倡导“绿水青山就是金山银山”这一理念,小明回到家和爸爸进行了一番争论。
小明认为:现在空气污染比较严重,应将汽车燃料改用新能源,或者污染较小的燃料。
小明的爸爸认为:现在城市污染不是很严重,新能源汽车价格高,续航能力差,不经济,汽油作燃料性价比高,适合长时间运行。
为了说服爸爸,小明又给爸爸展示了三张图片。
理解应用
燃料 液化石油气 天然气(CNG) 95号乙醇汽油
价格(元/升) 4.8 2.3 6.9
热值(kJ/kg) 4.5×104 4.0×104 4.6×104
图2 常用车用燃料热值及价格
图3 不同能源在各年代所占比例
最后小明的爸爸赞同了小明的观点,决定将汽油改为天然气。
(1)小明鼓励爸爸,将汽油改为CNG的目的是________________________
_______________________________________。
(2)结合图3,对于能源的选择,请你再提一条符合小明的目的的建议:____________________________________________________________________________________。
节约石油资源,减少对空气的污染,天然气作汽油燃料性价比相对较高
为减少化石能源对环境的影响,可以大力开发利用新能源,如太阳能、风能、海洋能、氢能等
练一练
1.判断正误。
(1)对于一个化学反应来说,当化学键断裂时吸收的能量大于化学键形成时放出的能量,则反应放热( )
(2)相同条件下形成1 mol H—Cl键放出的能量与断开1 mol H—Cl键吸收的能量相等( )
(3)任何化学反应,都有物质变化,同时伴随着能量变化( )
(4)放热反应为“贮存”能量的过程,吸热反应为“释放”能量的过程( )
(5)已知Fe与稀盐酸的反应为放热反应,即Fe的能量大于H2的能量( )
×
√
√
×
×
2.已知N2(g)和O2(g)反应生成2 mol NO(g)吸收
180 kJ能量,反应过程中能量变化如图所示。
根据图示回答下列问题:
(1)该反应中反应物所具有的总能量_____(填“高于”或“低于”)生成物的总能量。
(2)1 mol NO(g)分子中的化学键断裂时要吸收____ kJ能量。
(3)断裂1 mol N≡N吸收的能量x值为____。
低于
632
946
【解析】根据图示,断裂旧化学键所吸收能量为(x+498)kJ,形成新化学键所释放能量为2×632 kJ=1 264 kJ,每生成2 mol NO(g)所吸收能量为180 kJ,因此有180 kJ=(x+498)kJ-1 264 kJ,故x为946。
3.“开源节流”是应对能源危机的重要举措,下列做法有助于能源“开源节流”的是__ __(填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源,减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
acd
4.如图是某化学反应过程中能量变化的曲线图。下列叙述正确的是( )
A.该反应为吸热反应
B.该图可以表示Zn与HCl溶液反应的能量变化
C.该反应先发生物质变化后发生能量变化
D.断开反应物中化学键吸收的能量大于形成生成物中化学键放出的能量
B
5.已知2H→H2的能量变化如图所示。下列说法不正确的是( )
A.2H→H2过程中形成的化学键是共价键
B.相同质量的氢气分子的能量比氢原子的能量低
C.2H→H2过程中形成1 mol新化学键放出437.6 kJ的能量
D.1 mol H2离解成2 mol H要放出437.6 kJ热量
D
化学反应与热能
宏观角度(热量变化)
微观角度(化学键)
相互转化的应用
吸热反应
放热反应
吸收能量大于释放能量
释放能量大于吸收能量
旧化学键断裂吸收能量,新化学键形成放出能量
物质的燃烧
节能
寻找清洁的新能源
700多年前,著名的意大利旅行家马克·波罗到过中国,看见中国人烧煤炼铁,这是他生平第一次看到煤做燃料,马克·波罗在他的游记里记载了这件新鲜事。书中写到,中国有一种黑色石头,能燃烧,着起火来像火柴一样,而且终夜不灭。现代科学可以这样解释,煤中含有大量的碳,燃烧时放出热能。
这种能量从何而来?
它与化学物质和化学反应有什么关系?
高温条件提供的热能在石灰石的分解中有什么作用?
第六章 化学反应与能量
第一节 化学反应与能量变化 课时1
化学变化的特征:
我们利用化学反应可以:
化学变化中除有新物质生成外,常伴随着放热、发光、变色、放出气体、生成沉淀等现象发生。
①制取新物质
②利用反应中产生的能量
1.通过实验,知道常见的放热反应和吸热反应,强化物质变化中伴随能量变化的观念。
2.能从反应物和生成物所具有的能量、化学键的断裂与形成两个角度解释化学反应中能量变化的主要原因。
3.知道节能的意义与方法。
知识点一:化学反应中存在热量变化
1.放热反应与吸热反应
【实验6-1】
【实验6-2】
实验 操作
实验 现象 有 产生;用温度计测量,温度____ 闻到 气味;烧杯壁 ;玻璃片和烧杯 ,混合物呈_____
实验 结论 该反应产生 ,____ 热量 该反应产生NH3和H2O, 热量
气泡
升高
刺激性
发凉
黏结在一起
糊状
气体
放出
吸收
【实验探究】
Mg+2HCl===MgCl2+H2↑
Ba(OH)2·8H2O+2NH4Cl===BaCl2+2NH3↑+10H2O
【结论】
化学反应除了有新物质生成以外,还总会伴随着能量变化,通常主要表现为热能的变化,有的 热量,有的 热量。
放出
吸收
(1)概念
①放热反应:释放热量的化学反应。
②吸热反应:吸收热量的化学反应。
(1)硝酸铵固体溶于水,溶液的温度降低,该变化为吸热反应( )
(2)氢气燃烧,浓硫酸溶于水,都放出热量,这些变化都为放热反应( )
(3)化学反应既有物质变化,又有能量变化( )
(4)镁条在空气中燃烧是放热反应,反应过程中所释放的能量全部转化为热能( )
(5)吸热反应需要加热才能进行,放热反应都不需要加热就可以进行( )
判断正误
×
×
√
×
×
放热反应 吸热反应
①所有燃烧反应 ②酸碱中和反应 ③大多数化合反应 ④活泼金属跟水或酸的反应 ⑤物质的缓慢氧化 ①大多数分解反应
②铵盐与碱的反应,如Ba(OH)2·8H2O或Ca(OH)2与NH4Cl反应
③以C、H2、CO为还原剂的氧化还原反应,如C与H2O(g)反应,C与CO2反应
④NaHCO3与盐酸的反应
2.常见的放热反应和吸热反应
有关吸热反应和放热反应理解的三个“不一定”
(1)放热反应不一定容易发生,如合成氨反应需要在高温、高压和催化剂作用下才能发生;吸热反应不一定难发生,如Ba(OH)2·8H2O与NH4Cl的反应在常温下能发生。
(2)需要加热才能发生的反应不一定是吸热反应,如硫与铁的反应;吸热反应不一定需要加热,如Ba(OH)2·8H2O晶体和NH4Cl晶体的反应。
(3)放热过程不一定是放热反应,如NaOH固体的溶解和浓硫酸的稀释是放热过程,但不是放热反应;吸热过程不一定是吸热反应,如升华、蒸发等过程是吸热过程,但不是吸热反应。
归纳总结
氧化汞的分解
氧化汞分子
( HgO )
破裂成汞原子和氧原子
汞原子
(Hg)
氧分子
(O2)
加热
氧化汞
HgO
汞 + 氧气
Hg O2
加热
知识点二:化学反应中能量变化的原因
1.化学反应中能量变化的实质
宏观
微观
生成了新的物质,能量变化
旧化学键断裂、新化学键形成
吸收能量
放出能量
【微观探析】
(1)以H2+Cl2===2HCl反应为例探究化学反应中能量变化
①该反应过程中共吸收 kJ能量,共放出 kJ能量。
②该反应 (填“放出”或“吸收”) kJ热量,为 反应。
679
862
放出
183
放热
(2)化学反应中能量变化的实质原因
反
应
物
旧化学 键断裂
新化学 键形成
吸收能量
释放能量
生
成
物
决定
能
量
变
化
释放能量大于吸收能量:放热反应
吸收能量大于释放能量:吸热反应
一个化学反应是否为放热还是吸热取决于什么呢?
取决于所有断键吸收的总能量与所有形成新键放出的总能量的相对大小
2.化学反应中能量变化决定因素
放热反应 吸热反应
各种物质都具有能量。不同的物质不仅组成不同,结构不同,所具有的能量也不同。
化学能转化为热能
热能转化为化学能被生成物“储存”
知识点三:化学能与热能相互转化的应用
阅读课本p34-35页,回答下列问题。
1.现阶段人类获取热能的主要途径是: ;使用最多的常规能源是: ___ 。
2.化石燃料获取能量面临的问题
(1)储量有限,短期内不可再生。
(2)影响环境:煤、石油产品燃烧排放的 __ 等是大气污染物的主要来源。
物质的燃烧
化石燃料(煤、石油和天然气)
粉尘、SO2、NOx、CO
3.节能减排的措施
(1)燃料燃烧阶段提高燃料的燃烧效率。
(2)能量利用阶段提高能源的利用率。
(3)开发使用新能源,目前人们比较关注的新能源有_____ ____________
_ 等。
太阳能、风能、地热能、
海洋能和氢能
不同社会发展水平时期的人均耗能量
节能和寻找清洁的能源成为人类的必然选择
小明的爸爸是一名出租车司机,为倡导“绿水青山就是金山银山”这一理念,小明回到家和爸爸进行了一番争论。
小明认为:现在空气污染比较严重,应将汽车燃料改用新能源,或者污染较小的燃料。
小明的爸爸认为:现在城市污染不是很严重,新能源汽车价格高,续航能力差,不经济,汽油作燃料性价比高,适合长时间运行。
为了说服爸爸,小明又给爸爸展示了三张图片。
理解应用
燃料 液化石油气 天然气(CNG) 95号乙醇汽油
价格(元/升) 4.8 2.3 6.9
热值(kJ/kg) 4.5×104 4.0×104 4.6×104
图2 常用车用燃料热值及价格
图3 不同能源在各年代所占比例
最后小明的爸爸赞同了小明的观点,决定将汽油改为天然气。
(1)小明鼓励爸爸,将汽油改为CNG的目的是________________________
_______________________________________。
(2)结合图3,对于能源的选择,请你再提一条符合小明的目的的建议:____________________________________________________________________________________。
节约石油资源,减少对空气的污染,天然气作汽油燃料性价比相对较高
为减少化石能源对环境的影响,可以大力开发利用新能源,如太阳能、风能、海洋能、氢能等
练一练
1.判断正误。
(1)对于一个化学反应来说,当化学键断裂时吸收的能量大于化学键形成时放出的能量,则反应放热( )
(2)相同条件下形成1 mol H—Cl键放出的能量与断开1 mol H—Cl键吸收的能量相等( )
(3)任何化学反应,都有物质变化,同时伴随着能量变化( )
(4)放热反应为“贮存”能量的过程,吸热反应为“释放”能量的过程( )
(5)已知Fe与稀盐酸的反应为放热反应,即Fe的能量大于H2的能量( )
×
√
√
×
×
2.已知N2(g)和O2(g)反应生成2 mol NO(g)吸收
180 kJ能量,反应过程中能量变化如图所示。
根据图示回答下列问题:
(1)该反应中反应物所具有的总能量_____(填“高于”或“低于”)生成物的总能量。
(2)1 mol NO(g)分子中的化学键断裂时要吸收____ kJ能量。
(3)断裂1 mol N≡N吸收的能量x值为____。
低于
632
946
【解析】根据图示,断裂旧化学键所吸收能量为(x+498)kJ,形成新化学键所释放能量为2×632 kJ=1 264 kJ,每生成2 mol NO(g)所吸收能量为180 kJ,因此有180 kJ=(x+498)kJ-1 264 kJ,故x为946。
3.“开源节流”是应对能源危机的重要举措,下列做法有助于能源“开源节流”的是__ __(填字母)。
a.大力发展农村沼气,将废弃的秸秆转化为清洁高效的能源
b.大力开采煤、石油和天然气以满足人们日益增长的能源需求
c.开发太阳能、水能、风能、地热能等新能源,减少使用煤、石油等化石燃料
d.减少资源消耗,增加资源的重复使用、资源的循环再生
acd
4.如图是某化学反应过程中能量变化的曲线图。下列叙述正确的是( )
A.该反应为吸热反应
B.该图可以表示Zn与HCl溶液反应的能量变化
C.该反应先发生物质变化后发生能量变化
D.断开反应物中化学键吸收的能量大于形成生成物中化学键放出的能量
B
5.已知2H→H2的能量变化如图所示。下列说法不正确的是( )
A.2H→H2过程中形成的化学键是共价键
B.相同质量的氢气分子的能量比氢原子的能量低
C.2H→H2过程中形成1 mol新化学键放出437.6 kJ的能量
D.1 mol H2离解成2 mol H要放出437.6 kJ热量
D
化学反应与热能
宏观角度(热量变化)
微观角度(化学键)
相互转化的应用
吸热反应
放热反应
吸收能量大于释放能量
释放能量大于吸收能量
旧化学键断裂吸收能量,新化学键形成放出能量
物质的燃烧
节能
寻找清洁的新能源
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
