7.3 课时1 乙醇 课件 (共24张ppt)2023-2024学年高一化学人教版(2019)必修2
文档属性
| 名称 | 7.3 课时1 乙醇 课件 (共24张ppt)2023-2024学年高一化学人教版(2019)必修2 |
|
|
| 格式 | pptx | ||
| 文件大小 | 14.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-12 00:00:00 | ||
图片预览



文档简介
(共24张PPT)
第七章 有机化合物
第三节 乙醇和乙酸 课时1
早在几千年前,人类就掌握了发酵法酿酒的技术。各种酒类都含有浓度不等的乙醇。故乙醇俗称酒精。
1.知道乙醇的组成、结构、官能团、物理性质及用途。
2.知道烃的衍生物的概念及官能团与性质的关系,认识羟基与其性质的关系。
3.会运用乙醇的结构分析其化学性质。
知识点一:乙醇的物理性质与结构
①病人发烧通常用酒精擦拭全身,用此法降温。
②衣服上沾上少许汽油用酒精可以去除。
③酒香不怕巷子深
④白酒的主要成分是乙醇和水
⑤酒精灯用完后为什么要盖上灯帽
⑥用酒泡中药(药酒)—如泡枸杞
(易挥发)
(良好的有机溶剂)
(易挥发、有特殊香味)
(乙醇易溶于水)
(易挥发)
(良好的有机溶剂)
观察乙醇并联系生活归纳乙醇的物理性质
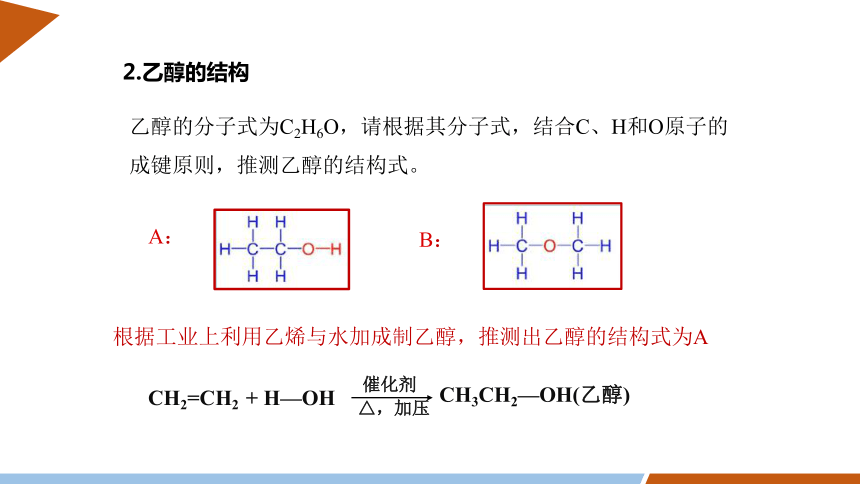
1.乙醇的物理性质
俗称 颜色 气味 沸点 状态 溶解性 密度
无色
特殊香味
液体
比水小
与水以任意比互溶,能溶解多种有机物和无机物
酒精
78.5℃易挥发
【思考】如何由工业酒精制备无水乙醇 怎样检验无水乙醇中有水
用工业酒精与新制生石灰后蒸馏,可得无水酒精。
取少量酒精,加入无水硫酸铜,若出现蓝色,则证明酒精含水。
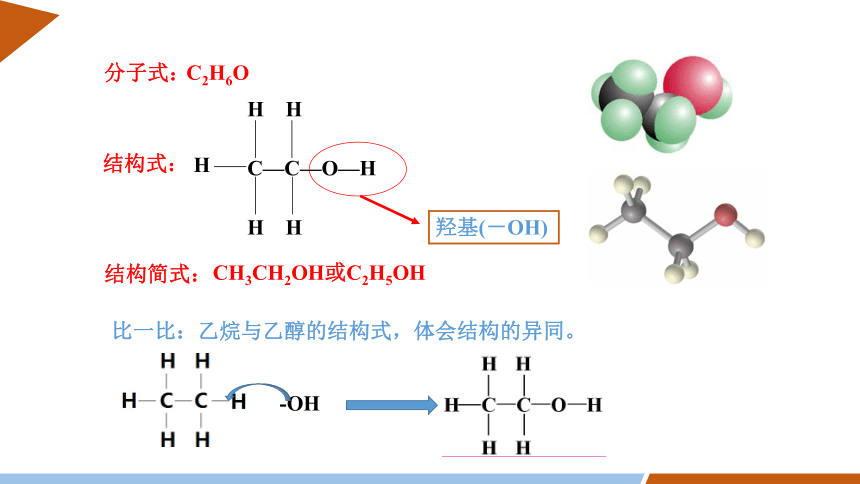
2.乙醇的结构
乙醇的分子式为C2H6O,请根据其分子式,结合C、H和O原子的成键原则,推测乙醇的结构式。
A:
B:
根据工业上利用乙烯与水加成制乙醇,推测出乙醇的结构式为A
CH2=CH2 + H—OH
催化剂
△,加压
CH3CH2—OH(乙醇)
羟基(-OH)
C—C—O—H
H
H
H
H
H
CH3CH2OH或C2H5OH
C2H6O
结构式:
分子式:
结构简式:
比一比:乙烷与乙醇的结构式,体会结构的异同。
-OH
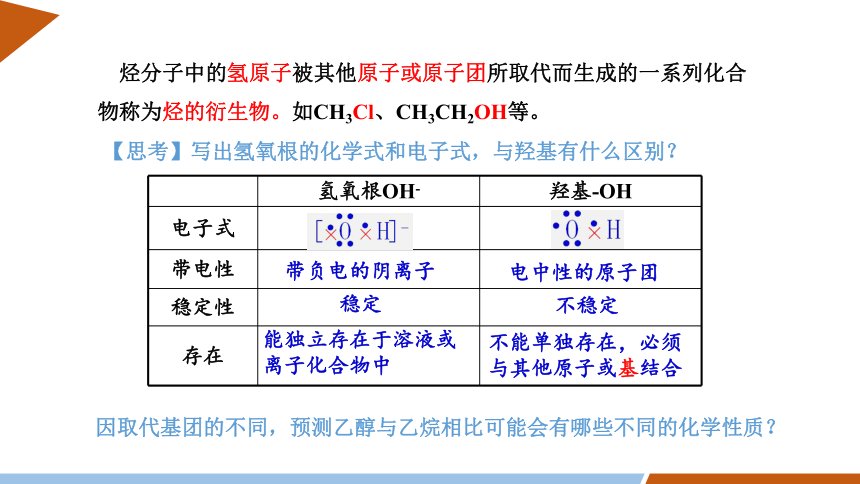
烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。如CH3Cl、CH3CH2OH等。
【思考】写出氢氧根的化学式和电子式,与羟基有什么区别?
因取代基团的不同,预测乙醇与乙烷相比可能会有哪些不同的化学性质?
氢氧根OH- 羟基-OH
电子式
带电性
稳定性
存在
带负电的阴离子
电中性的原子团
稳定
不稳定
能独立存在于溶液或离子化合物中
不能单独存在,必须与其他原子或基结合
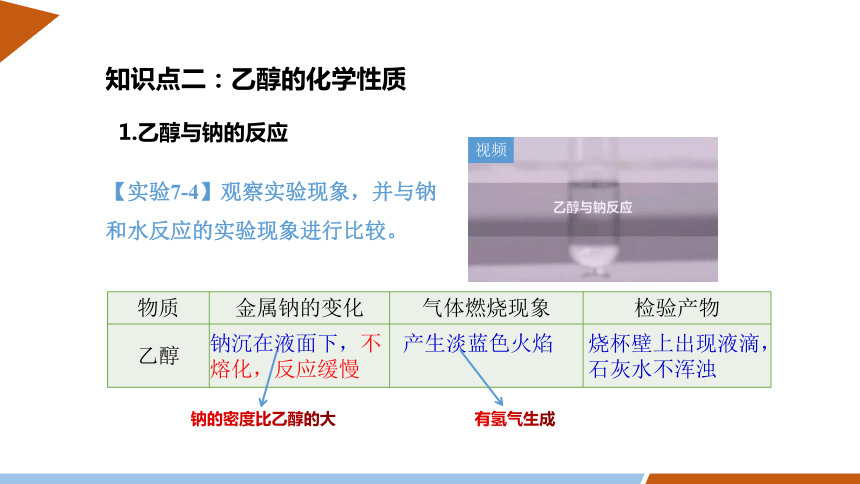
知识点二:乙醇的化学性质
1.乙醇与钠的反应
【实验7-4】观察实验现象,并与钠和水反应的实验现象进行比较。
物质 金属钠的变化 气体燃烧现象 检验产物
乙醇
钠沉在液面下,不熔化,反应缓慢
产生淡蓝色火焰
烧杯壁上出现液滴,石灰水不浑浊
钠的密度比乙醇的大
有氢气生成
视频
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
乙醇钠
类比:其它活泼金属如钾、镁和铝等也可与乙醇反应,均可产生H2 ,请写出镁与乙醇反应的化学方程式。
2CH3CH2OH + Mg (CH3CH2O)2Mg + H2↑
乙醇镁
置换反应
与水反应 与乙醇反应
钠是否浮在水面
钠的形状是否变化
有无声音
有无气泡
剧烈程度
剧烈
缓慢
浮在水面
熔成球形
发出嘶声
放出气泡
先沉后浮
仍为块状
没有声音
放出气泡
比较水和乙醇分别与Na反应
思考:从二者反应剧烈程度不同分析,乙醇和水分子的羟基中的H原子哪个较活泼?乙基对乙醇的性质有无影响?
1、羟基决定乙醇能和钠反应生成氢气
2、羟基中的H原子的活泼性:醇<水
则表明,乙醇与钠的反应相同条件下水与钠的反应缓和得多。
比较盐酸、水、乙醇反应置换氢气的难易:
盐酸>水>乙醇
【结论】
乙醇具有与乙烷不同的性质,从分子结构角度分析,是因为取代氢原子的羟基对乙醇的性质产生了影响。
像这种决定有机化合物特性的原子或原子团叫做官能团。羟基是醇类物质的官能团,碳碳双键和碳碳三键分别是烯烃和炔烃的官能团。
烃的衍生物分子一般可以看成是烃基和官能团相互结合组成的。例如,乙醇分子可以看成是由乙基和羟基组成的:CH3CH2-OH。
H—C≡C—H
常见的官能团:
卤素原子[-X(Cl、Br等)]、
羟基(-OH)、
羧基(-COOH)、醛基(-CHO)
碳碳双键、碳碳三键等。
注意:苯环( )不是官能团
2.氧化反应
2CO2 +3H2O
C2H5OH + 3O2
点燃
现象:产生淡蓝色火焰,同时放出大量热。
(1)燃烧反应(完全燃烧)
【思考】乙醇与氧气的反应,如果改变条件会发生怎样的变化。
【实验7-5】注意观察实验现象
视频
铜丝红
Δ
变黑
有刺激性气味
插入乙醇溶液中
又变红
Cu
Δ
CuO
乙醛CH3CHO
插入乙醇溶液中
Cu
分析:①发生反应 2Cu+O2==2CuO
分析:②生成新的物质—乙醛 CuO+CH3CH2OH Cu +CH3CHO+H2O
中间产物
现象及原因探究
(2)催化氧化
总反应:2C2H5OH + O2
Cu
2CH3CHO + 2 H2O
①
②
①
②
Cu作催化剂
Cu
Cu
反应历程
【思考】根据乙醇催化氧化的实质,推测的CH3OH、 催化氧化产物是什么?
能被催化氧化吗?它们和乙醇在分子结构上共同点是?都属于哪类有机物?不同点是分子组成上相差?它们的关系是?
【规律总结】
醇在有催化剂(铜或银)存在的条件下,可以发生催化氧化反应生成醛,但并不是所有的醇都能被氧化生成醛。只含有R—CH2OH(R代表烃基)结构的醇,在一定条件下才能被氧化成醛
世界卫生组织的事故调查显示,大约 50%~60% 交通事故与酒后驾车有关。
(3)被强氧化剂氧化
你知道吗
如何检查司机是否酒后驾车?
K 2 Cr2O7
CH3 CH2OH
Cr2(SO4 )3
CH3COOH
紫色褪去
CH3CH2OH
或酸性高锰酸钾溶液
酸性重铬酸钾溶液
橙色→绿色
乙醇
乙醛
乙酸
CO2+H2O
Cu/Ag,加热
O2
O2
KMnO4(H+)/K2Cr2O4(H+)
O2(点燃)
3.乙醇的用途
(1) 用作酒精灯、火锅、内燃机等的燃料。
(2) 用作化工原料、香料、化妆品、涂料等。
练一练
1.关于乙醇结构与性质方面的说法中正确的是( )
A.乙醇结构中有—OH,所以乙醇溶解于水,可以电离出OH-
B.乙醇能电离出H+,所以是电解质
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇、水分别与钠,乙醇的反应比水更平缓
D
C
2.可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以制酒精饮料
C.1 mol乙醇与足量的Na作用得到0.5 mol H2
D.乙醇与钠反应的产物为C2H5ONa
3.下列化合物结构中有两种官能团的是( )
A.CH2=CHCl B.CH3CH2OH
C.CH3COOH D.
4.乙醇分子中的各种化学键如图所示,对乙醇在各种反应中断键的说明不正确的是( )
A.与金属钠反应时,断裂①
B.与乙酸、浓硫酸共热时,断裂①
C.在Cu的催化作用下与O2反应,只断裂②
D.与浓硫酸共热到170℃时,断裂②⑤
C—C—O—H
H
H
H
H
H
⑤
④
②
③
①
A
C
5.已知乳酸的结构简式为 。
试回答:
(1)乳酸分子中含有 和 两种官能团(写名称);
(2)乳酸与金属钠溶液反应的化学方程
式 ;
(3)乳酸与Na2CO3溶液反应的化学方程式为 。
羟基
羧基
CH3-CH=COOH
OH
2CH3CH(OH)COOH+Na2CO3→2CH3CH(OH)COONa+CO2↑+H2O
乙醇
结构
分子式
结构式
官能团
性质
物理性质
化学性质
易挥发、无色有特殊香味的液体
与活泼金属反应
氧化反应
C2H6O
-OH羟基
第七章 有机化合物
第三节 乙醇和乙酸 课时1
早在几千年前,人类就掌握了发酵法酿酒的技术。各种酒类都含有浓度不等的乙醇。故乙醇俗称酒精。
1.知道乙醇的组成、结构、官能团、物理性质及用途。
2.知道烃的衍生物的概念及官能团与性质的关系,认识羟基与其性质的关系。
3.会运用乙醇的结构分析其化学性质。
知识点一:乙醇的物理性质与结构
①病人发烧通常用酒精擦拭全身,用此法降温。
②衣服上沾上少许汽油用酒精可以去除。
③酒香不怕巷子深
④白酒的主要成分是乙醇和水
⑤酒精灯用完后为什么要盖上灯帽
⑥用酒泡中药(药酒)—如泡枸杞
(易挥发)
(良好的有机溶剂)
(易挥发、有特殊香味)
(乙醇易溶于水)
(易挥发)
(良好的有机溶剂)
观察乙醇并联系生活归纳乙醇的物理性质
1.乙醇的物理性质
俗称 颜色 气味 沸点 状态 溶解性 密度
无色
特殊香味
液体
比水小
与水以任意比互溶,能溶解多种有机物和无机物
酒精
78.5℃易挥发
【思考】如何由工业酒精制备无水乙醇 怎样检验无水乙醇中有水
用工业酒精与新制生石灰后蒸馏,可得无水酒精。
取少量酒精,加入无水硫酸铜,若出现蓝色,则证明酒精含水。
2.乙醇的结构
乙醇的分子式为C2H6O,请根据其分子式,结合C、H和O原子的成键原则,推测乙醇的结构式。
A:
B:
根据工业上利用乙烯与水加成制乙醇,推测出乙醇的结构式为A
CH2=CH2 + H—OH
催化剂
△,加压
CH3CH2—OH(乙醇)
羟基(-OH)
C—C—O—H
H
H
H
H
H
CH3CH2OH或C2H5OH
C2H6O
结构式:
分子式:
结构简式:
比一比:乙烷与乙醇的结构式,体会结构的异同。
-OH
烃分子中的氢原子被其他原子或原子团所取代而生成的一系列化合物称为烃的衍生物。如CH3Cl、CH3CH2OH等。
【思考】写出氢氧根的化学式和电子式,与羟基有什么区别?
因取代基团的不同,预测乙醇与乙烷相比可能会有哪些不同的化学性质?
氢氧根OH- 羟基-OH
电子式
带电性
稳定性
存在
带负电的阴离子
电中性的原子团
稳定
不稳定
能独立存在于溶液或离子化合物中
不能单独存在,必须与其他原子或基结合
知识点二:乙醇的化学性质
1.乙醇与钠的反应
【实验7-4】观察实验现象,并与钠和水反应的实验现象进行比较。
物质 金属钠的变化 气体燃烧现象 检验产物
乙醇
钠沉在液面下,不熔化,反应缓慢
产生淡蓝色火焰
烧杯壁上出现液滴,石灰水不浑浊
钠的密度比乙醇的大
有氢气生成
视频
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2↑
乙醇钠
类比:其它活泼金属如钾、镁和铝等也可与乙醇反应,均可产生H2 ,请写出镁与乙醇反应的化学方程式。
2CH3CH2OH + Mg (CH3CH2O)2Mg + H2↑
乙醇镁
置换反应
与水反应 与乙醇反应
钠是否浮在水面
钠的形状是否变化
有无声音
有无气泡
剧烈程度
剧烈
缓慢
浮在水面
熔成球形
发出嘶声
放出气泡
先沉后浮
仍为块状
没有声音
放出气泡
比较水和乙醇分别与Na反应
思考:从二者反应剧烈程度不同分析,乙醇和水分子的羟基中的H原子哪个较活泼?乙基对乙醇的性质有无影响?
1、羟基决定乙醇能和钠反应生成氢气
2、羟基中的H原子的活泼性:醇<水
则表明,乙醇与钠的反应相同条件下水与钠的反应缓和得多。
比较盐酸、水、乙醇反应置换氢气的难易:
盐酸>水>乙醇
【结论】
乙醇具有与乙烷不同的性质,从分子结构角度分析,是因为取代氢原子的羟基对乙醇的性质产生了影响。
像这种决定有机化合物特性的原子或原子团叫做官能团。羟基是醇类物质的官能团,碳碳双键和碳碳三键分别是烯烃和炔烃的官能团。
烃的衍生物分子一般可以看成是烃基和官能团相互结合组成的。例如,乙醇分子可以看成是由乙基和羟基组成的:CH3CH2-OH。
H—C≡C—H
常见的官能团:
卤素原子[-X(Cl、Br等)]、
羟基(-OH)、
羧基(-COOH)、醛基(-CHO)
碳碳双键、碳碳三键等。
注意:苯环( )不是官能团
2.氧化反应
2CO2 +3H2O
C2H5OH + 3O2
点燃
现象:产生淡蓝色火焰,同时放出大量热。
(1)燃烧反应(完全燃烧)
【思考】乙醇与氧气的反应,如果改变条件会发生怎样的变化。
【实验7-5】注意观察实验现象
视频
铜丝红
Δ
变黑
有刺激性气味
插入乙醇溶液中
又变红
Cu
Δ
CuO
乙醛CH3CHO
插入乙醇溶液中
Cu
分析:①发生反应 2Cu+O2==2CuO
分析:②生成新的物质—乙醛 CuO+CH3CH2OH Cu +CH3CHO+H2O
中间产物
现象及原因探究
(2)催化氧化
总反应:2C2H5OH + O2
Cu
2CH3CHO + 2 H2O
①
②
①
②
Cu作催化剂
Cu
Cu
反应历程
【思考】根据乙醇催化氧化的实质,推测的CH3OH、 催化氧化产物是什么?
能被催化氧化吗?它们和乙醇在分子结构上共同点是?都属于哪类有机物?不同点是分子组成上相差?它们的关系是?
【规律总结】
醇在有催化剂(铜或银)存在的条件下,可以发生催化氧化反应生成醛,但并不是所有的醇都能被氧化生成醛。只含有R—CH2OH(R代表烃基)结构的醇,在一定条件下才能被氧化成醛
世界卫生组织的事故调查显示,大约 50%~60% 交通事故与酒后驾车有关。
(3)被强氧化剂氧化
你知道吗
如何检查司机是否酒后驾车?
K 2 Cr2O7
CH3 CH2OH
Cr2(SO4 )3
CH3COOH
紫色褪去
CH3CH2OH
或酸性高锰酸钾溶液
酸性重铬酸钾溶液
橙色→绿色
乙醇
乙醛
乙酸
CO2+H2O
Cu/Ag,加热
O2
O2
KMnO4(H+)/K2Cr2O4(H+)
O2(点燃)
3.乙醇的用途
(1) 用作酒精灯、火锅、内燃机等的燃料。
(2) 用作化工原料、香料、化妆品、涂料等。
练一练
1.关于乙醇结构与性质方面的说法中正确的是( )
A.乙醇结构中有—OH,所以乙醇溶解于水,可以电离出OH-
B.乙醇能电离出H+,所以是电解质
C.乙醇与钠反应可以产生氢气,所以乙醇显酸性
D.乙醇、水分别与钠,乙醇的反应比水更平缓
D
C
2.可以证明乙醇分子中有一个氢原子与另外的氢原子不同的方法是( )
A.1 mol乙醇完全燃烧生成3 mol水
B.乙醇可以制酒精饮料
C.1 mol乙醇与足量的Na作用得到0.5 mol H2
D.乙醇与钠反应的产物为C2H5ONa
3.下列化合物结构中有两种官能团的是( )
A.CH2=CHCl B.CH3CH2OH
C.CH3COOH D.
4.乙醇分子中的各种化学键如图所示,对乙醇在各种反应中断键的说明不正确的是( )
A.与金属钠反应时,断裂①
B.与乙酸、浓硫酸共热时,断裂①
C.在Cu的催化作用下与O2反应,只断裂②
D.与浓硫酸共热到170℃时,断裂②⑤
C—C—O—H
H
H
H
H
H
⑤
④
②
③
①
A
C
5.已知乳酸的结构简式为 。
试回答:
(1)乳酸分子中含有 和 两种官能团(写名称);
(2)乳酸与金属钠溶液反应的化学方程
式 ;
(3)乳酸与Na2CO3溶液反应的化学方程式为 。
羟基
羧基
CH3-CH=COOH
OH
2CH3CH(OH)COOH+Na2CO3→2CH3CH(OH)COONa+CO2↑+H2O
乙醇
结构
分子式
结构式
官能团
性质
物理性质
化学性质
易挥发、无色有特殊香味的液体
与活泼金属反应
氧化反应
C2H6O
-OH羟基
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
