第四章 章末复习 课件(共22页) 2023-2024学年高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 第四章 章末复习 课件(共22页) 2023-2024学年高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-12 22:49:01 | ||
图片预览






文档简介
(共22张PPT)
第四章 生物大分子
章末复习
1.能说明单糖,二糖和多糖的区别与联系,能探究葡萄糖的化学性质,描述淀粉和纤维素的典型性质;
2.能说明蛋白质的基本结构特点,辨识蛋白质结构中的肽键,判断氨基酸的缩合产物和多肽的水解产物;
3.能辨识核酸中的磷脂键,基于氢键分析碱基的配对原理,能说明核糖对于生命遗传的意义。
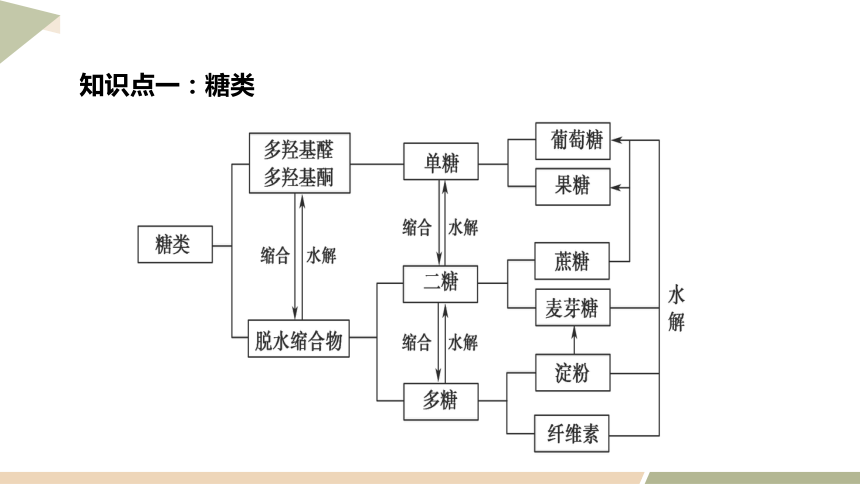
知识点一:糖类
1.葡萄糖
葡 萄 糖 分子式
结构简式
官能团
物理性质
化学性质
主要用途
C6H12O6
HOCH2(CHOH)4CHO
—OH、—CHO
白色晶体,有甜味,能溶于水
制镜业、糖果制造业、医药工业
加成(与H2)
氧化[与银氨溶液、与Cu(OH)2]
使溴水、酸性高锰酸钾溶液褪色
酯化(与羧酸)
2.果糖
(3)组成和结构:
C6H12O6
多羟基酮(5个羟基,1个羰基)属于酮糖,与葡萄糖互为同分异构体
(2)物理性质:
无色晶体,易溶于水,吸湿性强,比蔗糖的甜度高。
(1)分子式:
①加成反应
②酯化反应
③与活泼金属反应
(4)化学性质
CH2OH
C
HO—C—H
H—C—OH
H—C—OH
CH2OH
O
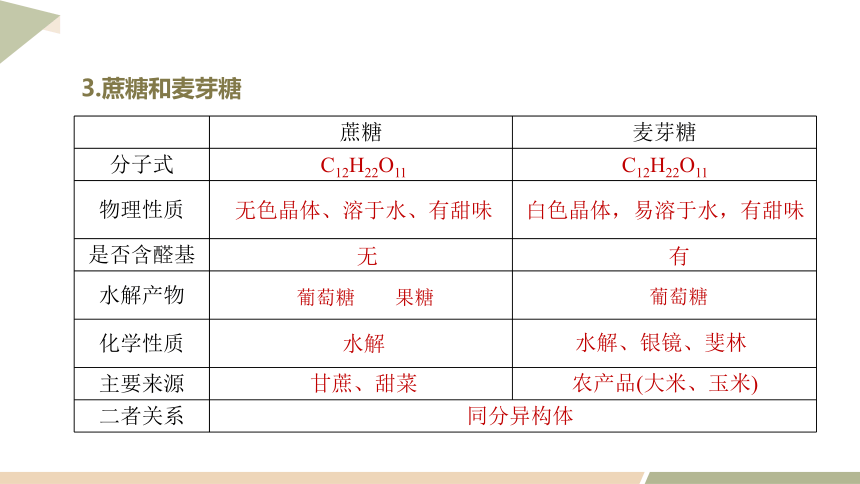
3.蔗糖和麦芽糖
蔗糖 麦芽糖
分子式
物理性质
是否含醛基
水解产物
化学性质
主要来源
二者关系
C12H22O11
C12H22O11
无色晶体、溶于水、有甜味
白色晶体,易溶于水,有甜味
无
有
葡萄糖 果糖
葡萄糖
甘蔗、甜菜
同分异构体
农产品(大米、玉米)
水解
水解、银镜、斐林
4.淀粉和纤维素
淀 粉 纤维素
通式
物理性质
化学性质
存在与 制法
用途
(C6H10O5)n
(C6H10O5)n
不溶于冷水,白色粉末
白色无嗅无味物质,不溶于
水,不溶于一般的有机溶剂
水解、酯化、与碘作用
呈蓝色
植物的种子、块茎和根里
食物、制葡萄糖、酒精
水解、酯化
木材、棉花
制硝酸纤维、纤维素乙酸酯、造纸、粘胶纤维
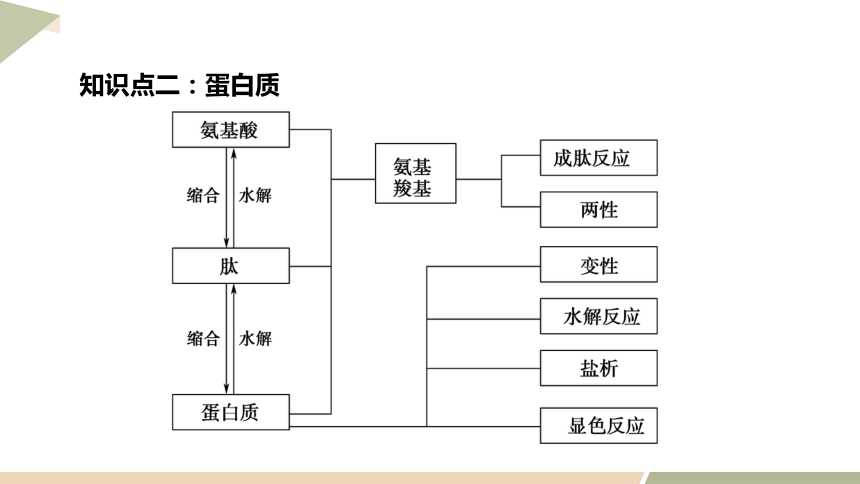
知识点二:蛋白质
1.氨基酸
(1)氨基酸的结构与物理性质性质
(2)氨基酸化学性质
R—CH—COOH
NH2
天然氨基酸均为 ,熔点 。
一般 溶于水,而 溶于乙醇、乙醚等有机溶剂。
无色晶体
较高
能
难
①两性
a.与盐酸的反应:
b.与氢氧化钠反应:
R—CH—COOH+NaOH
NH2
R—CH—COONa+H2O
NH2
R—CH—COOH+HCl
NH2
R—CH—COOH
NH3Cl
②成肽反应
一定条件下
H2N—CH—C—OH
R
O
H—N—CH—COOH
R1
H
+
二肽
O
H2N—CH—C
R
—N—CH—COOH
R1
H
+H2O
多种氨基酸分子间脱水以肽键相互结合,可形成蛋白质。
2.蛋白质
蛋白质含有 等元素,属于天然有机高分子化合物。
a.水解:在酸、碱或酶的作用下最终水解生成氨基酸。
b.两性:氨基-NH2有碱性,-COOH羧基有酸性。
c.盐析
d.变性
e.显色反应:含有苯环的蛋白质遇浓HNO3变黄色。
f.灼烧:蛋白质灼烧有烧焦羽毛的气味。
多种氨基酸分子按不同的排列顺序以肽键相互结合,可以形成千百万种具有不同的理化性质和生理活性的多肽链。相对分子量在10 000以上的,并具有一定空间结构的多肽,称为蛋白质。
C、H、O、N、S
化学性质
蛋白质的盐析和变性的比较
名称 盐析 变性
定义 当某些可溶性盐在蛋白质溶液中达到一定浓度时,会使蛋白质的溶解度降低而使其从溶液中析出 在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象称为蛋白质的变性
特征
实质
条 件
用途
碱金属、镁、铝等轻金属盐或铵盐的浓溶液
加热、加压、振荡、超声波、放射线、紫外线、强酸、强碱、重金属盐、甲醛、乙醇等
分离、提纯蛋白质
杀菌、消毒
溶解度降低,物理变化
结构、性质改变,化学变化
可逆
不可逆
①绝大多数酶是蛋白质,易变性。
②酶是一种生物催化剂,催化作用具有以下特点
3.酶
a.条件温和,不需加热;
b.具有高度的专一性;
c.具有高效催化作用。
知识点三:核酸
核酸是一类含磷的生物高分子化合物。它在生物体的生长、繁殖、遗传、变异等生命现象中起着决定性的作用。
分类 脱氧核糖核酸(DNA) 核糖核酸(RNA)
存在
生理作用
脱氧核糖核酸和核糖核酸的异同
磷酸
核苷 戊糖
碱基 相同
不同
大量存在于细胞核中
主要存在于细胞质中
生物体遗传信息的载体;
蛋白质合成的模板
参与生物体内蛋白质的合成
都含有
脱氧核糖
核糖
腺嘌呤(A)、鸟嘌呤(G)、胞嘧啶(C)
胸腺嘧啶(T)
尿嘧啶(U)
【考点一】有机化合物的水解反应及规律
1.下列有关有机化合物水解的叙述中不正确的是( )
A.油脂在酸性条件下水解与在碱性条件下水解程度不同,但产物完全相同
B.可用碘水检验淀粉水解是否完全
C.蛋白质水解的最终产物均为氨基酸
D.纤维素在牛、羊等食草动物的体内水解的最终产物为葡萄糖
A
【考点二】鉴别有机化合物的常用方法
1.可用于鉴别以下三种化合物的一组试剂是( )
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液④氢氧化钠溶液
A.②③ B.③④ C.①④ D.①②
A
鉴别有机化合物的常用方法
(1)溶解性法
有机化合物的溶解性不尽相同,有的易溶于水,如醇、醛、羧酸、单糖、二糖等;卤代烃、油脂等酯类化合物不溶于水易溶于有机溶剂。根据它们的溶解性不同,可以进行检验和鉴别。
(2)密度法
有机化合物的密度存在着差异。根据有机化合物密度的不同,尤其是相对于水的密度大小,通过观察不溶于水的有机化合物在水中的沉浮,而达到检验和鉴别的目的。如用水可以鉴别苯和硝基苯,也可以用水鉴别乙醇、苯和四氯化碳等。
(3)燃烧法
观察有机化合物能否燃烧,以及燃烧过程中的实验现象,燃烧后产生的气体气味等,可以检验和鉴别某些有机化合物。如观察燃烧时是否产生黑烟和黑烟的多少可以检验和鉴别乙烷、乙烯和乙炔等;通过观察是否燃烧可以区别四氯化碳和其他有机化合物,因为四氯化碳在空气中不燃烧;通过闻燃烧时的气味可以区别聚氯乙烯和蛋白质等。
(4)官能团法
有机化合物的性质差别在于其官能团,根据有机化合物官能团的差别检验和鉴别有机化合物,是最常用的化学方法。其一般思路是:官能团→性质→方法。常用的试剂和方法如下表。
鉴别有机化合物的常用方法
物质 试剂和方法 现象和结论
饱和烃和不饱和烃
苯和某些苯 的同系物
含醛基的物质
醇
羧酸
酯
酚类物质
淀粉溶液
蛋白质检验
溴水或酸性KMnO4溶液
褪色的是不饱和烃
酸性KMnO4溶液
褪色的是苯的同系物
银氨溶液、水浴加热或与新制Cu(OH)2共热
产生银镜;加热后出现
红色沉淀
金属钠
有气体放出
紫色石蕊溶液或NaHCO3溶液
显红色;有气体逸出
加稀硫酸
检验水解产物
FeCl3溶液或加溴水
显紫色;白色沉淀
碘水
显蓝色
浓硝酸或灼烧
显黄色;类似烧焦羽毛气味
2.鉴别下列物质所用试剂不正确的是( )
A.乙醇溶液和乙酸溶液用CaCO3固体
B.乙烷和乙烯用NaOH溶液
C.苯、CCl4和甲酸用水
D.乙烯和乙烷用溴水
3.在实验室中区别下列物质选用的试剂不正确的是(括号内为所选试剂,必要时可加热)( )
A.苯和己烯(溴水)
B.矿物油和植物油(NaOH溶液)
C.乙醛和乙酸[新制Cu(OH)2]
D.硝基苯和CCl4(水)
B
D
生物大分子
多糖
蛋白质
核酸
二糖
肽
核苷酸
单糖
氨基酸
水解缩合
水解缩合
水解缩合
水解缩合
水解缩合
第四章 生物大分子
章末复习
1.能说明单糖,二糖和多糖的区别与联系,能探究葡萄糖的化学性质,描述淀粉和纤维素的典型性质;
2.能说明蛋白质的基本结构特点,辨识蛋白质结构中的肽键,判断氨基酸的缩合产物和多肽的水解产物;
3.能辨识核酸中的磷脂键,基于氢键分析碱基的配对原理,能说明核糖对于生命遗传的意义。
知识点一:糖类
1.葡萄糖
葡 萄 糖 分子式
结构简式
官能团
物理性质
化学性质
主要用途
C6H12O6
HOCH2(CHOH)4CHO
—OH、—CHO
白色晶体,有甜味,能溶于水
制镜业、糖果制造业、医药工业
加成(与H2)
氧化[与银氨溶液、与Cu(OH)2]
使溴水、酸性高锰酸钾溶液褪色
酯化(与羧酸)
2.果糖
(3)组成和结构:
C6H12O6
多羟基酮(5个羟基,1个羰基)属于酮糖,与葡萄糖互为同分异构体
(2)物理性质:
无色晶体,易溶于水,吸湿性强,比蔗糖的甜度高。
(1)分子式:
①加成反应
②酯化反应
③与活泼金属反应
(4)化学性质
CH2OH
C
HO—C—H
H—C—OH
H—C—OH
CH2OH
O
3.蔗糖和麦芽糖
蔗糖 麦芽糖
分子式
物理性质
是否含醛基
水解产物
化学性质
主要来源
二者关系
C12H22O11
C12H22O11
无色晶体、溶于水、有甜味
白色晶体,易溶于水,有甜味
无
有
葡萄糖 果糖
葡萄糖
甘蔗、甜菜
同分异构体
农产品(大米、玉米)
水解
水解、银镜、斐林
4.淀粉和纤维素
淀 粉 纤维素
通式
物理性质
化学性质
存在与 制法
用途
(C6H10O5)n
(C6H10O5)n
不溶于冷水,白色粉末
白色无嗅无味物质,不溶于
水,不溶于一般的有机溶剂
水解、酯化、与碘作用
呈蓝色
植物的种子、块茎和根里
食物、制葡萄糖、酒精
水解、酯化
木材、棉花
制硝酸纤维、纤维素乙酸酯、造纸、粘胶纤维
知识点二:蛋白质
1.氨基酸
(1)氨基酸的结构与物理性质性质
(2)氨基酸化学性质
R—CH—COOH
NH2
天然氨基酸均为 ,熔点 。
一般 溶于水,而 溶于乙醇、乙醚等有机溶剂。
无色晶体
较高
能
难
①两性
a.与盐酸的反应:
b.与氢氧化钠反应:
R—CH—COOH+NaOH
NH2
R—CH—COONa+H2O
NH2
R—CH—COOH+HCl
NH2
R—CH—COOH
NH3Cl
②成肽反应
一定条件下
H2N—CH—C—OH
R
O
H—N—CH—COOH
R1
H
+
二肽
O
H2N—CH—C
R
—N—CH—COOH
R1
H
+H2O
多种氨基酸分子间脱水以肽键相互结合,可形成蛋白质。
2.蛋白质
蛋白质含有 等元素,属于天然有机高分子化合物。
a.水解:在酸、碱或酶的作用下最终水解生成氨基酸。
b.两性:氨基-NH2有碱性,-COOH羧基有酸性。
c.盐析
d.变性
e.显色反应:含有苯环的蛋白质遇浓HNO3变黄色。
f.灼烧:蛋白质灼烧有烧焦羽毛的气味。
多种氨基酸分子按不同的排列顺序以肽键相互结合,可以形成千百万种具有不同的理化性质和生理活性的多肽链。相对分子量在10 000以上的,并具有一定空间结构的多肽,称为蛋白质。
C、H、O、N、S
化学性质
蛋白质的盐析和变性的比较
名称 盐析 变性
定义 当某些可溶性盐在蛋白质溶液中达到一定浓度时,会使蛋白质的溶解度降低而使其从溶液中析出 在某些物理或化学因素的影响下,蛋白质的性质和生理功能发生改变的现象称为蛋白质的变性
特征
实质
条 件
用途
碱金属、镁、铝等轻金属盐或铵盐的浓溶液
加热、加压、振荡、超声波、放射线、紫外线、强酸、强碱、重金属盐、甲醛、乙醇等
分离、提纯蛋白质
杀菌、消毒
溶解度降低,物理变化
结构、性质改变,化学变化
可逆
不可逆
①绝大多数酶是蛋白质,易变性。
②酶是一种生物催化剂,催化作用具有以下特点
3.酶
a.条件温和,不需加热;
b.具有高度的专一性;
c.具有高效催化作用。
知识点三:核酸
核酸是一类含磷的生物高分子化合物。它在生物体的生长、繁殖、遗传、变异等生命现象中起着决定性的作用。
分类 脱氧核糖核酸(DNA) 核糖核酸(RNA)
存在
生理作用
脱氧核糖核酸和核糖核酸的异同
磷酸
核苷 戊糖
碱基 相同
不同
大量存在于细胞核中
主要存在于细胞质中
生物体遗传信息的载体;
蛋白质合成的模板
参与生物体内蛋白质的合成
都含有
脱氧核糖
核糖
腺嘌呤(A)、鸟嘌呤(G)、胞嘧啶(C)
胸腺嘧啶(T)
尿嘧啶(U)
【考点一】有机化合物的水解反应及规律
1.下列有关有机化合物水解的叙述中不正确的是( )
A.油脂在酸性条件下水解与在碱性条件下水解程度不同,但产物完全相同
B.可用碘水检验淀粉水解是否完全
C.蛋白质水解的最终产物均为氨基酸
D.纤维素在牛、羊等食草动物的体内水解的最终产物为葡萄糖
A
【考点二】鉴别有机化合物的常用方法
1.可用于鉴别以下三种化合物的一组试剂是( )
①银氨溶液 ②溴的四氯化碳溶液 ③氯化铁溶液④氢氧化钠溶液
A.②③ B.③④ C.①④ D.①②
A
鉴别有机化合物的常用方法
(1)溶解性法
有机化合物的溶解性不尽相同,有的易溶于水,如醇、醛、羧酸、单糖、二糖等;卤代烃、油脂等酯类化合物不溶于水易溶于有机溶剂。根据它们的溶解性不同,可以进行检验和鉴别。
(2)密度法
有机化合物的密度存在着差异。根据有机化合物密度的不同,尤其是相对于水的密度大小,通过观察不溶于水的有机化合物在水中的沉浮,而达到检验和鉴别的目的。如用水可以鉴别苯和硝基苯,也可以用水鉴别乙醇、苯和四氯化碳等。
(3)燃烧法
观察有机化合物能否燃烧,以及燃烧过程中的实验现象,燃烧后产生的气体气味等,可以检验和鉴别某些有机化合物。如观察燃烧时是否产生黑烟和黑烟的多少可以检验和鉴别乙烷、乙烯和乙炔等;通过观察是否燃烧可以区别四氯化碳和其他有机化合物,因为四氯化碳在空气中不燃烧;通过闻燃烧时的气味可以区别聚氯乙烯和蛋白质等。
(4)官能团法
有机化合物的性质差别在于其官能团,根据有机化合物官能团的差别检验和鉴别有机化合物,是最常用的化学方法。其一般思路是:官能团→性质→方法。常用的试剂和方法如下表。
鉴别有机化合物的常用方法
物质 试剂和方法 现象和结论
饱和烃和不饱和烃
苯和某些苯 的同系物
含醛基的物质
醇
羧酸
酯
酚类物质
淀粉溶液
蛋白质检验
溴水或酸性KMnO4溶液
褪色的是不饱和烃
酸性KMnO4溶液
褪色的是苯的同系物
银氨溶液、水浴加热或与新制Cu(OH)2共热
产生银镜;加热后出现
红色沉淀
金属钠
有气体放出
紫色石蕊溶液或NaHCO3溶液
显红色;有气体逸出
加稀硫酸
检验水解产物
FeCl3溶液或加溴水
显紫色;白色沉淀
碘水
显蓝色
浓硝酸或灼烧
显黄色;类似烧焦羽毛气味
2.鉴别下列物质所用试剂不正确的是( )
A.乙醇溶液和乙酸溶液用CaCO3固体
B.乙烷和乙烯用NaOH溶液
C.苯、CCl4和甲酸用水
D.乙烯和乙烷用溴水
3.在实验室中区别下列物质选用的试剂不正确的是(括号内为所选试剂,必要时可加热)( )
A.苯和己烯(溴水)
B.矿物油和植物油(NaOH溶液)
C.乙醛和乙酸[新制Cu(OH)2]
D.硝基苯和CCl4(水)
B
D
生物大分子
多糖
蛋白质
核酸
二糖
肽
核苷酸
单糖
氨基酸
水解缩合
水解缩合
水解缩合
水解缩合
水解缩合
