1.2 课时2 研究物质性质的基本程序 课件(共17张PPT,内嵌视频) 2023-2024学年高一化学鲁科版(2019)必修第一册
文档属性
| 名称 | 1.2 课时2 研究物质性质的基本程序 课件(共17张PPT,内嵌视频) 2023-2024学年高一化学鲁科版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 36.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-07-23 00:00:00 | ||
图片预览




文档简介
(共17张PPT)
第2节 研究物质性质的方法和程序 课时2
第一章 认识化学科学
1.了解研究物质性质的基本程序,能列举、描述、辨识氯气的重要物理性质。
2.掌握氯气与金属、非金属单质的反应及实验现象,并能正确书写相关方程式。
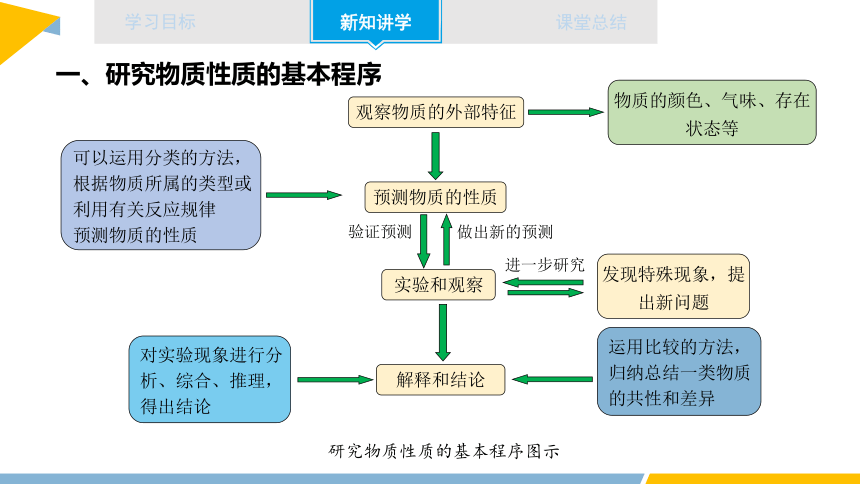
研究物质性质的基本程序图示
观察物质的外部特征
实验和观察
解释和结论
对实验现象进行分
析、综合、推理,
得出结论
运用比较的方法,
归纳总结一类物质
的共性和差异
发现特殊现象,提
出新问题
预测物质的性质
物质的颜色、气味、存在
状态等
验证预测
做出新的预测
进一步研究
可以运用分类的方法,
根据物质所属的类型或
利用有关反应规律
预测物质的性质
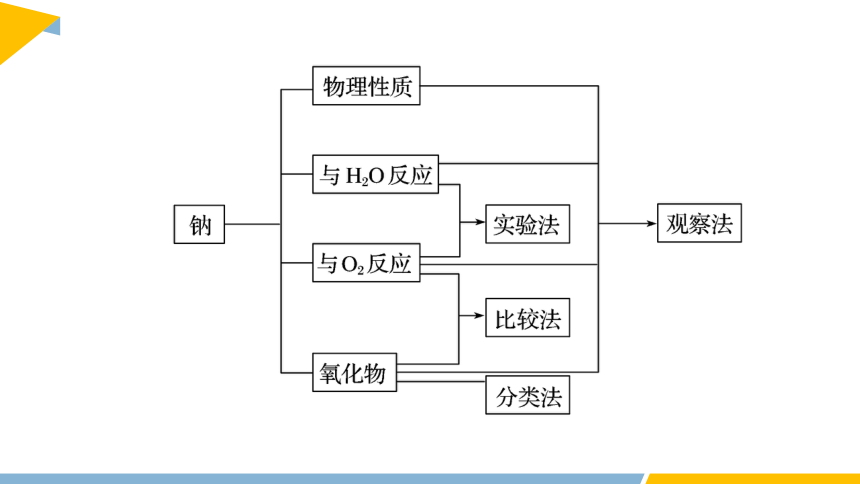
一、研究物质性质的基本程序
二、研究氯气的性质
氯的单质氯气是一种重要的化工原料。大量用于制造盐酸、有机溶剂、农药、杀菌消毒剂和药品等。
盐酸
有机溶剂
杀菌消毒剂
农药
药品
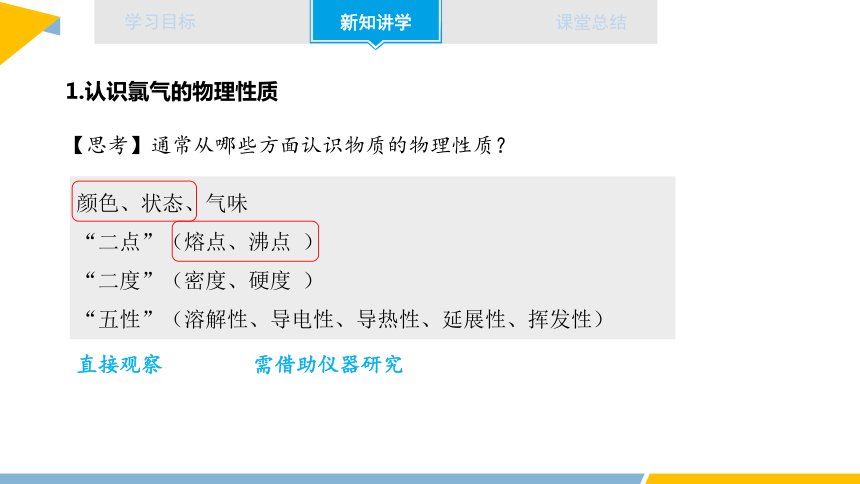
1.认识氯气的物理性质
【思考】通常从哪些方面认识物质的物理性质?
颜色、状态、气味
“二点”(熔点、沸点 )
“二度”(密度、硬度 )
“五性”(溶解性、导电性、导热性、延展性、挥发性)
直接观察
需借助仪器研究
颜色 气味 密度 水溶性 毒性 氯水颜色
色 强烈 气味 比空气___ 溶于水 _____ 色
黄绿
刺激性
大
能
有毒
浅黄绿
(1)氯气是一种非金属单质,根据氧气等非金属单质的化学性质,可以预测氯气具有哪些化学性质?
2.预测氯气的化学性质
(2)你将通过哪些实验来验证你的预测?
O2 能与钠、氢气、铁、铜等反应
Cl2 能与钠、氢气、铁、铜等反应
推断
3.实验验证
实验内容 实验现象 实验结论
氯气与金属钠的反应
氯气与铁丝的反应
氯气与铜丝的反应
实验内容及实验记录
a.氯气与金属单质的反应
视频
实验内容 实验现象 实验结论
氯气与金属钠的反应
氯气与铁丝的反应
氯气与铜丝的反应
实验内容及实验记录
熔化的钠球在氯气中剧烈的燃烧,产生白色的烟
2Na+Cl2 2NaCl
铁丝在氯气中剧烈的燃烧,产生棕红色的烟,溶于水得到黄色溶液
铜丝在氯气中剧烈的燃烧,产生棕黄色的烟,溶于水得到绿色溶液
2Fe+3Cl2 2FeCl3
Cu+Cl2 CuCl2
思考与讨论
1.在一定条件(点燃或灼热)下氯气能与金属反应,金属的价态变化有什么规律?
反应规律:金属与氯气反应生成高价态的金属氯化物
2.FeCl3和CuCl2能用金属与盐酸反应制取吗?为什么?
都不能,铁与盐酸反应生成氯化亚铁(FeCl2),铜与盐酸不反应。
2Na+Cl2 2NaCl
2Fe+3Cl2 2FeCl3
Cu+Cl2 CuCl2
b.氯气与非金属单质的反应
视频
实验内容 实验现象 实验结论
氯气与氢气的反应
实验内容及实验记录
纯净的氢气在氯气中安静燃烧,产生苍白色火焰,有白雾产生
H2 + Cl2 === 2HCl
点燃
将生成的HCl溶于水就能得到盐酸
注意:可燃性气体在加热或点燃前需要“验纯”!
如果将氯气和氢气混合再光照,可能会出现什么现象?
视频
H2 + Cl2 === 2HCl(爆炸)
光照
练一练
1.下列研究物质性质的基本程序排列正确的是( )
①观察物质的外观 ②实验和观察
③解释及结论 ④预测物质的性质
A.②①③④ B.①②③④
C.①④②③ D.④①②③
C
2.实验室中,下列行为不符合安全要求的是( )
A.在通风橱内制备有毒气体
B.金属钠着火时,立即用沙土覆盖
C.将过期的化学药品直接倒入下水道
D.闻气体时用手轻轻扇动,使少量气体飘进鼻孔
C
3.下列氯化物中,既能由金属和氯气直接化合生成,又能由金属和盐酸反应制得的是( )
A.CuCl2 B.FeCl2
C.FeCl3 D.AlCl3
D
氯气的性质
物理性质
化学性质
黄绿色、有刺激性气味气体,密度比空气大,能溶于水
与金属单质反应
与非金属单质反应
2Na + Cl2 ===== 2NaCl
2Fe + 3Cl2 ===== 2FeCl3
H2 + Cl2 ===== 2HCl
Cu + Cl2 ===== CuCl2
点燃
点燃
点燃
点燃
第2节 研究物质性质的方法和程序 课时2
第一章 认识化学科学
1.了解研究物质性质的基本程序,能列举、描述、辨识氯气的重要物理性质。
2.掌握氯气与金属、非金属单质的反应及实验现象,并能正确书写相关方程式。
研究物质性质的基本程序图示
观察物质的外部特征
实验和观察
解释和结论
对实验现象进行分
析、综合、推理,
得出结论
运用比较的方法,
归纳总结一类物质
的共性和差异
发现特殊现象,提
出新问题
预测物质的性质
物质的颜色、气味、存在
状态等
验证预测
做出新的预测
进一步研究
可以运用分类的方法,
根据物质所属的类型或
利用有关反应规律
预测物质的性质
一、研究物质性质的基本程序
二、研究氯气的性质
氯的单质氯气是一种重要的化工原料。大量用于制造盐酸、有机溶剂、农药、杀菌消毒剂和药品等。
盐酸
有机溶剂
杀菌消毒剂
农药
药品
1.认识氯气的物理性质
【思考】通常从哪些方面认识物质的物理性质?
颜色、状态、气味
“二点”(熔点、沸点 )
“二度”(密度、硬度 )
“五性”(溶解性、导电性、导热性、延展性、挥发性)
直接观察
需借助仪器研究
颜色 气味 密度 水溶性 毒性 氯水颜色
色 强烈 气味 比空气___ 溶于水 _____ 色
黄绿
刺激性
大
能
有毒
浅黄绿
(1)氯气是一种非金属单质,根据氧气等非金属单质的化学性质,可以预测氯气具有哪些化学性质?
2.预测氯气的化学性质
(2)你将通过哪些实验来验证你的预测?
O2 能与钠、氢气、铁、铜等反应
Cl2 能与钠、氢气、铁、铜等反应
推断
3.实验验证
实验内容 实验现象 实验结论
氯气与金属钠的反应
氯气与铁丝的反应
氯气与铜丝的反应
实验内容及实验记录
a.氯气与金属单质的反应
视频
实验内容 实验现象 实验结论
氯气与金属钠的反应
氯气与铁丝的反应
氯气与铜丝的反应
实验内容及实验记录
熔化的钠球在氯气中剧烈的燃烧,产生白色的烟
2Na+Cl2 2NaCl
铁丝在氯气中剧烈的燃烧,产生棕红色的烟,溶于水得到黄色溶液
铜丝在氯气中剧烈的燃烧,产生棕黄色的烟,溶于水得到绿色溶液
2Fe+3Cl2 2FeCl3
Cu+Cl2 CuCl2
思考与讨论
1.在一定条件(点燃或灼热)下氯气能与金属反应,金属的价态变化有什么规律?
反应规律:金属与氯气反应生成高价态的金属氯化物
2.FeCl3和CuCl2能用金属与盐酸反应制取吗?为什么?
都不能,铁与盐酸反应生成氯化亚铁(FeCl2),铜与盐酸不反应。
2Na+Cl2 2NaCl
2Fe+3Cl2 2FeCl3
Cu+Cl2 CuCl2
b.氯气与非金属单质的反应
视频
实验内容 实验现象 实验结论
氯气与氢气的反应
实验内容及实验记录
纯净的氢气在氯气中安静燃烧,产生苍白色火焰,有白雾产生
H2 + Cl2 === 2HCl
点燃
将生成的HCl溶于水就能得到盐酸
注意:可燃性气体在加热或点燃前需要“验纯”!
如果将氯气和氢气混合再光照,可能会出现什么现象?
视频
H2 + Cl2 === 2HCl(爆炸)
光照
练一练
1.下列研究物质性质的基本程序排列正确的是( )
①观察物质的外观 ②实验和观察
③解释及结论 ④预测物质的性质
A.②①③④ B.①②③④
C.①④②③ D.④①②③
C
2.实验室中,下列行为不符合安全要求的是( )
A.在通风橱内制备有毒气体
B.金属钠着火时,立即用沙土覆盖
C.将过期的化学药品直接倒入下水道
D.闻气体时用手轻轻扇动,使少量气体飘进鼻孔
C
3.下列氯化物中,既能由金属和氯气直接化合生成,又能由金属和盐酸反应制得的是( )
A.CuCl2 B.FeCl2
C.FeCl3 D.AlCl3
D
氯气的性质
物理性质
化学性质
黄绿色、有刺激性气味气体,密度比空气大,能溶于水
与金属单质反应
与非金属单质反应
2Na + Cl2 ===== 2NaCl
2Fe + 3Cl2 ===== 2FeCl3
H2 + Cl2 ===== 2HCl
Cu + Cl2 ===== CuCl2
点燃
点燃
点燃
点燃
