3.1 课时2 铁、铁的氧化物和铁的氢氧化物 课件 (共18页)2023-2024学年高一化学鲁科版(2019)必修第一册
文档属性
| 名称 | 3.1 课时2 铁、铁的氧化物和铁的氢氧化物 课件 (共18页)2023-2024学年高一化学鲁科版(2019)必修第一册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 21.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-14 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
铁的多样性 课时2
第三章 物质的性质与转化
1.掌握铁单质、铁的氧化物、铁的氢氧化物的性质。
2.通过绘制“价—类”二维图掌握铁与铁的化合物的相互转化。
3.了解铁及其重要化合物在生产、生活中的应用。
交流 研讨
从物质类别和铁元素化合价的角度分析,铁单质、铁的各种氧化物、铁的两种氢氧化物分别可能具有哪些性质?为什么?
一、铁、铁的氧化物和铁的氢氧化物
(1)铁的物理性质:
光亮的银白色金属,密度较大。
熔沸点较高:熔点1538℃,沸点2750℃。
纯铁有良好的导电性和导热性,导电性比铜、铝差,能被磁铁吸引。
1、铁的性质
(2)铁的化学性质
①金属通性
与非金属单质反应
与酸反应
与盐溶液反应
与水反应
3Fe+2O2===Fe3O4
点燃
2Fe+3Cl2===2FeCl3
点燃
棕红色的烟
Fe+2HCl===FeCl2+H2↑
Fe+CuSO4===FeSO4+Cu
3Fe+4H2O(g) Fe3O4+4H2
高温
‖
该实验体现了铁的什么性质?
②铁粉与水蒸气的反应
放出大量的热,并产生一种无色无味、点燃产生爆鸣声的气体
化合价升高,Fe具有还原性
实验现象
视频
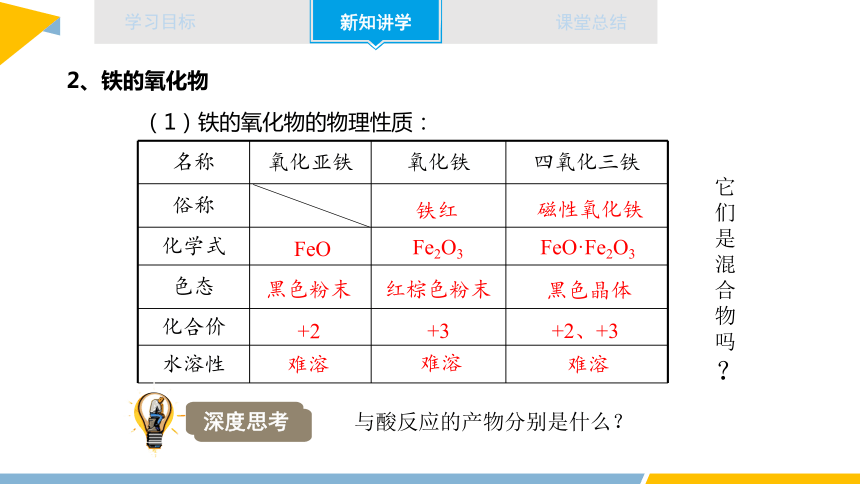
2、铁的氧化物
名称 氧化亚铁 氧化铁 四氧化三铁
俗称
化学式
色态
化合价
水溶性
铁红
磁性氧化铁
FeO
Fe2O3
Fe3O4
黑色粉末
红棕色粉末
黑色晶体
+2
+3
+2、+3
难溶
难溶
难溶
与酸反应的产物分别是什么?
深度思考
FeO·Fe2O3
它们是混合物吗
?
(1)铁的氧化物的物理性质:
FeO+2HCl=FeCl2+H2O
Fe2O3+6HCl=2FeCl3+3H2O
Fe3O4+8HCl=2FeCl3+FeCl2+4H2O
①与酸反应
Fe2O3+2Al===2Fe+Al2O3
高温
②与还原剂反应(铝热反应)
离子方程式
FeO+2H+=Fe2++H2O
Fe2O3+6H+=2Fe3++3H2O
Fe3O4+8H+=2Fe3++Fe2++4H2O
得到2×3e-
(2)铁的氧化物的化学性质:
失去2×3e-
(3)铁的氧化物在生活中的应用:
FeO可做色素
Fe3O4可做磁性材料
Fe2O3常做油漆、涂料
3、铁的氢氧化物
Fe(OH)2
Fe(OH)3
溶解度
化学式
色态
白色固体
红褐色固体
难溶
难溶
(1)铁的氢氧化物的物理性质:
(2)铁的氢氧化物的化学性质:
①与盐酸反应
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=Fe3++3H2O
深度思考
如何制备铁的氢氧化物?
Fe(OH)2不稳定,易被空气氧化
4 Fe(OH)2+ 2H2O + O2===4 Fe(OH)3
铁盐与亚铁盐分别与碱溶液的反应
在实验室中,常在亚铁盐溶液中加入少量铁粉,防氧化
实验现象
①生成红褐色沉淀。
②生成白色沉淀,迅速变为灰绿色,最终变为红褐色。
视频
二、铁及其化合物之间的转化关系
交流 研讨
1.请根据之前所学的有关铁及其化合物的知识,在铁及其化合物的“价—类”二维图中适当位置标注含铁物质,并用箭头标明物质之间的转化关系
铁及其化合物的“价—类”二维图
盐
单质
碱
氧化物
+2
0
+3
铁元素化合价
物质类别
Fe
Fe(OH)3
Fe(OH)2
Fe2+
Fe3+
Fe2O3
FeO
2.说明实现铁及其化合物之间转化的思路与方法。
①含有相同价态铁元素的物质之间的转化,可借助复分解反应实现
②含有不同价态铁元素的物质之间的转化,可借助氧化还原反应实现。
FeCl3+ 3NaOH = Fe(OH)3 +3NaCl
↓
Fe2O3+2Al====2Fe+Al2O3
高温
3Fe+4H2O(g) Fe3O4+4H2
高温
‖
Fe(OH)2+2HCl = FeCl2+2H2O
1.下列叙述正确的是( )
①铁能被磁铁吸引
②可以通过化合反应得到FeCl2和Fe3O4
③Fe在纯氧中燃烧可得Fe2O3
④Fe2O3不可与水反应得Fe(OH)3,所以不能通过化合反应制Fe(OH)3
⑤Fe(OH)2在空气中加热,可得FeO
A.①② B.②④
C.②③④⑤ D.①②⑤
A
练一练
2.下列转化关系不能通过一步反应实现的是( )
A.Fe→FeCl2 B.Fe2O3→Fe(OH)3
C.FeCl3→FeCl2 D.Fe(OH)3→FeCl3
B
3.下列反应的离子方程式正确的是( )
A.Fe与FeCl3溶液反应:Fe+Fe3+===2Fe2+
B.Fe3O4与盐酸反应:Fe3O4+8H+===3Fe3++4H2O
C.Fe(OH)3与稀H2SO4反应:OH-+H+===H2O
D.Fe与CuSO4溶液反应:Fe+Cu2+===Cu+Fe2+
D
4.判断下列说法是否正确,正确的打“√”,错误的打“×”。
1.Fe分别与氯气和盐酸反应所得氯化物不相同。( )
2.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2。 ( )
3.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3。( )
4.将水蒸气通过灼热的铁粉,铁与水在高温下反应,粉末变红。( )
x
x
x
√
铁及其化合物
铁单质
铁的氧化物
铁的氢氧化物
物质之间转化
与非金属单质反应
与酸反应
与盐溶液反应
与水蒸气反应
与酸反应
氢氧化亚铁
FeO、Fe2O3、Fe3O4
与酸反应
铝热反应
在空气中易氧化
应用
FeO用于瓷器制作
氢氧化铁
Fe3O4可做磁性材料
Fe2O3可做油漆、涂料
亚铁盐溶液中加铁粉防氧化
相同价态
不同价态
复分解反应
氧化还原反应
铁的多样性 课时2
第三章 物质的性质与转化
1.掌握铁单质、铁的氧化物、铁的氢氧化物的性质。
2.通过绘制“价—类”二维图掌握铁与铁的化合物的相互转化。
3.了解铁及其重要化合物在生产、生活中的应用。
交流 研讨
从物质类别和铁元素化合价的角度分析,铁单质、铁的各种氧化物、铁的两种氢氧化物分别可能具有哪些性质?为什么?
一、铁、铁的氧化物和铁的氢氧化物
(1)铁的物理性质:
光亮的银白色金属,密度较大。
熔沸点较高:熔点1538℃,沸点2750℃。
纯铁有良好的导电性和导热性,导电性比铜、铝差,能被磁铁吸引。
1、铁的性质
(2)铁的化学性质
①金属通性
与非金属单质反应
与酸反应
与盐溶液反应
与水反应
3Fe+2O2===Fe3O4
点燃
2Fe+3Cl2===2FeCl3
点燃
棕红色的烟
Fe+2HCl===FeCl2+H2↑
Fe+CuSO4===FeSO4+Cu
3Fe+4H2O(g) Fe3O4+4H2
高温
‖
该实验体现了铁的什么性质?
②铁粉与水蒸气的反应
放出大量的热,并产生一种无色无味、点燃产生爆鸣声的气体
化合价升高,Fe具有还原性
实验现象
视频
2、铁的氧化物
名称 氧化亚铁 氧化铁 四氧化三铁
俗称
化学式
色态
化合价
水溶性
铁红
磁性氧化铁
FeO
Fe2O3
Fe3O4
黑色粉末
红棕色粉末
黑色晶体
+2
+3
+2、+3
难溶
难溶
难溶
与酸反应的产物分别是什么?
深度思考
FeO·Fe2O3
它们是混合物吗
?
(1)铁的氧化物的物理性质:
FeO+2HCl=FeCl2+H2O
Fe2O3+6HCl=2FeCl3+3H2O
Fe3O4+8HCl=2FeCl3+FeCl2+4H2O
①与酸反应
Fe2O3+2Al===2Fe+Al2O3
高温
②与还原剂反应(铝热反应)
离子方程式
FeO+2H+=Fe2++H2O
Fe2O3+6H+=2Fe3++3H2O
Fe3O4+8H+=2Fe3++Fe2++4H2O
得到2×3e-
(2)铁的氧化物的化学性质:
失去2×3e-
(3)铁的氧化物在生活中的应用:
FeO可做色素
Fe3O4可做磁性材料
Fe2O3常做油漆、涂料
3、铁的氢氧化物
Fe(OH)2
Fe(OH)3
溶解度
化学式
色态
白色固体
红褐色固体
难溶
难溶
(1)铁的氢氧化物的物理性质:
(2)铁的氢氧化物的化学性质:
①与盐酸反应
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=Fe3++3H2O
深度思考
如何制备铁的氢氧化物?
Fe(OH)2不稳定,易被空气氧化
4 Fe(OH)2+ 2H2O + O2===4 Fe(OH)3
铁盐与亚铁盐分别与碱溶液的反应
在实验室中,常在亚铁盐溶液中加入少量铁粉,防氧化
实验现象
①生成红褐色沉淀。
②生成白色沉淀,迅速变为灰绿色,最终变为红褐色。
视频
二、铁及其化合物之间的转化关系
交流 研讨
1.请根据之前所学的有关铁及其化合物的知识,在铁及其化合物的“价—类”二维图中适当位置标注含铁物质,并用箭头标明物质之间的转化关系
铁及其化合物的“价—类”二维图
盐
单质
碱
氧化物
+2
0
+3
铁元素化合价
物质类别
Fe
Fe(OH)3
Fe(OH)2
Fe2+
Fe3+
Fe2O3
FeO
2.说明实现铁及其化合物之间转化的思路与方法。
①含有相同价态铁元素的物质之间的转化,可借助复分解反应实现
②含有不同价态铁元素的物质之间的转化,可借助氧化还原反应实现。
FeCl3+ 3NaOH = Fe(OH)3 +3NaCl
↓
Fe2O3+2Al====2Fe+Al2O3
高温
3Fe+4H2O(g) Fe3O4+4H2
高温
‖
Fe(OH)2+2HCl = FeCl2+2H2O
1.下列叙述正确的是( )
①铁能被磁铁吸引
②可以通过化合反应得到FeCl2和Fe3O4
③Fe在纯氧中燃烧可得Fe2O3
④Fe2O3不可与水反应得Fe(OH)3,所以不能通过化合反应制Fe(OH)3
⑤Fe(OH)2在空气中加热,可得FeO
A.①② B.②④
C.②③④⑤ D.①②⑤
A
练一练
2.下列转化关系不能通过一步反应实现的是( )
A.Fe→FeCl2 B.Fe2O3→Fe(OH)3
C.FeCl3→FeCl2 D.Fe(OH)3→FeCl3
B
3.下列反应的离子方程式正确的是( )
A.Fe与FeCl3溶液反应:Fe+Fe3+===2Fe2+
B.Fe3O4与盐酸反应:Fe3O4+8H+===3Fe3++4H2O
C.Fe(OH)3与稀H2SO4反应:OH-+H+===H2O
D.Fe与CuSO4溶液反应:Fe+Cu2+===Cu+Fe2+
D
4.判断下列说法是否正确,正确的打“√”,错误的打“×”。
1.Fe分别与氯气和盐酸反应所得氯化物不相同。( )
2.Fe在足量Cl2中燃烧生成FeCl3,在少量Cl2中燃烧生成FeCl2。 ( )
3.Fe与Cl2反应生成FeCl3,推测Fe与I2反应生成FeI3。( )
4.将水蒸气通过灼热的铁粉,铁与水在高温下反应,粉末变红。( )
x
x
x
√
铁及其化合物
铁单质
铁的氧化物
铁的氢氧化物
物质之间转化
与非金属单质反应
与酸反应
与盐溶液反应
与水蒸气反应
与酸反应
氢氧化亚铁
FeO、Fe2O3、Fe3O4
与酸反应
铝热反应
在空气中易氧化
应用
FeO用于瓷器制作
氢氧化铁
Fe3O4可做磁性材料
Fe2O3可做油漆、涂料
亚铁盐溶液中加铁粉防氧化
相同价态
不同价态
复分解反应
氧化还原反应
