专题六 选择题专攻 2.溶液中粒子浓度大小比较(共36张PPT)-2024年高考化学二轮复习
文档属性
| 名称 | 专题六 选择题专攻 2.溶液中粒子浓度大小比较(共36张PPT)-2024年高考化学二轮复习 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-13 00:00:00 | ||
图片预览











文档简介
(共36张PPT)
选择题专攻
2.溶液中粒子浓度大小比较
核心精讲
01
1.单一溶液
(1)Na2S溶液
水解方程式:________________________________________________;
离子浓度大小关系:___________________________________;
电荷守恒:________________________________________;
元素质量守恒:_________________________________;
质子守恒:________________________________。
S2-+H2O HS-+OH-、HS-+H2O H2S+OH-
c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)
c(Na+)=2[c(S2-)+c(HS-)+c(H2S)]
c(OH-)=c(H+)+c(HS-)+2c(H2S)
(2)NaHS溶液
水解方程式:_________________________;
离子浓度大小关系:____________________________________;
电荷守恒:________________________________________;
元素质量守恒:_______________________________;
质子守恒:_______________________________。
HS-+H2O H2S+OH-
c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)
c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-)
c(Na+)=c(S2-)+c(HS-)+c(H2S)
c(OH-)+c(S2-)=c(H+)+c(H2S)
NaHS既能发生水解又能发生电离,水溶液呈碱性:
HS-+H2O H2S+OH-(主要);
HS- H++S2-(次要)。
2.混合溶液
(1)等物质的量浓度、等体积的CH3COOH、CH3COONa溶液
水解方程式:____________________________________;
离子浓度大小关系:__________________________________;
电荷守恒:_____________________________________;
元素质量守恒:____________________________________;
质子守恒:____________________________________________。
CH3COO-+H2O CH3COOH+OH-
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
2c(Na+)=c(CH3COO-)+c(CH3COOH)
c(CH3COO-)+2c(OH-)=c(CH3COOH)+2c(H+)
CH3COOH CH3COO-+H+(主要),CH3COO-+H2O
CH3COOH+OH-(次要),水溶液呈酸性。
(2)CH3COOH、CH3COONa混合溶液呈中性
离子浓度大小关系:____________________________________;
电荷守恒:_____________________________________;
元素质量守恒:_____________________。
c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
c(Na+)=c(CH3COO-)
CH3COOH CH3COO-+H+
CH3COO-+H2O CH3COOH+OH-
若溶液呈中性,则电离和水解相互抵消。
(3)常温下pH=2的CH3COOH与pH=12的NaOH等体积混合的溶液
离子浓度大小关系:__________________________________;
电荷守恒:_____________________________________。
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
由于CH3COOH是弱酸,所以当完全反应后,CH3COOH仍过量许多,溶液呈酸性。
(4)等物质的量浓度、等体积的Na2CO3—NaHCO3混合溶液
电荷守恒:__________________________________________;
元素质量守恒:______________________________________;
质子守恒:_____________________________________________;
离子浓度大小关系:________________________________________。
真题演练
02
1
2
3
1.(2023·江苏,12)室温下,用含少量Mg2+的MnSO4溶液制备MnCO3的过程如图所示。已知Ksp(MgF2)=5.2×10-11,Ka(HF)=6.3×10-4。下列说法正确的是
√
1
2
3
0.1 mol·L-1NaF溶液中存在电荷
守恒:c(OH-)+c(F-)=c(Na+)+
c(H+),A错误;
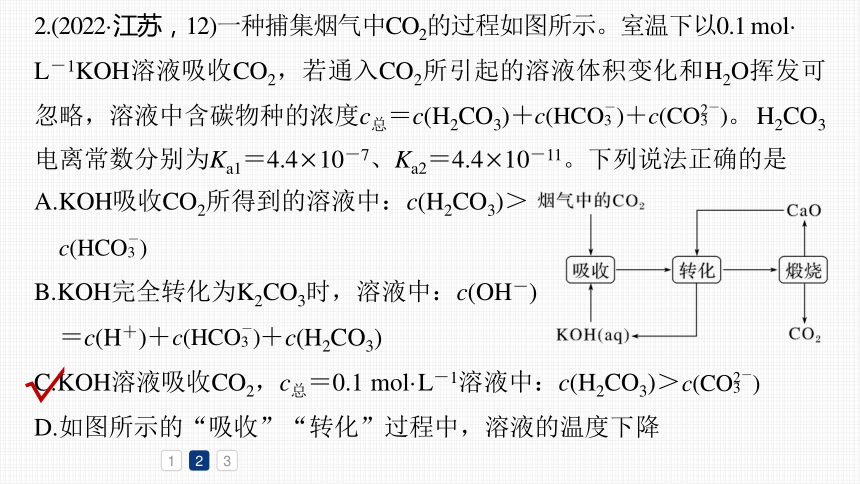
2.(2022·江苏,12)一种捕集烟气中CO2的过程如图所示。室温下以0.1 mol·
L-1KOH溶液吸收CO2,若通入CO2所引起的溶液体积变化和H2O挥发可忽略,溶液中含碳物种的浓度c总=c(H2CO3)+ 。H2CO3电离常数分别为Ka1=4.4×10-7、Ka2=4.4×10-11。下列说法正确的是
A.KOH吸收CO2所得到的溶液中:c(H2CO3)>
B.KOH完全转化为K2CO3时,溶液中:c(OH-)
=c(H+)+ +c(H2CO3)
C.KOH溶液吸收CO2,c总=0.1 mol·L-1溶液中:c(H2CO3)>
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
√
1
2
3
1
2
3
如图所示的“吸收”“转化”过程中,发生的反应为CO2+2KOH
===K2CO3+H2O、K2CO3+CaO+H2O===CaCO3↓+2KOH(若生成KHCO3或K2CO3与KHCO3的混合物,则原理相同),上述反应均放热,溶液的温度升高,D不正确。
1
2
3
1
2
3
3.(2020·江苏,14改编)室温下,将两种浓度均为0.10 mol·L-1的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
√
1
2
3
C项,溶液呈酸性,说明CH3COOH电离的程度大于CH3COO-水解的程度,则溶液中微粒浓度关系为c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+),错误;
1
2
3
考向预测
03
1
2
3
4
5
1.(2023·江苏省百校高三下学期第三次联考)一种吸收SO2再经氧化得到硫酸盐的过程如图所示。室温下,用0.1 mol·L-1的NaOH溶液吸收SO2,若通入SO2所引起的溶液体积变化和H2O挥发可忽略,溶液中含硫物种的浓度c(总)=
+c(H2SO3)。H2SO3的电离常数为Ka1=1.29×10-2、Ka2=6.24×10-8。下列说法正确的是
√
1
2
3
4
5
NaOH溶液的物质的量浓度为0.1 mol·
L-1,c(总)=0.1 mol·L-1溶液中的溶
质为NaHSO3,在NaHSO3溶液中存在质子守恒:c(OH-)+ =
c(H+)+c(H2SO3),故A错误;
1
2
3
4
5
1
2
3
4
5
√
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
3.(2023·江苏苏北四市统考)工业上可利用氨水吸收SO2和NO2,原理如图所示。已知: 25 ℃时,NH3·H2O的Kb=1.7×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8,下列说法正确的是
√
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
√
1
2
3
4
5
NaHCO3溶液呈碱性,人体血液碱中毒时,应注射酸性溶液缓解,A错误;
1
2
3
4
5
1
2
3
4
5
√
1
2
3
4
5
1
2
3
4
5
本课结束
选择题专攻
2.溶液中粒子浓度大小比较
核心精讲
01
1.单一溶液
(1)Na2S溶液
水解方程式:________________________________________________;
离子浓度大小关系:___________________________________;
电荷守恒:________________________________________;
元素质量守恒:_________________________________;
质子守恒:________________________________。
S2-+H2O HS-+OH-、HS-+H2O H2S+OH-
c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
c(Na+)+c(H+)=2c(S2-)+c(HS-)+c(OH-)
c(Na+)=2[c(S2-)+c(HS-)+c(H2S)]
c(OH-)=c(H+)+c(HS-)+2c(H2S)
(2)NaHS溶液
水解方程式:_________________________;
离子浓度大小关系:____________________________________;
电荷守恒:________________________________________;
元素质量守恒:_______________________________;
质子守恒:_______________________________。
HS-+H2O H2S+OH-
c(Na+)>c(HS-)>c(OH-)>c(H+)>c(S2-)
c(Na+)+c(H+)=c(HS-)+2c(S2-)+c(OH-)
c(Na+)=c(S2-)+c(HS-)+c(H2S)
c(OH-)+c(S2-)=c(H+)+c(H2S)
NaHS既能发生水解又能发生电离,水溶液呈碱性:
HS-+H2O H2S+OH-(主要);
HS- H++S2-(次要)。
2.混合溶液
(1)等物质的量浓度、等体积的CH3COOH、CH3COONa溶液
水解方程式:____________________________________;
离子浓度大小关系:__________________________________;
电荷守恒:_____________________________________;
元素质量守恒:____________________________________;
质子守恒:____________________________________________。
CH3COO-+H2O CH3COOH+OH-
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
2c(Na+)=c(CH3COO-)+c(CH3COOH)
c(CH3COO-)+2c(OH-)=c(CH3COOH)+2c(H+)
CH3COOH CH3COO-+H+(主要),CH3COO-+H2O
CH3COOH+OH-(次要),水溶液呈酸性。
(2)CH3COOH、CH3COONa混合溶液呈中性
离子浓度大小关系:____________________________________;
电荷守恒:_____________________________________;
元素质量守恒:_____________________。
c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
c(Na+)=c(CH3COO-)
CH3COOH CH3COO-+H+
CH3COO-+H2O CH3COOH+OH-
若溶液呈中性,则电离和水解相互抵消。
(3)常温下pH=2的CH3COOH与pH=12的NaOH等体积混合的溶液
离子浓度大小关系:__________________________________;
电荷守恒:_____________________________________。
c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
c(Na+)+c(H+)=c(CH3COO-)+c(OH-)
由于CH3COOH是弱酸,所以当完全反应后,CH3COOH仍过量许多,溶液呈酸性。
(4)等物质的量浓度、等体积的Na2CO3—NaHCO3混合溶液
电荷守恒:__________________________________________;
元素质量守恒:______________________________________;
质子守恒:_____________________________________________;
离子浓度大小关系:________________________________________。
真题演练
02
1
2
3
1.(2023·江苏,12)室温下,用含少量Mg2+的MnSO4溶液制备MnCO3的过程如图所示。已知Ksp(MgF2)=5.2×10-11,Ka(HF)=6.3×10-4。下列说法正确的是
√
1
2
3
0.1 mol·L-1NaF溶液中存在电荷
守恒:c(OH-)+c(F-)=c(Na+)+
c(H+),A错误;
2.(2022·江苏,12)一种捕集烟气中CO2的过程如图所示。室温下以0.1 mol·
L-1KOH溶液吸收CO2,若通入CO2所引起的溶液体积变化和H2O挥发可忽略,溶液中含碳物种的浓度c总=c(H2CO3)+ 。H2CO3电离常数分别为Ka1=4.4×10-7、Ka2=4.4×10-11。下列说法正确的是
A.KOH吸收CO2所得到的溶液中:c(H2CO3)>
B.KOH完全转化为K2CO3时,溶液中:c(OH-)
=c(H+)+ +c(H2CO3)
C.KOH溶液吸收CO2,c总=0.1 mol·L-1溶液中:c(H2CO3)>
D.如图所示的“吸收”“转化”过程中,溶液的温度下降
√
1
2
3
1
2
3
如图所示的“吸收”“转化”过程中,发生的反应为CO2+2KOH
===K2CO3+H2O、K2CO3+CaO+H2O===CaCO3↓+2KOH(若生成KHCO3或K2CO3与KHCO3的混合物,则原理相同),上述反应均放热,溶液的温度升高,D不正确。
1
2
3
1
2
3
3.(2020·江苏,14改编)室温下,将两种浓度均为0.10 mol·L-1的溶液等体积混合,若溶液混合引起的体积变化可忽略,下列各混合溶液中微粒物质的量浓度关系正确的是
√
1
2
3
C项,溶液呈酸性,说明CH3COOH电离的程度大于CH3COO-水解的程度,则溶液中微粒浓度关系为c(CH3COO-)>c(Na+)>c(CH3COOH)>c(H+),错误;
1
2
3
考向预测
03
1
2
3
4
5
1.(2023·江苏省百校高三下学期第三次联考)一种吸收SO2再经氧化得到硫酸盐的过程如图所示。室温下,用0.1 mol·L-1的NaOH溶液吸收SO2,若通入SO2所引起的溶液体积变化和H2O挥发可忽略,溶液中含硫物种的浓度c(总)=
+c(H2SO3)。H2SO3的电离常数为Ka1=1.29×10-2、Ka2=6.24×10-8。下列说法正确的是
√
1
2
3
4
5
NaOH溶液的物质的量浓度为0.1 mol·
L-1,c(总)=0.1 mol·L-1溶液中的溶
质为NaHSO3,在NaHSO3溶液中存在质子守恒:c(OH-)+ =
c(H+)+c(H2SO3),故A错误;
1
2
3
4
5
1
2
3
4
5
√
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
3.(2023·江苏苏北四市统考)工业上可利用氨水吸收SO2和NO2,原理如图所示。已知: 25 ℃时,NH3·H2O的Kb=1.7×10-5,H2SO3的Ka1=1.3×10-2,Ka2=6.2×10-8,下列说法正确的是
√
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
1
2
3
4
5
√
1
2
3
4
5
NaHCO3溶液呈碱性,人体血液碱中毒时,应注射酸性溶液缓解,A错误;
1
2
3
4
5
1
2
3
4
5
√
1
2
3
4
5
1
2
3
4
5
本课结束
同课章节目录
