第1章第2节第2课时化学研究物质的组成和结构、用途与制法课件(共32张PPT 内嵌视频)2023-2024学年度沪教版化学九年级上册
文档属性
| 名称 | 第1章第2节第2课时化学研究物质的组成和结构、用途与制法课件(共32张PPT 内嵌视频)2023-2024学年度沪教版化学九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 51.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-16 00:00:00 | ||
图片预览








文档简介
(共32张PPT)
九年级上册
沪教版
课时2 化学研究物质的组成和结构、用途与制法
学习目标
新课引入
新知学习
课堂小结
1
2
3
4
1. 能说出空气的主要成分,以及氮气、氧气的体积分数。
2. 能对“空气中氧气含量的测定”的实验现象进行分析和解释,并得出氧气在空气中约占1/5体积的结论。
3. 初步学习科学实验的方法,观察、记录并初步学会分析实验现象。
4. 初步体会“性质决定用途(或用途反映性质)”的思维方法,感受并赞赏人类运用科学改造自然的成就。
5. 能根据物质的组成区分纯净物和混合物。
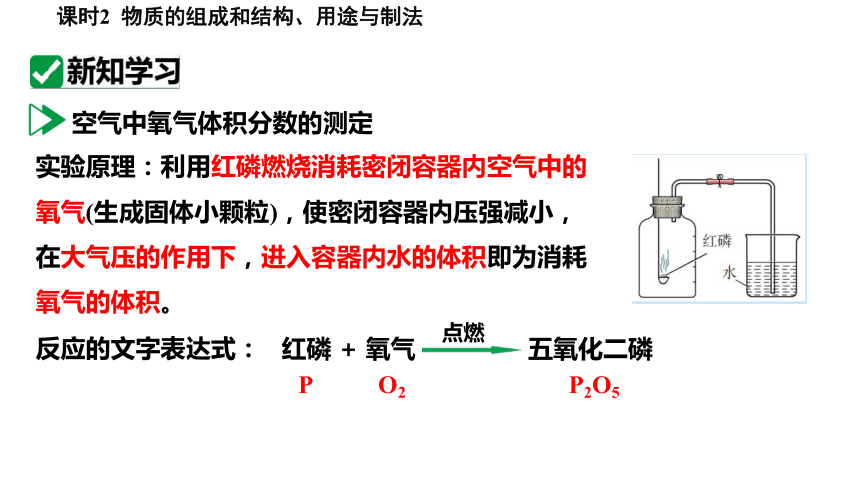
实验原理:利用红磷燃烧消耗密闭容器内空气中的氧气(生成固体小颗粒),使密闭容器内压强减小,在大气压的作用下,进入容器内水的体积即为消耗氧气的体积。
空气中氧气体积分数的测定
反应的文字表达式:
红磷 + 氧气 五氧化二磷
点燃
P2O5
P
O2
实验步骤:
1.将如图所示集气瓶中水上方空间划分为五等份,并加以标记。
2.在带橡皮塞和导管的燃烧匙内装满红磷,将胶管上的止水夹夹紧,把燃烧匙内的红磷放在酒精灯火焰上点燃,并迅速伸入集气瓶内,塞紧橡皮塞,观察现象。
3.待集气瓶冷却到室温后,把导管插入盛水的烧杯中,打开止水夹,观察现象。
观看实验视频,注意记录实验现象
实验现象
实验结论
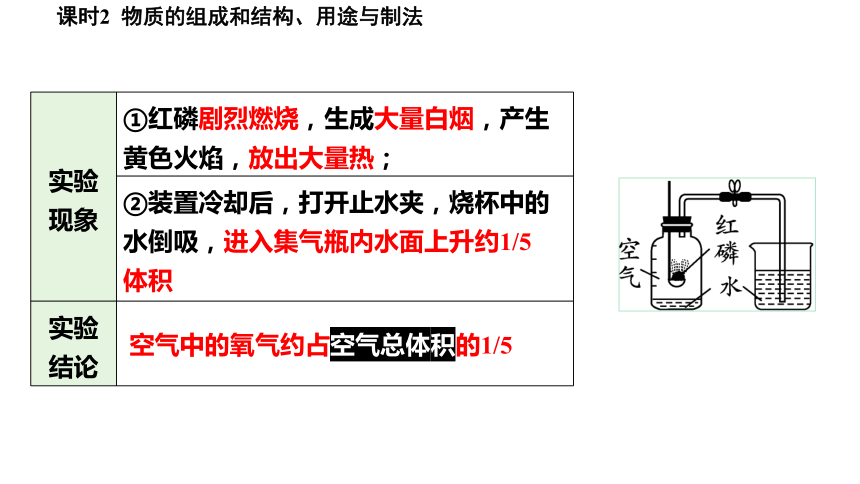
①红磷剧烈燃烧,生成大量白烟,产生黄色火焰,放出大量热;
②装置冷却后,打开止水夹,烧杯中的水倒吸,进入集气瓶内水面上升约1/5体积
空气中的氧气约占空气总体积的1/5
实验过程,水面最终并不在 1/5刻度处?其可能原
因是什么?
测量结果偏小或偏大的原因
测量结果偏小:
1. 装置漏气;
2. 红磷的量不足;
3. 装置未冷却到室温就打开弹簧夹。
测量结果偏大:
1. 实验前未夹紧弹簧夹,红磷燃烧时气体沿导管逸出;
2. 燃烧匙伸入过慢或未立即塞上胶塞,瓶内空气受热逸出。
(1)集气瓶中水的作用是什么?
交流
红磷与氧气 ;氧气来自于空气
确保瓶内的氧气消耗完全;没有氧气支持燃烧
①保护装置,红磷燃烧产生的白烟五氧化二磷是一种固体,同时反应放热,使得生成的固体温度比较高,生成的高温固体溅落瓶底,容易使得瓶底炸裂
②五氧化二磷是一种有毒物质,用水可以跟它反应并吸收
(2)为什么红磷要过量?剩余的红磷为什么不燃烧?
(3)红磷燃烧时哪两种物质发生化学反应?另一种物质来自哪里?
(4)试猜想一下,实验结束后,集气瓶中剩余的主要是气体是什么,有何性质?
交流
氮气(N2);不可燃,不助燃,难溶于水。
(5)可不可以用蜡烛代替红磷进行相同的实验。原因是什么?红磷的代替品必须满足的条件是什么?
①不能,因为蜡烛燃烧消耗瓶内氧气后又生成二氧化碳气体,使瓶内压强无明显变化,水无法倒吸。
②能和空气中的氧气反应,同时生成物不能为气体。
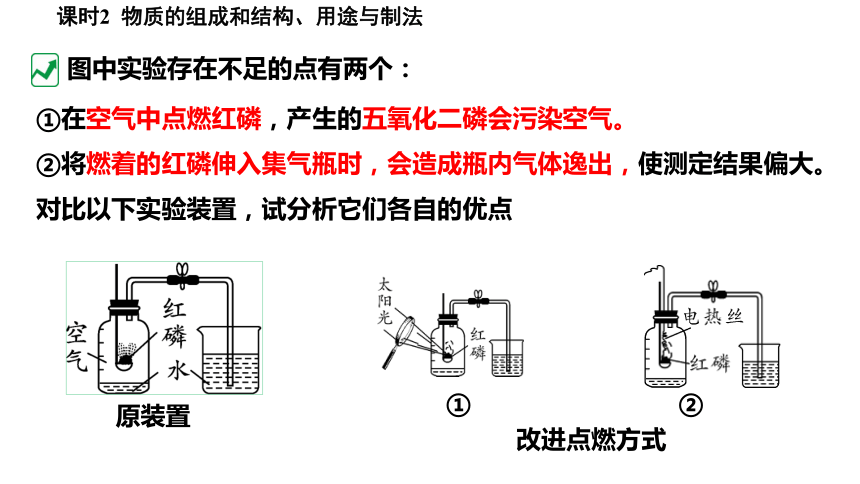
图中实验存在不足的点有两个:
①
②
原装置
改进点燃方式
①在空气中点燃红磷,产生的五氧化二磷会污染空气。
②将燃着的红磷伸入集气瓶时,会造成瓶内气体逸出,使测定结果偏大。
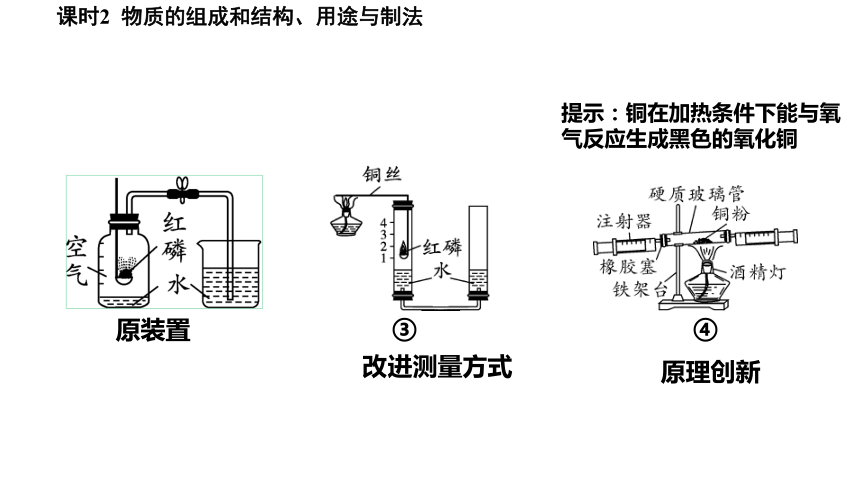
对比以下实验装置,试分析它们各自的优点
原装置
③
④
提示:铜在加热条件下能与氧气反应生成黑色的氧化铜
改进测量方式
原理创新
混合物
两种或两种以上的物质混合而成
空气
如:海水、矿泉水等
通过实验,我们知道空气是含有氮气、氧气、二氧化碳等多种成分的气体。我们把空气这样的物质成为混合物。
纯净物
只由一种物质组成
氧气
可以用化学符号来表示,如:氮气(N2)、氧气(O2)、二氧化碳(CO2)等
只由一种物质组成的物质统称为什么呢?
纯净物 混合物
组成 只由一种物质组成 由两种或两种以上的物质混合而成
性质 固定 组成混合物的各种成分保持各自的性质
表示方法 有化学符号 无固定符号
举例 氧气(O2) 、 五氧化二磷 (P2O5) 空气、海水
你能总结出纯净物与混合物的不同点吗?
温馨提示
1. 纯净物是相对的,不是绝对的,也就是说绝对纯净的物质是没有的。
2. 带“混合”字样的不一定是混合物,
如:冰水混合物(纯净物);
带“纯净”字样的不一定为纯净物,
如:纯净的空气(混合物)。
许多科学家研究发现,空气中还含有氦(He)、氖(Ne)、氩(Ar)、氪(Kr)、氙(Xe)等稀有气体。
空气是由氧气和氮气组成
法国化学家
拉瓦锡
瑞典科学家舍勒
英国化学家普里斯特利
制得了氧气
空气中还有哪些成分呢?你知道空气的成分是怎么被发现的吗?
空气的组成
约占78%
氮气(N2)
约占21%
氧气(O2)
稀有气体约占0.94%
按体积分数计算
二氧化碳约占0.03%
其他气体和杂质约占0.03%
氮气的用途
稀有气体的用途
研究发现,物质发生化学变化时虽转化为其他物质,但元素不改变,即反应物与生成物应含同种元素。如,红磷及其燃烧后生成的五氧化二磷均含磷元素;蜡烛含碳、氢元素,其燃烧产物也含碳、氢元素。我们可利用此规律进行物质组成研究。
取少量葡萄糖、砂糖、面粉,分别放在燃烧匙中,在酒精灯上加热,直至完全烧焦,会观察到什么现象?
现象:都有黑色残渣生成
结论:这些物质中都含有碳元素
还有哪些物质中含有碳元素呢?
物质的组成
铁矿石中含有铁元素,所以可以炼成铁,而不能炼成金。
水中含有氢元素和氧元素,不含碳元素,所以水不能变成油。
铁矿石可以炼成铁,为什么不能炼成金?水为什么不可以变成油?
一种物质可以通过化学变化变成其他物质,但是反应物和生成物中应含有同种元素。
物质之间相互转化需要具备哪些条件?
金刚石
石墨
金刚石和石墨都是由碳元素组成的,为什么两者的性质却不同?
金刚石和石墨都是由碳元素组成,由碳原子构成,但原子排列方式不同导致了性质的差异
物质的结构与性质
金刚石
硬度大
无色透明晶体,有特殊光学性质
切割玻璃
石墨
能导电
质软
作为电池的电极
制作钻石
制作铅笔的笔芯
你可以根据金刚石和石墨的不同性质,说出它们各自的用途吗?
物质的性质与用途
决定
反映
性质
金刚石硬度大
用途
金刚石可以切割玻璃
归纳
决定
反映
人类一直在开采煤、石油、天然气,利用这些自然资源可以制造哪些产品?
药物
合成橡胶制品
塑料制品
合成纤维
人们用煤和石油制造出许多产品
物质的制备
通过本节课的学习,请回答以下问题
1.空气的组成成分有哪些,它们体积分数分别是多少?
2.氮气和氧气的用途分别有哪些?
3.测定空气中氧气含量的实验原理是什么?注意事项有哪些?
4.列举示例简要说明物质的性质和用途之间关系。
5.常见的混合物和纯净物都分别有哪些?
1. 生活中用到的下列物质,属于纯净物的是( )
A. 调味用的食醋 B. 取暖用的煤炭
C. 温度计中的水银 D. 炒菜用的铁锅
C
2. 下列关于空气成分的认识正确的是( )
A. 氧气约占空气质量的21%
B. 空气中氧气和氮气的体积比约为1∶5
C. 灯泡中充氮气以延长使用寿命
D. 空气是一种物质,属于纯净物
C
3. 下列研究课题不属于化学研究领域的是( )
A. 研究物质的组成和结构
B. 研究物质的性质与变化
C. 研究物体的运动规律
D. 研究物质的用途与制法
C
4.如图是空气中氧气体积分数的测定实验,请回答
下列问题:
(1)请写出红磷燃烧的文字表达式
____________________________。
(2)将装有足量红磷的燃烧匙中的红磷点燃后伸入集气瓶中,塞紧橡胶塞,红磷燃烧的现象为_______________________,红磷熄灭后冷却至室温,打开止水夹,若观察到_____________________________,说明空气中氧气的体积分数约为 ,若测定结果大于 ,可能的原因是______________
_____________。
红磷+氧气 五氧化二磷
产生大量白烟,放出热量
进入集气瓶内水的体积约为1格
燃着的红磷伸
点燃
入集气瓶过慢
(3)该实验中______(填“能”或“不能”)将燃烧匙中的红磷换为木炭,理由是_________________________________________________________
________________________________________________________。
(4)推测实验结束后集气瓶内剩余的主要气体为______(填名称),该气体________(填“支持”或“不支持”)燃烧。
不能
木炭燃烧产物中有二氧化碳和一氧化碳,反应消耗了氧气,但却增加了新的气体,不能用于测定空气中氧气的体积分数
氮气
不支持
九年级上册
沪教版
课时2 化学研究物质的组成和结构、用途与制法
学习目标
新课引入
新知学习
课堂小结
1
2
3
4
1. 能说出空气的主要成分,以及氮气、氧气的体积分数。
2. 能对“空气中氧气含量的测定”的实验现象进行分析和解释,并得出氧气在空气中约占1/5体积的结论。
3. 初步学习科学实验的方法,观察、记录并初步学会分析实验现象。
4. 初步体会“性质决定用途(或用途反映性质)”的思维方法,感受并赞赏人类运用科学改造自然的成就。
5. 能根据物质的组成区分纯净物和混合物。
实验原理:利用红磷燃烧消耗密闭容器内空气中的氧气(生成固体小颗粒),使密闭容器内压强减小,在大气压的作用下,进入容器内水的体积即为消耗氧气的体积。
空气中氧气体积分数的测定
反应的文字表达式:
红磷 + 氧气 五氧化二磷
点燃
P2O5
P
O2
实验步骤:
1.将如图所示集气瓶中水上方空间划分为五等份,并加以标记。
2.在带橡皮塞和导管的燃烧匙内装满红磷,将胶管上的止水夹夹紧,把燃烧匙内的红磷放在酒精灯火焰上点燃,并迅速伸入集气瓶内,塞紧橡皮塞,观察现象。
3.待集气瓶冷却到室温后,把导管插入盛水的烧杯中,打开止水夹,观察现象。
观看实验视频,注意记录实验现象
实验现象
实验结论
①红磷剧烈燃烧,生成大量白烟,产生黄色火焰,放出大量热;
②装置冷却后,打开止水夹,烧杯中的水倒吸,进入集气瓶内水面上升约1/5体积
空气中的氧气约占空气总体积的1/5
实验过程,水面最终并不在 1/5刻度处?其可能原
因是什么?
测量结果偏小或偏大的原因
测量结果偏小:
1. 装置漏气;
2. 红磷的量不足;
3. 装置未冷却到室温就打开弹簧夹。
测量结果偏大:
1. 实验前未夹紧弹簧夹,红磷燃烧时气体沿导管逸出;
2. 燃烧匙伸入过慢或未立即塞上胶塞,瓶内空气受热逸出。
(1)集气瓶中水的作用是什么?
交流
红磷与氧气 ;氧气来自于空气
确保瓶内的氧气消耗完全;没有氧气支持燃烧
①保护装置,红磷燃烧产生的白烟五氧化二磷是一种固体,同时反应放热,使得生成的固体温度比较高,生成的高温固体溅落瓶底,容易使得瓶底炸裂
②五氧化二磷是一种有毒物质,用水可以跟它反应并吸收
(2)为什么红磷要过量?剩余的红磷为什么不燃烧?
(3)红磷燃烧时哪两种物质发生化学反应?另一种物质来自哪里?
(4)试猜想一下,实验结束后,集气瓶中剩余的主要是气体是什么,有何性质?
交流
氮气(N2);不可燃,不助燃,难溶于水。
(5)可不可以用蜡烛代替红磷进行相同的实验。原因是什么?红磷的代替品必须满足的条件是什么?
①不能,因为蜡烛燃烧消耗瓶内氧气后又生成二氧化碳气体,使瓶内压强无明显变化,水无法倒吸。
②能和空气中的氧气反应,同时生成物不能为气体。
图中实验存在不足的点有两个:
①
②
原装置
改进点燃方式
①在空气中点燃红磷,产生的五氧化二磷会污染空气。
②将燃着的红磷伸入集气瓶时,会造成瓶内气体逸出,使测定结果偏大。
对比以下实验装置,试分析它们各自的优点
原装置
③
④
提示:铜在加热条件下能与氧气反应生成黑色的氧化铜
改进测量方式
原理创新
混合物
两种或两种以上的物质混合而成
空气
如:海水、矿泉水等
通过实验,我们知道空气是含有氮气、氧气、二氧化碳等多种成分的气体。我们把空气这样的物质成为混合物。
纯净物
只由一种物质组成
氧气
可以用化学符号来表示,如:氮气(N2)、氧气(O2)、二氧化碳(CO2)等
只由一种物质组成的物质统称为什么呢?
纯净物 混合物
组成 只由一种物质组成 由两种或两种以上的物质混合而成
性质 固定 组成混合物的各种成分保持各自的性质
表示方法 有化学符号 无固定符号
举例 氧气(O2) 、 五氧化二磷 (P2O5) 空气、海水
你能总结出纯净物与混合物的不同点吗?
温馨提示
1. 纯净物是相对的,不是绝对的,也就是说绝对纯净的物质是没有的。
2. 带“混合”字样的不一定是混合物,
如:冰水混合物(纯净物);
带“纯净”字样的不一定为纯净物,
如:纯净的空气(混合物)。
许多科学家研究发现,空气中还含有氦(He)、氖(Ne)、氩(Ar)、氪(Kr)、氙(Xe)等稀有气体。
空气是由氧气和氮气组成
法国化学家
拉瓦锡
瑞典科学家舍勒
英国化学家普里斯特利
制得了氧气
空气中还有哪些成分呢?你知道空气的成分是怎么被发现的吗?
空气的组成
约占78%
氮气(N2)
约占21%
氧气(O2)
稀有气体约占0.94%
按体积分数计算
二氧化碳约占0.03%
其他气体和杂质约占0.03%
氮气的用途
稀有气体的用途
研究发现,物质发生化学变化时虽转化为其他物质,但元素不改变,即反应物与生成物应含同种元素。如,红磷及其燃烧后生成的五氧化二磷均含磷元素;蜡烛含碳、氢元素,其燃烧产物也含碳、氢元素。我们可利用此规律进行物质组成研究。
取少量葡萄糖、砂糖、面粉,分别放在燃烧匙中,在酒精灯上加热,直至完全烧焦,会观察到什么现象?
现象:都有黑色残渣生成
结论:这些物质中都含有碳元素
还有哪些物质中含有碳元素呢?
物质的组成
铁矿石中含有铁元素,所以可以炼成铁,而不能炼成金。
水中含有氢元素和氧元素,不含碳元素,所以水不能变成油。
铁矿石可以炼成铁,为什么不能炼成金?水为什么不可以变成油?
一种物质可以通过化学变化变成其他物质,但是反应物和生成物中应含有同种元素。
物质之间相互转化需要具备哪些条件?
金刚石
石墨
金刚石和石墨都是由碳元素组成的,为什么两者的性质却不同?
金刚石和石墨都是由碳元素组成,由碳原子构成,但原子排列方式不同导致了性质的差异
物质的结构与性质
金刚石
硬度大
无色透明晶体,有特殊光学性质
切割玻璃
石墨
能导电
质软
作为电池的电极
制作钻石
制作铅笔的笔芯
你可以根据金刚石和石墨的不同性质,说出它们各自的用途吗?
物质的性质与用途
决定
反映
性质
金刚石硬度大
用途
金刚石可以切割玻璃
归纳
决定
反映
人类一直在开采煤、石油、天然气,利用这些自然资源可以制造哪些产品?
药物
合成橡胶制品
塑料制品
合成纤维
人们用煤和石油制造出许多产品
物质的制备
通过本节课的学习,请回答以下问题
1.空气的组成成分有哪些,它们体积分数分别是多少?
2.氮气和氧气的用途分别有哪些?
3.测定空气中氧气含量的实验原理是什么?注意事项有哪些?
4.列举示例简要说明物质的性质和用途之间关系。
5.常见的混合物和纯净物都分别有哪些?
1. 生活中用到的下列物质,属于纯净物的是( )
A. 调味用的食醋 B. 取暖用的煤炭
C. 温度计中的水银 D. 炒菜用的铁锅
C
2. 下列关于空气成分的认识正确的是( )
A. 氧气约占空气质量的21%
B. 空气中氧气和氮气的体积比约为1∶5
C. 灯泡中充氮气以延长使用寿命
D. 空气是一种物质,属于纯净物
C
3. 下列研究课题不属于化学研究领域的是( )
A. 研究物质的组成和结构
B. 研究物质的性质与变化
C. 研究物体的运动规律
D. 研究物质的用途与制法
C
4.如图是空气中氧气体积分数的测定实验,请回答
下列问题:
(1)请写出红磷燃烧的文字表达式
____________________________。
(2)将装有足量红磷的燃烧匙中的红磷点燃后伸入集气瓶中,塞紧橡胶塞,红磷燃烧的现象为_______________________,红磷熄灭后冷却至室温,打开止水夹,若观察到_____________________________,说明空气中氧气的体积分数约为 ,若测定结果大于 ,可能的原因是______________
_____________。
红磷+氧气 五氧化二磷
产生大量白烟,放出热量
进入集气瓶内水的体积约为1格
燃着的红磷伸
点燃
入集气瓶过慢
(3)该实验中______(填“能”或“不能”)将燃烧匙中的红磷换为木炭,理由是_________________________________________________________
________________________________________________________。
(4)推测实验结束后集气瓶内剩余的主要气体为______(填名称),该气体________(填“支持”或“不支持”)燃烧。
不能
木炭燃烧产物中有二氧化碳和一氧化碳,反应消耗了氧气,但却增加了新的气体,不能用于测定空气中氧气的体积分数
氮气
不支持
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
