陕西省咸阳市重点中学2023-2024学年高一上学期段性检测(三)化学试题(含答案)
文档属性
| 名称 | 陕西省咸阳市重点中学2023-2024学年高一上学期段性检测(三)化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 755.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-16 00:00:00 | ||
图片预览



文档简介
咸阳市重点中学2023-2024学年高一上学期段性检测(三)
化学试题
注意事项:
1.本试卷共8页,满分100分,时间75分钟。
2.答卷前,考生务必将自己的姓名、班级和准考证号填写在答题卡上。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,监考员将答题卡按顺序收回,装袋整理;试题不回收。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Al-27 S-32 Cl-35.5 Fe-56 Cu-64
第I卷(选择题 共45分)
一、选择题(本大题共15小题,每小题3分,计45分。每小题只有一个选项是符合题意的)
1.三星堆是中华文明的重要组成部分。下列出土文物属于合金的是( )
A.青铜神树 B.丝绸黑炭 C.陶瓷马头 D.雕花象牙
2.下列生产活动不涉及氧化还原反应的是( )
A.柴火烤肉 B.铁杵磨针 C.谷物酿酒 D.高炉炼铁
3.无色溶液中,下列各组离子能大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
4.分类法可用于预测物质的性质及其变化规律。下列物质的分类与性质预测对应关系不正确的是( )
选项 物质 类别 性质预测
A 酸性氧化物 能与水反应生成酸
B 还原剂 能与等氧化剂反应
C 钾盐 能与酸反应
D 酸 能与反应生成盐
5.化学与生产生活密切相关,下列叙述不正确的是( )
A.《吕氏春秋·别类编》中“金(即铜)柔锡柔,合两柔则刚”,体现了合金硬度方面的特征
B.“84”消毒液的有效成分是,可用于环境的杀菌消毒
C.“墨滴无声入水惊,如烟袅袅幻形生”中的“墨滴”具有胶体的性质
D.《本草经集注》中关于鉴别硝石和朴硝的记载:“以火烧之,紫青烟起,乃真硝石也”,该方法应用了焰色试验
6.关于钠及其化合物的说法不正确的是( )
A.金属钠着火时,可用泡沫灭火器或干燥的沙土灭火
B.可作漂白剂和呼吸面具中的供氧剂
C.实验室切割钠时,不能用手直接接触钠
D.既可用于焙制糕点也可用来制药
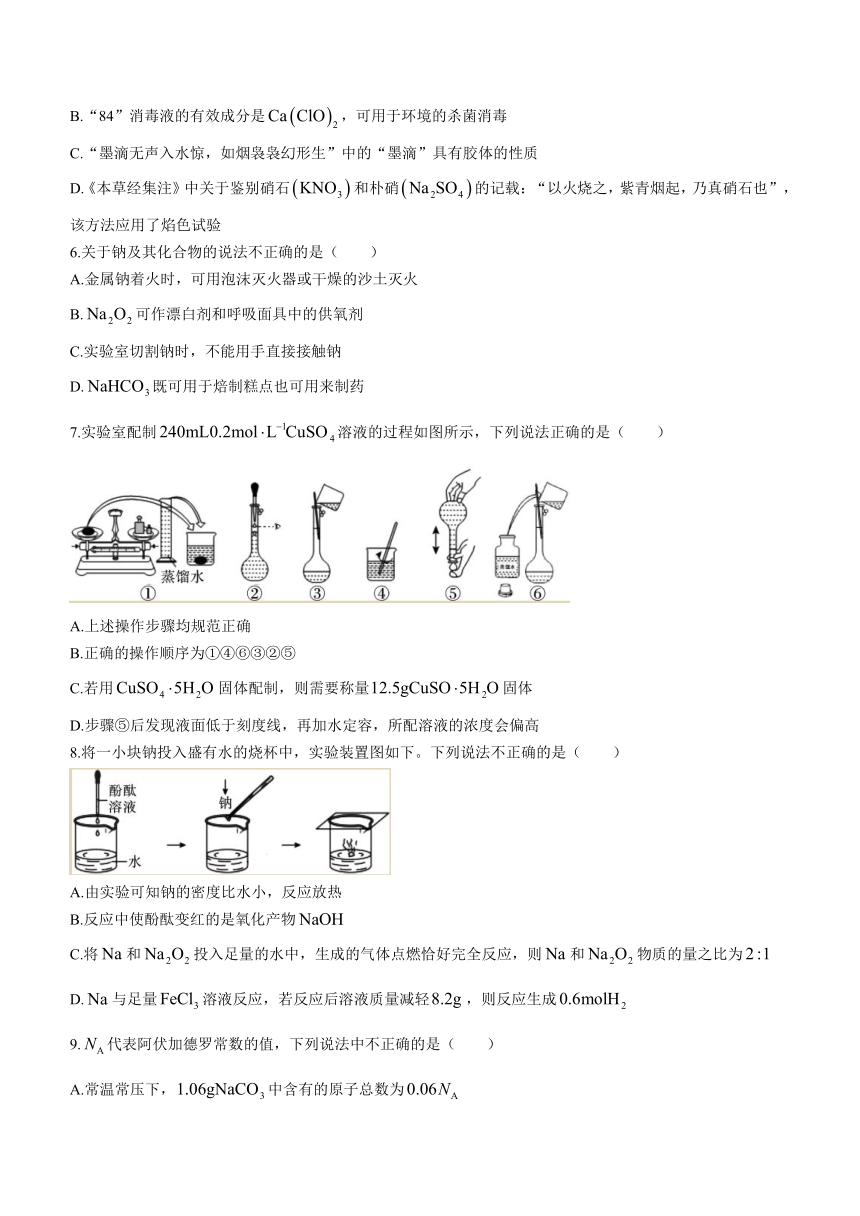
7.实验室配制溶液的过程如图所示,下列说法正确的是( )
A.上述操作步骤均规范正确
B.正确的操作顺序为①④⑥③②⑤
C.若用固体配制,则需要称量固体
D.步骤⑤后发现液面低于刻度线,再加水定容,所配溶液的浓度会偏高
8.将一小块钠投入盛有水的烧杯中,实验装置图如下。下列说法不正确的是( )
A.由实验可知钠的密度比水小,反应放热
B.反应中使酚酞变红的是氧化产物
C.将和投入足量的水中,生成的气体点燃恰好完全反应,则和物质的量之比为
D.与足量溶液反应,若反应后溶液质量减轻,则反应生成
9.代表阿伏加德罗常数的值,下列说法中不正确的是( )
A.常温常压下,中含有的原子总数为
B.和固体混合物中阴、阳离子总数为
C.标准状况下,中含有的分子数目为
D.氯气与氢氧化钙完全反应生成氯化钙和次氯酸钙,转移的电子数为
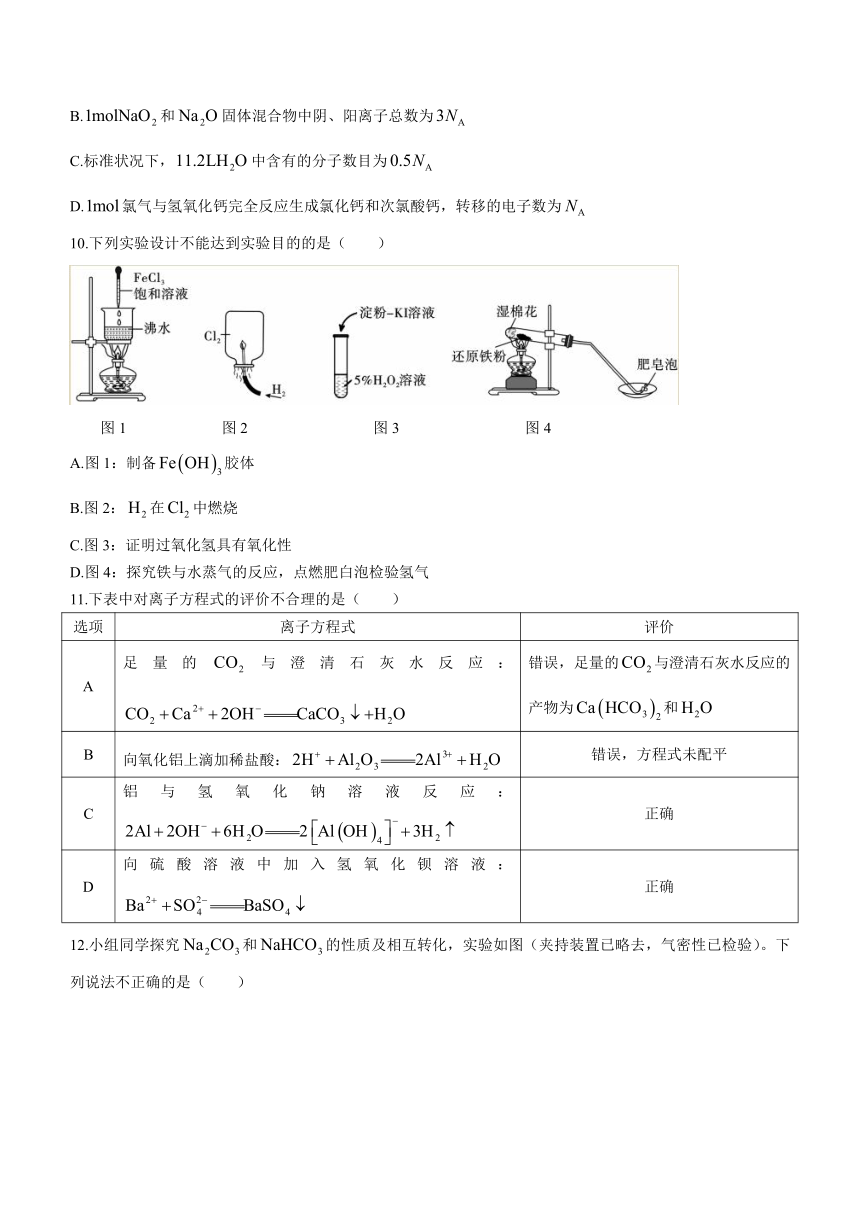
10.下列实验设计不能达到实验目的的是( )
图1 图2 图3 图4
A.图1:制备胶体
B.图2:在中燃烧
C.图3:证明过氧化氢具有氧化性
D.图4:探究铁与水蒸气的反应,点燃肥白泡检验氢气
11.下表中对离子方程式的评价不合理的是( )
选项 离子方程式 评价
A 足量的与澄清石灰水反应: 错误,足量的与澄清石灰水反应的产物为和
B 向氧化铝上滴加稀盐酸: 错误,方程式未配平
C 铝与氢氧化钠溶液反应: 正确
D 向硫酸溶液中加入氢氧化钡溶液: 正确
12.小组同学探究和的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是( )
实验I 实验II
A.实验I,A中澄清石灰水无明显变化,B中澄清石灰水变浑浊
B.实验II,C中发生反应的离子方程式为:
C.实验II中,一段时间之后,可观察到中有细小晶体析出
D.等物质的量的、分别与足量盐酸反应,生成的更多
13.某含有、、三种溶质的无土栽培营养液中部分离子的浓度如图甲所示。取样品加水稀释,测得的浓度随溶液体积的变化如图乙曲线所示。下列判断正确的是( )
甲 乙
A.营养液中物质的量为
B.图乙中
C.营养液中的浓度是
D.营养液中与的物质的量之比为
14.某小组欲测定与呼出气体反应后的混合物(含有、、)中剩余的质量分数,下列方案中合理的是( )
A.取克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得克固体
B.取克混合物与足量稀硫酸充分反应,逸出气体用碱石灰(氧化钙和氢氧化钠固体混合物)吸收,增重克
C.取克混合物与足量溶液充分反应,过滤、洗涤、烘干,得到克固体
D.取克混合物与足量水充分反应,加热,收集到标准状况下干燥气体
15.向含有和的混合溶液中加入,充分反应后(忽略溶液体积变化),下列说法正确的是( )
A.溶液中 B.剩余
C.析出 D.溶液中
第II卷(非选择题 共55分)
二、非选择题(本大题共4小题,计55分)
16.(13分)饮用水安全对公众健康至关重要。
(1)自来水厂通常用明矾作净水剂,是因为它能在水中生成胶体,吸附水中的悬浮物。实验室区分胶体和溶液的一种常用物理方法是________________________。
(2)某水样中、、含量较多,硬度较大。“石灰—纯碱法”是软化硬水的常见方法,原理是通过离子反应将、转化为沉淀降低其含量。
①先向该水样中加入足量的石灰水,反应的离子方程式为__________________;
②再加入足量的纯碱溶液,反应的离子方程式为__________________。
(3)、是人类使用的新型自来水消毒剂。
①根据元素组成,和互为______。比具有更强的氧化性,它与溶液反应的化学方程式为:,用双线桥法标出该反应电子转移的方向和数目____________。
②是一种黄绿色气体,氯酸钠与足量浓盐酸在加热的条件下反应得到和的混合气体。写出该反应的化学方程式__________________。
(4)高铁酸钠是一种新型绿色消毒剂,工业上制备高铁酸钠的一种方法可用离子方程式表示为:(未配平),该反应中氧化剂和还原剂的物质的量之比为______。
17.(15分)如图为铁元素的“价—类”二维图,请回答下列问题。
(1)图中“”代表的物质类别为______。图中物质只具有还原性的是______(填化学式)。
(2)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成______(填字母,下同)而制得红色砖瓦;若烘烧后期从窑顶向下慢慢浇水,窑内会产生大量、气体,它们把该红色物质还原成黑色的______,同时还有未燃烧的碳的颗粒,而制得了青色砖瓦。
A. B. C. D.
(3)根据上述“价—类”二维图判断中元素的价态,写出与稀盐酸反应的离子方程式__________________。
(4)用坩埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是铁丝剧烈燃烧,________________________。
(5)以绿矾(主要成分,部分已被氧化为)为原料,生产铁红的工艺流程如图:
①“转化”过程中,加入过量粉时发生反应的离子方程式为__________________。
②“结晶”时,加入过量稀硫酸的目的是________________________。
③“结晶”时,控制温度在左右进行(相关物质的溶解度见图),从溶液中析出的晶体是______(填化学式)。
④“煅烧”时生成铁红的化学方程式为__________________。
18.(14分)化学兴趣小组为研究的性质,设计如图所示装置进行实验。装置III中夹持装置已略去,其中为干燥的品红试纸,为湿润的品红试纸。
(1)装置I中仪器c的名称是______。
(2)实验结束后,同学们在装置III中观察到的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置II与III之间添加下图中的______(填序号)装置。
(3)若产生的足量,装置IV中的实验现象是________________________。
(4)写出装置V中发生反应的离子方程式__________________。
(5)将制得的氯气通入如图装置可制备无水,已知在升华,遇潮湿空气立即产生大量白雾。
①实验开始时应先_______(填“通入氯气”或“点燃酒精灯”)。
②用粗短导管连接A、B的目的是________________________。C中碱石灰的作用是____________________________。
③若制备氯气时消耗为和铝粉均足量,所得产品经纯化后测得质量为,则该实验中的产率为_______()。
(6)若将通入热的烧碱溶液中,可以得到和的混合液。当混合液中和的个数比为时,混合液中和的个数比为______。
19.(13分)某化学课外小组在制备过程中观察到生成的白色沉淀迅速变为灰绿色,一段时间后变为红褐色。该小组同学对产生灰绿色沉淀的原因进行了实验探究。
已知:检验溶液中的可用溶液,与反应生成蓝色沉淀。
I.甲同学猜测灰绿色沉淀是和的混合物,设计并完成了实验1和实验2。
编号 实验操作 实验现象
实验1 向溶液中滴加溶液(两溶液中均先加几滴维生素溶液) 液面上方出现白色沉淀,一段时间后变为灰绿色,长时间后变为红褐色
实验2 取实验1中少量灰绿色沉淀,洗净后加盐酸溶解,分成两份。①中加入试剂,②中加入试剂 ①中出现蓝色沉淀,②中溶液未变成红色
(1)实验1中产生红褐色沉淀的化学方程式为__________________。
(2)实验1中加入维生素溶液是利用了该物质的______性,实验2中检验加入的试剂为______溶液。
(3)实验2的现象说明甲同学的猜测______(填“正确”或“不正确”)。
II.乙同学查阅资料得知,沉淀具有较强的吸附性,猜测灰绿色可能是吸附引起的,设计并完成了实验3~验5。
编号 实验操作 实验现象
实验3 向溶液中逐滴加入溶液(两溶液中均先加几滴维生素溶液) 液面上方产生白色沉淀(带有较多灰绿色)。沉淀下沉后,部分灰绿色沉淀变为白色
实验4 向溶液中逐滴加入溶液(两溶液中均先加几滴维生素溶液) 液面上方产生白色沉淀(无灰绿色)。沉淀下沉后,仍为白色
实验5 取实验4中白色沉淀,洗净后放在潮湿的空气中
(4)依据乙同学的猜测,实验4中沉淀无灰绿色的原因为________________________。
(5)该小组同学依据实验5的实验现象,间接证明了乙同学猜测的正确性,则实验5的实验现象可能为________________________。
III.该小组同学尝试用如图装置制取。
(6)为了制得白色沉淀,在上述装置中加入试剂,塞紧塞子后,应先______(填“打开”或“关闭”)止水夹,一段时间后,再______(填“打开”或“关闭”)止水夹,最终可在______(填“A”或“B”)中观察到白色沉淀。
咸阳市重点中学2023-2024学年高一上学期段性检测(三)
化学试题参考答案及评分标准
一、选择题(本大题共15小题,每小题3分,计45分。每小题只有一个选项符合题意)
1.A 2.B 3.B 4.C 5.B 6.A 7.C 8.D 9.C 10.B
11.D 12.D 13.C 14.D 15.A
二、非选择题(本大题共4小题,计55分)
16.(13分)(1)丁达尔效应或用一束光或激光笔照射待测液,产生光亮通路的是胶体,不能产生光亮通路的是溶液
(2)①
②
(3)①同素异形体(1分)
②
(4)(其余每空2分)
17.(15分)(1)盐(1分) (1分)
(2)A(1分) B(1分)
(3)
(4)产生红棕色的烟
(5)①
②除去过量的铁粉
③(1分)
④(其余每空2分)
18.(14分)(1)分液漏斗(1分)
(2)④(1分)
(3)紫色石蕊试液先变红后褪色(1分)
(4)
(5)①通入氯气(1分)
②确保能顺利进入中,不会堵塞导管 吸收多余的氯气,同时防止空气中的水蒸气进入装置B
③
(6)(其余每空2分)
19.(13分)(1)
(2)还原(1分) KSCN或硫氰化钾(1分)
(3)不正确
(4)溶液浓度高,反应后溶液中浓度较小,不易被吸附在表面
(5)白色沉淀变为红褐色,中间过程无灰绿色出现
(6)打开(1分) 关闭(1分) B(1分)(其余每空2分)
化学试题
注意事项:
1.本试卷共8页,满分100分,时间75分钟。
2.答卷前,考生务必将自己的姓名、班级和准考证号填写在答题卡上。
3.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其它答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,监考员将答题卡按顺序收回,装袋整理;试题不回收。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Al-27 S-32 Cl-35.5 Fe-56 Cu-64
第I卷(选择题 共45分)
一、选择题(本大题共15小题,每小题3分,计45分。每小题只有一个选项是符合题意的)
1.三星堆是中华文明的重要组成部分。下列出土文物属于合金的是( )
A.青铜神树 B.丝绸黑炭 C.陶瓷马头 D.雕花象牙
2.下列生产活动不涉及氧化还原反应的是( )
A.柴火烤肉 B.铁杵磨针 C.谷物酿酒 D.高炉炼铁
3.无色溶液中,下列各组离子能大量共存的是( )
A.、、、 B.、、、
C.、、、 D.、、、
4.分类法可用于预测物质的性质及其变化规律。下列物质的分类与性质预测对应关系不正确的是( )
选项 物质 类别 性质预测
A 酸性氧化物 能与水反应生成酸
B 还原剂 能与等氧化剂反应
C 钾盐 能与酸反应
D 酸 能与反应生成盐
5.化学与生产生活密切相关,下列叙述不正确的是( )
A.《吕氏春秋·别类编》中“金(即铜)柔锡柔,合两柔则刚”,体现了合金硬度方面的特征
B.“84”消毒液的有效成分是,可用于环境的杀菌消毒
C.“墨滴无声入水惊,如烟袅袅幻形生”中的“墨滴”具有胶体的性质
D.《本草经集注》中关于鉴别硝石和朴硝的记载:“以火烧之,紫青烟起,乃真硝石也”,该方法应用了焰色试验
6.关于钠及其化合物的说法不正确的是( )
A.金属钠着火时,可用泡沫灭火器或干燥的沙土灭火
B.可作漂白剂和呼吸面具中的供氧剂
C.实验室切割钠时,不能用手直接接触钠
D.既可用于焙制糕点也可用来制药
7.实验室配制溶液的过程如图所示,下列说法正确的是( )
A.上述操作步骤均规范正确
B.正确的操作顺序为①④⑥③②⑤
C.若用固体配制,则需要称量固体
D.步骤⑤后发现液面低于刻度线,再加水定容,所配溶液的浓度会偏高
8.将一小块钠投入盛有水的烧杯中,实验装置图如下。下列说法不正确的是( )
A.由实验可知钠的密度比水小,反应放热
B.反应中使酚酞变红的是氧化产物
C.将和投入足量的水中,生成的气体点燃恰好完全反应,则和物质的量之比为
D.与足量溶液反应,若反应后溶液质量减轻,则反应生成
9.代表阿伏加德罗常数的值,下列说法中不正确的是( )
A.常温常压下,中含有的原子总数为
B.和固体混合物中阴、阳离子总数为
C.标准状况下,中含有的分子数目为
D.氯气与氢氧化钙完全反应生成氯化钙和次氯酸钙,转移的电子数为
10.下列实验设计不能达到实验目的的是( )
图1 图2 图3 图4
A.图1:制备胶体
B.图2:在中燃烧
C.图3:证明过氧化氢具有氧化性
D.图4:探究铁与水蒸气的反应,点燃肥白泡检验氢气
11.下表中对离子方程式的评价不合理的是( )
选项 离子方程式 评价
A 足量的与澄清石灰水反应: 错误,足量的与澄清石灰水反应的产物为和
B 向氧化铝上滴加稀盐酸: 错误,方程式未配平
C 铝与氢氧化钠溶液反应: 正确
D 向硫酸溶液中加入氢氧化钡溶液: 正确
12.小组同学探究和的性质及相互转化,实验如图(夹持装置已略去,气密性已检验)。下列说法不正确的是( )
实验I 实验II
A.实验I,A中澄清石灰水无明显变化,B中澄清石灰水变浑浊
B.实验II,C中发生反应的离子方程式为:
C.实验II中,一段时间之后,可观察到中有细小晶体析出
D.等物质的量的、分别与足量盐酸反应,生成的更多
13.某含有、、三种溶质的无土栽培营养液中部分离子的浓度如图甲所示。取样品加水稀释,测得的浓度随溶液体积的变化如图乙曲线所示。下列判断正确的是( )
甲 乙
A.营养液中物质的量为
B.图乙中
C.营养液中的浓度是
D.营养液中与的物质的量之比为
14.某小组欲测定与呼出气体反应后的混合物(含有、、)中剩余的质量分数,下列方案中合理的是( )
A.取克混合物与足量稀盐酸充分反应,加热、蒸干、灼烧,得克固体
B.取克混合物与足量稀硫酸充分反应,逸出气体用碱石灰(氧化钙和氢氧化钠固体混合物)吸收,增重克
C.取克混合物与足量溶液充分反应,过滤、洗涤、烘干,得到克固体
D.取克混合物与足量水充分反应,加热,收集到标准状况下干燥气体
15.向含有和的混合溶液中加入,充分反应后(忽略溶液体积变化),下列说法正确的是( )
A.溶液中 B.剩余
C.析出 D.溶液中
第II卷(非选择题 共55分)
二、非选择题(本大题共4小题,计55分)
16.(13分)饮用水安全对公众健康至关重要。
(1)自来水厂通常用明矾作净水剂,是因为它能在水中生成胶体,吸附水中的悬浮物。实验室区分胶体和溶液的一种常用物理方法是________________________。
(2)某水样中、、含量较多,硬度较大。“石灰—纯碱法”是软化硬水的常见方法,原理是通过离子反应将、转化为沉淀降低其含量。
①先向该水样中加入足量的石灰水,反应的离子方程式为__________________;
②再加入足量的纯碱溶液,反应的离子方程式为__________________。
(3)、是人类使用的新型自来水消毒剂。
①根据元素组成,和互为______。比具有更强的氧化性,它与溶液反应的化学方程式为:,用双线桥法标出该反应电子转移的方向和数目____________。
②是一种黄绿色气体,氯酸钠与足量浓盐酸在加热的条件下反应得到和的混合气体。写出该反应的化学方程式__________________。
(4)高铁酸钠是一种新型绿色消毒剂,工业上制备高铁酸钠的一种方法可用离子方程式表示为:(未配平),该反应中氧化剂和还原剂的物质的量之比为______。
17.(15分)如图为铁元素的“价—类”二维图,请回答下列问题。
(1)图中“”代表的物质类别为______。图中物质只具有还原性的是______(填化学式)。
(2)在烧制砖瓦时,用黏土做成的坯经过烘烧后,铁的化合物转化成______(填字母,下同)而制得红色砖瓦;若烘烧后期从窑顶向下慢慢浇水,窑内会产生大量、气体,它们把该红色物质还原成黑色的______,同时还有未燃烧的碳的颗粒,而制得了青色砖瓦。
A. B. C. D.
(3)根据上述“价—类”二维图判断中元素的价态,写出与稀盐酸反应的离子方程式__________________。
(4)用坩埚钳夹住一束铁丝,灼烧后立即放入充满氯气的集气瓶中,观察到的现象是铁丝剧烈燃烧,________________________。
(5)以绿矾(主要成分,部分已被氧化为)为原料,生产铁红的工艺流程如图:
①“转化”过程中,加入过量粉时发生反应的离子方程式为__________________。
②“结晶”时,加入过量稀硫酸的目的是________________________。
③“结晶”时,控制温度在左右进行(相关物质的溶解度见图),从溶液中析出的晶体是______(填化学式)。
④“煅烧”时生成铁红的化学方程式为__________________。
18.(14分)化学兴趣小组为研究的性质,设计如图所示装置进行实验。装置III中夹持装置已略去,其中为干燥的品红试纸,为湿润的品红试纸。
(1)装置I中仪器c的名称是______。
(2)实验结束后,同学们在装置III中观察到的红色褪去,但并未观察到“a无明显变化”这一预期现象。为达到这一实验目的,你认为还需在装置II与III之间添加下图中的______(填序号)装置。
(3)若产生的足量,装置IV中的实验现象是________________________。
(4)写出装置V中发生反应的离子方程式__________________。
(5)将制得的氯气通入如图装置可制备无水,已知在升华,遇潮湿空气立即产生大量白雾。
①实验开始时应先_______(填“通入氯气”或“点燃酒精灯”)。
②用粗短导管连接A、B的目的是________________________。C中碱石灰的作用是____________________________。
③若制备氯气时消耗为和铝粉均足量,所得产品经纯化后测得质量为,则该实验中的产率为_______()。
(6)若将通入热的烧碱溶液中,可以得到和的混合液。当混合液中和的个数比为时,混合液中和的个数比为______。
19.(13分)某化学课外小组在制备过程中观察到生成的白色沉淀迅速变为灰绿色,一段时间后变为红褐色。该小组同学对产生灰绿色沉淀的原因进行了实验探究。
已知:检验溶液中的可用溶液,与反应生成蓝色沉淀。
I.甲同学猜测灰绿色沉淀是和的混合物,设计并完成了实验1和实验2。
编号 实验操作 实验现象
实验1 向溶液中滴加溶液(两溶液中均先加几滴维生素溶液) 液面上方出现白色沉淀,一段时间后变为灰绿色,长时间后变为红褐色
实验2 取实验1中少量灰绿色沉淀,洗净后加盐酸溶解,分成两份。①中加入试剂,②中加入试剂 ①中出现蓝色沉淀,②中溶液未变成红色
(1)实验1中产生红褐色沉淀的化学方程式为__________________。
(2)实验1中加入维生素溶液是利用了该物质的______性,实验2中检验加入的试剂为______溶液。
(3)实验2的现象说明甲同学的猜测______(填“正确”或“不正确”)。
II.乙同学查阅资料得知,沉淀具有较强的吸附性,猜测灰绿色可能是吸附引起的,设计并完成了实验3~验5。
编号 实验操作 实验现象
实验3 向溶液中逐滴加入溶液(两溶液中均先加几滴维生素溶液) 液面上方产生白色沉淀(带有较多灰绿色)。沉淀下沉后,部分灰绿色沉淀变为白色
实验4 向溶液中逐滴加入溶液(两溶液中均先加几滴维生素溶液) 液面上方产生白色沉淀(无灰绿色)。沉淀下沉后,仍为白色
实验5 取实验4中白色沉淀,洗净后放在潮湿的空气中
(4)依据乙同学的猜测,实验4中沉淀无灰绿色的原因为________________________。
(5)该小组同学依据实验5的实验现象,间接证明了乙同学猜测的正确性,则实验5的实验现象可能为________________________。
III.该小组同学尝试用如图装置制取。
(6)为了制得白色沉淀,在上述装置中加入试剂,塞紧塞子后,应先______(填“打开”或“关闭”)止水夹,一段时间后,再______(填“打开”或“关闭”)止水夹,最终可在______(填“A”或“B”)中观察到白色沉淀。
咸阳市重点中学2023-2024学年高一上学期段性检测(三)
化学试题参考答案及评分标准
一、选择题(本大题共15小题,每小题3分,计45分。每小题只有一个选项符合题意)
1.A 2.B 3.B 4.C 5.B 6.A 7.C 8.D 9.C 10.B
11.D 12.D 13.C 14.D 15.A
二、非选择题(本大题共4小题,计55分)
16.(13分)(1)丁达尔效应或用一束光或激光笔照射待测液,产生光亮通路的是胶体,不能产生光亮通路的是溶液
(2)①
②
(3)①同素异形体(1分)
②
(4)(其余每空2分)
17.(15分)(1)盐(1分) (1分)
(2)A(1分) B(1分)
(3)
(4)产生红棕色的烟
(5)①
②除去过量的铁粉
③(1分)
④(其余每空2分)
18.(14分)(1)分液漏斗(1分)
(2)④(1分)
(3)紫色石蕊试液先变红后褪色(1分)
(4)
(5)①通入氯气(1分)
②确保能顺利进入中,不会堵塞导管 吸收多余的氯气,同时防止空气中的水蒸气进入装置B
③
(6)(其余每空2分)
19.(13分)(1)
(2)还原(1分) KSCN或硫氰化钾(1分)
(3)不正确
(4)溶液浓度高,反应后溶液中浓度较小,不易被吸附在表面
(5)白色沉淀变为红褐色,中间过程无灰绿色出现
(6)打开(1分) 关闭(1分) B(1分)(其余每空2分)
同课章节目录
