山东省枣庄市滕州市育才中学2023~2024学年九年级上学期期末模拟考试化学试题(无答案)
文档属性
| 名称 | 山东省枣庄市滕州市育才中学2023~2024学年九年级上学期期末模拟考试化学试题(无答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 363.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-16 00:00:00 | ||
图片预览

文档简介
2023~2024学年度第一学期期末模拟考试
九年级化学试题
可能用到的相对原子质量C:12 H:1 O:16 N:14 Na:23 Cl:35.5 Ca:40
一、选择题(本题包括20个小题,每小题2分,共10分,每小题只有一个正确选项.)
1. 下列四组物质只用水不能区分开的是
A. 氢氧化钠固体和氯化钠固体 B. 硝酸铵固体和氯化钠固体
C. 氯化镁固体和氯化钠固体 D. 生石灰和氯化钠固体
2. 下列物质露置于空气中,没有发生化学变化而质量增大的是
A. 浓硫酸 B. 浓盐酸 C. 生石灰 D. 氢氧化钠
3. 下列说法正确的是
A. 爆炸都是由剧烈燃烧引起的 B. 原子核都由质子和中子构成
C. 由一种元素组成的物质一定是单质 D. 干冰升华是物理变化
4. 如图是铜元素和硫元素常见的化合价坐标图,试判断C点上形成化合物的化学式( )
A. CuS B. CuS2 C. Cu2S D. Cu2S2
5. 有关2H2 +O22H2O的叙述正确的是( )
A. 两个氢分子加一个氧分子等于两个水分子
B. 氢气和氧气在点燃条件下反应生成水
C. 氢气加氧气点燃等于水 D. 2g氢气和lg氧气反应生成2g水
6. 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确表示①、②、③、④所属物质类别的是
A. ②化合物、④氧化物 B. ①单质、③氧化物
C. ①单质、③化合物 D. ②含氧化合物、④氧化物
7.下列几种常用的灭火方法及灭火原理均正确的是 ( )
选项 实例 灭火方法 灭火原理
A 油锅着火 用水浇灭 使温度降到可燃物的着火点以下
B 液化气起火 关闭阀门 隔绝空气
C 住宅失火 用高压水枪灭火 降低可燃物着火点
D 森林着火 砍伐出隔离带 移走可燃物
8. 碳化硅(SiC)陶瓷基复合材料是一种新型热结构材料.在空气中,碳化硅能与熔融的氢氧化钠发生反应:SiC+2NaOH+2O2Na2SiO3+X+H2O,下列有关X物质的化学式推断中,正确的是( )
A. SiO2 B. CO C. CO2 D. Na2CO3
9.下列有关“CO2”的说法正确的是
A. ① B. ②
C. ③ D. ④
10. 燃烧与人类的生活以及社会的发展有着密切的联系,下列有关燃烧和灭火说法错误的是
A. 釜底抽薪——移除可燃物 B. 电器着火——用水浇灭,使温度降到可燃物的着火点以下
C. 钻木取火——使温度达到可燃物的着火点以上 D. 架空篝火——使木材与空气有足够大的接触面积
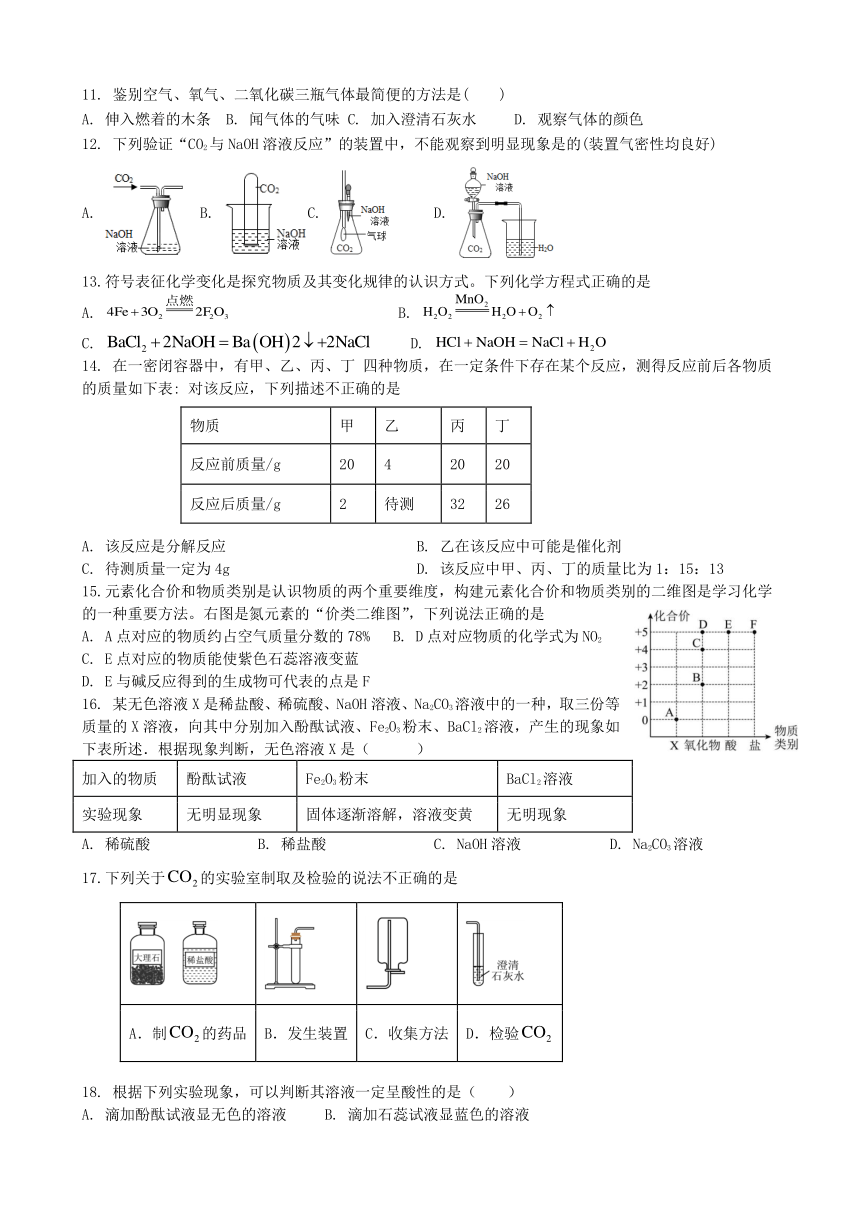
11. 鉴别空气、氧气、二氧化碳三瓶气体最简便的方法是( )
A. 伸入燃着的木条 B. 闻气体的气味 C. 加入澄清石灰水 D. 观察气体的颜色
12. 下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象是的(装置气密性均良好)
A. B. C. D.
13.符号表征化学变化是探究物质及其变化规律的认识方式。下列化学方程式正确的是
A. B.
C. D.
14. 在一密闭容器中,有甲、乙、丙、丁 四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表: 对该反应,下列描述不正确的是
物质 甲 乙 丙 丁
反应前质量/g 20 4 20 20
反应后质量/g 2 待测 32 26
A. 该反应是分解反应 B. 乙在该反应中可能是催化剂
C. 待测质量一定为4g D. 该反应中甲、丙、丁的质量比为1:15:13
15.元素化合价和物质类别是认识物质的两个重要维度,构建元素化合价和物质类别的二维图是学习化学的一种重要方法。右图是氮元素的“价类二维图”,下列说法正确的是
A. A点对应的物质约占空气质量分数的78% B. D点对应物质的化学式为NO2
C. E点对应的物质能使紫色石蕊溶液变蓝
D. E与碱反应得到的生成物可代表的点是F
16. 某无色溶液X是稀盐酸、稀硫酸、NaOH溶液、Na2CO3溶液中的一种,取三份等质量的X溶液,向其中分别加入酚酞试液、Fe2O3粉末、BaCl2溶液,产生的现象如下表所述.根据现象判断,无色溶液X是( )
加入的物质 酚酞试液 Fe2O3粉末 BaCl2溶液
实验现象 无明显现象 固体逐渐溶解,溶液变黄 无明现象
A. 稀硫酸 B. 稀盐酸 C. NaOH溶液 D. Na2CO3溶液
17.下列关于的实验室制取及检验的说法不正确的是
A.制的药品 B.发生装置 C.收集方法 D.检验
18. 根据下列实验现象,可以判断其溶液一定呈酸性的是( )
A. 滴加酚酞试液显无色的溶液 B. 滴加石蕊试液显蓝色的溶液
C. 能够与碱发生反应的溶液 D. 常温下,pH<7 的溶液
二、填空题
19. 实验是科学探究重要方法。请根据下列装置图,回答问题。
(1)现要测定某酸性溶液的 pH 如图①,若先将玻璃棒润湿,会导致测定值与实际值比较_____(填“偏大’·或“偏小”或“无法确定”)。
(2)利用图②装置稀释浓硫酸时,为确保实验安全,倾倒的B为 _____(填“浓硫酸”或“水”)。
(3)利用图③装置测得空气中氧气的体积分数小于 21%,可能的原因是____ _ (任写一条 )。
(4)利用图④装置验证质量守恒定律时,烧杯内盛有氯化铁溶液,为达到实验 目的,试管中可放入一种与氯化铁溶液反应的 C物质,请写出发生反应的化学方程式 _____(只写一个)。
20.化学是以实验为基础的学科,正确选择实验装置是实验成功的关键。下图所示装置常用于实验室制取气体,请回答下列问题。
(1)标号①的仪器名称是______。
(2)你认为选用B作发生装置,优点是______;请指出装置C中存在的一处错误______。
(3)改进上述装置图中存在的错误,并以过氧化氢溶液为原料,在实验室中制取并收集干燥的氧气。按照要求选择实验装置,连接仪器后,先______,再装入药品,进行实验。
①所选装置的连接顺序为___ ___(从左到右填写装置序号字母)。
②上述方法制氧气的化学方程式为___ ___。
③若把G装置中的浓硫酸换成水并盛满,用来收集难溶于水的气体时,气体从______(填“a”或“b”)端通入。
(4)甲烷(CH4)是最简单、难溶于水的有机物类气体,实验室常用加热无水醋酸钠与氢氧化钠的固体混合物来制得。实验室制取甲烷应选用的发生、收集装置是______(填序号)。
21. 如图是A、B、C三种固体物质的溶解度曲线,据图做答:
(1)A与C的曲线相交于P点,则P点的意义是_________。
(2)A、B、C三种物质中,溶解度随着温度的上升而减小的物质是_____。
(3)t2℃时,将30gA 物质加入到50g 水中可形成_____g 溶液,此时溶液是______(填“饱和”或“不饱和”)溶液。
(4)将 t2℃时A、B、C三种物质的饱和溶液均降温至t1℃,所得溶液中溶质质量分数由大到小的顺序是________。
(5)A物质中混有少量的C物质,若提纯A物质,可采用的结晶方法是 _________。
(6)将t2℃时 A、B两种物质的饱和溶液均降温至t1℃,则析出晶体的质量关系为_______(填“A>B”或“A<B”或“无法判断”)。
22.海水是一种重要资源,利用海水可制取金属镁等物质。某化学兴趣小组的同学设计了如下实验流程:
根据流程回答下列问题:
(1)操作Ⅰ的名称是______,该操作用到的玻璃仪器有烧杯,漏斗和______;该仪器在操作Ⅰ中的作用是______。操作Ⅰ中加入的NaOH溶液应过量,其目的是______。
(2)试剂X是______(填名称),写出溶液A中加入试剂X发生反应的化学方程式______。
三、实验探究题
23. 通过化学学习,你已经掌握了实验室制取气体的有关规律。请结合下图回答问题:
(1)写出图中标号仪器的名称:①____ __;②___ ___。
(2)已知过氧化钠(Na2O2)是一种淡黄色固体粉末,常温下可与水反应生成氢氧化钠和氧气。如果在实验室中用过氧化钠和水反应来制取一瓶氧气,通常选用B装置来做发生装置,优点是______。反应的化学方程式______。利用F装置收集氧气的最佳时刻是______。
(3)制取二氧化碳气体时,想控制反应的随时发生和停止,应当选用______装置。检验该气体是否收集满的方式是______。
(4)实验室选用如图G装置收集二氧化碳,气体应该从______(填“a”或“b”)进入,若G装置内装满水时,再连接一个用于量度液体的体积的仪器______,就可以用于测定不溶于水且不与水反应的气体体积,则气体应从______(填“a”或“b”)进入广口瓶中。
24.某化学兴趣小组三位同学在学习了硫酸与氢氧化钠反应后,分别结合自己在实验室中所做的实验,从不同方面对其进行图像描述。图A是实际操作图,图B是反应过程中溶液的酸碱度变化图,图C是微观粒子结合过程的示意图。
根据以上图示,回答下列问题:(1)依据图A、图B可知,该实验是将_______滴加到另一种溶液中。写出图C中方框内乙粒子的符号_______。
(2)图B中b点溶液中溶质是_______,向其中加入石蕊试液,溶液呈______色。
(3)向的溶液中滴加氯化钡,发生反应的化学方程式为____ ___。
(4)中和反应的实质是______。在工农业生产中有着非常要的作用,请写出用熟石灰处理含有(H2SO4)的工业废水的反应原理______。
25.某同学总结了碱的化学性质如下图,“ ”表示短线两端的物质互相之间能够发生化学反应。请你根据要求完成下列问题。
(1)该同学在取用氢氧化钠溶液时,发现试剂瓶瓶塞没有塞。据反应④说明NaOH必须密封保存,否则在空气中就要变质为 (填化学式)
(2)要检验该氢氧化钠溶液已变质,选择下列试剂不能达到目的是 (填字母代号)。A.稀HCl B.酚酞试液 C.CaCl2 D. Ca(OH)2
(3)为了验证反应③,该同学将无色酞试液分别滴入NaOH溶液和澄清石灰水中,溶液由无色变成红色,原因是它们在水溶液中都能解离出一种共同的阴离子
(4)氢氧化钾(KOH)也是一种碱。依据反应②,氢氧化钾能与下列物质反应的是
A.硫酸 B.氯化钡 C.硫酸铜 D.碳酸钠
发生反应的化学方程式为 .
四、计算题
26. 某化工产品是NaCl和NaOH组成的混合物。课外活动小组为测定该产品中NaCl的质量分数,进行了以下实验。取10.0g该固体样品置于锥形瓶中,加入适量的水配成溶液,逐滴加入溶质质量分数为10%的稀盐酸,用pH传感器等电子设备测得滴加过程中溶液的pH与加入稀盐酸的质量关系如图所示。请回答下列问题:
(1)恰好完全反应时,消耗稀盐酸中溶质的质量为________g。(2)计算样品中NaCl的质量分数。
九年级化学试题
可能用到的相对原子质量C:12 H:1 O:16 N:14 Na:23 Cl:35.5 Ca:40
一、选择题(本题包括20个小题,每小题2分,共10分,每小题只有一个正确选项.)
1. 下列四组物质只用水不能区分开的是
A. 氢氧化钠固体和氯化钠固体 B. 硝酸铵固体和氯化钠固体
C. 氯化镁固体和氯化钠固体 D. 生石灰和氯化钠固体
2. 下列物质露置于空气中,没有发生化学变化而质量增大的是
A. 浓硫酸 B. 浓盐酸 C. 生石灰 D. 氢氧化钠
3. 下列说法正确的是
A. 爆炸都是由剧烈燃烧引起的 B. 原子核都由质子和中子构成
C. 由一种元素组成的物质一定是单质 D. 干冰升华是物理变化
4. 如图是铜元素和硫元素常见的化合价坐标图,试判断C点上形成化合物的化学式( )
A. CuS B. CuS2 C. Cu2S D. Cu2S2
5. 有关2H2 +O22H2O的叙述正确的是( )
A. 两个氢分子加一个氧分子等于两个水分子
B. 氢气和氧气在点燃条件下反应生成水
C. 氢气加氧气点燃等于水 D. 2g氢气和lg氧气反应生成2g水
6. 如图表示的是纯净物、单质、化合物、含氧化合物、氧化物之间的包含与不包含关系,若整个大圆圈代表纯净物,则在下列选项中,能正确表示①、②、③、④所属物质类别的是
A. ②化合物、④氧化物 B. ①单质、③氧化物
C. ①单质、③化合物 D. ②含氧化合物、④氧化物
7.下列几种常用的灭火方法及灭火原理均正确的是 ( )
选项 实例 灭火方法 灭火原理
A 油锅着火 用水浇灭 使温度降到可燃物的着火点以下
B 液化气起火 关闭阀门 隔绝空气
C 住宅失火 用高压水枪灭火 降低可燃物着火点
D 森林着火 砍伐出隔离带 移走可燃物
8. 碳化硅(SiC)陶瓷基复合材料是一种新型热结构材料.在空气中,碳化硅能与熔融的氢氧化钠发生反应:SiC+2NaOH+2O2Na2SiO3+X+H2O,下列有关X物质的化学式推断中,正确的是( )
A. SiO2 B. CO C. CO2 D. Na2CO3
9.下列有关“CO2”的说法正确的是
A. ① B. ②
C. ③ D. ④
10. 燃烧与人类的生活以及社会的发展有着密切的联系,下列有关燃烧和灭火说法错误的是
A. 釜底抽薪——移除可燃物 B. 电器着火——用水浇灭,使温度降到可燃物的着火点以下
C. 钻木取火——使温度达到可燃物的着火点以上 D. 架空篝火——使木材与空气有足够大的接触面积
11. 鉴别空气、氧气、二氧化碳三瓶气体最简便的方法是( )
A. 伸入燃着的木条 B. 闻气体的气味 C. 加入澄清石灰水 D. 观察气体的颜色
12. 下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象是的(装置气密性均良好)
A. B. C. D.
13.符号表征化学变化是探究物质及其变化规律的认识方式。下列化学方程式正确的是
A. B.
C. D.
14. 在一密闭容器中,有甲、乙、丙、丁 四种物质,在一定条件下存在某个反应,测得反应前后各物质的质量如下表: 对该反应,下列描述不正确的是
物质 甲 乙 丙 丁
反应前质量/g 20 4 20 20
反应后质量/g 2 待测 32 26
A. 该反应是分解反应 B. 乙在该反应中可能是催化剂
C. 待测质量一定为4g D. 该反应中甲、丙、丁的质量比为1:15:13
15.元素化合价和物质类别是认识物质的两个重要维度,构建元素化合价和物质类别的二维图是学习化学的一种重要方法。右图是氮元素的“价类二维图”,下列说法正确的是
A. A点对应的物质约占空气质量分数的78% B. D点对应物质的化学式为NO2
C. E点对应的物质能使紫色石蕊溶液变蓝
D. E与碱反应得到的生成物可代表的点是F
16. 某无色溶液X是稀盐酸、稀硫酸、NaOH溶液、Na2CO3溶液中的一种,取三份等质量的X溶液,向其中分别加入酚酞试液、Fe2O3粉末、BaCl2溶液,产生的现象如下表所述.根据现象判断,无色溶液X是( )
加入的物质 酚酞试液 Fe2O3粉末 BaCl2溶液
实验现象 无明显现象 固体逐渐溶解,溶液变黄 无明现象
A. 稀硫酸 B. 稀盐酸 C. NaOH溶液 D. Na2CO3溶液
17.下列关于的实验室制取及检验的说法不正确的是
A.制的药品 B.发生装置 C.收集方法 D.检验
18. 根据下列实验现象,可以判断其溶液一定呈酸性的是( )
A. 滴加酚酞试液显无色的溶液 B. 滴加石蕊试液显蓝色的溶液
C. 能够与碱发生反应的溶液 D. 常温下,pH<7 的溶液
二、填空题
19. 实验是科学探究重要方法。请根据下列装置图,回答问题。
(1)现要测定某酸性溶液的 pH 如图①,若先将玻璃棒润湿,会导致测定值与实际值比较_____(填“偏大’·或“偏小”或“无法确定”)。
(2)利用图②装置稀释浓硫酸时,为确保实验安全,倾倒的B为 _____(填“浓硫酸”或“水”)。
(3)利用图③装置测得空气中氧气的体积分数小于 21%,可能的原因是____ _ (任写一条 )。
(4)利用图④装置验证质量守恒定律时,烧杯内盛有氯化铁溶液,为达到实验 目的,试管中可放入一种与氯化铁溶液反应的 C物质,请写出发生反应的化学方程式 _____(只写一个)。
20.化学是以实验为基础的学科,正确选择实验装置是实验成功的关键。下图所示装置常用于实验室制取气体,请回答下列问题。
(1)标号①的仪器名称是______。
(2)你认为选用B作发生装置,优点是______;请指出装置C中存在的一处错误______。
(3)改进上述装置图中存在的错误,并以过氧化氢溶液为原料,在实验室中制取并收集干燥的氧气。按照要求选择实验装置,连接仪器后,先______,再装入药品,进行实验。
①所选装置的连接顺序为___ ___(从左到右填写装置序号字母)。
②上述方法制氧气的化学方程式为___ ___。
③若把G装置中的浓硫酸换成水并盛满,用来收集难溶于水的气体时,气体从______(填“a”或“b”)端通入。
(4)甲烷(CH4)是最简单、难溶于水的有机物类气体,实验室常用加热无水醋酸钠与氢氧化钠的固体混合物来制得。实验室制取甲烷应选用的发生、收集装置是______(填序号)。
21. 如图是A、B、C三种固体物质的溶解度曲线,据图做答:
(1)A与C的曲线相交于P点,则P点的意义是_________。
(2)A、B、C三种物质中,溶解度随着温度的上升而减小的物质是_____。
(3)t2℃时,将30gA 物质加入到50g 水中可形成_____g 溶液,此时溶液是______(填“饱和”或“不饱和”)溶液。
(4)将 t2℃时A、B、C三种物质的饱和溶液均降温至t1℃,所得溶液中溶质质量分数由大到小的顺序是________。
(5)A物质中混有少量的C物质,若提纯A物质,可采用的结晶方法是 _________。
(6)将t2℃时 A、B两种物质的饱和溶液均降温至t1℃,则析出晶体的质量关系为_______(填“A>B”或“A<B”或“无法判断”)。
22.海水是一种重要资源,利用海水可制取金属镁等物质。某化学兴趣小组的同学设计了如下实验流程:
根据流程回答下列问题:
(1)操作Ⅰ的名称是______,该操作用到的玻璃仪器有烧杯,漏斗和______;该仪器在操作Ⅰ中的作用是______。操作Ⅰ中加入的NaOH溶液应过量,其目的是______。
(2)试剂X是______(填名称),写出溶液A中加入试剂X发生反应的化学方程式______。
三、实验探究题
23. 通过化学学习,你已经掌握了实验室制取气体的有关规律。请结合下图回答问题:
(1)写出图中标号仪器的名称:①____ __;②___ ___。
(2)已知过氧化钠(Na2O2)是一种淡黄色固体粉末,常温下可与水反应生成氢氧化钠和氧气。如果在实验室中用过氧化钠和水反应来制取一瓶氧气,通常选用B装置来做发生装置,优点是______。反应的化学方程式______。利用F装置收集氧气的最佳时刻是______。
(3)制取二氧化碳气体时,想控制反应的随时发生和停止,应当选用______装置。检验该气体是否收集满的方式是______。
(4)实验室选用如图G装置收集二氧化碳,气体应该从______(填“a”或“b”)进入,若G装置内装满水时,再连接一个用于量度液体的体积的仪器______,就可以用于测定不溶于水且不与水反应的气体体积,则气体应从______(填“a”或“b”)进入广口瓶中。
24.某化学兴趣小组三位同学在学习了硫酸与氢氧化钠反应后,分别结合自己在实验室中所做的实验,从不同方面对其进行图像描述。图A是实际操作图,图B是反应过程中溶液的酸碱度变化图,图C是微观粒子结合过程的示意图。
根据以上图示,回答下列问题:(1)依据图A、图B可知,该实验是将_______滴加到另一种溶液中。写出图C中方框内乙粒子的符号_______。
(2)图B中b点溶液中溶质是_______,向其中加入石蕊试液,溶液呈______色。
(3)向的溶液中滴加氯化钡,发生反应的化学方程式为____ ___。
(4)中和反应的实质是______。在工农业生产中有着非常要的作用,请写出用熟石灰处理含有(H2SO4)的工业废水的反应原理______。
25.某同学总结了碱的化学性质如下图,“ ”表示短线两端的物质互相之间能够发生化学反应。请你根据要求完成下列问题。
(1)该同学在取用氢氧化钠溶液时,发现试剂瓶瓶塞没有塞。据反应④说明NaOH必须密封保存,否则在空气中就要变质为 (填化学式)
(2)要检验该氢氧化钠溶液已变质,选择下列试剂不能达到目的是 (填字母代号)。A.稀HCl B.酚酞试液 C.CaCl2 D. Ca(OH)2
(3)为了验证反应③,该同学将无色酞试液分别滴入NaOH溶液和澄清石灰水中,溶液由无色变成红色,原因是它们在水溶液中都能解离出一种共同的阴离子
(4)氢氧化钾(KOH)也是一种碱。依据反应②,氢氧化钾能与下列物质反应的是
A.硫酸 B.氯化钡 C.硫酸铜 D.碳酸钠
发生反应的化学方程式为 .
四、计算题
26. 某化工产品是NaCl和NaOH组成的混合物。课外活动小组为测定该产品中NaCl的质量分数,进行了以下实验。取10.0g该固体样品置于锥形瓶中,加入适量的水配成溶液,逐滴加入溶质质量分数为10%的稀盐酸,用pH传感器等电子设备测得滴加过程中溶液的pH与加入稀盐酸的质量关系如图所示。请回答下列问题:
(1)恰好完全反应时,消耗稀盐酸中溶质的质量为________g。(2)计算样品中NaCl的质量分数。
同课章节目录
