3.2 课时4 盐类水解的应用 课件 (共16张PPT)2023-2024学年高二化学鲁科版(2019)选择性必修1
文档属性
| 名称 | 3.2 课时4 盐类水解的应用 课件 (共16张PPT)2023-2024学年高二化学鲁科版(2019)选择性必修1 |

|
|
| 格式 | pptx | ||
| 文件大小 | 510.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-18 00:00:00 | ||
图片预览





文档简介
(共16张PPT)
第2节 弱电解质的电离 盐类的水解 课时4
了解盐类水解在生产生活、化学实验、科学研究中的应用。
交流 · 研讨
交流 · 研讨
你能用水解平衡的知识解释泡沫灭火器的灭火原理吗?
泡沫灭火器中装有NaHCO3浓溶液和Al2(SO4)3浓溶液。二者混合时会发生剧烈反应,产生气体和沉淀,在起泡剂的作用下迅速产生大量泡沫,用以灭火。
NaHCO3溶液
Al2(SO4)3溶液
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
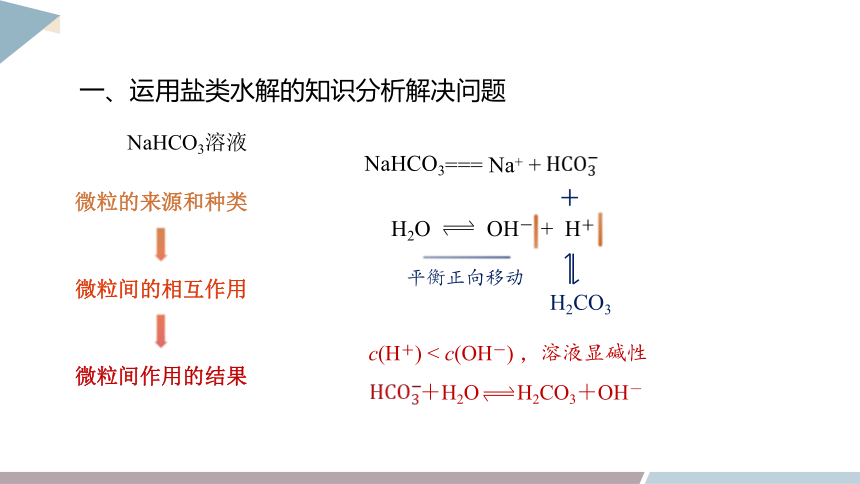
H2O OH- + H+
+
H2CO3
平衡正向移动
c(H+) < c(OH-) ,溶液显碱性
一、运用盐类水解的知识分析解决问题
NaHCO3溶液
NaHCO3
=== Na+ +
+H2O H2CO3+OH-
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
一、运用盐类水解的知识分析解决问题
Al2(SO4)3溶液
H2O OH- + H+
+
Al(OH)3
平衡正向移动
Al2(SO4)3
===2 +3
Al3+
c(H+)>c(OH-) ,溶液显酸性
Al3++3H2O Al(OH)3+3H+
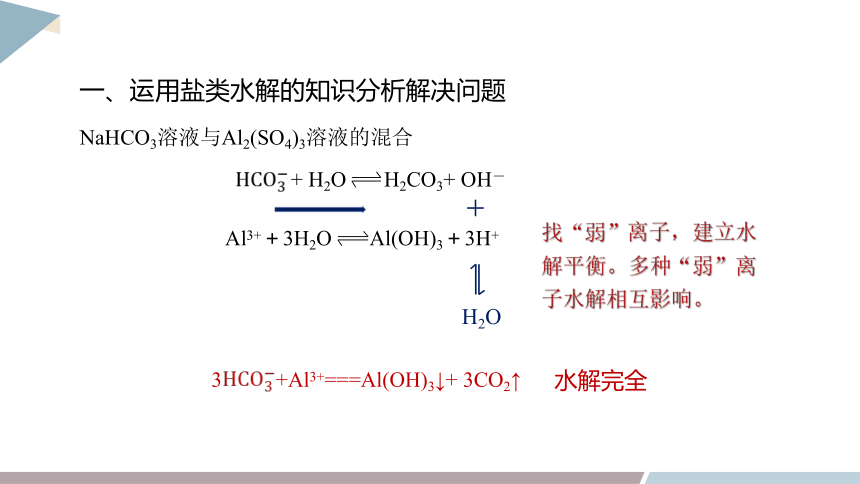
NaHCO3溶液与Al2(SO4)3溶液的混合
一、运用盐类水解的知识分析解决问题
+ H2O H2CO3+ OH-
Al3++3H2O Al(OH)3+3H+
+
H2O
找“弱”离子,建立水解平衡。多种“弱”离子水解相互影响。
3 +Al3+===Al(OH)3↓+ 3CO2↑
水解完全
思考与交流
Ⅰ.硫化铝固体溶于水后会产生什么现象?
Al2S3 ===3S2- +2Al3+
Al3++3H2O 3H+ + Al(OH)3
S2-+H2O OH- + HS-
HS- +H2O OH- + H2S
Al2S3 + 6H2O===2Al(OH)3↓+ 3H2S↑
水解完全
同时产生沉淀和气体
注:硫化铝等盐,其阴、阳离子都能水解并分别生成气体和沉淀,因此这样的盐在水中是不能存在的。
思考与交流
Ⅱ.醋酸铵固体溶于水后,醋酸根和铵根离子都能水解,其水溶液能稳定存在吗?
能稳定存在
H2O NH3·H2O + H+
CH3COO-+ H2O CH3COOH + OH-
H2O
+
CH3COO-+NH4+H2O NH3·H2O+CH3COOH
+
部分水解
二、盐类水解的应用
活动 · 探究
活动 · 探究
【实验目的】制备氢氧化铁胶体
【实验用品】
饱和FeCl3溶液、稀盐酸;
试管、烧杯、胶头滴管、酒精灯、三脚架、石棉网,激光笔。
Fe3+ + 3H2O Fe(OH)3 + 3H+
加热,促进水解,生成氢氧化铁胶体
Fe3+ + 3H2O Fe(OH)3(胶体)+ 3H+
△
二、盐类水解的应用
活动 · 探究
活动 · 探究
【实验目的】除去略浑浊的天然淡水中的悬浮颗粒物
【实验用品】
Al2(SO4)3溶液、略浑浊的天然淡水;
试管、烧杯、胶头滴管、酒精灯、三脚架、石棉网,激光笔。
Al3+ + 3H2O Al(OH)3 + 3H+
Al3+与HCO3水解互促,生成氢氧化铝胶体
-
Al3++3H2O Al(OH)3(胶体)+3H+
-
含HCO3离子
二、盐类水解的应用
活动 · 探究
活动 · 探究
【实验目的】清除厨房的油污
【实验用品】
Na2CO3溶液、植物油、蒸馏水;
试管、烧杯、胶头滴管、酒精灯、三脚架、石棉网,激光笔。
油脂可在一定条件下与水发生反应,生成甘油和脂肪酸。该反应属于可逆反应。
+H2O +OH-
+H2O H2CO3+OH-
加热促进水解,碱性增强,利用碱性除油污
思考与交流
解释下列事实:
Ⅰ.铵态氮肥与草木灰(成分含有K2CO3)混合使用会大大降低氮肥的肥效。
Ⅱ.配制FeCl3溶液时,需要加入适量的盐酸
配制、保存易水解的盐溶液时,加入相应的酸(或碱)可抑制水解。配制FeCl3溶液时,加入适量盐酸可抑制Fe3+的水解,得到澄清的溶液。
H2O NH3·H2O + H+
+H2O +OH-
两个水解反应相互促进,NH3·H2O分解产生氨气逸出,造成氮肥损失。
【练一练】
1.判断下列说法是否正确,正确的打“√”,错误的打“×”。
(1)实验室保存Na2S溶液用带有玻璃塞的试剂瓶。( )
(2)将Cu(NO3)2固体溶于稀硝酸配制Cu(NO3)2溶液。( )
(3)在FeCl3溶液中加入镁粉既有气体产生又有红褐色沉淀产生。( )
(4)把镁粉投入到NH4Cl溶液中,有两种气体产生。( )
(5)水解平衡右移,弱离子的水解程度一定增大。( )
(6)施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用。 ( )
2.下列应用与碳酸钠或碳酸氢钠能发生水解反应无关的是( )
A.实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞
B.泡沫灭火器中含有碳酸氢钠溶液和硫酸铝溶液,使用时只需将二者混合就可产生大量二氧化碳
C.厨房中常用碳酸钠溶液洗涤餐具上的油污
D.可利用碳酸钠与醋酸反应制取少量二氧化碳
D
4.(双选)已知Fe3+在pH为4~5时就可以完全形成Fe(OH)3沉淀,若要除去MgCl2酸性溶液中的Fe3+,可以加入一种试剂,充分搅拌作用后过滤,就可得到纯净的MgCl2溶液,这种试剂可以是( )
A.NH3·H2O B.NaOH C.Mg(OH)2 D.MgCO3
3.分别将下列物质:①FeCl3 ②CaO ③NaCl ④Ca(HCO3)2 ⑤Na2SO3 ⑥K2SO4投入水中,在蒸发皿中对其溶液加热蒸干,能得到原物质的是 ( )
A.②③ B.③⑥ C.①④ D.⑤⑥
B
CD
盐类水解的应用
制备胶体、净水、除污
热碱水清洗油污
泡沫灭火器等
第2节 弱电解质的电离 盐类的水解 课时4
了解盐类水解在生产生活、化学实验、科学研究中的应用。
交流 · 研讨
交流 · 研讨
你能用水解平衡的知识解释泡沫灭火器的灭火原理吗?
泡沫灭火器中装有NaHCO3浓溶液和Al2(SO4)3浓溶液。二者混合时会发生剧烈反应,产生气体和沉淀,在起泡剂的作用下迅速产生大量泡沫,用以灭火。
NaHCO3溶液
Al2(SO4)3溶液
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
H2O OH- + H+
+
H2CO3
平衡正向移动
c(H+) < c(OH-) ,溶液显碱性
一、运用盐类水解的知识分析解决问题
NaHCO3溶液
NaHCO3
=== Na+ +
+H2O H2CO3+OH-
微粒的来源和种类
微粒间的相互作用
微粒间作用的结果
一、运用盐类水解的知识分析解决问题
Al2(SO4)3溶液
H2O OH- + H+
+
Al(OH)3
平衡正向移动
Al2(SO4)3
===2 +3
Al3+
c(H+)>c(OH-) ,溶液显酸性
Al3++3H2O Al(OH)3+3H+
NaHCO3溶液与Al2(SO4)3溶液的混合
一、运用盐类水解的知识分析解决问题
+ H2O H2CO3+ OH-
Al3++3H2O Al(OH)3+3H+
+
H2O
找“弱”离子,建立水解平衡。多种“弱”离子水解相互影响。
3 +Al3+===Al(OH)3↓+ 3CO2↑
水解完全
思考与交流
Ⅰ.硫化铝固体溶于水后会产生什么现象?
Al2S3 ===3S2- +2Al3+
Al3++3H2O 3H+ + Al(OH)3
S2-+H2O OH- + HS-
HS- +H2O OH- + H2S
Al2S3 + 6H2O===2Al(OH)3↓+ 3H2S↑
水解完全
同时产生沉淀和气体
注:硫化铝等盐,其阴、阳离子都能水解并分别生成气体和沉淀,因此这样的盐在水中是不能存在的。
思考与交流
Ⅱ.醋酸铵固体溶于水后,醋酸根和铵根离子都能水解,其水溶液能稳定存在吗?
能稳定存在
H2O NH3·H2O + H+
CH3COO-+ H2O CH3COOH + OH-
H2O
+
CH3COO-+NH4+H2O NH3·H2O+CH3COOH
+
部分水解
二、盐类水解的应用
活动 · 探究
活动 · 探究
【实验目的】制备氢氧化铁胶体
【实验用品】
饱和FeCl3溶液、稀盐酸;
试管、烧杯、胶头滴管、酒精灯、三脚架、石棉网,激光笔。
Fe3+ + 3H2O Fe(OH)3 + 3H+
加热,促进水解,生成氢氧化铁胶体
Fe3+ + 3H2O Fe(OH)3(胶体)+ 3H+
△
二、盐类水解的应用
活动 · 探究
活动 · 探究
【实验目的】除去略浑浊的天然淡水中的悬浮颗粒物
【实验用品】
Al2(SO4)3溶液、略浑浊的天然淡水;
试管、烧杯、胶头滴管、酒精灯、三脚架、石棉网,激光笔。
Al3+ + 3H2O Al(OH)3 + 3H+
Al3+与HCO3水解互促,生成氢氧化铝胶体
-
Al3++3H2O Al(OH)3(胶体)+3H+
-
含HCO3离子
二、盐类水解的应用
活动 · 探究
活动 · 探究
【实验目的】清除厨房的油污
【实验用品】
Na2CO3溶液、植物油、蒸馏水;
试管、烧杯、胶头滴管、酒精灯、三脚架、石棉网,激光笔。
油脂可在一定条件下与水发生反应,生成甘油和脂肪酸。该反应属于可逆反应。
+H2O +OH-
+H2O H2CO3+OH-
加热促进水解,碱性增强,利用碱性除油污
思考与交流
解释下列事实:
Ⅰ.铵态氮肥与草木灰(成分含有K2CO3)混合使用会大大降低氮肥的肥效。
Ⅱ.配制FeCl3溶液时,需要加入适量的盐酸
配制、保存易水解的盐溶液时,加入相应的酸(或碱)可抑制水解。配制FeCl3溶液时,加入适量盐酸可抑制Fe3+的水解,得到澄清的溶液。
H2O NH3·H2O + H+
+H2O +OH-
两个水解反应相互促进,NH3·H2O分解产生氨气逸出,造成氮肥损失。
【练一练】
1.判断下列说法是否正确,正确的打“√”,错误的打“×”。
(1)实验室保存Na2S溶液用带有玻璃塞的试剂瓶。( )
(2)将Cu(NO3)2固体溶于稀硝酸配制Cu(NO3)2溶液。( )
(3)在FeCl3溶液中加入镁粉既有气体产生又有红褐色沉淀产生。( )
(4)把镁粉投入到NH4Cl溶液中,有两种气体产生。( )
(5)水解平衡右移,弱离子的水解程度一定增大。( )
(6)施肥时,草木灰(有效成分为K2CO3)不能与NH4Cl混合使用。 ( )
2.下列应用与碳酸钠或碳酸氢钠能发生水解反应无关的是( )
A.实验室盛放碳酸钠溶液的试剂瓶必须用橡胶塞而不能用玻璃塞
B.泡沫灭火器中含有碳酸氢钠溶液和硫酸铝溶液,使用时只需将二者混合就可产生大量二氧化碳
C.厨房中常用碳酸钠溶液洗涤餐具上的油污
D.可利用碳酸钠与醋酸反应制取少量二氧化碳
D
4.(双选)已知Fe3+在pH为4~5时就可以完全形成Fe(OH)3沉淀,若要除去MgCl2酸性溶液中的Fe3+,可以加入一种试剂,充分搅拌作用后过滤,就可得到纯净的MgCl2溶液,这种试剂可以是( )
A.NH3·H2O B.NaOH C.Mg(OH)2 D.MgCO3
3.分别将下列物质:①FeCl3 ②CaO ③NaCl ④Ca(HCO3)2 ⑤Na2SO3 ⑥K2SO4投入水中,在蒸发皿中对其溶液加热蒸干,能得到原物质的是 ( )
A.②③ B.③⑥ C.①④ D.⑤⑥
B
CD
盐类水解的应用
制备胶体、净水、除污
热碱水清洗油污
泡沫灭火器等
同课章节目录
- 第1章 化学反应与能量转化
- 第1节 化学反应的热效应
- 第2节 化学能转化为电能——电池
- 第3节 电能转化为化学能——电解
- 第4节 金属的腐蚀与防护
- 微项目 设计载人航天器用化学电池与氧气再生方案——化学反应中能量及物质的转化利用
- 第2章 化学反应的方向、 限度与速率
- 第1节 化学反应的方向
- 第2节 化学反应的限度
- 第3节 化学反应的速率
- 第4节 化学反应条件的优化——工业合成氨
- 微项目 探讨如何利用工业废气中的二氧化碳合成甲醇——化学反应选择与反应条件优化
- 第3章 物质在水溶液中的行为
- 第1节 水与水溶液
- 第2节 弱电解质的电离 盐类的水解
- 第3节 沉淀溶解平衡
- 第4节 离子反应
- 微项目 揭秘索尔维制碱法和侯氏制碱法——化学平衡思想的创造性应用
