第2章《官能团与有机化学反应烃的衍生物》(含解析)练习卷2023-2024学年下学期高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第2章《官能团与有机化学反应烃的衍生物》(含解析)练习卷2023-2024学年下学期高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 822.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-18 00:00:00 | ||
图片预览




文档简介
第2章《官能团与有机化学反应 烃的衍生物》练习卷
一、单选题
1.关于酯类物质,下列说法不正确的是
A.三油酸甘油酯可表示为
B.酯类物质只能由含氧酸和醇类通过酯化反应获得
C.1mol乙酸苯酚酯()与足量NaOH溶液反应,最多消耗2molNaOH
D.酯类物质在酸性或碱性条件下都可以发生水解反应
2.某学生用1mol/LCuSO4溶液2mL和0.5mol/LNaOH溶液4mL混合后,加入福尔马林0.5mL,加热到沸腾未见红色沉淀生成,主要原因是
A.福尔马林不能发生反应 B.CuSO4的量太少
C.NaOH的量太少 D.加热时间太短
3.下列反应中,属于加成反应的是
A.乙烯与氢气反应生成乙烷 B.乙醇与氧气反应生成二氧化碳和水
C.乙醇与钠反应生成乙醇钠和氢气 D.苯和浓硝酸反应生成硝基苯和水
4.关于醇的说法中正确的是
A.乙醇燃烧生成二氧化碳和水,说明乙醇具有氧化性
B.乙醇可以和金属钠反应很缓慢地放出氢气,说明乙醇的酸性很弱
C.用浓硫酸和乙醇在加热条件下制备乙烯,应该迅速升温到140℃
D.有机物可以发生消去反应和催化氧化
5.下列叙述错误的是
A.乙炔和乙醛都能使溴水褪色,褪色的原因相同
B.聚乙炔可以使酸性高锰酸钾褪色
C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
D.乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
6.将等质量的铜片在酒精灯上加热后,分别插入溶液中,放置片刻铜片质量减小的是
A.水 B.无水乙醇 C.石灰水 D.盐酸
7.黄芩素、野黄芩素和汉黄芩素在医药上均有广泛应用。黄芩素是“清肺排毒汤”的重要活性成分,三种物质的结构简式如下图所示。下列说法正确的是
A.均只含三种官能团
B.都能发生氧化、取代、加成反应
C.汉黄芩素分子()内共面的原子最多有30个
D.等物质的量的三种物质与溶液充分反应,消耗物质的量相同
8.下列说法正确的是
A.蛋白质是仅由碳、氢、氧、氮四种元素组成的物质
B.柴油、奶油、牛油它们所含的物质类别相同
C.分子式为C4H8O2且能与氢氧化钠溶液反应的物质有6种
D.聚合物( ),它是一种纯净物,可由单体CH3CH=CH2和CH2=CH2加聚制得
9.下列物质(括号内为杂质)的除杂方法正确的是
选项 物质(杂质) 除杂方法
A. SO2(HCl) 将气体通入饱和亚硫酸氢钠水溶液
B. CuCl2溶液(FeCl3) 加入过量铜粉充分反应,过滤
C. 乙酸乙酯(乙酸) 加入饱和氢氧化钠溶液,振荡后静置分液
D. NaCl溶液(KI) 通入过量氯气后,过滤
A.A B.B C.C D.D
10.我国科学家制备的新型磁性纳米材料实现了农产品中黄酮的快速高效分离与富集。二苯基色原酮的球棍模型如图所示(仅含C、H、O元素)。下列有关二苯基色原酮的说法正确的是
A.分子中含2种官能团 B.能发生加成反应和水解反应
C.不能使酸性KMnO4溶液褪色 D.分子中所有原子可能共平面
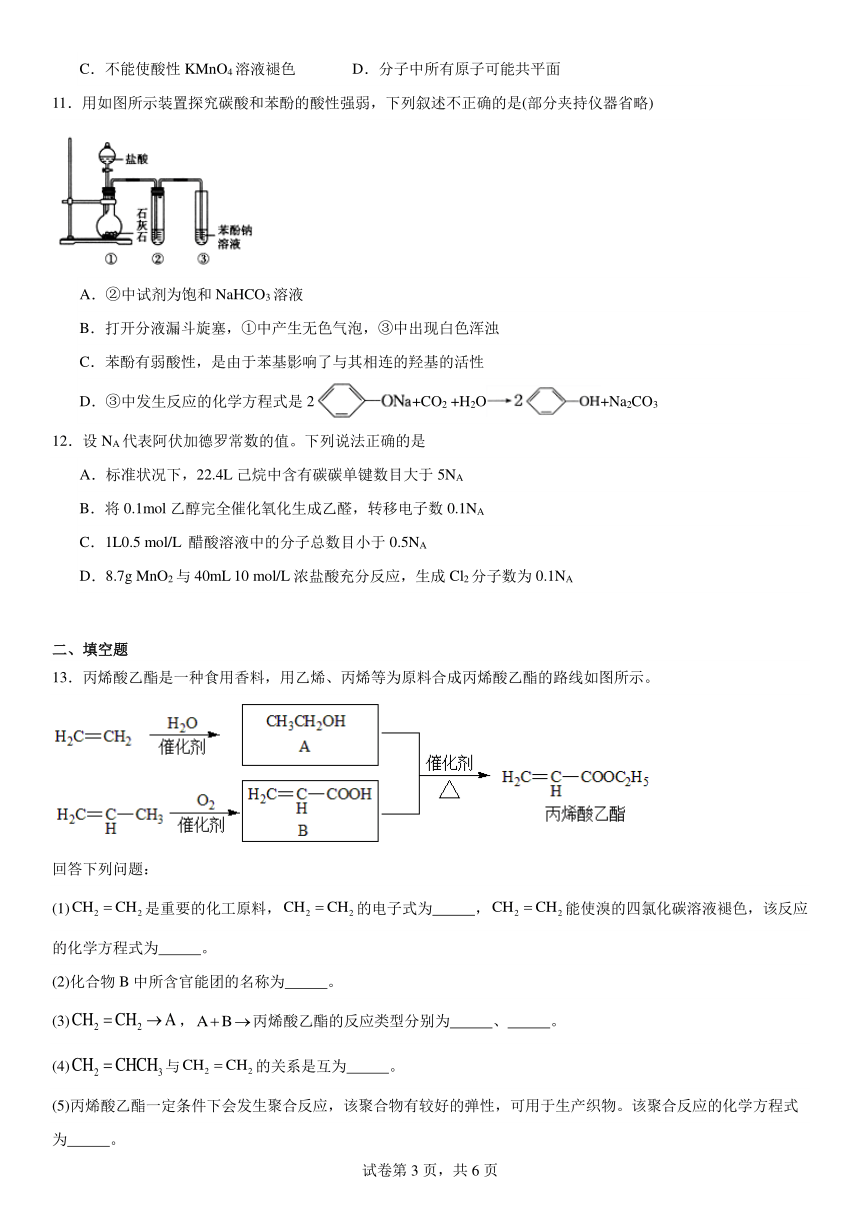
11.用如图所示装置探究碳酸和苯酚的酸性强弱,下列叙述不正确的是(部分夹持仪器省略)
A.②中试剂为饱和NaHCO3溶液
B.打开分液漏斗旋塞,①中产生无色气泡,③中出现白色浑浊
C.苯酚有弱酸性,是由于苯基影响了与其相连的羟基的活性
D.③中发生反应的化学方程式是2+CO2 +H2O+Na2CO3
12.设NA代表阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,22.4L己烷中含有碳碳单键数目大于5NA
B.将0.1mol乙醇完全催化氧化生成乙醛,转移电子数0.1NA
C.1L0.5 mol/L 醋酸溶液中的分子总数目小于0.5NA
D.8.7g MnO2与40mL 10 mol/L浓盐酸充分反应,生成Cl2分子数为0.1NA
二、填空题
13.丙烯酸乙酯是一种食用香料,用乙烯、丙烯等为原料合成丙烯酸乙酯的路线如图所示。
回答下列问题:
(1)是重要的化工原料,的电子式为 ,能使溴的四氯化碳溶液褪色,该反应的化学方程式为 。
(2)化合物B中所含官能团的名称为 。
(3),丙烯酸乙酯的反应类型分别为 、 。
(4)与的关系是互为 。
(5)丙烯酸乙酯一定条件下会发生聚合反应,该聚合物有较好的弹性,可用于生产织物。该聚合反应的化学方程式为 。
14.按要求书写酯化反应的化学方程式。
(1)一元羧酸与多元醇之间的酯化反应,如乙酸与乙二醇的物质的量之比为 。
(2)多元羧酸与一元醇之间的酯化反应,如乙二酸与乙醇的物质的量之比为 。
(3)多元羧酸与多元醇之间的酯化反应,如乙二酸与乙二醇酯化
①生成环酯: 。
②生成高聚酯: 。
(4)羟基酸自身的酯化反应,如自身酯化
①生成环酯: 。②生成高聚酯: 。
15.按要求填空:
(1)键线式 表示的分子式为 ,名称是 。
(2)用银氨溶液检验福尔马林溶液中官能团的化学方程式为 。
(3) 含有的官能团的名称为 ,写出该物质在一定条件与氢氧化钠溶液反应的化学方程式 。
(4) 最多 个原子共平面,写出该物质发生加聚反应的化学方程式 。
16.分子式为C7H16O的饱和一元醇的同分异构体有多种,在下列该醇的同分异构体中,
A.
B.
C.
D.CH3(CH2)5CH2OH
(1)可以发生消去反应,生成两种单烯烃的是 ;
(2)可以发生催化氧化生成醛的是 ;
(3)不能发生催化氧化的是 ;
(4)能被催化氧化为酮的有 种;
17.回答下列问题
(1)硬脂酸的结构简式为 。
(2)苯和乙烯反应获得乙苯的反应类型为 。
(3)1─溴丙烷与氢氧化钾醇溶液共热的化学方程式为 。
(4)苯和液溴在铁催化下生产溴苯,而苯酚和溴水反应生成2,4,6─三溴苯酚,两者存在明显差异的原因是 。
18.2,3-吡啶二羧酸,俗称喹啉酸,是一种中枢神经毒素,阿尔茨海默症、帕金森症等都与它有关。常温下喹啉酸呈固态,在185~190°C下释放CO2转化为烟酸。
(1)晶体中,喹啉酸采取能量最低的构型,画出此构型 (碳原子上的氢原子以及孤对电子可不画)。
(2)喹啉酸在水溶液中的pKa1=2.41,写出其一级电离的方程式 (共轭酸碱用结构简式表示)。
(3)画出烟酸的结构 。
19.判断下列指定分子式和条件的各种同分异构体的数目。
分子式 (芳香族)
(1)属于羧酸的种类数
(2)属于酯的种类数
(3)属于酯,水解后的酸和醇(或酚)重新组合后生成的酯的种类数
(4)属于醛,同时能与钠反应放出氢气
20.分子的性质是由分子的结构决定的,通过对下列分子结构的观察来推测它的性质:
(1)苯基部分可发生 反应和 反应。
(2)—CHCH2部分可发生 反应和 反应。
(3)写出此有机物形成的高分子化合物的结构简式: 。
(4)试判断此有机物的—C(CH2Cl)3部分 (填“能”或“不能”)发生消去反应。
21.有机物的种类繁多,在日常生活中有重要的用途,回答下列问题:
(1)汽油辛烷值越高,品质越好。汽油中的异辛烷的键线式为,其分子式为 ,系统命名法名称为 。
(2)阿司匹林可缓解疼痛,如牙痛、头痛、神经痛,对感冒、流感等发热疾病的退热效果较好。阿司匹林的结构式为,其中含有的官能团的名称为 、 。
(3)掺杂碘、溴等卤素的聚乙炔可用作太阳能电池、半导体材料。写出工业上制取聚乙炔的化学方程式: 。
(4)A~G是几种烃的分子球棍模型,回答下列问题:
①分子中所有原子在同一平面上的是 (填标号,下同);
②常温下含碳量最高的液态烃是 ;
③能使酸性高锰酸钾溶液褪色的烃是 ;
④写出C与溴水反应的化学方程式: ;
⑤写出G与足量发生硝化反应的化学方程式: 。
(5)下列关于有机物的说法正确的是_______(填标号)
A.除去甲烷中混有少量的乙烯,可将混合气体通入酸性高锰酸钾溶液
B.1—丁烯和1,3—丁二烯互为同系物
C.和二者互为同分异构体
D.可采用点燃并观察火焰的明亮程度及产生黑烟量的多少,鉴别甲烷、乙烯、乙炔
(6)环己二烯的结构简式为:,1mol环己二烯与等物质的量的发生加成反应,其可能的产物有 种(不考虑顺反异构)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】A.甘油是丙三醇、油酸是C17H33COOH,两者发生酯化反应得到三油酸甘油酯,结构简式为,A正确;
B.若羟基直接连接在苯环上,类别属于酚类,即羧酸和苯酚类也可通过酯化反应得到酯类物质,B错误;
C.与NaOH溶液反应先断裂酯基的键,得到羟基是连接在苯环上,即为苯酚,其具有酸性,可再消耗NaOH,所以1mol乙酸苯酚酯最多消耗2molNaOH,C正确;
D.酯类物质在酸性条件如浓硫酸加热下可发生水解得到羧酸类和醇类,在碱性条件下如NaOH溶液加热下可得到钠盐,两种条件下都可以发生水解反应,D正确;
故选:B。
2.C
【详解】醛基与新制氢氧化铜反应需在碱性环境下进行:;根据题目所给信息硫酸铜与氢氧化钠恰好完全反应,使得溶液中碱性不足,无法出现相应实验现象;
本题选C。
【点睛】含醛基的有机物与银氨溶液或与新制氢氧化铜反应均需碱性环境。
3.A
【详解】A.乙烯含有碳碳双键,与氢气发生加成反应生成乙烷,所以此反应属于加成反应,故选A项;
B.乙醇与氧气反应生成二氧化碳和水,此反应为氧化反应,故B项不选;
C.乙醇与钠反应生成乙醇钠和氢气,属于置换反应,不符合加成反应概念,故C项不选;
D.苯和浓硝酸反应生成硝基苯和水,为取代反应,故D项不选;
答案为A。
4.D
【详解】A.乙醇燃烧生成二氧化碳和水,说明乙醇作燃料,具有还原性,A错误;
B.乙醇可以和金属钠反应很缓慢地放出氢气,只能说明乙醇分子中含有-OH,不能说明乙醇有酸性,B错误;
C.浓硫酸和乙醇混合加热到170℃,发生消去反应生成乙烯,C错误;
D.有机物中,由于羟基连接的C原子上有H原子,所以可以发生催化氧化反应;由于羟基连接的C原子邻位C原子上有H原子,因此可以发生消去反应,D正确;
故合理选项是D。
5.A
【详解】A. 乙炔能使溴水褪色,发生的是加成反应,但乙醛能使溴水褪色,发生的是氧化反应,褪色的原因不相同,故A错误;
B. 聚乙炔中含碳碳双键,可以使酸性高锰酸钾褪色,故B正确;
C. 煤油可由石油分馏获得,煤油燃烧放出大量的热,可用作燃料,煤油的密度比钠小且不与钠反应,可以隔绝空气和水,故煤油可用于保存少量金属钠,故C正确;
D. 乙酸可与饱和碳酸钠溶液反应生成乙酸钠、水和二氧化碳,而乙酸乙酯不反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去,故D正确;
故选A。
6.D
【详解】A.铜加热后生成CuO,插入水中后不反应,故铜片质量增加,故A不选;
B.铜加热后生成CuO,插入乙醇中,生成乙醛和Cu,质量不变,故B不选;
C.铜加热后生成CuO,插入石灰水中后不反应,铜片质量增加,故C不选;
D.铜加热后生成CuO,插入盐酸中,CuO和盐酸反应生成CuCl2溶于水,故铜片质量减少,故D选;
答案选D。
7.B
【详解】A.三种物质均含羟基、醚键、羰基、碳碳双键,共4种官能团,故A错误;
B.含酚羟基,可发生氧化、取代反应,含碳碳双键可发生氧化、加成反应,故B正确;
C.甲基上最多有1个H原子与其它原子共面时,共面原子最多,则共面原子最多为33-2=31个,故C错误;
D.只有酚羟基与碳酸钠溶液反应,野黄芩素含4个酚羟基、汉黄芩素含2个酚羟基,汉黄芩素消耗的碳酸钠最少,故D错误;
故选:B。
8.C
【详解】A.蛋白质中除含有C、H、N、O四种元素外,还可能含有S、P等元素,选项A错误;
B.柴油是烃类物质,奶油、牛油是饱和高级脂肪酸甘油酯,属于酯类,它们所含的物质类别不相同,选项B错误;
C.对于羧酸而言,根据羧基位置异构可以得到两种丁酸;根据酯基位置异构和碳链异构可得:甲酸丙酯2种(丙基2种异构)、乙酸乙酯1种、丙酸甲酯1种,共6种,选项C正确;
D.聚合物( )可由单体CH3CH=CH2和CH2=CH2加聚制得,但该聚合物为混合物,选项D错误;
答案选C。
9.A
【详解】A.HCl与饱和亚硫酸钠反应,二氧化硫不与亚硫酸氢钠水溶液反应,可以进行除杂,A正确;
B.氯化铁与铜反应生成氯化亚铁与氯化铜,引进氯化亚铁杂质,B错误;
C.二者均与NaOH溶液反应,不能除杂,应选饱和碳酸钠溶液,C错误;
D.氯水与KI反应生成KCl、I2,用萃取分离出碘,但NaCl溶液中引入新杂质KCl,D错误;
答案选A。
10.D
【分析】结构中白色球形成2个共价键,小黑色球形成1个共价键,故白色球为O原子,小黑色球为H原子,大黑色球为C原子,该有机物结构简式为;
【详解】A.该有机物含有碳碳双键、羰基、醚键共3种官能团,A错误;
B.该有机物含有苯环、碳碳双键、羰基,可以发生加成反应,但不能发生水解反应,B错误;
C.该有机物含有碳碳双键,可以被酸性KMnO4溶液氧化,能使酸性KMnO4溶液褪色,C错误;
D.单键可以旋转,苯环平面与双键平面可以共平面,分子中所有原子可能共平面,D正确;
故选D。
11.D
【分析】探究碳酸和苯酚的酸性强弱,由图可知,①中发生盐酸与碳酸钙的反应生成二氧化碳,②中饱和碳酸氢钠溶液可除去HCl,③中发生苯酚钠与二氧化碳的反应生成苯酚,由强酸制取弱酸的原理可比较酸性。
【详解】A.由上述分析可知,②中试剂为饱和NaHCO3溶液,故A正确;
B.打开分液漏斗旋塞,①中有二氧化碳生成,观察到产生无色气泡,③中生成苯酚沉淀,观察到出现白色浑浊,故B正确;
C.由③中强酸制取弱酸的原理可知,苯酚的酸性弱于碳酸,是由于苯基影响了与其相连的羟基的活性,故C正确;
D.③中反应的化学方程式为C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,故D错误;
故选D。
【点睛】本题考查酸性比较的实验方案的设计,把握实验装置的作用、反应原理为解答的关键。本题中要注意除去二氧化碳中的氯化氢气体,因为盐酸能够与苯酚钠反应生成苯酚,影响实验结果。
12.A
【详解】A.己烷在标准状况下是液态,22.4L己烷的物质的量大于1mol,正己烷碳骨架为C-C-C-C-C-C,则含有碳碳单键数目大于5NA,故A正确;
B.乙醇中碳元素为-2价,乙醛中碳元素为-1价,则有C2H5OH~CH3CHO~2e-,0.1mol乙醇反应转移0.2NA个电子,故B错误;
C.在1L 0.5mol/L的醋酸溶液中含有溶质醋酸n=cV=0.5mol,由于醋酸溶液中含有水分子,所以溶液中含有的分子的物质的量大于0.5mol,所含分子数目大于0.5NA,故C错误;
D.8.7g MnO2的物质的量,40mL 10 mol/L浓盐酸物质的量为n=cV=0.4mol,反应方程式为4HCl(浓)+MnO2MnCl2+Cl2↑+2H2O,MnO2只能与浓盐酸反应,和稀盐酸不反应,故当盐酸变稀后反应即停止,故生成的氯气分子个数小于0.1NA个,故D错误;
故选:A。
13. CH2=CH2+Br2→CH2BrCH2Br 碳碳双键、羧基 加成反应 酯化反应(取代反应) 同系物
【详解】(1) 的电子式为,与溴的四氯化碳溶液发生加成反应生成1,2-二溴乙烷,反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br;
(2)CH2=CH-COOH中所含官能团的名称为碳碳双键、羧基。
(3) CH2=CH2和水发生加成反应生成乙醇,是加成反应,乙醇和丙烯酸发生酯化反应生成丙烯酸乙酯,丙烯酸乙酯属于酯化反应(取代反应)。
(4)与都含有1个碳碳双键,分子组成相差1个“CH2”,互为同系物。
(5)丙烯酸乙酯一定条件下会发生聚合反应生成聚丙烯酸乙酯,反应的化学方程式为。
14.(1)
(2)
(3)
(4)
【详解】(1)乙酸与乙二醇的物质的量之比为发生酯化反应,形成1个酯基,化学方程式。
(2)乙二酸与乙醇的物质的量之比为发生酯化反应,形成2个酯基,化学方程式。
(3)①乙二酸与乙二醇酯化生成环酯,脱去2分子水,化学方程式。
②乙二酸与乙二醇生成高聚酯同时脱去水,化学方程式:,答案:。
(4)分子中既含羟基又含羧基,能自身酯化
①生成环酯化学方程式: ;
②生成高聚酯化学方程式。
15.(1) C6H12O 4—甲基戊醛
(2)HCHO+4Ag(NH3)2OH(NH4)2CO3+2H2O+4Ag↓+6NH3
(3) 溴原子 +2NaOH+2NaBr+H2O
(4) 18
【详解】(1)根据键线式可知,其分子式为:C6H12O,含官能团的最长的碳链为5,从右侧开始编写碳号,其名称是:4—甲基戊醛;
(2)福尔马林的成分是甲醛,可以和银氨溶液反应,生成碳酸铵和单质银,方程式为:HCHO+4Ag(NH3)2OH(NH4)2CO3+2H2O+4Ag↓+6NH3;
(3)根据该有机物的结构简式可知,其含有的官能团的名称为溴原子;该物质属于卤代烃,可以和氢氧化钠反应,且水解后生成的是酚类物质,可以继续和氢氧化钠反应,则方程式为:+2NaOH+2NaBr+H2O;
(4)苯环,碳碳双键,醛基分别确定一个平面,通过旋转碳碳单键,可以使三个平面重合,此时所有的原子都共面,一共是18个原子;该物质结构中含有碳碳双键,可以发生加聚反应,方程式为:n。
16. C D B 2
【分析】(1)与-OH相连C的邻位C上有H可发生消去反应;
(2)与-OH相连C上有2个H,可催化氧化生成醛;
(3) 与-OH相连C上不含H原子,不会被催化氧化;
(4) 与-OH相连C上含有1个H原子,催化氧化会生成酮;
据此分析判断。
【详解】(1) 与-OH相连C的邻位C上有H可发生消去反应,要生成两种单烯烃,说明该醇中与-OH相连C有两个邻位C,且均有H,具有不对称结构,满足条件的为C.,故答案为:C;
(2)可以发生催化氧化生成醛,说明分子中与-OH相连C上有2个H,满足条件的为D.CH3(CH2)5CH2OH,故答案为:D;
(3)不能发生催化氧化,说明连接羟基的C原子上不含H原子,满足条件的为B.,故答案为:B;
(4)能被催化氧化为酮,说明连接羟基的C原子上含有1个H原子,满足条件的为A. 、C.,2种,故答案为:2。
17.(1)C17H35COOH
(2)加成反应
(3)CH3CH2CH2Br + KOHCH3CH=CH2↑+ KBr + H2O
(4)苯酚分子中的羟基影响苯基上的氢原子,使邻、对位的氢原子更活泼,易被取代
【解析】(1)
硬脂酸为饱和十八羧酸,结构简式为C17H35COOH。
(2)
苯和乙烯发生加成反应生成乙苯。
(3)
1─溴丙烷与氢氧化钾醇溶液共热发生消去反应生成丙烯、溴化钾和水,故化学方程式为CH3CH2CH2Br + KOHCH3CH=CH2↑+ KBr + H2O。
(4)
苯和液溴在铁催化下发生取代反应生产溴苯,而苯酚和溴水发生取代反应生成2,4,6─三溴苯酚,是因为苯酚分子中的羟基影响苯基上的氢原子,使邻、对位的氢原子更活泼,易被取代。
18. +H2O +H3O
【解析】略
19. 2 4 4 4 9 6 12 40 18 5 12 17
【详解】(1)属于羧酸即C3H7COOH,- C3H7有两种结构,所以属于羧酸的种类数为2种;属于羧酸即C4H9COOH,- C4H9有4种结构,所以属于羧酸的种类数为4种;属于羧酸且为芳香族,结构可能为、、、共4种结构;
(2) 属于酯类的结构有:C2H5COOCH3、CH3COOC2H5、HCOOC3H7(2种),共4种结构;属于酯类的结构有:C3H7COOCH3(2种)、C2H5COOC2H5、CH3COOC3H7(2种)、HCOOC4H9(4种),共9种结构;属于酯类的结构有:、、、(邻、间、对3种),共6种结构;
(3) C4H8O2属于酯的结构有:HCOOCH2CH2CH3、HCOOCH(CH3)CH3、CH3COOCH2CH3、CH3CH2COOCH3共4种,水解后的酸有:HCOOH、CH3COOH和CH3CH2COOH,醇有:CH3OH、CH3CH2OH、CH3CH2CH2OH、HOCH(CH3)CH3,重新组合后生成的酯的种类数:3×4=12种;C5H10O2属于酯的结构有HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3、CH3COOCH2CH2CH3、CH3COOCH(CH3)2、CH3CH2COOCH2CH3、CH3CH2CH2COOCH3、(CH3)2CHCOOCH3共9种,水解后的酸有5种,醇有8种,重新组合后生成的酯的种类数:5×8=40种;C8H8O2属于芳香族的酯的结构:苯环、剩余2个C,可以是甲酸苯甲醇酯、甲酸苯酚酯和甲基(有邻间对三种位置关系)、乙酸苯酚酯和苯甲酸甲酯,共6种,水解后的酸有3种,醇(或酚)有6种,重新组合后生成的酯的种类数:3×6=18种;
(4)属于醛,同时能与钠反应放出氢气,说明同时含有 CHO和 OH,C4H8O2:HO C3H6 CHO,类似于丙烷的二取代物,两个取代基不相同,共有5种;C5H10O2:HO C4H8 CHO,类似于丁烷的二取代物,两个取代基不相同,共有12种;C8H8O2属于芳香族:苯环上连接 CH2CHO和 OH,有邻间对3种,苯环上连接 CH2OH和 CHO,有邻间对3种,苯环上连接 CH3、 CHO和 OH,有10种,苯环上连接,有1种,共有17种。
20. 取代 加成 加成 氧化 不能
【详解】由分子结构可知,访物质分子中有碳碳双键、苯环、氯原子。碳碳双键可以发生加成反应、加聚反应和氧化反应;苯环上可以发生取代反应和加成反应;含氯原子可以发生卤代烃水解反应,但是由于没有H原子,所以不能发生消去反应。
(1)苯基部分可发生加成反应和取代反应。
(2)—CHCH2部分可发生加成反应和氧化反应。
(3)此有机物形成的高分子化合物的结构简式为 。
(4)卤代烃发生消去反应的机理是H消去,即与卤素原子直接相连的C原子()的邻位C原子()上有氢原子的能发生消去反应中。此有机物没有H,所以—C(CH2Cl)3部分不能发生消去反应。
21.(1) 2,2,3—三甲基戊烷
(2) 酯基 羧基
(3)
(4) CDF F CDG CH2=CH2+B2→BrCH2CH2Br +3HNO3+3H2O
(5)D
(6)2
【解析】(1)
由键线式可知,汽油中的异辛烷的分子式为,名称为2,2,3—三甲基戊烷,故答案为:;2,2,3—三甲基戊烷;
(2)
由阿司匹林的结构简式可知,官能团为酯基、羧基,故答案为:酯基;羧基;
(3)
乙炔一定条件下发生加聚反应生成聚乙炔,反应的化学方程式为,故答案为:;
(4)
①由球棍模型可知,乙烯、乙炔和苯分子中的所有原子在同一平面上,故选CDF;
②由球棍模型可知,苯和甲苯常温下为液态,则含碳量最高的液态烃是苯,故选F;
③由球棍模型可知,乙烯、乙炔和甲苯能与酸性高锰酸钾溶液发生氧化反应,使溶液褪色,故选CDG;
④乙烯分子中含有碳碳双键,能与溴水发生加成反应生成1,2—二溴乙烷,反应的化学方程式为CH2=CH2+B2→BrCH2CH2Br,故答案为:CH2=CH2+B2→BrCH2CH2Br;
⑤在浓硫酸作用下,甲苯与足量浓硝酸共热发生硝化反应生成2,4,6—三硝基甲苯和水,反应的化学方程式为+3HNO3+3H2O,故答案为:+3HNO3+3H2O;
(5)
A.乙烯与酸性高锰酸钾溶液发生氧化反应生成二氧化碳,则除去甲烷中混有少量的乙烯不能将混合气体通入酸性高锰酸钾溶液,否则会引入新杂质二氧化碳,故错误;
B.1—丁烯和1,3—丁二烯含有的碳碳双键数目不同,不是同类物质,不可能互为同系物,故错误;
C.甲烷是正四面体结构,二氯甲烷只有1种结构,不可能存在同分异构体,故错误;
D.甲烷、乙烯、乙炔的含碳量不同,燃烧时火焰的明亮程度及产生黑烟量的多少不同,则可采用点燃并观察火焰的明亮程度及产生黑烟量的多少鉴别甲烷、乙烯、乙炔,故正确;
故选D;
(6)
1mol环己二烯与等物质的量的溴水发生加成反应时,可发生1,2加成生成3,4—二溴—1—环己烯,也可发生1,4加成生成4,6—二溴—1—环己烯,所得加成产物共有2种,故答案为:2。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.关于酯类物质,下列说法不正确的是
A.三油酸甘油酯可表示为
B.酯类物质只能由含氧酸和醇类通过酯化反应获得
C.1mol乙酸苯酚酯()与足量NaOH溶液反应,最多消耗2molNaOH
D.酯类物质在酸性或碱性条件下都可以发生水解反应
2.某学生用1mol/LCuSO4溶液2mL和0.5mol/LNaOH溶液4mL混合后,加入福尔马林0.5mL,加热到沸腾未见红色沉淀生成,主要原因是
A.福尔马林不能发生反应 B.CuSO4的量太少
C.NaOH的量太少 D.加热时间太短
3.下列反应中,属于加成反应的是
A.乙烯与氢气反应生成乙烷 B.乙醇与氧气反应生成二氧化碳和水
C.乙醇与钠反应生成乙醇钠和氢气 D.苯和浓硝酸反应生成硝基苯和水
4.关于醇的说法中正确的是
A.乙醇燃烧生成二氧化碳和水,说明乙醇具有氧化性
B.乙醇可以和金属钠反应很缓慢地放出氢气,说明乙醇的酸性很弱
C.用浓硫酸和乙醇在加热条件下制备乙烯,应该迅速升温到140℃
D.有机物可以发生消去反应和催化氧化
5.下列叙述错误的是
A.乙炔和乙醛都能使溴水褪色,褪色的原因相同
B.聚乙炔可以使酸性高锰酸钾褪色
C.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
D.乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
6.将等质量的铜片在酒精灯上加热后,分别插入溶液中,放置片刻铜片质量减小的是
A.水 B.无水乙醇 C.石灰水 D.盐酸
7.黄芩素、野黄芩素和汉黄芩素在医药上均有广泛应用。黄芩素是“清肺排毒汤”的重要活性成分,三种物质的结构简式如下图所示。下列说法正确的是
A.均只含三种官能团
B.都能发生氧化、取代、加成反应
C.汉黄芩素分子()内共面的原子最多有30个
D.等物质的量的三种物质与溶液充分反应,消耗物质的量相同
8.下列说法正确的是
A.蛋白质是仅由碳、氢、氧、氮四种元素组成的物质
B.柴油、奶油、牛油它们所含的物质类别相同
C.分子式为C4H8O2且能与氢氧化钠溶液反应的物质有6种
D.聚合物( ),它是一种纯净物,可由单体CH3CH=CH2和CH2=CH2加聚制得
9.下列物质(括号内为杂质)的除杂方法正确的是
选项 物质(杂质) 除杂方法
A. SO2(HCl) 将气体通入饱和亚硫酸氢钠水溶液
B. CuCl2溶液(FeCl3) 加入过量铜粉充分反应,过滤
C. 乙酸乙酯(乙酸) 加入饱和氢氧化钠溶液,振荡后静置分液
D. NaCl溶液(KI) 通入过量氯气后,过滤
A.A B.B C.C D.D
10.我国科学家制备的新型磁性纳米材料实现了农产品中黄酮的快速高效分离与富集。二苯基色原酮的球棍模型如图所示(仅含C、H、O元素)。下列有关二苯基色原酮的说法正确的是
A.分子中含2种官能团 B.能发生加成反应和水解反应
C.不能使酸性KMnO4溶液褪色 D.分子中所有原子可能共平面
11.用如图所示装置探究碳酸和苯酚的酸性强弱,下列叙述不正确的是(部分夹持仪器省略)
A.②中试剂为饱和NaHCO3溶液
B.打开分液漏斗旋塞,①中产生无色气泡,③中出现白色浑浊
C.苯酚有弱酸性,是由于苯基影响了与其相连的羟基的活性
D.③中发生反应的化学方程式是2+CO2 +H2O+Na2CO3
12.设NA代表阿伏加德罗常数的值。下列说法正确的是
A.标准状况下,22.4L己烷中含有碳碳单键数目大于5NA
B.将0.1mol乙醇完全催化氧化生成乙醛,转移电子数0.1NA
C.1L0.5 mol/L 醋酸溶液中的分子总数目小于0.5NA
D.8.7g MnO2与40mL 10 mol/L浓盐酸充分反应,生成Cl2分子数为0.1NA
二、填空题
13.丙烯酸乙酯是一种食用香料,用乙烯、丙烯等为原料合成丙烯酸乙酯的路线如图所示。
回答下列问题:
(1)是重要的化工原料,的电子式为 ,能使溴的四氯化碳溶液褪色,该反应的化学方程式为 。
(2)化合物B中所含官能团的名称为 。
(3),丙烯酸乙酯的反应类型分别为 、 。
(4)与的关系是互为 。
(5)丙烯酸乙酯一定条件下会发生聚合反应,该聚合物有较好的弹性,可用于生产织物。该聚合反应的化学方程式为 。
14.按要求书写酯化反应的化学方程式。
(1)一元羧酸与多元醇之间的酯化反应,如乙酸与乙二醇的物质的量之比为 。
(2)多元羧酸与一元醇之间的酯化反应,如乙二酸与乙醇的物质的量之比为 。
(3)多元羧酸与多元醇之间的酯化反应,如乙二酸与乙二醇酯化
①生成环酯: 。
②生成高聚酯: 。
(4)羟基酸自身的酯化反应,如自身酯化
①生成环酯: 。②生成高聚酯: 。
15.按要求填空:
(1)键线式 表示的分子式为 ,名称是 。
(2)用银氨溶液检验福尔马林溶液中官能团的化学方程式为 。
(3) 含有的官能团的名称为 ,写出该物质在一定条件与氢氧化钠溶液反应的化学方程式 。
(4) 最多 个原子共平面,写出该物质发生加聚反应的化学方程式 。
16.分子式为C7H16O的饱和一元醇的同分异构体有多种,在下列该醇的同分异构体中,
A.
B.
C.
D.CH3(CH2)5CH2OH
(1)可以发生消去反应,生成两种单烯烃的是 ;
(2)可以发生催化氧化生成醛的是 ;
(3)不能发生催化氧化的是 ;
(4)能被催化氧化为酮的有 种;
17.回答下列问题
(1)硬脂酸的结构简式为 。
(2)苯和乙烯反应获得乙苯的反应类型为 。
(3)1─溴丙烷与氢氧化钾醇溶液共热的化学方程式为 。
(4)苯和液溴在铁催化下生产溴苯,而苯酚和溴水反应生成2,4,6─三溴苯酚,两者存在明显差异的原因是 。
18.2,3-吡啶二羧酸,俗称喹啉酸,是一种中枢神经毒素,阿尔茨海默症、帕金森症等都与它有关。常温下喹啉酸呈固态,在185~190°C下释放CO2转化为烟酸。
(1)晶体中,喹啉酸采取能量最低的构型,画出此构型 (碳原子上的氢原子以及孤对电子可不画)。
(2)喹啉酸在水溶液中的pKa1=2.41,写出其一级电离的方程式 (共轭酸碱用结构简式表示)。
(3)画出烟酸的结构 。
19.判断下列指定分子式和条件的各种同分异构体的数目。
分子式 (芳香族)
(1)属于羧酸的种类数
(2)属于酯的种类数
(3)属于酯,水解后的酸和醇(或酚)重新组合后生成的酯的种类数
(4)属于醛,同时能与钠反应放出氢气
20.分子的性质是由分子的结构决定的,通过对下列分子结构的观察来推测它的性质:
(1)苯基部分可发生 反应和 反应。
(2)—CHCH2部分可发生 反应和 反应。
(3)写出此有机物形成的高分子化合物的结构简式: 。
(4)试判断此有机物的—C(CH2Cl)3部分 (填“能”或“不能”)发生消去反应。
21.有机物的种类繁多,在日常生活中有重要的用途,回答下列问题:
(1)汽油辛烷值越高,品质越好。汽油中的异辛烷的键线式为,其分子式为 ,系统命名法名称为 。
(2)阿司匹林可缓解疼痛,如牙痛、头痛、神经痛,对感冒、流感等发热疾病的退热效果较好。阿司匹林的结构式为,其中含有的官能团的名称为 、 。
(3)掺杂碘、溴等卤素的聚乙炔可用作太阳能电池、半导体材料。写出工业上制取聚乙炔的化学方程式: 。
(4)A~G是几种烃的分子球棍模型,回答下列问题:
①分子中所有原子在同一平面上的是 (填标号,下同);
②常温下含碳量最高的液态烃是 ;
③能使酸性高锰酸钾溶液褪色的烃是 ;
④写出C与溴水反应的化学方程式: ;
⑤写出G与足量发生硝化反应的化学方程式: 。
(5)下列关于有机物的说法正确的是_______(填标号)
A.除去甲烷中混有少量的乙烯,可将混合气体通入酸性高锰酸钾溶液
B.1—丁烯和1,3—丁二烯互为同系物
C.和二者互为同分异构体
D.可采用点燃并观察火焰的明亮程度及产生黑烟量的多少,鉴别甲烷、乙烯、乙炔
(6)环己二烯的结构简式为:,1mol环己二烯与等物质的量的发生加成反应,其可能的产物有 种(不考虑顺反异构)。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
【详解】A.甘油是丙三醇、油酸是C17H33COOH,两者发生酯化反应得到三油酸甘油酯,结构简式为,A正确;
B.若羟基直接连接在苯环上,类别属于酚类,即羧酸和苯酚类也可通过酯化反应得到酯类物质,B错误;
C.与NaOH溶液反应先断裂酯基的键,得到羟基是连接在苯环上,即为苯酚,其具有酸性,可再消耗NaOH,所以1mol乙酸苯酚酯最多消耗2molNaOH,C正确;
D.酯类物质在酸性条件如浓硫酸加热下可发生水解得到羧酸类和醇类,在碱性条件下如NaOH溶液加热下可得到钠盐,两种条件下都可以发生水解反应,D正确;
故选:B。
2.C
【详解】醛基与新制氢氧化铜反应需在碱性环境下进行:;根据题目所给信息硫酸铜与氢氧化钠恰好完全反应,使得溶液中碱性不足,无法出现相应实验现象;
本题选C。
【点睛】含醛基的有机物与银氨溶液或与新制氢氧化铜反应均需碱性环境。
3.A
【详解】A.乙烯含有碳碳双键,与氢气发生加成反应生成乙烷,所以此反应属于加成反应,故选A项;
B.乙醇与氧气反应生成二氧化碳和水,此反应为氧化反应,故B项不选;
C.乙醇与钠反应生成乙醇钠和氢气,属于置换反应,不符合加成反应概念,故C项不选;
D.苯和浓硝酸反应生成硝基苯和水,为取代反应,故D项不选;
答案为A。
4.D
【详解】A.乙醇燃烧生成二氧化碳和水,说明乙醇作燃料,具有还原性,A错误;
B.乙醇可以和金属钠反应很缓慢地放出氢气,只能说明乙醇分子中含有-OH,不能说明乙醇有酸性,B错误;
C.浓硫酸和乙醇混合加热到170℃,发生消去反应生成乙烯,C错误;
D.有机物中,由于羟基连接的C原子上有H原子,所以可以发生催化氧化反应;由于羟基连接的C原子邻位C原子上有H原子,因此可以发生消去反应,D正确;
故合理选项是D。
5.A
【详解】A. 乙炔能使溴水褪色,发生的是加成反应,但乙醛能使溴水褪色,发生的是氧化反应,褪色的原因不相同,故A错误;
B. 聚乙炔中含碳碳双键,可以使酸性高锰酸钾褪色,故B正确;
C. 煤油可由石油分馏获得,煤油燃烧放出大量的热,可用作燃料,煤油的密度比钠小且不与钠反应,可以隔绝空气和水,故煤油可用于保存少量金属钠,故C正确;
D. 乙酸可与饱和碳酸钠溶液反应生成乙酸钠、水和二氧化碳,而乙酸乙酯不反应,乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去,故D正确;
故选A。
6.D
【详解】A.铜加热后生成CuO,插入水中后不反应,故铜片质量增加,故A不选;
B.铜加热后生成CuO,插入乙醇中,生成乙醛和Cu,质量不变,故B不选;
C.铜加热后生成CuO,插入石灰水中后不反应,铜片质量增加,故C不选;
D.铜加热后生成CuO,插入盐酸中,CuO和盐酸反应生成CuCl2溶于水,故铜片质量减少,故D选;
答案选D。
7.B
【详解】A.三种物质均含羟基、醚键、羰基、碳碳双键,共4种官能团,故A错误;
B.含酚羟基,可发生氧化、取代反应,含碳碳双键可发生氧化、加成反应,故B正确;
C.甲基上最多有1个H原子与其它原子共面时,共面原子最多,则共面原子最多为33-2=31个,故C错误;
D.只有酚羟基与碳酸钠溶液反应,野黄芩素含4个酚羟基、汉黄芩素含2个酚羟基,汉黄芩素消耗的碳酸钠最少,故D错误;
故选:B。
8.C
【详解】A.蛋白质中除含有C、H、N、O四种元素外,还可能含有S、P等元素,选项A错误;
B.柴油是烃类物质,奶油、牛油是饱和高级脂肪酸甘油酯,属于酯类,它们所含的物质类别不相同,选项B错误;
C.对于羧酸而言,根据羧基位置异构可以得到两种丁酸;根据酯基位置异构和碳链异构可得:甲酸丙酯2种(丙基2种异构)、乙酸乙酯1种、丙酸甲酯1种,共6种,选项C正确;
D.聚合物( )可由单体CH3CH=CH2和CH2=CH2加聚制得,但该聚合物为混合物,选项D错误;
答案选C。
9.A
【详解】A.HCl与饱和亚硫酸钠反应,二氧化硫不与亚硫酸氢钠水溶液反应,可以进行除杂,A正确;
B.氯化铁与铜反应生成氯化亚铁与氯化铜,引进氯化亚铁杂质,B错误;
C.二者均与NaOH溶液反应,不能除杂,应选饱和碳酸钠溶液,C错误;
D.氯水与KI反应生成KCl、I2,用萃取分离出碘,但NaCl溶液中引入新杂质KCl,D错误;
答案选A。
10.D
【分析】结构中白色球形成2个共价键,小黑色球形成1个共价键,故白色球为O原子,小黑色球为H原子,大黑色球为C原子,该有机物结构简式为;
【详解】A.该有机物含有碳碳双键、羰基、醚键共3种官能团,A错误;
B.该有机物含有苯环、碳碳双键、羰基,可以发生加成反应,但不能发生水解反应,B错误;
C.该有机物含有碳碳双键,可以被酸性KMnO4溶液氧化,能使酸性KMnO4溶液褪色,C错误;
D.单键可以旋转,苯环平面与双键平面可以共平面,分子中所有原子可能共平面,D正确;
故选D。
11.D
【分析】探究碳酸和苯酚的酸性强弱,由图可知,①中发生盐酸与碳酸钙的反应生成二氧化碳,②中饱和碳酸氢钠溶液可除去HCl,③中发生苯酚钠与二氧化碳的反应生成苯酚,由强酸制取弱酸的原理可比较酸性。
【详解】A.由上述分析可知,②中试剂为饱和NaHCO3溶液,故A正确;
B.打开分液漏斗旋塞,①中有二氧化碳生成,观察到产生无色气泡,③中生成苯酚沉淀,观察到出现白色浑浊,故B正确;
C.由③中强酸制取弱酸的原理可知,苯酚的酸性弱于碳酸,是由于苯基影响了与其相连的羟基的活性,故C正确;
D.③中反应的化学方程式为C6H5ONa+CO2+H2O→C6H5OH+NaHCO3,故D错误;
故选D。
【点睛】本题考查酸性比较的实验方案的设计,把握实验装置的作用、反应原理为解答的关键。本题中要注意除去二氧化碳中的氯化氢气体,因为盐酸能够与苯酚钠反应生成苯酚,影响实验结果。
12.A
【详解】A.己烷在标准状况下是液态,22.4L己烷的物质的量大于1mol,正己烷碳骨架为C-C-C-C-C-C,则含有碳碳单键数目大于5NA,故A正确;
B.乙醇中碳元素为-2价,乙醛中碳元素为-1价,则有C2H5OH~CH3CHO~2e-,0.1mol乙醇反应转移0.2NA个电子,故B错误;
C.在1L 0.5mol/L的醋酸溶液中含有溶质醋酸n=cV=0.5mol,由于醋酸溶液中含有水分子,所以溶液中含有的分子的物质的量大于0.5mol,所含分子数目大于0.5NA,故C错误;
D.8.7g MnO2的物质的量,40mL 10 mol/L浓盐酸物质的量为n=cV=0.4mol,反应方程式为4HCl(浓)+MnO2MnCl2+Cl2↑+2H2O,MnO2只能与浓盐酸反应,和稀盐酸不反应,故当盐酸变稀后反应即停止,故生成的氯气分子个数小于0.1NA个,故D错误;
故选:A。
13. CH2=CH2+Br2→CH2BrCH2Br 碳碳双键、羧基 加成反应 酯化反应(取代反应) 同系物
【详解】(1) 的电子式为,与溴的四氯化碳溶液发生加成反应生成1,2-二溴乙烷,反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br;
(2)CH2=CH-COOH中所含官能团的名称为碳碳双键、羧基。
(3) CH2=CH2和水发生加成反应生成乙醇,是加成反应,乙醇和丙烯酸发生酯化反应生成丙烯酸乙酯,丙烯酸乙酯属于酯化反应(取代反应)。
(4)与都含有1个碳碳双键,分子组成相差1个“CH2”,互为同系物。
(5)丙烯酸乙酯一定条件下会发生聚合反应生成聚丙烯酸乙酯,反应的化学方程式为。
14.(1)
(2)
(3)
(4)
【详解】(1)乙酸与乙二醇的物质的量之比为发生酯化反应,形成1个酯基,化学方程式。
(2)乙二酸与乙醇的物质的量之比为发生酯化反应,形成2个酯基,化学方程式。
(3)①乙二酸与乙二醇酯化生成环酯,脱去2分子水,化学方程式。
②乙二酸与乙二醇生成高聚酯同时脱去水,化学方程式:,答案:。
(4)分子中既含羟基又含羧基,能自身酯化
①生成环酯化学方程式: ;
②生成高聚酯化学方程式。
15.(1) C6H12O 4—甲基戊醛
(2)HCHO+4Ag(NH3)2OH(NH4)2CO3+2H2O+4Ag↓+6NH3
(3) 溴原子 +2NaOH+2NaBr+H2O
(4) 18
【详解】(1)根据键线式可知,其分子式为:C6H12O,含官能团的最长的碳链为5,从右侧开始编写碳号,其名称是:4—甲基戊醛;
(2)福尔马林的成分是甲醛,可以和银氨溶液反应,生成碳酸铵和单质银,方程式为:HCHO+4Ag(NH3)2OH(NH4)2CO3+2H2O+4Ag↓+6NH3;
(3)根据该有机物的结构简式可知,其含有的官能团的名称为溴原子;该物质属于卤代烃,可以和氢氧化钠反应,且水解后生成的是酚类物质,可以继续和氢氧化钠反应,则方程式为:+2NaOH+2NaBr+H2O;
(4)苯环,碳碳双键,醛基分别确定一个平面,通过旋转碳碳单键,可以使三个平面重合,此时所有的原子都共面,一共是18个原子;该物质结构中含有碳碳双键,可以发生加聚反应,方程式为:n。
16. C D B 2
【分析】(1)与-OH相连C的邻位C上有H可发生消去反应;
(2)与-OH相连C上有2个H,可催化氧化生成醛;
(3) 与-OH相连C上不含H原子,不会被催化氧化;
(4) 与-OH相连C上含有1个H原子,催化氧化会生成酮;
据此分析判断。
【详解】(1) 与-OH相连C的邻位C上有H可发生消去反应,要生成两种单烯烃,说明该醇中与-OH相连C有两个邻位C,且均有H,具有不对称结构,满足条件的为C.,故答案为:C;
(2)可以发生催化氧化生成醛,说明分子中与-OH相连C上有2个H,满足条件的为D.CH3(CH2)5CH2OH,故答案为:D;
(3)不能发生催化氧化,说明连接羟基的C原子上不含H原子,满足条件的为B.,故答案为:B;
(4)能被催化氧化为酮,说明连接羟基的C原子上含有1个H原子,满足条件的为A. 、C.,2种,故答案为:2。
17.(1)C17H35COOH
(2)加成反应
(3)CH3CH2CH2Br + KOHCH3CH=CH2↑+ KBr + H2O
(4)苯酚分子中的羟基影响苯基上的氢原子,使邻、对位的氢原子更活泼,易被取代
【解析】(1)
硬脂酸为饱和十八羧酸,结构简式为C17H35COOH。
(2)
苯和乙烯发生加成反应生成乙苯。
(3)
1─溴丙烷与氢氧化钾醇溶液共热发生消去反应生成丙烯、溴化钾和水,故化学方程式为CH3CH2CH2Br + KOHCH3CH=CH2↑+ KBr + H2O。
(4)
苯和液溴在铁催化下发生取代反应生产溴苯,而苯酚和溴水发生取代反应生成2,4,6─三溴苯酚,是因为苯酚分子中的羟基影响苯基上的氢原子,使邻、对位的氢原子更活泼,易被取代。
18. +H2O +H3O
【解析】略
19. 2 4 4 4 9 6 12 40 18 5 12 17
【详解】(1)属于羧酸即C3H7COOH,- C3H7有两种结构,所以属于羧酸的种类数为2种;属于羧酸即C4H9COOH,- C4H9有4种结构,所以属于羧酸的种类数为4种;属于羧酸且为芳香族,结构可能为、、、共4种结构;
(2) 属于酯类的结构有:C2H5COOCH3、CH3COOC2H5、HCOOC3H7(2种),共4种结构;属于酯类的结构有:C3H7COOCH3(2种)、C2H5COOC2H5、CH3COOC3H7(2种)、HCOOC4H9(4种),共9种结构;属于酯类的结构有:、、、(邻、间、对3种),共6种结构;
(3) C4H8O2属于酯的结构有:HCOOCH2CH2CH3、HCOOCH(CH3)CH3、CH3COOCH2CH3、CH3CH2COOCH3共4种,水解后的酸有:HCOOH、CH3COOH和CH3CH2COOH,醇有:CH3OH、CH3CH2OH、CH3CH2CH2OH、HOCH(CH3)CH3,重新组合后生成的酯的种类数:3×4=12种;C5H10O2属于酯的结构有HCOOCH2CH2CH2CH3、HCOOCH2CH(CH3)2、HCOOCH(CH3)CH2CH3、HCOOC(CH3)3、CH3COOCH2CH2CH3、CH3COOCH(CH3)2、CH3CH2COOCH2CH3、CH3CH2CH2COOCH3、(CH3)2CHCOOCH3共9种,水解后的酸有5种,醇有8种,重新组合后生成的酯的种类数:5×8=40种;C8H8O2属于芳香族的酯的结构:苯环、剩余2个C,可以是甲酸苯甲醇酯、甲酸苯酚酯和甲基(有邻间对三种位置关系)、乙酸苯酚酯和苯甲酸甲酯,共6种,水解后的酸有3种,醇(或酚)有6种,重新组合后生成的酯的种类数:3×6=18种;
(4)属于醛,同时能与钠反应放出氢气,说明同时含有 CHO和 OH,C4H8O2:HO C3H6 CHO,类似于丙烷的二取代物,两个取代基不相同,共有5种;C5H10O2:HO C4H8 CHO,类似于丁烷的二取代物,两个取代基不相同,共有12种;C8H8O2属于芳香族:苯环上连接 CH2CHO和 OH,有邻间对3种,苯环上连接 CH2OH和 CHO,有邻间对3种,苯环上连接 CH3、 CHO和 OH,有10种,苯环上连接,有1种,共有17种。
20. 取代 加成 加成 氧化 不能
【详解】由分子结构可知,访物质分子中有碳碳双键、苯环、氯原子。碳碳双键可以发生加成反应、加聚反应和氧化反应;苯环上可以发生取代反应和加成反应;含氯原子可以发生卤代烃水解反应,但是由于没有H原子,所以不能发生消去反应。
(1)苯基部分可发生加成反应和取代反应。
(2)—CHCH2部分可发生加成反应和氧化反应。
(3)此有机物形成的高分子化合物的结构简式为 。
(4)卤代烃发生消去反应的机理是H消去,即与卤素原子直接相连的C原子()的邻位C原子()上有氢原子的能发生消去反应中。此有机物没有H,所以—C(CH2Cl)3部分不能发生消去反应。
21.(1) 2,2,3—三甲基戊烷
(2) 酯基 羧基
(3)
(4) CDF F CDG CH2=CH2+B2→BrCH2CH2Br +3HNO3+3H2O
(5)D
(6)2
【解析】(1)
由键线式可知,汽油中的异辛烷的分子式为,名称为2,2,3—三甲基戊烷,故答案为:;2,2,3—三甲基戊烷;
(2)
由阿司匹林的结构简式可知,官能团为酯基、羧基,故答案为:酯基;羧基;
(3)
乙炔一定条件下发生加聚反应生成聚乙炔,反应的化学方程式为,故答案为:;
(4)
①由球棍模型可知,乙烯、乙炔和苯分子中的所有原子在同一平面上,故选CDF;
②由球棍模型可知,苯和甲苯常温下为液态,则含碳量最高的液态烃是苯,故选F;
③由球棍模型可知,乙烯、乙炔和甲苯能与酸性高锰酸钾溶液发生氧化反应,使溶液褪色,故选CDG;
④乙烯分子中含有碳碳双键,能与溴水发生加成反应生成1,2—二溴乙烷,反应的化学方程式为CH2=CH2+B2→BrCH2CH2Br,故答案为:CH2=CH2+B2→BrCH2CH2Br;
⑤在浓硫酸作用下,甲苯与足量浓硝酸共热发生硝化反应生成2,4,6—三硝基甲苯和水,反应的化学方程式为+3HNO3+3H2O,故答案为:+3HNO3+3H2O;
(5)
A.乙烯与酸性高锰酸钾溶液发生氧化反应生成二氧化碳,则除去甲烷中混有少量的乙烯不能将混合气体通入酸性高锰酸钾溶液,否则会引入新杂质二氧化碳,故错误;
B.1—丁烯和1,3—丁二烯含有的碳碳双键数目不同,不是同类物质,不可能互为同系物,故错误;
C.甲烷是正四面体结构,二氯甲烷只有1种结构,不可能存在同分异构体,故错误;
D.甲烷、乙烯、乙炔的含碳量不同,燃烧时火焰的明亮程度及产生黑烟量的多少不同,则可采用点燃并观察火焰的明亮程度及产生黑烟量的多少鉴别甲烷、乙烯、乙炔,故正确;
故选D;
(6)
1mol环己二烯与等物质的量的溴水发生加成反应时,可发生1,2加成生成3,4—二溴—1—环己烯,也可发生1,4加成生成4,6—二溴—1—环己烯,所得加成产物共有2种,故答案为:2。
答案第1页,共2页
答案第1页,共2页
