2.4.2 酯和油脂 酰胺 课件 (共25张PPT)2023-2024学年高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 2.4.2 酯和油脂 酰胺 课件 (共25张PPT)2023-2024学年高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-18 00:00:00 | ||
图片预览








文档简介
(共25张PPT)
第4节 羧酸 氨基酸和蛋白质 课时2
1.认识酯的组成和结构特点、性质、转化关系及其在生产、生活中的重要应用;
2.知道酰胺的结构特点及其应用。
知识回顾
知识回顾
请写出羧酸生成酯、酰胺的化学方程式。
羧酸衍生物:羧酸分子中羧基上的羟基被其他原子或原子团取代得到的产物。
—C—
O
R
酰基
一、酯
低级酯是有香味的液体,存在于各种水果和花草中。
丁酸乙酯
CH3(CH2)2C—O—CH2CH3
O
果味粉
1.酯的组成结构及物理性质
分子由酰基和烃氧基相连构成的一种羧酸衍生物。
(1)概念:
—C—O—
O
(2)官能团:
酯基 —COO—或
饱和一元酯的通式:
CnH2nO2 (n ≥ 2)
酯的命名
根据生成酯的酸和醇的名称来命名,称为某酸某酯。
如CH3COOC2H5
称为乙酸乙酯
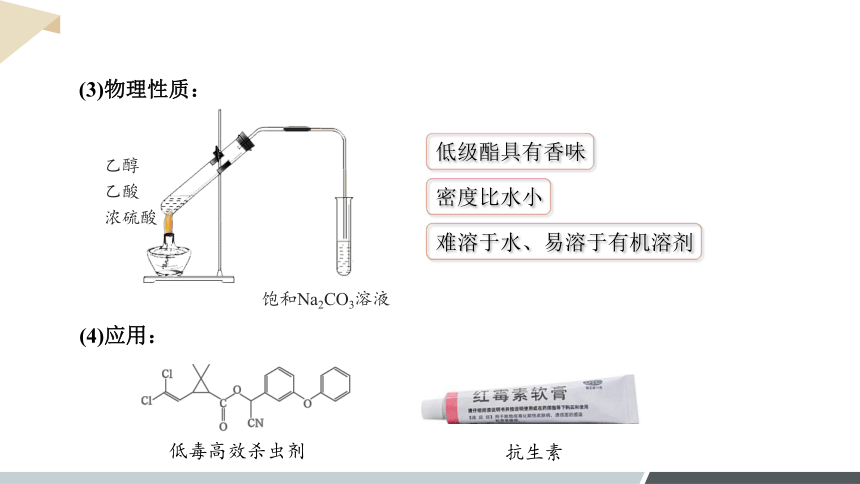
(3)物理性质:
密度比水小
难溶于水、易溶于有机溶剂
低级酯具有香味
(4)应用:
乙醇
乙酸
浓硫酸
饱和Na2CO3溶液
低毒高效杀虫剂
抗生素
2.酯的化学性质
酯+水 酸+醇
酸或碱
△
(1)水解反应
在酸或碱催化的条件下,酯可以发生水解反应生成相应的酸和醇。酯的水解反应是酯化反应的逆反应。
活动 · 探究
活动 · 探究
乙酸乙酯的水解
【实验目的】
【实验用品】
完成乙酸乙酯在酸性和碱性条件下的水解。
乙酸乙酯,稀硫酸,NaOH 溶液,蒸馏水; 试管,烧杯,酒精灯,三脚架,石棉网。
实验操作
(1)向三支试管中分别加入等体积(约2 mL)的稀硫酸、NaOH溶液、蒸馏水
(2)向上述三支试管中分别缓慢加入等体积(约1 mL)的乙酸乙酯
(3)将三支试管放在70 ℃水浴中加热几分钟,观察实验现象
实验操作 实验现象
蒸馏水中无明显现象;
稀硫酸中酯层变薄,速率慢;
NaOH 溶液中酯层基本消失,速率快。
【实验结论】
蒸馏水的试管中,乙酸乙酯未水解;稀硫酸的试管中乙酸乙酯部分水解;
NaOH溶液的试管中乙酸乙酯全部水解且水解程度比在酸性条件下的大。
NaOH溶液
蒸馏水
稀硫酸
在稀硫酸存在下水解:
CH3—C—O—C2H5 + H2O
CH3—C—OH+H—O—C2H5
碱性条件下水解:
CH3—C—OC2H5 + NaOH
CH3—C—ONa + HOC2H5
取代反应
O
O
△
稀硫酸
△
O
O
[思考]乙酸乙酯在酸性或碱性条件下的水解有什么不同?
酸性条件下,乙酸乙酯的水解反应为可逆反应;碱性条件下,由于生成了羧酸盐,水解反应不可逆。
思考与交流
Ⅰ.制备乙酸乙酯时,要提高酯的收率,可以采取哪些方法?
增加羧酸或醇的量;不断地从反应体系中移走生成的酯和水。
Ⅱ.乙酸乙酯的水解实验中,为什么要用稀硫酸?
若用浓硫酸不利于乙酸乙酯的水解,而是有利于乙酸和乙醇反应生成乙酸乙酯,若用盐酸或硝酸,它们在加热的条件下很容易挥发。
Ⅲ.乙酸乙酯的水解实验中,为什么用70~80 ℃ 的水浴加热?
乙酸乙酯的沸点为 77 ℃,为了便于控制温度以 防止乙酸乙酯的挥发。
油脂的主要成分是高级脂肪酸甘油酯
高级脂肪酸甘油酯
R1、R2、R3代表饱和烃基或不饱和烃基
天然油脂中R1、R2、R3一般不同
二、油脂
高级脂肪酸甘油酯
1.油脂的结构
甘油(丙三醇)
HO—CH2
HO—CH
HO—CH2
高级脂肪酸
①软脂酸:C15H31COOH
③油酸:C17H33COOH
②硬脂酸:C17H35COOH
饱和脂肪酸
不饱和脂肪酸
植物油
动物脂肪
油脂
液态
固态
2.油脂的分类
饱和脂肪酸甘油酯,熔点高
不饱和脂肪酸甘油酯,熔点低
油脂具有哪些化学性质呢?
3.油脂的化学性质
(1)水解反应——以硬脂酸甘油酯为例
硬脂酸
硬脂酸甘油酯
甘油
工业上利用这一原理
制取高级脂肪酸和甘油
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3H2O
稀硫酸
△
HO—CH2
HO—CH
HO—CH2
3C17H35COOH +
①酸性条件下水解
3C17H35COONa+
硬脂酸钠
②碱性条件下水解:
油脂在碱性溶液中的水解反应又称为皂化反应。
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3NaOH
△
HO—CH2
HO—CH
HO—CH2
肥皂的主要成分
(2)油脂的氢化——油脂的加成反应
①油脂氢化(油脂的硬化)
催化加氢
不饱和程度较高
熔点较低的液态油
半固态的脂肪
(硬化油)
由此制得的油脂叫做人造脂肪,通常又称为硬化油。硬化油不易被空气氧化变质,便于储存和运输,可作为制造肥皂、人造奶油的原料。
催化剂
△
C17H33COOCH2
C17H33COOCH
C17H33COOCH2
+ 3H2
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
硬脂酸甘油酯
油酸甘油酯
三、酰胺
含酰胺基的降压药缬沙坦的结构简式
1.酰胺的结构和物理性质
分子由酰基和氨基相连构成的羧酸衍生物
H
—C—N—
O
官能团:酰胺基
R—C—NH2
O
除甲酰胺( )是液体外,其他酰胺多为无色晶体。
低级的酰胺可溶于水,随着相对分子质量的增大,酰胺的溶解度逐渐减小。
H—C—NH2
O
2.酰胺的化学性质
酰胺在通常情况下较难水解,在强酸或强碱存在下长时间加热可水解成羧酸(或羧酸盐)和氨(或胺)。
胺
氨分子中的氢原子被烃基取代后的有机化合物称为胺,其通式一般写作 R—NH2,其官能团是氨基(-NH2)。
胺类具有碱性,能与盐酸、醋酸等反应生成水溶性较强的铵盐,铵盐遇强碱重新生成胺,故此性质常用于胺的分离。以苯胺为例,苯胺是合成染料和农药的重要中间体,它能与盐酸反应生成可溶于水的盐酸苯胺。
酰卤
酸酐
乙酰氯
乙酸酐
羧酸衍生物——酰卤、酸酐
酰氧基
卤原子
R—C—X
O
R—C—
O
O—C—R`
O
【练一练】
1.判断正误
(1)酯类在碱性条件下的水解程度大。 ( )
(2)油脂的相对分子质量较大,故属于有机高分子。( )
(3)汽油、甘油都属于油脂。( )
(4)油脂的水解反应叫做皂化反应。( )
(5)酯化反应与酯的水解反应均为取代反应。( )
(6)乙酸乙酯在碱性条件下也能发生水解反应,也称皂化反应。( )
2.已知分子式为C4H8O2的有机物既能发生银镜反应,又能发生水解反应,此有机物可能的结构有( )
A.5种 B.4种 C.3种 D.2种
D
3.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是( )
D
4.下列物质中既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ②(NH4)2S ③Al(OH)3 ④NH4Cl
⑤H2N—CH2—COOH ⑥CH3COOH
A.只有①②③ B.只有①②④⑤
C.只有⑤⑥ D.只有①②③⑤
D
结构
性质
结构
分类
性质
结构
性质
水解
羧酸(羧酸盐)+醇
高级脂肪酸甘油酯
油、脂肪
水解、不饱和油脂的氢化
水解
羧酸(或羧酸盐)+氨(或胺)
羧酸衍生物
酯
油脂
酰胺
酰卤
酸酐
第4节 羧酸 氨基酸和蛋白质 课时2
1.认识酯的组成和结构特点、性质、转化关系及其在生产、生活中的重要应用;
2.知道酰胺的结构特点及其应用。
知识回顾
知识回顾
请写出羧酸生成酯、酰胺的化学方程式。
羧酸衍生物:羧酸分子中羧基上的羟基被其他原子或原子团取代得到的产物。
—C—
O
R
酰基
一、酯
低级酯是有香味的液体,存在于各种水果和花草中。
丁酸乙酯
CH3(CH2)2C—O—CH2CH3
O
果味粉
1.酯的组成结构及物理性质
分子由酰基和烃氧基相连构成的一种羧酸衍生物。
(1)概念:
—C—O—
O
(2)官能团:
酯基 —COO—或
饱和一元酯的通式:
CnH2nO2 (n ≥ 2)
酯的命名
根据生成酯的酸和醇的名称来命名,称为某酸某酯。
如CH3COOC2H5
称为乙酸乙酯
(3)物理性质:
密度比水小
难溶于水、易溶于有机溶剂
低级酯具有香味
(4)应用:
乙醇
乙酸
浓硫酸
饱和Na2CO3溶液
低毒高效杀虫剂
抗生素
2.酯的化学性质
酯+水 酸+醇
酸或碱
△
(1)水解反应
在酸或碱催化的条件下,酯可以发生水解反应生成相应的酸和醇。酯的水解反应是酯化反应的逆反应。
活动 · 探究
活动 · 探究
乙酸乙酯的水解
【实验目的】
【实验用品】
完成乙酸乙酯在酸性和碱性条件下的水解。
乙酸乙酯,稀硫酸,NaOH 溶液,蒸馏水; 试管,烧杯,酒精灯,三脚架,石棉网。
实验操作
(1)向三支试管中分别加入等体积(约2 mL)的稀硫酸、NaOH溶液、蒸馏水
(2)向上述三支试管中分别缓慢加入等体积(约1 mL)的乙酸乙酯
(3)将三支试管放在70 ℃水浴中加热几分钟,观察实验现象
实验操作 实验现象
蒸馏水中无明显现象;
稀硫酸中酯层变薄,速率慢;
NaOH 溶液中酯层基本消失,速率快。
【实验结论】
蒸馏水的试管中,乙酸乙酯未水解;稀硫酸的试管中乙酸乙酯部分水解;
NaOH溶液的试管中乙酸乙酯全部水解且水解程度比在酸性条件下的大。
NaOH溶液
蒸馏水
稀硫酸
在稀硫酸存在下水解:
CH3—C—O—C2H5 + H2O
CH3—C—OH+H—O—C2H5
碱性条件下水解:
CH3—C—OC2H5 + NaOH
CH3—C—ONa + HOC2H5
取代反应
O
O
△
稀硫酸
△
O
O
[思考]乙酸乙酯在酸性或碱性条件下的水解有什么不同?
酸性条件下,乙酸乙酯的水解反应为可逆反应;碱性条件下,由于生成了羧酸盐,水解反应不可逆。
思考与交流
Ⅰ.制备乙酸乙酯时,要提高酯的收率,可以采取哪些方法?
增加羧酸或醇的量;不断地从反应体系中移走生成的酯和水。
Ⅱ.乙酸乙酯的水解实验中,为什么要用稀硫酸?
若用浓硫酸不利于乙酸乙酯的水解,而是有利于乙酸和乙醇反应生成乙酸乙酯,若用盐酸或硝酸,它们在加热的条件下很容易挥发。
Ⅲ.乙酸乙酯的水解实验中,为什么用70~80 ℃ 的水浴加热?
乙酸乙酯的沸点为 77 ℃,为了便于控制温度以 防止乙酸乙酯的挥发。
油脂的主要成分是高级脂肪酸甘油酯
高级脂肪酸甘油酯
R1、R2、R3代表饱和烃基或不饱和烃基
天然油脂中R1、R2、R3一般不同
二、油脂
高级脂肪酸甘油酯
1.油脂的结构
甘油(丙三醇)
HO—CH2
HO—CH
HO—CH2
高级脂肪酸
①软脂酸:C15H31COOH
③油酸:C17H33COOH
②硬脂酸:C17H35COOH
饱和脂肪酸
不饱和脂肪酸
植物油
动物脂肪
油脂
液态
固态
2.油脂的分类
饱和脂肪酸甘油酯,熔点高
不饱和脂肪酸甘油酯,熔点低
油脂具有哪些化学性质呢?
3.油脂的化学性质
(1)水解反应——以硬脂酸甘油酯为例
硬脂酸
硬脂酸甘油酯
甘油
工业上利用这一原理
制取高级脂肪酸和甘油
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3H2O
稀硫酸
△
HO—CH2
HO—CH
HO—CH2
3C17H35COOH +
①酸性条件下水解
3C17H35COONa+
硬脂酸钠
②碱性条件下水解:
油脂在碱性溶液中的水解反应又称为皂化反应。
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3NaOH
△
HO—CH2
HO—CH
HO—CH2
肥皂的主要成分
(2)油脂的氢化——油脂的加成反应
①油脂氢化(油脂的硬化)
催化加氢
不饱和程度较高
熔点较低的液态油
半固态的脂肪
(硬化油)
由此制得的油脂叫做人造脂肪,通常又称为硬化油。硬化油不易被空气氧化变质,便于储存和运输,可作为制造肥皂、人造奶油的原料。
催化剂
△
C17H33COOCH2
C17H33COOCH
C17H33COOCH2
+ 3H2
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
硬脂酸甘油酯
油酸甘油酯
三、酰胺
含酰胺基的降压药缬沙坦的结构简式
1.酰胺的结构和物理性质
分子由酰基和氨基相连构成的羧酸衍生物
H
—C—N—
O
官能团:酰胺基
R—C—NH2
O
除甲酰胺( )是液体外,其他酰胺多为无色晶体。
低级的酰胺可溶于水,随着相对分子质量的增大,酰胺的溶解度逐渐减小。
H—C—NH2
O
2.酰胺的化学性质
酰胺在通常情况下较难水解,在强酸或强碱存在下长时间加热可水解成羧酸(或羧酸盐)和氨(或胺)。
胺
氨分子中的氢原子被烃基取代后的有机化合物称为胺,其通式一般写作 R—NH2,其官能团是氨基(-NH2)。
胺类具有碱性,能与盐酸、醋酸等反应生成水溶性较强的铵盐,铵盐遇强碱重新生成胺,故此性质常用于胺的分离。以苯胺为例,苯胺是合成染料和农药的重要中间体,它能与盐酸反应生成可溶于水的盐酸苯胺。
酰卤
酸酐
乙酰氯
乙酸酐
羧酸衍生物——酰卤、酸酐
酰氧基
卤原子
R—C—X
O
R—C—
O
O—C—R`
O
【练一练】
1.判断正误
(1)酯类在碱性条件下的水解程度大。 ( )
(2)油脂的相对分子质量较大,故属于有机高分子。( )
(3)汽油、甘油都属于油脂。( )
(4)油脂的水解反应叫做皂化反应。( )
(5)酯化反应与酯的水解反应均为取代反应。( )
(6)乙酸乙酯在碱性条件下也能发生水解反应,也称皂化反应。( )
2.已知分子式为C4H8O2的有机物既能发生银镜反应,又能发生水解反应,此有机物可能的结构有( )
A.5种 B.4种 C.3种 D.2种
D
3.在生成和纯化乙酸乙酯的实验过程中,下列操作未涉及的是( )
D
4.下列物质中既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ②(NH4)2S ③Al(OH)3 ④NH4Cl
⑤H2N—CH2—COOH ⑥CH3COOH
A.只有①②③ B.只有①②④⑤
C.只有⑤⑥ D.只有①②③⑤
D
结构
性质
结构
分类
性质
结构
性质
水解
羧酸(羧酸盐)+醇
高级脂肪酸甘油酯
油、脂肪
水解、不饱和油脂的氢化
水解
羧酸(或羧酸盐)+氨(或胺)
羧酸衍生物
酯
油脂
酰胺
酰卤
酸酐
