2.4.3 氨基酸和蛋白质 课件 (共21张PPT)2023-2024学年高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 2.4.3 氨基酸和蛋白质 课件 (共21张PPT)2023-2024学年高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-18 00:00:00 | ||
图片预览




文档简介
(共21张PPT)
第4节 羧酸 氨基酸和蛋白质 课时3
1.了解氨基酸、蛋白质的结构特点和主要性质,了解酶的催化作用的特点;
2.了解我国科学家在生命科学研究领域中的贡献,体会化学科学在生命科学发展中的重要作用。
联想 · 质疑
联想 · 质疑
蛋白质是生命的物质基础,是生命活动的主要承担者。蛋白质在机体中发挥着多种生 理功能,能够供给机体营养、提供保护机能、输送氧气、防御病菌侵袭、控制代谢过程等。
酶
抗体
激素
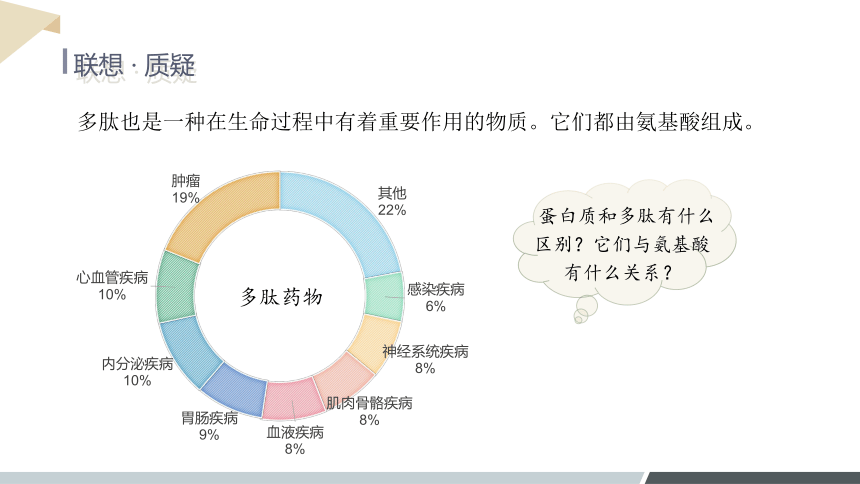
多肽也是一种在生命过程中有着重要作用的物质。它们都由氨基酸组成。
联想 · 质疑
联想 · 质疑
多肽药物
蛋白质和多肽有什么区别?它们与氨基酸有什么关系?
一、氨基酸和蛋白质
1.氨基酸
(1)分子结构
①定义:羧酸分子烃基上的氢原子被氨基取代得到的化合物。
组成蛋白质的氨基酸主要是α-氨基酸
R—CH—COOH
NH2
α-氨基酸
②α-氨基酸:
氨基酸分子中含有______和_______,属于_________。
氨基
羧基
取代羧酸
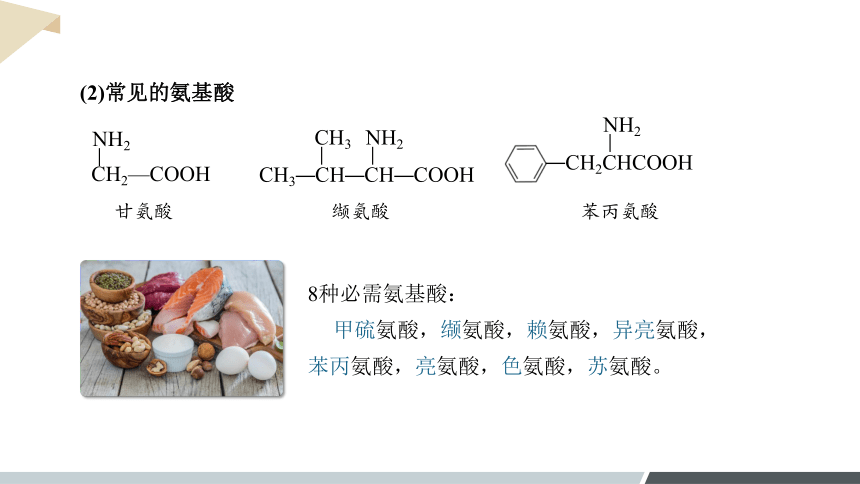
8种必需氨基酸:
甲硫氨酸,缬氨酸,赖氨酸,异亮氨酸,苯丙氨酸,亮氨酸,色氨酸,苏氨酸。
(2)常见的氨基酸
CH2—COOH
甘氨酸
苯丙氨酸
CH2CHCOOH
NH2
—
缬氨酸
CH3—CH—CH—COOH
NH2
CH3
NH2
观察 · 思考
观察 · 思考
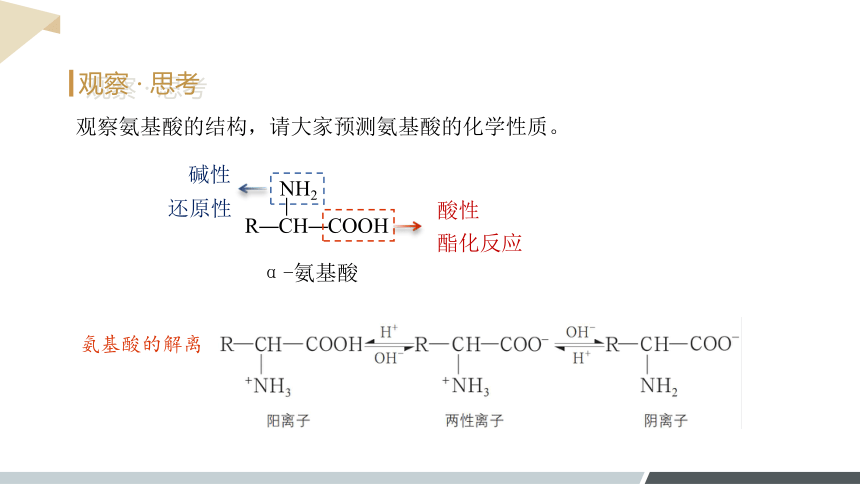
观察氨基酸的结构,请大家预测氨基酸的化学性质。
R—CH—COOH
NH2
α-氨基酸
酸性
酯化反应
碱性
还原性
氨基酸的解离
(3)化学性质
①两性
氨基酸分子中含有酸性基团—COOH和碱性基团—NH2,因此氨基酸是两性化合物,能与酸、碱反应生成盐。
a.与盐酸的反应:
b.与氢氧化钠反应:
R—CH—COOH+NaOH
NH2
R—CH—COONa+H2O
NH2
R—CH—COOH+HCl
NH2
R—CH—COOH
NH3Cl
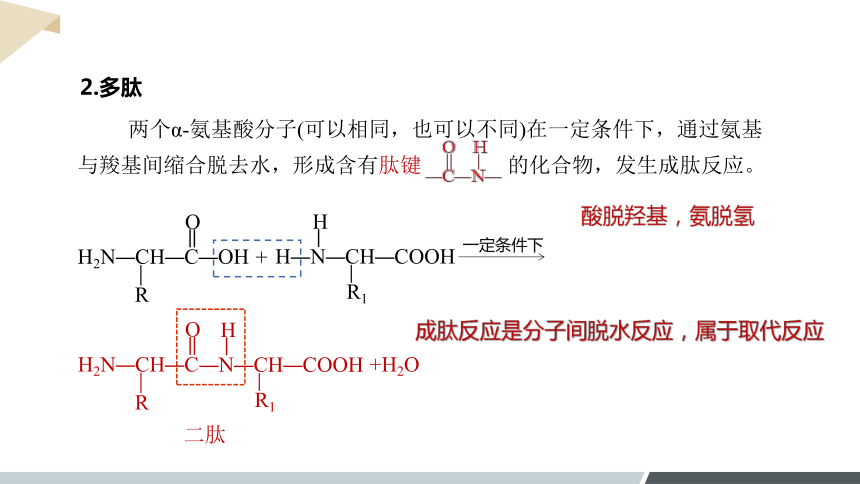
2.多肽
两个α-氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基与羧基间缩合脱去水,形成含有肽键 的化合物,发生成肽反应。
成肽反应是分子间脱水反应,属于取代反应
一定条件下
H2N—CH—C—OH
R
O
H—N—CH—COOH
R1
H
+
二肽
O
H2N—CH—C
R
—N—CH—COOH
R1
H
+H2O
酸脱羟基,氨脱氢
(1)多肽:由两个氨基酸分子脱水缩合形成的是二肽,由三个氨基酸分子脱水缩合形成的是三肽,以此类推。二肽及以上均可称为多肽。
[举一反三]请写出甘氨酸分子和丙氨酸分子结合生成二肽的化学方程式。
丙氨酸
NH2CH2COOH
甘氨酸
NH2CHCOOH
CH3
+
-H2O
NH2—CH2—C—N—CH—COOH
O
H
CH3
NH2CH2COOH
甘氨酸
丙氨酸
NH2CHCOOH
CH3
+
-H2O
NH2—CH—C—N—CH2—COOH
O
H
CH3
多肽类型:氨基酸分子种类、数目、排列顺序
缩合
两分子氨基酸
二肽
+氨基酸
缩合
三肽
+氨基酸
缩合
多肽
蛋白质
肽链
链状
盘曲、折叠
相互结合
Mr>10000
3.蛋白质
(1)组成元素:C、H、O、N、S 等
(2)结构:
由α 氨基酸分子按一定的顺序以肽键连接起来的生物大分子称为蛋白质,其一定含有的官能团是肽键。
α-氨基酸是构成蛋白质的结构单元,其分子的排列顺序决定了蛋白质的功能。
蛋白质的四级结构
血红蛋白分子
缬氨酸
谷氨酸
镰状细胞贫血
①α-氨基酸分子脱水缩合形成的多肽是按一定顺序排列的链状结构,这种顺序就是蛋白质的基本结构,也称蛋白质的一级结构。
蛋白质的四级结构
②肽键中的氧原子与氢原子之间存在氢键,会使肽链盘绕或折叠成特定的空间结构,形成蛋白质的二级结构,主要有α-螺旋和β-折叠两种形式。
③肽链在二级结构基础上还会进一步盘曲折叠,形成更复杂的三级结构
④由几条相同的多肽链组成的空间结构状态称为蛋白质的均一四级结构,由几条不同的多肽链组成的空间结构状态称为蛋白质的非均一四级结构。它们是蛋白质分子具有一定生物学功能的高级结构。
氨基酸种类、数目、排列顺序
空间结构多样
种类繁多
功能多样
知识回顾
知识回顾
回顾必修内容,思考总结蛋白质的主要性质由哪些?
①溶解性:有些蛋白质能溶解在水里形成溶液,具有胶体的性质。
②水解:天然蛋白质水解的最终产物为α-氨基酸。
③具有两性——因为它由氨基酸组成。
④盐析——可逆。
⑤变性——不可逆。
⑥颜色反应——含有苯环的蛋白质遇浓硝酸变黄。
⑦灼烧蛋白质会产生烧焦羽毛的气味。
4.酶
酶是一种高效的生物催化剂,生物体新陈代谢过程中的许多化学反应都是在酶的催化作用下进行的。大多数酶属于蛋白质。
①需要比较温和的条件(体温约为37℃,血液pH约为7)
②具有高度的专一性
③效率非常高
酶催化的主要特点:
酶-底物复合物
底物
酶
我国科学家在生命科学研究领域中的贡献
蛋白质作为生命存在的形式,一直是生命科学研究的焦点,我国科学家在此研究领域中作出了巨大贡献。
1965 年,我国科学家汪猷、邢其毅、钮经义等
首次由氨基酸合成了结晶牛胰岛素,这是第一个全
人工合成的、与天然产物性质完全相同的、有生物活性的蛋白质。
20 世纪 90 年代,我国科学家参加了人类基因组计划。
2002 年,由我国科学家领导的人类肝脏蛋白质组计划正式启动。我国科学家已站在了生命科学研究领域的前沿。
【练一练】
1.判断下列说法是否正确,正确的画“√”,错误的画“×”。
(1)氨基酸既能与强酸反应,也能与强碱反应。( )
(2)天然蛋白质水解的最终产物都是α-氨基酸。( )
(3)蛋白质遇浓硝酸都会显黄色。( )
(4)医疗器械的高温消毒的实质是蛋白质的变性。( )
(5)温度越高酶的催化作用越好。( )
(6)羊毛完全燃烧只生成CO2和H2O。( )
2.有一分子式为C8H14N2O5的二肽,经水解得丙氨酸 和另一种氨基酸X,则X的化学式可能是( )
A.C3H7NO3 B.C5H9NO4
C.C5H11NO5 D.C5H7NO4
B
3.青霉素是一种良效广谱抗生素,经酸性水解后得到青霉素氨基酸分子的结构简式如图,下列关于该物质的叙述不正确的是 ( )
A.属于α-氨基酸
B.能发生加聚反应生成多肽
C.核磁共振氢谱上共有5个峰
D.青霉素过敏严重者会导致死亡,用药前一定要进行皮肤敏感试验
B
蛋白质
氨基酸
蛋白质
酶
官能团
结构
性质
水解、盐析、两性、变性、颜色反应、灼烧有类似烧焦羽毛的气味
高效生物催化剂
高效性、专一性、条件温和
羧基
氨基
能与碱反应
能与酸反应
成肽反应
多肽
由氨基酸分子脱水缩合形成的二肽及以上物质
结构单元
α-氨基酸
一级结构、二级结构、三级结构、四级结构
第4节 羧酸 氨基酸和蛋白质 课时3
1.了解氨基酸、蛋白质的结构特点和主要性质,了解酶的催化作用的特点;
2.了解我国科学家在生命科学研究领域中的贡献,体会化学科学在生命科学发展中的重要作用。
联想 · 质疑
联想 · 质疑
蛋白质是生命的物质基础,是生命活动的主要承担者。蛋白质在机体中发挥着多种生 理功能,能够供给机体营养、提供保护机能、输送氧气、防御病菌侵袭、控制代谢过程等。
酶
抗体
激素
多肽也是一种在生命过程中有着重要作用的物质。它们都由氨基酸组成。
联想 · 质疑
联想 · 质疑
多肽药物
蛋白质和多肽有什么区别?它们与氨基酸有什么关系?
一、氨基酸和蛋白质
1.氨基酸
(1)分子结构
①定义:羧酸分子烃基上的氢原子被氨基取代得到的化合物。
组成蛋白质的氨基酸主要是α-氨基酸
R—CH—COOH
NH2
α-氨基酸
②α-氨基酸:
氨基酸分子中含有______和_______,属于_________。
氨基
羧基
取代羧酸
8种必需氨基酸:
甲硫氨酸,缬氨酸,赖氨酸,异亮氨酸,苯丙氨酸,亮氨酸,色氨酸,苏氨酸。
(2)常见的氨基酸
CH2—COOH
甘氨酸
苯丙氨酸
CH2CHCOOH
NH2
—
缬氨酸
CH3—CH—CH—COOH
NH2
CH3
NH2
观察 · 思考
观察 · 思考
观察氨基酸的结构,请大家预测氨基酸的化学性质。
R—CH—COOH
NH2
α-氨基酸
酸性
酯化反应
碱性
还原性
氨基酸的解离
(3)化学性质
①两性
氨基酸分子中含有酸性基团—COOH和碱性基团—NH2,因此氨基酸是两性化合物,能与酸、碱反应生成盐。
a.与盐酸的反应:
b.与氢氧化钠反应:
R—CH—COOH+NaOH
NH2
R—CH—COONa+H2O
NH2
R—CH—COOH+HCl
NH2
R—CH—COOH
NH3Cl
2.多肽
两个α-氨基酸分子(可以相同,也可以不同)在一定条件下,通过氨基与羧基间缩合脱去水,形成含有肽键 的化合物,发生成肽反应。
成肽反应是分子间脱水反应,属于取代反应
一定条件下
H2N—CH—C—OH
R
O
H—N—CH—COOH
R1
H
+
二肽
O
H2N—CH—C
R
—N—CH—COOH
R1
H
+H2O
酸脱羟基,氨脱氢
(1)多肽:由两个氨基酸分子脱水缩合形成的是二肽,由三个氨基酸分子脱水缩合形成的是三肽,以此类推。二肽及以上均可称为多肽。
[举一反三]请写出甘氨酸分子和丙氨酸分子结合生成二肽的化学方程式。
丙氨酸
NH2CH2COOH
甘氨酸
NH2CHCOOH
CH3
+
-H2O
NH2—CH2—C—N—CH—COOH
O
H
CH3
NH2CH2COOH
甘氨酸
丙氨酸
NH2CHCOOH
CH3
+
-H2O
NH2—CH—C—N—CH2—COOH
O
H
CH3
多肽类型:氨基酸分子种类、数目、排列顺序
缩合
两分子氨基酸
二肽
+氨基酸
缩合
三肽
+氨基酸
缩合
多肽
蛋白质
肽链
链状
盘曲、折叠
相互结合
Mr>10000
3.蛋白质
(1)组成元素:C、H、O、N、S 等
(2)结构:
由α 氨基酸分子按一定的顺序以肽键连接起来的生物大分子称为蛋白质,其一定含有的官能团是肽键。
α-氨基酸是构成蛋白质的结构单元,其分子的排列顺序决定了蛋白质的功能。
蛋白质的四级结构
血红蛋白分子
缬氨酸
谷氨酸
镰状细胞贫血
①α-氨基酸分子脱水缩合形成的多肽是按一定顺序排列的链状结构,这种顺序就是蛋白质的基本结构,也称蛋白质的一级结构。
蛋白质的四级结构
②肽键中的氧原子与氢原子之间存在氢键,会使肽链盘绕或折叠成特定的空间结构,形成蛋白质的二级结构,主要有α-螺旋和β-折叠两种形式。
③肽链在二级结构基础上还会进一步盘曲折叠,形成更复杂的三级结构
④由几条相同的多肽链组成的空间结构状态称为蛋白质的均一四级结构,由几条不同的多肽链组成的空间结构状态称为蛋白质的非均一四级结构。它们是蛋白质分子具有一定生物学功能的高级结构。
氨基酸种类、数目、排列顺序
空间结构多样
种类繁多
功能多样
知识回顾
知识回顾
回顾必修内容,思考总结蛋白质的主要性质由哪些?
①溶解性:有些蛋白质能溶解在水里形成溶液,具有胶体的性质。
②水解:天然蛋白质水解的最终产物为α-氨基酸。
③具有两性——因为它由氨基酸组成。
④盐析——可逆。
⑤变性——不可逆。
⑥颜色反应——含有苯环的蛋白质遇浓硝酸变黄。
⑦灼烧蛋白质会产生烧焦羽毛的气味。
4.酶
酶是一种高效的生物催化剂,生物体新陈代谢过程中的许多化学反应都是在酶的催化作用下进行的。大多数酶属于蛋白质。
①需要比较温和的条件(体温约为37℃,血液pH约为7)
②具有高度的专一性
③效率非常高
酶催化的主要特点:
酶-底物复合物
底物
酶
我国科学家在生命科学研究领域中的贡献
蛋白质作为生命存在的形式,一直是生命科学研究的焦点,我国科学家在此研究领域中作出了巨大贡献。
1965 年,我国科学家汪猷、邢其毅、钮经义等
首次由氨基酸合成了结晶牛胰岛素,这是第一个全
人工合成的、与天然产物性质完全相同的、有生物活性的蛋白质。
20 世纪 90 年代,我国科学家参加了人类基因组计划。
2002 年,由我国科学家领导的人类肝脏蛋白质组计划正式启动。我国科学家已站在了生命科学研究领域的前沿。
【练一练】
1.判断下列说法是否正确,正确的画“√”,错误的画“×”。
(1)氨基酸既能与强酸反应,也能与强碱反应。( )
(2)天然蛋白质水解的最终产物都是α-氨基酸。( )
(3)蛋白质遇浓硝酸都会显黄色。( )
(4)医疗器械的高温消毒的实质是蛋白质的变性。( )
(5)温度越高酶的催化作用越好。( )
(6)羊毛完全燃烧只生成CO2和H2O。( )
2.有一分子式为C8H14N2O5的二肽,经水解得丙氨酸 和另一种氨基酸X,则X的化学式可能是( )
A.C3H7NO3 B.C5H9NO4
C.C5H11NO5 D.C5H7NO4
B
3.青霉素是一种良效广谱抗生素,经酸性水解后得到青霉素氨基酸分子的结构简式如图,下列关于该物质的叙述不正确的是 ( )
A.属于α-氨基酸
B.能发生加聚反应生成多肽
C.核磁共振氢谱上共有5个峰
D.青霉素过敏严重者会导致死亡,用药前一定要进行皮肤敏感试验
B
蛋白质
氨基酸
蛋白质
酶
官能团
结构
性质
水解、盐析、两性、变性、颜色反应、灼烧有类似烧焦羽毛的气味
高效生物催化剂
高效性、专一性、条件温和
羧基
氨基
能与碱反应
能与酸反应
成肽反应
多肽
由氨基酸分子脱水缩合形成的二肽及以上物质
结构单元
α-氨基酸
一级结构、二级结构、三级结构、四级结构
