第2章 章末复习 课件 (共53页)2023-2024学年高二化学鲁科版(2019)选择性必修3
文档属性
| 名称 | 第2章 章末复习 课件 (共53页)2023-2024学年高二化学鲁科版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-18 00:00:00 | ||
图片预览





文档简介
(共53张PPT)
章末复习
1.能写出烃的衍生物的类别通式、官能团、简单代表物的结构简式及名称,能列举各类烃的衍生物的典型代表物的主要物理性质;
2.能描述说明、分析解释各类烃的衍生物的典型代表物的重要反应,能书写相应反应式;
3.能列举典型糖类物质,描述葡萄糖、淀粉、纤维素的化学性质;
4.能辨识蛋白质结构中的肽键,认识蛋白质的结构特点,能判断氨基酸的缩合产物,多肽的水解产物;
5.能辨识核糖核酸、脱氧核糖核酸中的磷脂键,能基于氢键分析碱基的配对原理。
知识点一:有机化学反应类型
1. 加成反应
有机化合物分子中不饱和键两端的两个原子与其他原子或原子团结合,生成新的有机化合物的反应。
(1)定义:
(2)加成反应规律:
不饱和键打开,结合原子或原子团形成新的化学键,“有上无下”。
生成物只有一种,原子利用率100%。
(3)不对称烯烃的加成反应:
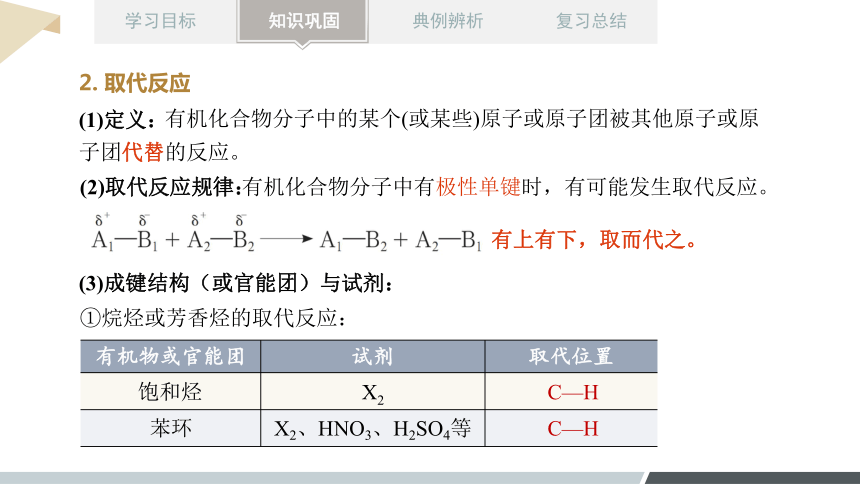
2. 取代反应
有机化合物分子中的某个(或某些)原子或原子团被其他原子或原子团代替的反应。
(1)定义:
(2)取代反应规律:
有机化合物分子中有极性单键时,有可能发生取代反应。
有上有下,取而代之。
(3)成键结构(或官能团)与试剂:
有机物或官能团 试剂 取代位置
X2、HNO3、H2SO4等
C—H
饱和烃
X2
C—H
苯环
①烷烃或芳香烃的取代反应:
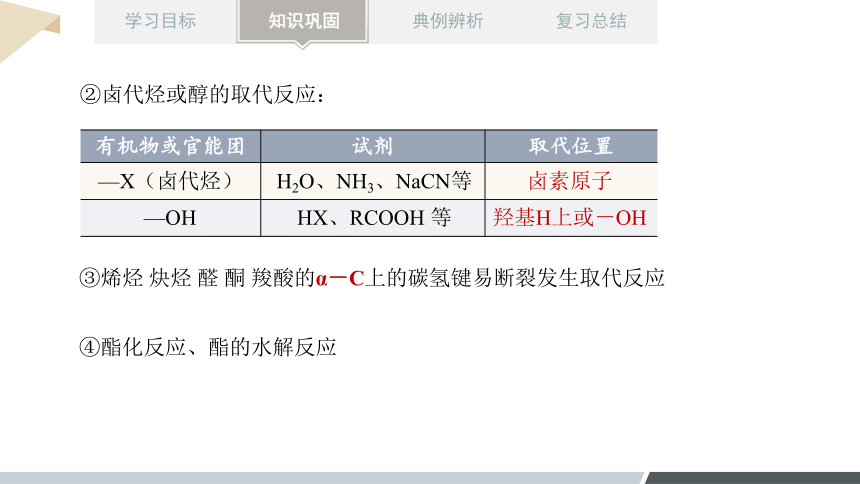
有机物或官能团 试剂 取代位置
H2O、NH3、NaCN等
HX、RCOOH 等
卤素原子
羟基H上或-OH
—X(卤代烃)
—OH
②卤代烃或醇的取代反应:
③烯烃 炔烃 醛 酮 羧酸的α-C上的碳氢键易断裂发生取代反应
④酯化反应、酯的水解反应
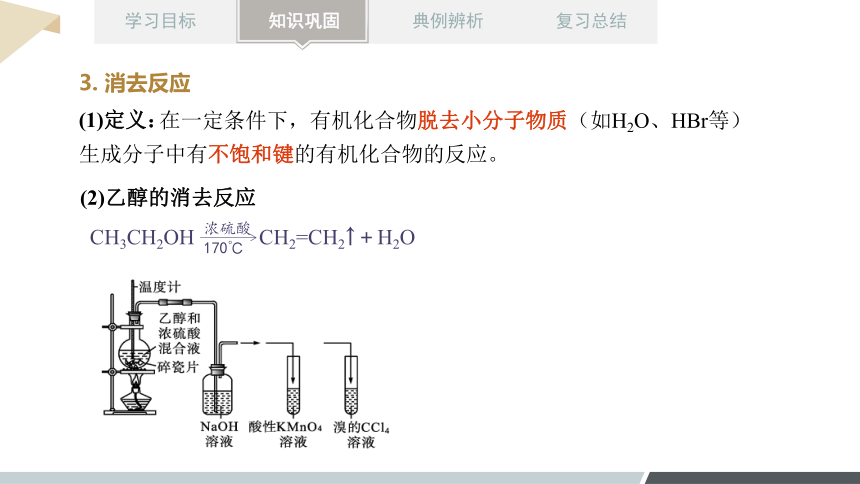
3. 消去反应
在一定条件下,有机化合物脱去小分子物质(如H2O、HBr等)生成分子中有不饱和键的有机化合物的反应。
(1)定义:
(2)乙醇的消去反应
CH3CH2OH CH2=CH2↑+H2O
浓硫酸
170℃
4. 氧化反应、还原反应
氧化反应:
还原反应:
有机化合物分子中增加氧原子或减少氢原子的反应。
有机化合物分子中增加氢原子或减少氧原子的反应。
常见的氧化剂
氧气、酸性KMnO4溶液、臭氧、银氨溶液和新制氢氧化铜悬浊液等。
常见的还原剂
氢气、氢化铝锂(LiAlH4)和硼氢化钠(NaBH4)等。
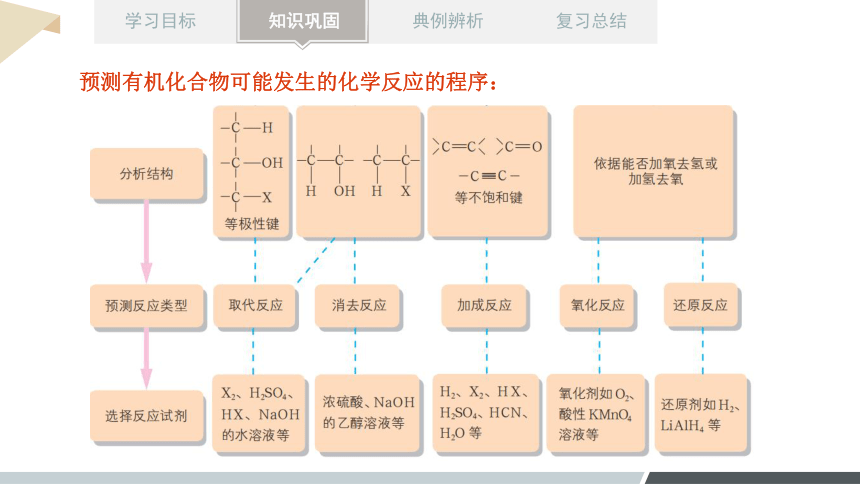
预测有机化合物可能发生的化学反应的程序:
知识点二:有机化学反应类型的应用
1. 卤代烃的性质
(1)定义:
烃分子中的一个或多个氢原子被卤素原子取代后生成的化合物称为卤代烃。官能团是-X(Cl、Br、I、F)。
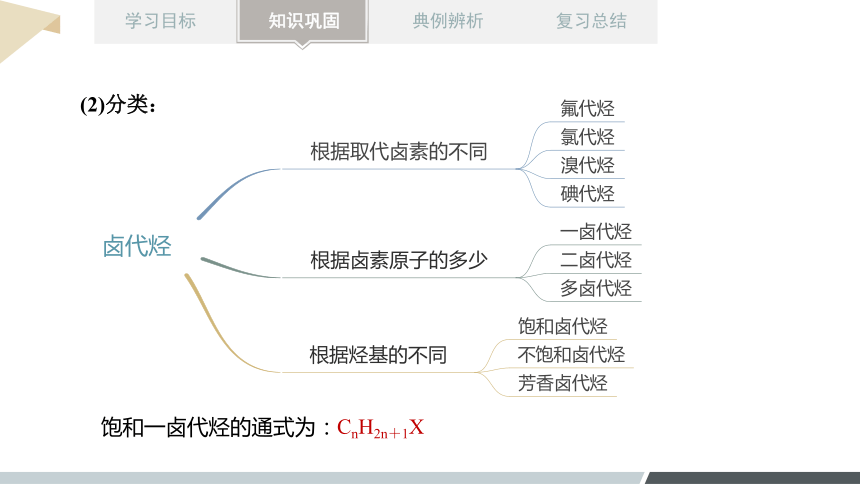
饱和一卤代烃的通式为:
CnH2n+1X
卤代烃
根据取代卤素的不同
氟代烃
氯代烃
溴代烃
碘代烃
根据卤素原子的多少
一卤代烃
二卤代烃
多卤代烃
根据烃基的不同
饱和卤代烃
不饱和卤代烃
芳香卤代烃
(2)分类:
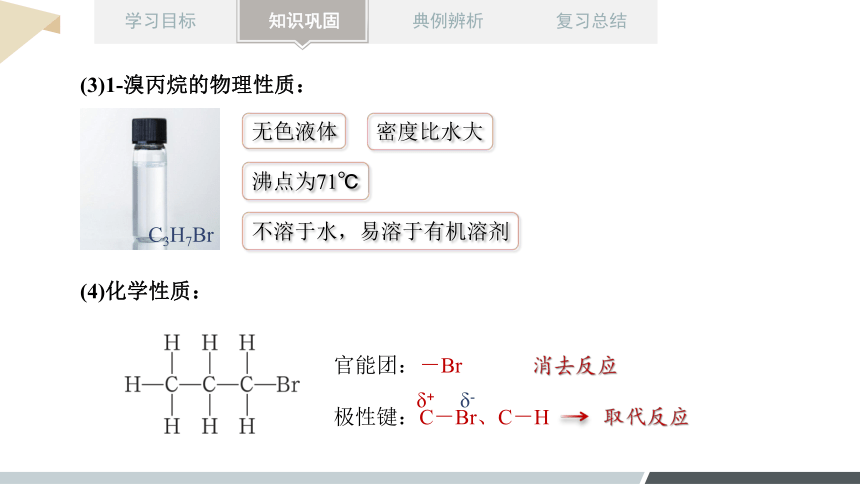
(3)1-溴丙烷的物理性质:
无色液体
沸点为71℃
密度比水大
不溶于水,易溶于有机溶剂
C3H7Br
(4)化学性质:
官能团:-Br
极性键:C-Br、C-H
取代反应
δ+
δ-
消去反应
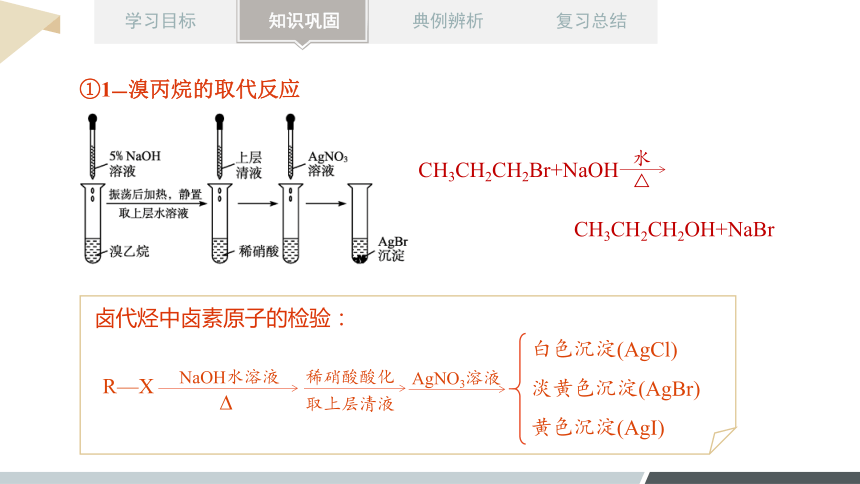
①1―溴丙烷的取代反应
CH3CH2CH2Br+NaOH
水
△
稀硝酸酸化
白色沉淀(AgCl)
淡黄色沉淀(AgBr)
黄色沉淀(AgI)
NaOH水溶液
R—X
AgNO3溶液
卤代烃中卤素原子的检验:
取上层清液
CH3CH2CH2OH+NaBr
②1―溴丙烷的消去反应
△
NaOH的水溶液
醇
NaOH的乙醇溶液
△
烯烃/炔烃
注意:a.没有β-C原子的卤代烃不能发生消去反应。
b.有β-C原子,但β-C原子上没有氢原子的卤代烃也不能发生消去反应。
2. 卤代烃的制备
知识点三:醇和酚
1.醇
(1)定义:
脂肪烃分子中的氢原子或芳香烃侧链上的氢原子被羟基取代后的有机化合物。
(2)分类:
CnH2n+1OH
醇
根据醇分子中所含羟基的数目
一元醇
二元醇
多元醇
按羟基所连烃基种类分类
脂肪醇
脂环醇
饱和醇
不饱和醇
芳香醇
(3)物理性质:
①沸点
a.饱和一元醇的沸点比与其相对分子质量接近的烷烃或烯烃的沸点要高。
c.碳原子数相同时,羟基个数越多,沸点越高。
b.饱和一元醇,随分子中碳原子数的增加沸点逐渐升高。
②溶解度:
含羟基较多的醇极易溶于水。
常温常压,饱和一元醇在水中的溶解性
醇分子中碳原子数 1~3 4~11 > 11
溶解性 能与水以任意比例互溶 油状液体,仅可部分溶于水 固体,
难溶于水
(4)化学性质:
①取代反应
反应试剂:
浓的氢卤酸(HCl、HBr、HI)
C2H5OH+HBr C2H5Br+H2O
乙醇 溴乙烷
反应条件:
酸做催化剂及加热
C2H5—OH+H—O—C2H5 C2H5—O—C2H5+H2O
乙醚
浓硫酸
140℃
浓硫酸
CH3
C
OH + H18O—C2H5
O
CH3
C
18O—C2H5 + H2O
O
“酸脱羟基醇脱氢”
②消去反应
反应条件:
浓硫酸、加热
CH3—CH2—CH2OH
CH3—CH CH2
↑ + H2O
浓硫酸
170℃
③与活泼金属的反应
2C2H5OH+2Na→2C2H5ONa+H2↑
④氧化反应
-OH所在的碳原子上要
有氢原子才可以被氧化
醇的催化氧化规律
氢
原
子
数
生成醛(或羧酸)
生成酮
不能被催化氧化
2~3个H
1个H
没有H
如:
R2
R1
R3
C
OH
O
R1
R2
C
H
H
Cu,O2
△
O
R1
R2
C
如:
如:
KMnO4(H+)或
K2Cr2O7(H+)
R
COOH
O
R
H
C
H
H
O
R
H
C
H
H
Cu,O2
△
CHO或
R
2.酚
(1)定义:
芳香烃分子中苯环上的氢原子被羟基取代后的有机化合物。
(2)化学性质:
①酸性——俗称石炭酸
苯酚钠
+H2O
+NaOH
OH
ONa
酸性强弱:
H2CO3 > C2H5OH > HCO3-
苯环对羟基的影响使得酚羟基的氢原子较为活泼
②取代反应
2,4,6-三溴苯酚(白色沉淀)
+3Br2
+3HBr
OH
OH
Br
Br
Br
酚羟基对苯环影响,使苯环上羟基邻、对位的氢原子的活性增强,易被取代
③苯酚与甲醛的缩聚反应
酚醛树脂
H+
+nHCHO
OH
n
+ (n-1)H2O
OH
CH2
n
OH
H
④苯酚与Fe3+显色反应
现象:苯酚遇到氯化铁溶液变紫色
用途:检验苯酚或Fe3+ 的存在
⑤苯酚也能像苯一样发生硝化、磺化、加成等反应。
+3HNO3
+3H2O
OH
OH
NO2
O2N
NO2
浓硫酸
+3H2
OH
Ni
OH
环己醇
知识点四:醛和酮 糖类和核酸
1.醛和酮
(1)结构:
—C—
O
羰基
醛
酮
羰基碳原子分别与氢原子和烃基(或氢原子)相连。
羰基碳原子相连的两个基团均为烃基,烃基可以相同也可以不同。
官能团:醛基
官能团:酮羰基
—C—H
O
(R`)—C—(R`)
O
—CHO
(2)醛、酮的化学性质:
①羰基的加成反应
CH3—C—H
O
δ+
δ-
+ H—CN
δ+
δ-
催化剂
CH3—C—CN
OH
H
增长碳链
羰基上的不饱和键在一定条件下可与H2、HX、HCN、氨及氨的衍生物、醇类等发生加成反应。
②氧化反应
醛的还原性较强比酮容易发生氧化反应。空气中的氧气就能氧化醛,而酮一般需很强的氧化剂(如KMnO4(H+)溶液、溴水等)才能被氧化。
银镜反应
[银氨溶液的配制和使用]
AgNO3+NH3·H2O=AgOH↓+NH4NO3
AgOH+2NH3·H2O=Ag(NH3)2OH+2H2O
试管内壁必须光滑、洁净;
实验的银氨溶液应现配现用,银氨溶液不能久置,氨水不能太浓,否则会生成易爆炸的物质;
必须用水浴加热;
加热时不能振荡和摇动试管;
剩液及时处理,防止产生爆炸性物质,试管用稀硝酸洗涤
【实验中注意的事项】
CH3CHO+2Ag(NH3)2OH 2Ag↓+CH3COONH4+3NH3+H2O
【反应方程式】
与新制的氢氧化铜反应
【反应方程式】
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
必须使用新制的Cu(OH)2,久置的Cu(OH)2易发生变质;
碱一定要过量,否则生成乙酸。
加热时须将混合溶液加热至沸腾。
【实验中注意的事项】
银氨溶液和新制Cu(OH)2悬浊液常用于鉴别有机化合物分子中是否含有醛基。
③还原反应
2.糖类和核酸
(1)单糖
①还原性
②葡萄糖在人体内的氧化反应
③不饱和性
④酯化反应
①加成反应(催化加氢)
②酯化反应
③与活泼金属反应
葡萄糖
果糖
(2)双糖
蔗糖 麦芽糖
分子式
分子结构
化学性质
C12H22O11
C12H22O11
分子中无醛基
分子中有醛基
非还原性糖
还原性糖
(3)多糖
淀 粉 纤维素
通式
物理性质
化学性质
存在与 制法
用途
(C6H10O5)n
(C6H10O5)n
不溶于冷水,白色粉末
白色无嗅无味物质,不溶于
水,不溶于一般的有机溶剂
水解、酯化、与碘作用
呈蓝色
植物的种子、块茎和根里
食物、制葡萄糖、酒精
水解、酯化
木材、棉花
制硝酸纤维、纤维素乙酸酯、造纸、粘胶纤维
(4)五碳醛糖与核酸
脱氧
核糖
磷酸
碱 基
A:腺嘌呤
G:鸟嘌呤
T:胸腺嘧啶
C:胞嘧啶
脱氧
核糖
磷酸
碱 基
脱氧
核糖
磷酸
碱 基
脱氧核糖核酸
DNA
多个脱氧核糖核苷酸分子间脱水形成磷酯键后聚合而成的脱氧核糖核苷酸链。
核糖
磷酸
碱 基
核糖
磷酸
碱 基
核糖
磷酸
碱 基
多个核糖核苷酸分子间脱水形成磷酯键后聚合而成的核糖核苷酸链。
核糖核酸
RNA
A:腺嘌呤
G:鸟嘌呤
U:尿嘧啶
C:胞嘧啶
A-U
G-C
知识点四:羧酸 氨基酸和蛋白质
1.羧酸
(1)定义:
由烃基(或氢原子)与羧基相连而构成的有机化合物。
—C—OH
O
或
—COOH
(2)分类:
羧酸
按烃基分类
脂肪酸
芳香酸,如苯甲酸
按羧基数目
一元羧酸,如乙酸 CH3COOH
二元羧酸,如乙二酸 HOOC—COOH
……
(3)羧酸的物理性质
氢键
熔、沸点
溶解度
羧酸的沸点比相应的醇的高。
分子中碳原子数目小于4的羧酸与水互溶;
随着分子中碳链的增长,羧酸在水中的溶解度迅速减小,直至与相对分子质量相近的烷烃的溶解度相近。
(4)羧酸的化学性质
δ+
δ-
α
①难加成
羟基对羰基的影响,使羧基中的羰基较难发生加成反应,只有在特定条件或催化剂作用下,反应才能进行。
②C—O断裂:—OH被取代,生成酯、酰胺等
③O—H断裂:解离出氢离子,表现酸性
酸性:乙酸>碳酸
④断裂C-H键,α-H被取代
2.羧酸的衍生物
(1)酯:
分子由酰基和烃氧基相连构成的一种羧酸衍生物。
—C—O—
O
①水解反应
在稀硫酸存在下水解:
碱性条件下水解:
CH3—C—O—C2H5 + H2O
CH3—C—OH+H—O—C2H5
O
O
稀硫酸
△
CH3—C—OC2H5 + NaOH
CH3—C—ONa + HOC2H5
△
O
O
(2)油脂:
高级脂肪酸甘油酯
甘油(丙三醇)
HO—CH2
HO—CH
HO—CH2
高级脂肪酸
①软脂酸:C15H31COOH
③油酸:C17H33COOH
②硬脂酸:C17H35COOH
饱和脂肪酸
不饱和脂肪酸
①水解反应
②油脂氢化
(3)酰胺:
分子由酰基和氨基相连构成的羧酸衍生物
R—C—NH2
O
酰胺在通常情况下较难水解,在强酸或强碱存在下长时间加热可水解成羧酸(或羧酸盐)和氨(或胺)。
3.氨基酸和蛋白质
(1)氨基酸
①两性
a.与盐酸的反应:
b.与氢氧化钠反应:
R—CH—COOH+NaOH
NH2
R—CH—COONa+H2O
NH2
R—CH—COOH+HCl
NH2
R—CH—COOH
NH3Cl
②成肽反应
(2)蛋白质
氨基酸种类、数目、排列顺序
空间结构多样
种类繁多
功能多样
①水解:天然蛋白质水解的最终产物为α-氨基酸。
②具有两性——因为它由氨基酸组成。
③盐析——可逆。
④变性——不可逆。
⑤颜色反应——含有苯环的蛋白质遇浓硝酸变黄。
⑥灼烧蛋白质会产生烧焦羽毛的气味。
(3)酶
①条件温和 ②专一性 ③高效率
1.氯普鲁卡因盐酸盐是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下:
写出序号相应的反应类型,供选择的反应类型如下:氧化、还原、硝化、氯代、酸化、碱化、成盐、酯化、酯交换、水解。
①硝化 ②氯代 ③氧化 ④酯化 ⑥还原
【考点一】有机反应类型的判断
(1)判断有机化学反应类型的基本思路
(2)常见的反应类型
①取代反应——“一上一下,取而代之”
②加成反应——“只上不下,合二为一”
③消去反应——“一分为二,只下不上”
(3)根据反应条件推断反应类型
NaOH的水溶液
酯或卤代烃的水解反应等
NaOH的乙醇溶液中加热
卤代烃的消去反应
浓硫酸,加热
醇的消去反应、酯化反应、成醚反应或硝化反应等
溴水或溴的CCl4溶液
烯烃、炔烃的加成反应
H2,Ni
烯烃、炔烃、芳香烃、醛的加成反应或还原反应
O2、Cu(或Ag)、加热(或CuO、加热)
醇的氧化反应
O2或新制的Cu(OH)2或银氨溶液
—CHO的氧化反应
稀硫酸,加热
酯、低聚糖、多糖的水解反应
光照、X2
烷基上的取代反应
FeX3、X2
苯环上的取代反应
【练一练】
A.取代、消去、酯化、加成
B.酯化、消去、缩聚、取代
C.酯化、取代、缩聚、取代
D.取代、消去、加聚、取代
B
1.结构简式为 的有机化合物可以通过不同的反应得到下列四种物质,生成这四种有机化合物的反应类型依次为( )
COOH
CH2CH2OH
【考点二】限定条件的同分异构体数目的判断
1.某有机化合物的分子式为C9H10O2,分子中含有苯环,苯环上有2个取代基,且其中一个为甲基,则能与NaOH溶液反应的该物质的结构有( )
A.4种 B.7种
C.9种 D.12种
D
2.已知下面反应可以发生:
(1)若A、C都能发生银镜反应,则C6H12O2可能的结构简式有 种。
(2)若A能发生银镜反应而C不能,则C6H12O2可能的结构简式有 种。
(3)若A、C都不能发生银镜反应,则C6H12O2可能的结构简式有 种。
(4)若A不能发生银镜反应,C氧化可得A,则C6H12O2可能的结构简式有 种。
1
4
3
2
【考点三】含氧衍生物结构与性质的综合
1.某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之比为( )
A.1∶1∶1 B.2∶4∶1 C.1∶2∶1 D.1∶2∶2
B
【考点四】含氧衍生物结构与性质的综合
1.某有机化合物X的结构简式如图所示,下列有关X的说法不正确的是( )
A.既能与Br2的CCl4溶液发生加成反应,又可在光
照条件下与Br2发生取代反应
B.1 mol该有机化合物最多可与3 mol NaOH反应
C.既可催化加氢,又可使酸性KMnO4溶液褪色
D.既可与FeCl3溶液发生显色反应,又可与NaHCO3溶液反应放出CO2气体
D
2.Y是一种皮肤病用药,它可以由原料X经过多步反应合成。
下列说法正确的是( )
A.X与Y互为同分异构体
B.1 mol X最多可以与5 mol H2发生加成反应
C.产物Y能发生氧化、加成、取代、消去反应
D.1 mol Y最多能与2 mol NaOH发生反应
A
官能团与有机化学反应
烃的衍生物
有机化学反应类型
加成反应
取代反应
消去反应
氧化反应
还原反应
烃的衍生物
醇
酚
醛、酮
糖类
羧酸
羧酸衍生物:酯、酰胺
取代羧酸
氨基酸
章末复习
1.能写出烃的衍生物的类别通式、官能团、简单代表物的结构简式及名称,能列举各类烃的衍生物的典型代表物的主要物理性质;
2.能描述说明、分析解释各类烃的衍生物的典型代表物的重要反应,能书写相应反应式;
3.能列举典型糖类物质,描述葡萄糖、淀粉、纤维素的化学性质;
4.能辨识蛋白质结构中的肽键,认识蛋白质的结构特点,能判断氨基酸的缩合产物,多肽的水解产物;
5.能辨识核糖核酸、脱氧核糖核酸中的磷脂键,能基于氢键分析碱基的配对原理。
知识点一:有机化学反应类型
1. 加成反应
有机化合物分子中不饱和键两端的两个原子与其他原子或原子团结合,生成新的有机化合物的反应。
(1)定义:
(2)加成反应规律:
不饱和键打开,结合原子或原子团形成新的化学键,“有上无下”。
生成物只有一种,原子利用率100%。
(3)不对称烯烃的加成反应:
2. 取代反应
有机化合物分子中的某个(或某些)原子或原子团被其他原子或原子团代替的反应。
(1)定义:
(2)取代反应规律:
有机化合物分子中有极性单键时,有可能发生取代反应。
有上有下,取而代之。
(3)成键结构(或官能团)与试剂:
有机物或官能团 试剂 取代位置
X2、HNO3、H2SO4等
C—H
饱和烃
X2
C—H
苯环
①烷烃或芳香烃的取代反应:
有机物或官能团 试剂 取代位置
H2O、NH3、NaCN等
HX、RCOOH 等
卤素原子
羟基H上或-OH
—X(卤代烃)
—OH
②卤代烃或醇的取代反应:
③烯烃 炔烃 醛 酮 羧酸的α-C上的碳氢键易断裂发生取代反应
④酯化反应、酯的水解反应
3. 消去反应
在一定条件下,有机化合物脱去小分子物质(如H2O、HBr等)生成分子中有不饱和键的有机化合物的反应。
(1)定义:
(2)乙醇的消去反应
CH3CH2OH CH2=CH2↑+H2O
浓硫酸
170℃
4. 氧化反应、还原反应
氧化反应:
还原反应:
有机化合物分子中增加氧原子或减少氢原子的反应。
有机化合物分子中增加氢原子或减少氧原子的反应。
常见的氧化剂
氧气、酸性KMnO4溶液、臭氧、银氨溶液和新制氢氧化铜悬浊液等。
常见的还原剂
氢气、氢化铝锂(LiAlH4)和硼氢化钠(NaBH4)等。
预测有机化合物可能发生的化学反应的程序:
知识点二:有机化学反应类型的应用
1. 卤代烃的性质
(1)定义:
烃分子中的一个或多个氢原子被卤素原子取代后生成的化合物称为卤代烃。官能团是-X(Cl、Br、I、F)。
饱和一卤代烃的通式为:
CnH2n+1X
卤代烃
根据取代卤素的不同
氟代烃
氯代烃
溴代烃
碘代烃
根据卤素原子的多少
一卤代烃
二卤代烃
多卤代烃
根据烃基的不同
饱和卤代烃
不饱和卤代烃
芳香卤代烃
(2)分类:
(3)1-溴丙烷的物理性质:
无色液体
沸点为71℃
密度比水大
不溶于水,易溶于有机溶剂
C3H7Br
(4)化学性质:
官能团:-Br
极性键:C-Br、C-H
取代反应
δ+
δ-
消去反应
①1―溴丙烷的取代反应
CH3CH2CH2Br+NaOH
水
△
稀硝酸酸化
白色沉淀(AgCl)
淡黄色沉淀(AgBr)
黄色沉淀(AgI)
NaOH水溶液
R—X
AgNO3溶液
卤代烃中卤素原子的检验:
取上层清液
CH3CH2CH2OH+NaBr
②1―溴丙烷的消去反应
△
NaOH的水溶液
醇
NaOH的乙醇溶液
△
烯烃/炔烃
注意:a.没有β-C原子的卤代烃不能发生消去反应。
b.有β-C原子,但β-C原子上没有氢原子的卤代烃也不能发生消去反应。
2. 卤代烃的制备
知识点三:醇和酚
1.醇
(1)定义:
脂肪烃分子中的氢原子或芳香烃侧链上的氢原子被羟基取代后的有机化合物。
(2)分类:
CnH2n+1OH
醇
根据醇分子中所含羟基的数目
一元醇
二元醇
多元醇
按羟基所连烃基种类分类
脂肪醇
脂环醇
饱和醇
不饱和醇
芳香醇
(3)物理性质:
①沸点
a.饱和一元醇的沸点比与其相对分子质量接近的烷烃或烯烃的沸点要高。
c.碳原子数相同时,羟基个数越多,沸点越高。
b.饱和一元醇,随分子中碳原子数的增加沸点逐渐升高。
②溶解度:
含羟基较多的醇极易溶于水。
常温常压,饱和一元醇在水中的溶解性
醇分子中碳原子数 1~3 4~11 > 11
溶解性 能与水以任意比例互溶 油状液体,仅可部分溶于水 固体,
难溶于水
(4)化学性质:
①取代反应
反应试剂:
浓的氢卤酸(HCl、HBr、HI)
C2H5OH+HBr C2H5Br+H2O
乙醇 溴乙烷
反应条件:
酸做催化剂及加热
C2H5—OH+H—O—C2H5 C2H5—O—C2H5+H2O
乙醚
浓硫酸
140℃
浓硫酸
CH3
C
OH + H18O—C2H5
O
CH3
C
18O—C2H5 + H2O
O
“酸脱羟基醇脱氢”
②消去反应
反应条件:
浓硫酸、加热
CH3—CH2—CH2OH
CH3—CH CH2
↑ + H2O
浓硫酸
170℃
③与活泼金属的反应
2C2H5OH+2Na→2C2H5ONa+H2↑
④氧化反应
-OH所在的碳原子上要
有氢原子才可以被氧化
醇的催化氧化规律
氢
原
子
数
生成醛(或羧酸)
生成酮
不能被催化氧化
2~3个H
1个H
没有H
如:
R2
R1
R3
C
OH
O
R1
R2
C
H
H
Cu,O2
△
O
R1
R2
C
如:
如:
KMnO4(H+)或
K2Cr2O7(H+)
R
COOH
O
R
H
C
H
H
O
R
H
C
H
H
Cu,O2
△
CHO或
R
2.酚
(1)定义:
芳香烃分子中苯环上的氢原子被羟基取代后的有机化合物。
(2)化学性质:
①酸性——俗称石炭酸
苯酚钠
+H2O
+NaOH
OH
ONa
酸性强弱:
H2CO3 > C2H5OH > HCO3-
苯环对羟基的影响使得酚羟基的氢原子较为活泼
②取代反应
2,4,6-三溴苯酚(白色沉淀)
+3Br2
+3HBr
OH
OH
Br
Br
Br
酚羟基对苯环影响,使苯环上羟基邻、对位的氢原子的活性增强,易被取代
③苯酚与甲醛的缩聚反应
酚醛树脂
H+
+nHCHO
OH
n
+ (n-1)H2O
OH
CH2
n
OH
H
④苯酚与Fe3+显色反应
现象:苯酚遇到氯化铁溶液变紫色
用途:检验苯酚或Fe3+ 的存在
⑤苯酚也能像苯一样发生硝化、磺化、加成等反应。
+3HNO3
+3H2O
OH
OH
NO2
O2N
NO2
浓硫酸
+3H2
OH
Ni
OH
环己醇
知识点四:醛和酮 糖类和核酸
1.醛和酮
(1)结构:
—C—
O
羰基
醛
酮
羰基碳原子分别与氢原子和烃基(或氢原子)相连。
羰基碳原子相连的两个基团均为烃基,烃基可以相同也可以不同。
官能团:醛基
官能团:酮羰基
—C—H
O
(R`)—C—(R`)
O
—CHO
(2)醛、酮的化学性质:
①羰基的加成反应
CH3—C—H
O
δ+
δ-
+ H—CN
δ+
δ-
催化剂
CH3—C—CN
OH
H
增长碳链
羰基上的不饱和键在一定条件下可与H2、HX、HCN、氨及氨的衍生物、醇类等发生加成反应。
②氧化反应
醛的还原性较强比酮容易发生氧化反应。空气中的氧气就能氧化醛,而酮一般需很强的氧化剂(如KMnO4(H+)溶液、溴水等)才能被氧化。
银镜反应
[银氨溶液的配制和使用]
AgNO3+NH3·H2O=AgOH↓+NH4NO3
AgOH+2NH3·H2O=Ag(NH3)2OH+2H2O
试管内壁必须光滑、洁净;
实验的银氨溶液应现配现用,银氨溶液不能久置,氨水不能太浓,否则会生成易爆炸的物质;
必须用水浴加热;
加热时不能振荡和摇动试管;
剩液及时处理,防止产生爆炸性物质,试管用稀硝酸洗涤
【实验中注意的事项】
CH3CHO+2Ag(NH3)2OH 2Ag↓+CH3COONH4+3NH3+H2O
【反应方程式】
与新制的氢氧化铜反应
【反应方程式】
CH3CHO+2Cu(OH)2+NaOH CH3COONa+Cu2O↓+3H2O
必须使用新制的Cu(OH)2,久置的Cu(OH)2易发生变质;
碱一定要过量,否则生成乙酸。
加热时须将混合溶液加热至沸腾。
【实验中注意的事项】
银氨溶液和新制Cu(OH)2悬浊液常用于鉴别有机化合物分子中是否含有醛基。
③还原反应
2.糖类和核酸
(1)单糖
①还原性
②葡萄糖在人体内的氧化反应
③不饱和性
④酯化反应
①加成反应(催化加氢)
②酯化反应
③与活泼金属反应
葡萄糖
果糖
(2)双糖
蔗糖 麦芽糖
分子式
分子结构
化学性质
C12H22O11
C12H22O11
分子中无醛基
分子中有醛基
非还原性糖
还原性糖
(3)多糖
淀 粉 纤维素
通式
物理性质
化学性质
存在与 制法
用途
(C6H10O5)n
(C6H10O5)n
不溶于冷水,白色粉末
白色无嗅无味物质,不溶于
水,不溶于一般的有机溶剂
水解、酯化、与碘作用
呈蓝色
植物的种子、块茎和根里
食物、制葡萄糖、酒精
水解、酯化
木材、棉花
制硝酸纤维、纤维素乙酸酯、造纸、粘胶纤维
(4)五碳醛糖与核酸
脱氧
核糖
磷酸
碱 基
A:腺嘌呤
G:鸟嘌呤
T:胸腺嘧啶
C:胞嘧啶
脱氧
核糖
磷酸
碱 基
脱氧
核糖
磷酸
碱 基
脱氧核糖核酸
DNA
多个脱氧核糖核苷酸分子间脱水形成磷酯键后聚合而成的脱氧核糖核苷酸链。
核糖
磷酸
碱 基
核糖
磷酸
碱 基
核糖
磷酸
碱 基
多个核糖核苷酸分子间脱水形成磷酯键后聚合而成的核糖核苷酸链。
核糖核酸
RNA
A:腺嘌呤
G:鸟嘌呤
U:尿嘧啶
C:胞嘧啶
A-U
G-C
知识点四:羧酸 氨基酸和蛋白质
1.羧酸
(1)定义:
由烃基(或氢原子)与羧基相连而构成的有机化合物。
—C—OH
O
或
—COOH
(2)分类:
羧酸
按烃基分类
脂肪酸
芳香酸,如苯甲酸
按羧基数目
一元羧酸,如乙酸 CH3COOH
二元羧酸,如乙二酸 HOOC—COOH
……
(3)羧酸的物理性质
氢键
熔、沸点
溶解度
羧酸的沸点比相应的醇的高。
分子中碳原子数目小于4的羧酸与水互溶;
随着分子中碳链的增长,羧酸在水中的溶解度迅速减小,直至与相对分子质量相近的烷烃的溶解度相近。
(4)羧酸的化学性质
δ+
δ-
α
①难加成
羟基对羰基的影响,使羧基中的羰基较难发生加成反应,只有在特定条件或催化剂作用下,反应才能进行。
②C—O断裂:—OH被取代,生成酯、酰胺等
③O—H断裂:解离出氢离子,表现酸性
酸性:乙酸>碳酸
④断裂C-H键,α-H被取代
2.羧酸的衍生物
(1)酯:
分子由酰基和烃氧基相连构成的一种羧酸衍生物。
—C—O—
O
①水解反应
在稀硫酸存在下水解:
碱性条件下水解:
CH3—C—O—C2H5 + H2O
CH3—C—OH+H—O—C2H5
O
O
稀硫酸
△
CH3—C—OC2H5 + NaOH
CH3—C—ONa + HOC2H5
△
O
O
(2)油脂:
高级脂肪酸甘油酯
甘油(丙三醇)
HO—CH2
HO—CH
HO—CH2
高级脂肪酸
①软脂酸:C15H31COOH
③油酸:C17H33COOH
②硬脂酸:C17H35COOH
饱和脂肪酸
不饱和脂肪酸
①水解反应
②油脂氢化
(3)酰胺:
分子由酰基和氨基相连构成的羧酸衍生物
R—C—NH2
O
酰胺在通常情况下较难水解,在强酸或强碱存在下长时间加热可水解成羧酸(或羧酸盐)和氨(或胺)。
3.氨基酸和蛋白质
(1)氨基酸
①两性
a.与盐酸的反应:
b.与氢氧化钠反应:
R—CH—COOH+NaOH
NH2
R—CH—COONa+H2O
NH2
R—CH—COOH+HCl
NH2
R—CH—COOH
NH3Cl
②成肽反应
(2)蛋白质
氨基酸种类、数目、排列顺序
空间结构多样
种类繁多
功能多样
①水解:天然蛋白质水解的最终产物为α-氨基酸。
②具有两性——因为它由氨基酸组成。
③盐析——可逆。
④变性——不可逆。
⑤颜色反应——含有苯环的蛋白质遇浓硝酸变黄。
⑥灼烧蛋白质会产生烧焦羽毛的气味。
(3)酶
①条件温和 ②专一性 ③高效率
1.氯普鲁卡因盐酸盐是一种局部麻醉剂,麻醉作用较快、较强,毒性较低,其合成路线如下:
写出序号相应的反应类型,供选择的反应类型如下:氧化、还原、硝化、氯代、酸化、碱化、成盐、酯化、酯交换、水解。
①硝化 ②氯代 ③氧化 ④酯化 ⑥还原
【考点一】有机反应类型的判断
(1)判断有机化学反应类型的基本思路
(2)常见的反应类型
①取代反应——“一上一下,取而代之”
②加成反应——“只上不下,合二为一”
③消去反应——“一分为二,只下不上”
(3)根据反应条件推断反应类型
NaOH的水溶液
酯或卤代烃的水解反应等
NaOH的乙醇溶液中加热
卤代烃的消去反应
浓硫酸,加热
醇的消去反应、酯化反应、成醚反应或硝化反应等
溴水或溴的CCl4溶液
烯烃、炔烃的加成反应
H2,Ni
烯烃、炔烃、芳香烃、醛的加成反应或还原反应
O2、Cu(或Ag)、加热(或CuO、加热)
醇的氧化反应
O2或新制的Cu(OH)2或银氨溶液
—CHO的氧化反应
稀硫酸,加热
酯、低聚糖、多糖的水解反应
光照、X2
烷基上的取代反应
FeX3、X2
苯环上的取代反应
【练一练】
A.取代、消去、酯化、加成
B.酯化、消去、缩聚、取代
C.酯化、取代、缩聚、取代
D.取代、消去、加聚、取代
B
1.结构简式为 的有机化合物可以通过不同的反应得到下列四种物质,生成这四种有机化合物的反应类型依次为( )
COOH
CH2CH2OH
【考点二】限定条件的同分异构体数目的判断
1.某有机化合物的分子式为C9H10O2,分子中含有苯环,苯环上有2个取代基,且其中一个为甲基,则能与NaOH溶液反应的该物质的结构有( )
A.4种 B.7种
C.9种 D.12种
D
2.已知下面反应可以发生:
(1)若A、C都能发生银镜反应,则C6H12O2可能的结构简式有 种。
(2)若A能发生银镜反应而C不能,则C6H12O2可能的结构简式有 种。
(3)若A、C都不能发生银镜反应,则C6H12O2可能的结构简式有 种。
(4)若A不能发生银镜反应,C氧化可得A,则C6H12O2可能的结构简式有 种。
1
4
3
2
【考点三】含氧衍生物结构与性质的综合
1.某有机物M的结构简式如图所示,若等物质的量的M在一定条件下分别与金属钠、氢氧化钠溶液、碳酸氢钠溶液反应,则消耗的钠、氢氧化钠、碳酸氢钠的物质的量之比为( )
A.1∶1∶1 B.2∶4∶1 C.1∶2∶1 D.1∶2∶2
B
【考点四】含氧衍生物结构与性质的综合
1.某有机化合物X的结构简式如图所示,下列有关X的说法不正确的是( )
A.既能与Br2的CCl4溶液发生加成反应,又可在光
照条件下与Br2发生取代反应
B.1 mol该有机化合物最多可与3 mol NaOH反应
C.既可催化加氢,又可使酸性KMnO4溶液褪色
D.既可与FeCl3溶液发生显色反应,又可与NaHCO3溶液反应放出CO2气体
D
2.Y是一种皮肤病用药,它可以由原料X经过多步反应合成。
下列说法正确的是( )
A.X与Y互为同分异构体
B.1 mol X最多可以与5 mol H2发生加成反应
C.产物Y能发生氧化、加成、取代、消去反应
D.1 mol Y最多能与2 mol NaOH发生反应
A
官能团与有机化学反应
烃的衍生物
有机化学反应类型
加成反应
取代反应
消去反应
氧化反应
还原反应
烃的衍生物
醇
酚
醛、酮
糖类
羧酸
羧酸衍生物:酯、酰胺
取代羧酸
氨基酸
