2024北京昌平高二(上)期末化学(PDF版含答案)
文档属性
| 名称 | 2024北京昌平高二(上)期末化学(PDF版含答案) |
|
|
| 格式 | |||
| 文件大小 | 9.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-19 00:00:00 | ||
图片预览


文档简介
昌平区2023一2024学年第一学期高二年级期末质量抽测
化学试卷
2024.1
本试卷共9页,共100分。考试时长90分钟。考生务必将答案答在答题卡上,在
试卷上作答无效。考试结束后,将答题卡交回。
可能用到的相对原子质量:H1C12016Zn65
第一部分
选择题(共42分)
在下列各题的四个选项中,只有一个选项符合题意。(每小题2分,共42分)
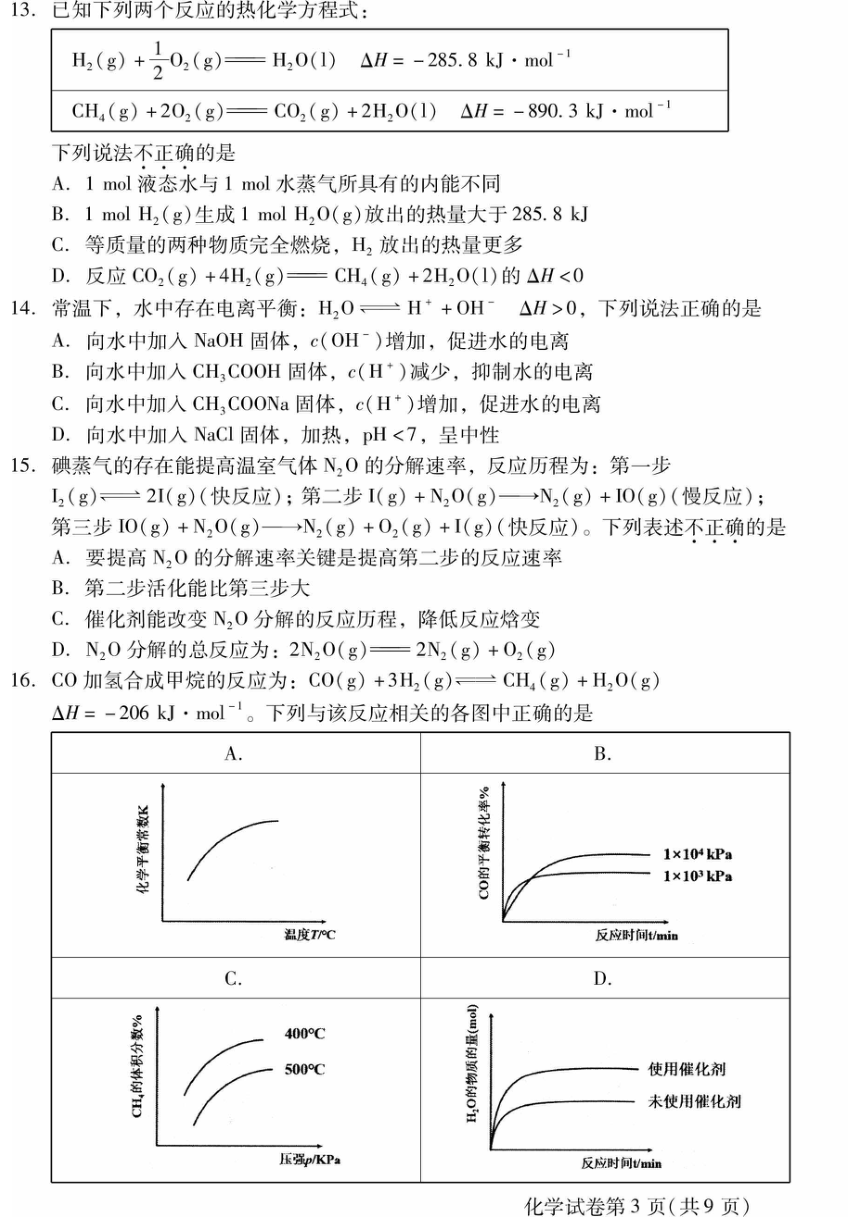
1.下列装置或过程能实现电能转化为化学能的是
地面
镁七
导线
石墨
石墨
负极室
下极室
电解质
钢铁输水管
溶液
质子
熔融NaCI
交换膜
A.砷化镓太阳能
B.氢氧燃料电池
C.牺牲阳极保护法
D.冶炼金属钠
电池
保护铁管道
2.下列物质的溶液呈碱性的是
A.NH CI
B.HCIO
C.NaHCO
D.KNO3
3.下列电离方程式书写正确的是
A.CH COOH-CH,COO+H*
B.CH,COONa=CH,C0O Na*
C.HP04=3H++P043-
D.KOH≌K++OH
4.铜锌原电池的装置如右图,下列说法正确的是
A
A.Zn极发生还原反应
Zn
网Cu
B.Cu极电极反应式为Cu+2e一Cu2+
C.盐桥中Clˉ进入ZnSO4溶液
D.电子由Cu电极流向Zn电极
盐
桥
5.下列过程与水解反应无关的是
(含KC饱和溶液的琼胶)
A.用食醋CH,COOH除去水垢
B.用热的纯诚Na,CO3溶液去除油污
C.用硫酸铝A山2(S04)3做净水剂净化天然水
D.向沸水中滴入饱和FeCl,溶液制备Fe(OH)3胶体
化学试卷第1页(共9页)
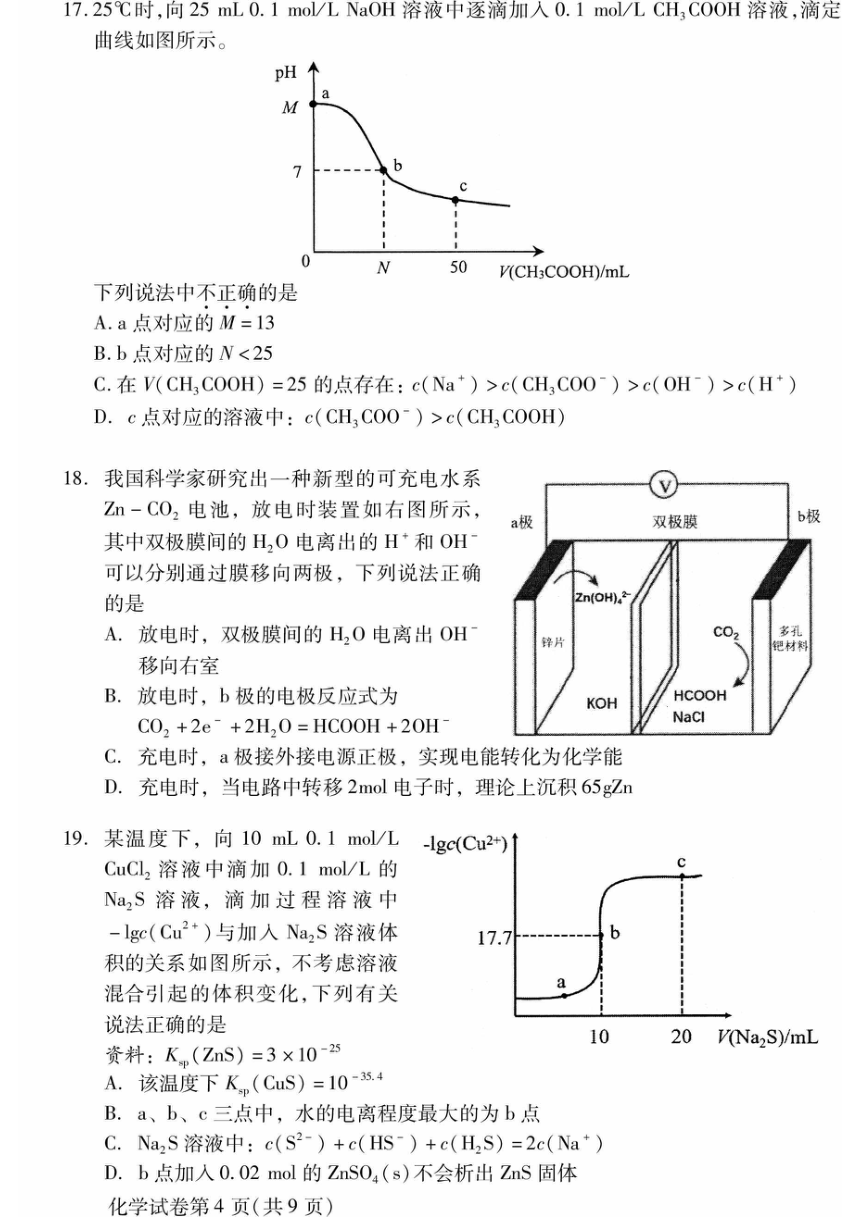
6.一定温度下反应H2(g)+L2(g)三2HI(g)的能量与
能
反应过程的关系如右图,下列说法不正确的是
A.断开I-I键需要吸收能量
kJ/mol
B.H2(g)和L2(g)生成2Hl(g)的反应为放热反应
a kJ/mel
ckJ/mol
H2(g)+21(g)
C.1molH,(g)和1molL2(g)的总能量高于2mol
H2(g)+I2(g)
HT(g)的能量
2FI(g)
D.该反应的H=-(c-b-a)kJ·mol-1
友疵避程
7.在恒容绝热的密闭容器中,发生可逆反应2S02(g)+02(g)一2S0,(g)△H<0,
下列情况不能说明该反应达到平衡状态的是
A.容器内的压强不再改变
B.浓度商等于该温度下的化学平衡常数
C.容器内气体的浓度c(S02):c(02):c(S03)=2:1:2
D.容器内的温度不再变化
8.在2L密闭容器中发生反应:A(g)+4B(g)一2C(g)+2D(g)。已知2in内B的
物质的量由6mol变为2mol,下列叙述不正确的是
A.v(A)=0.25mol·L-1·min-l
B.v(B)=1mol·L-1·min1
C.x(C)=0.5mol·L.-1·min1
D.v(B):(D)=1:2
9.常温下,下列各组离子一定能大量共存的是
A.Na+、Mg2+、Cl、OH
B.Na+、K+、MnO4、NO3
C.H+、Na+、Fe2+、No,
D.Na+、Cl0、C032-、H+
10.下列事实能用平衡移动原理解释的是
A.H,02溶液中加人少量MnO2固体,促进H202分解
B.密闭烧瓶内的NO2和N2O4的混合气体,受热后颜色加深
C.带活塞密闭容器内存在H,(g)+【(g)一2HⅢ(g)平衡,向外拉动活塞颜色变浅
D.锌片与稀H2SO4反应过程中,加人少量CuSO4固体,促进H2的产生
11.下列化学用语与所给事实不相符的是
A.电解食盐水制备烧碱、氢气和氯气:C+H,0通电OH+H,↑+C,↑
B.钢铁中性条件下吸氧腐蚀的正极反应:02+4e+2H20一40H
C.用FeS做沉淀剂除去废水中的Cu2+:FeS(s)+Cu2+(aq)一CuS(s)+Fe2+(aq)
D.泡沫灭火器原理:A3++3HC03—A1(OH)3↓+3C02个
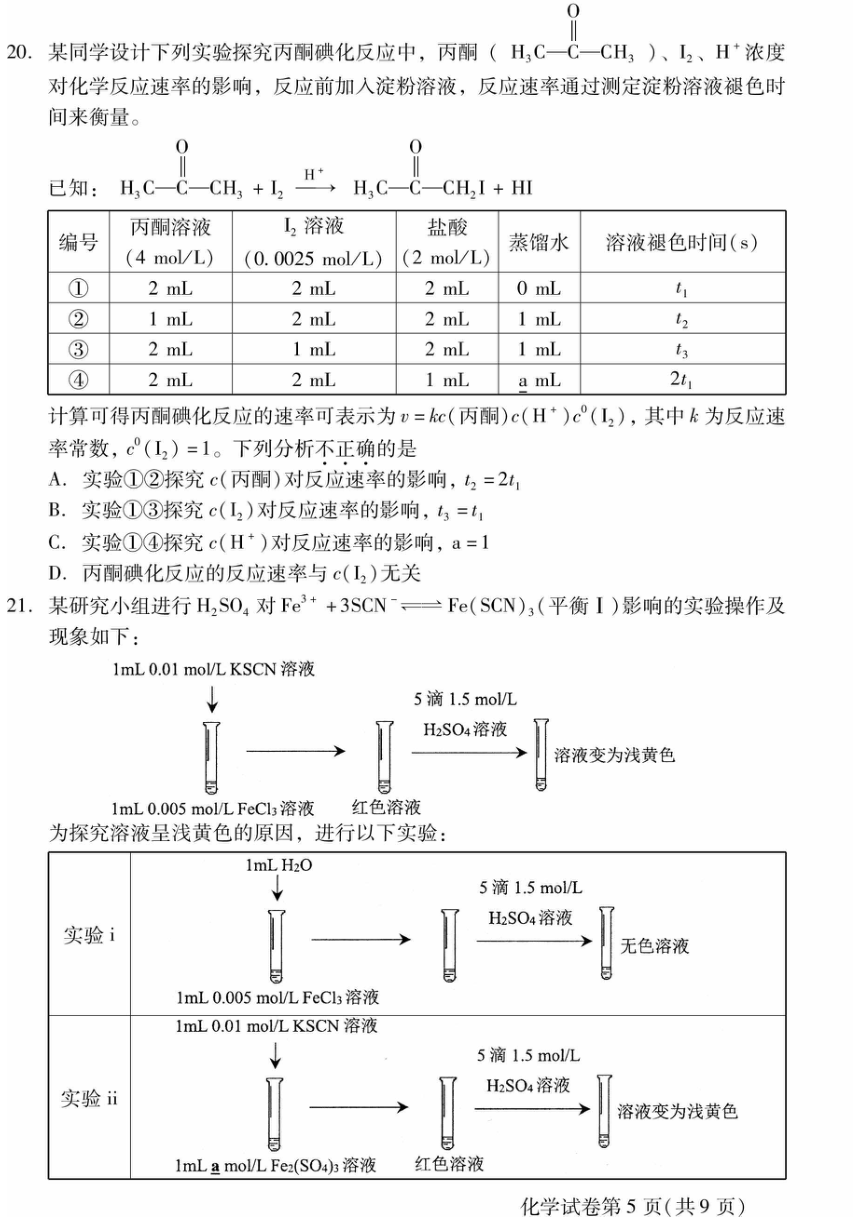
12.铁制品镀铜的电镀装置如右图所示,下列说法中
A
不正确的是
电源
资料:Cu2++4NH3=[Cu(NH3)4]2+
A.铜片接电源的正极
B.电镀过程中S0,2-向阳极移动
铜片
待镀
CuSO
铁制品
C.随铜单质析出电解质溶液中c(Cu2+)减小
溶液
D.加入氨水后可使铜缓慢析出,镀层更致密
化学试卷第2页(共9页)
化学试卷
2024.1
本试卷共9页,共100分。考试时长90分钟。考生务必将答案答在答题卡上,在
试卷上作答无效。考试结束后,将答题卡交回。
可能用到的相对原子质量:H1C12016Zn65
第一部分
选择题(共42分)
在下列各题的四个选项中,只有一个选项符合题意。(每小题2分,共42分)
1.下列装置或过程能实现电能转化为化学能的是
地面
镁七
导线
石墨
石墨
负极室
下极室
电解质
钢铁输水管
溶液
质子
熔融NaCI
交换膜
A.砷化镓太阳能
B.氢氧燃料电池
C.牺牲阳极保护法
D.冶炼金属钠
电池
保护铁管道
2.下列物质的溶液呈碱性的是
A.NH CI
B.HCIO
C.NaHCO
D.KNO3
3.下列电离方程式书写正确的是
A.CH COOH-CH,COO+H*
B.CH,COONa=CH,C0O Na*
C.HP04=3H++P043-
D.KOH≌K++OH
4.铜锌原电池的装置如右图,下列说法正确的是
A
A.Zn极发生还原反应
Zn
网Cu
B.Cu极电极反应式为Cu+2e一Cu2+
C.盐桥中Clˉ进入ZnSO4溶液
D.电子由Cu电极流向Zn电极
盐
桥
5.下列过程与水解反应无关的是
(含KC饱和溶液的琼胶)
A.用食醋CH,COOH除去水垢
B.用热的纯诚Na,CO3溶液去除油污
C.用硫酸铝A山2(S04)3做净水剂净化天然水
D.向沸水中滴入饱和FeCl,溶液制备Fe(OH)3胶体
化学试卷第1页(共9页)
6.一定温度下反应H2(g)+L2(g)三2HI(g)的能量与
能
反应过程的关系如右图,下列说法不正确的是
A.断开I-I键需要吸收能量
kJ/mol
B.H2(g)和L2(g)生成2Hl(g)的反应为放热反应
a kJ/mel
ckJ/mol
H2(g)+21(g)
C.1molH,(g)和1molL2(g)的总能量高于2mol
H2(g)+I2(g)
HT(g)的能量
2FI(g)
D.该反应的H=-(c-b-a)kJ·mol-1
友疵避程
7.在恒容绝热的密闭容器中,发生可逆反应2S02(g)+02(g)一2S0,(g)△H<0,
下列情况不能说明该反应达到平衡状态的是
A.容器内的压强不再改变
B.浓度商等于该温度下的化学平衡常数
C.容器内气体的浓度c(S02):c(02):c(S03)=2:1:2
D.容器内的温度不再变化
8.在2L密闭容器中发生反应:A(g)+4B(g)一2C(g)+2D(g)。已知2in内B的
物质的量由6mol变为2mol,下列叙述不正确的是
A.v(A)=0.25mol·L-1·min-l
B.v(B)=1mol·L-1·min1
C.x(C)=0.5mol·L.-1·min1
D.v(B):(D)=1:2
9.常温下,下列各组离子一定能大量共存的是
A.Na+、Mg2+、Cl、OH
B.Na+、K+、MnO4、NO3
C.H+、Na+、Fe2+、No,
D.Na+、Cl0、C032-、H+
10.下列事实能用平衡移动原理解释的是
A.H,02溶液中加人少量MnO2固体,促进H202分解
B.密闭烧瓶内的NO2和N2O4的混合气体,受热后颜色加深
C.带活塞密闭容器内存在H,(g)+【(g)一2HⅢ(g)平衡,向外拉动活塞颜色变浅
D.锌片与稀H2SO4反应过程中,加人少量CuSO4固体,促进H2的产生
11.下列化学用语与所给事实不相符的是
A.电解食盐水制备烧碱、氢气和氯气:C+H,0通电OH+H,↑+C,↑
B.钢铁中性条件下吸氧腐蚀的正极反应:02+4e+2H20一40H
C.用FeS做沉淀剂除去废水中的Cu2+:FeS(s)+Cu2+(aq)一CuS(s)+Fe2+(aq)
D.泡沫灭火器原理:A3++3HC03—A1(OH)3↓+3C02个
12.铁制品镀铜的电镀装置如右图所示,下列说法中
A
不正确的是
电源
资料:Cu2++4NH3=[Cu(NH3)4]2+
A.铜片接电源的正极
B.电镀过程中S0,2-向阳极移动
铜片
待镀
CuSO
铁制品
C.随铜单质析出电解质溶液中c(Cu2+)减小
溶液
D.加入氨水后可使铜缓慢析出,镀层更致密
化学试卷第2页(共9页)
同课章节目录
