3.1 溶液的形成 第2课时 课件(共17张PPT 内嵌视频 ) 2023-2024学年鲁教版化学九年级上册
文档属性
| 名称 | 3.1 溶液的形成 第2课时 课件(共17张PPT 内嵌视频 ) 2023-2024学年鲁教版化学九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 10.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-19 00:00:00 | ||
图片预览






文档简介
(共17张PPT)
第一节 溶液的形成
第2课时
思考问题
如果将大量的糖放入一杯水中,会产生什么现象?
物质能不能无限制地溶解在一定量的水中呢?它受什么因素影响?
1.知道饱和溶液与不饱和溶液的概念。会判断饱和溶液、不饱和溶液。
2.知道饱和溶液与不饱和溶液如何进行相互转化。
一、饱和溶液与不饱和溶液
饱和溶液:在 ,向 里加入某种溶质,当溶质___________溶解时所得到的溶液
一定温度下
一定量溶剂
1.饱和溶液与不饱和溶液的概念
不饱和溶液在 ,向 里加入某种溶质,当溶质___________溶解时所得到的溶液
一定温度下
一定量溶剂
不能继续
还能继续
饱和溶液 不饱和溶液
( )、( )、( )
( )、( )、( )
增加溶剂
减少溶质
改变温度
增加溶质
减少溶剂
改变温度
2.饱和溶液与不饱和溶液的转化
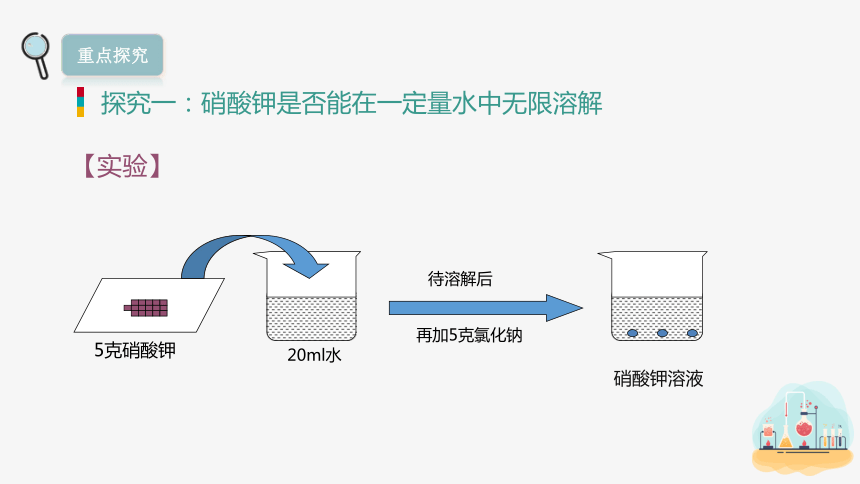
探究一:硝酸钾是否能在一定量水中无限溶解
【实验】
5克硝酸钾
20ml水
再加5克氯化钠
待溶解后
硝酸钾溶液
操作 加入5克硝酸钾,搅拌 再加入5克硝酸钾,搅拌
现象
结论
烧杯中形成无色溶液
烧杯底部有未溶解的固体
20ml水能完全溶解5g的硝酸钾
20ml水不能完全溶解10g的硝酸钾
【记录】
[思考交流]
1.通过上述操作和现象,你能得出什么结论?
一定温度下,硝酸钾在一定量的水中不能无限地溶解。
2.如何判断一种溶液是否饱和呢?
取适当体积的溶液,向这种溶液是添加同样的溶质,如果继续溶解,那么可以知道,溶液不是饱和溶液;如果溶质不溶解,说明此溶液是饱和溶液。
3.一定温度下,向某溶质的饱和溶液中加入其他溶质能溶解吗?
往装有少量硝酸钾饱和溶液的试管中加入1~2小粒KMnO4
加入少量高锰酸钾
结论:饱和溶液还能溶解其他溶质。
溶液变紫
4.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液吗?
①稀、浓溶液仅指一定量溶液中含有溶质的多少。
饱和溶液与不饱和溶液仅指在一定温度下,一定量溶剂中还能不能继续溶解某种溶质。溶液是否饱和与溶液的浓稀没有必然关系。
②对于不同溶质或同种溶质在不同温度下来说,饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
在相同温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液浓度大。
探究二:饱和溶液与不饱和溶液的互相转化
【实验】
【记录】
实验操作 实验现象
1. 在盛有10 mL水的小烧杯中,加入5 g硝酸钾,充分搅拌。观察现象。
2. 将上述得到的液体静置后,取少量上层清液于试管中,加入少量硝酸钾固体,充分振荡,观察现象。然后将该试管加热,观察现象。待试管冷却后观察,又有什么现象?
3. 在步骤1的小烧杯中再加入10 mL水并充分搅拌。观察现象。
有部分未溶解
固体未溶解;
加热后固体溶解;
冷却后又有固体析出
固体全部溶解
[思考交流]
1.上述实验中,属于饱和溶液、不饱和溶液有哪些?
饱和溶液
不饱和溶液
操作1所得溶液
操作2取得上层清液
操作2加入硝酸钾后溶液
操作2加热后溶液
操作2冷却后溶液
操作3加水后溶液
2.本实验中采用哪些方法实现了饱和溶液与不饱和溶液的相互转化?你还能想到其他方法吗?
不饱和溶液
饱和溶液
增加溶质、蒸发溶剂、改变温度
增加溶剂、减少溶质、改变温度
(_______________________)
(_______________________)
1.100℃硝酸钾饱和溶液冷却至30℃,滤去晶体后,所得溶液是________溶液(饱和、不饱和)。
2.把60℃时的氯化铵饱和溶液冷却到10℃,有氯化铵晶体析出,剩余溶液是( )
A.浓溶液 B.稀溶液
C.饱和溶液 D. 不饱和溶液
饱和
C
3.20℃时,要使硝酸钾不饱和溶液,变为饱和溶液,可采取下列措施中的( )
A.温度升高至60℃ B.加入硝酸钾
C.加入水 D.加入20℃硝酸钾饱和溶液
B
4.室温时,在各盛有10ml水的两个小烧杯中,分别缓缓地加入氯化钠和硝酸钾的固体,边加入边搅拌,到烧杯里有剩余固体,不能再溶解为止。这个实验说明 。
在一定温度下物质不能无限制地溶解到一定量的溶剂中
3.饱和溶液与不饱和溶液的相互转化。
1.不能再继续溶解某种溶质的溶液叫做该溶质的饱和溶液
2.还能继续溶解某种溶质的溶液叫做该溶质的不饱和溶液
饱和溶液 不饱和溶液
增加溶剂,减少溶质,改变温度
增加溶质,蒸发溶剂,改变温度
第一节 溶液的形成
第2课时
思考问题
如果将大量的糖放入一杯水中,会产生什么现象?
物质能不能无限制地溶解在一定量的水中呢?它受什么因素影响?
1.知道饱和溶液与不饱和溶液的概念。会判断饱和溶液、不饱和溶液。
2.知道饱和溶液与不饱和溶液如何进行相互转化。
一、饱和溶液与不饱和溶液
饱和溶液:在 ,向 里加入某种溶质,当溶质___________溶解时所得到的溶液
一定温度下
一定量溶剂
1.饱和溶液与不饱和溶液的概念
不饱和溶液在 ,向 里加入某种溶质,当溶质___________溶解时所得到的溶液
一定温度下
一定量溶剂
不能继续
还能继续
饱和溶液 不饱和溶液
( )、( )、( )
( )、( )、( )
增加溶剂
减少溶质
改变温度
增加溶质
减少溶剂
改变温度
2.饱和溶液与不饱和溶液的转化
探究一:硝酸钾是否能在一定量水中无限溶解
【实验】
5克硝酸钾
20ml水
再加5克氯化钠
待溶解后
硝酸钾溶液
操作 加入5克硝酸钾,搅拌 再加入5克硝酸钾,搅拌
现象
结论
烧杯中形成无色溶液
烧杯底部有未溶解的固体
20ml水能完全溶解5g的硝酸钾
20ml水不能完全溶解10g的硝酸钾
【记录】
[思考交流]
1.通过上述操作和现象,你能得出什么结论?
一定温度下,硝酸钾在一定量的水中不能无限地溶解。
2.如何判断一种溶液是否饱和呢?
取适当体积的溶液,向这种溶液是添加同样的溶质,如果继续溶解,那么可以知道,溶液不是饱和溶液;如果溶质不溶解,说明此溶液是饱和溶液。
3.一定温度下,向某溶质的饱和溶液中加入其他溶质能溶解吗?
往装有少量硝酸钾饱和溶液的试管中加入1~2小粒KMnO4
加入少量高锰酸钾
结论:饱和溶液还能溶解其他溶质。
溶液变紫
4.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液吗?
①稀、浓溶液仅指一定量溶液中含有溶质的多少。
饱和溶液与不饱和溶液仅指在一定温度下,一定量溶剂中还能不能继续溶解某种溶质。溶液是否饱和与溶液的浓稀没有必然关系。
②对于不同溶质或同种溶质在不同温度下来说,饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液;浓溶液不一定是饱和溶液,稀溶液不一定是不饱和溶液。
在相同温度下,同种溶剂、同种溶质的饱和溶液要比其不饱和溶液浓度大。
探究二:饱和溶液与不饱和溶液的互相转化
【实验】
【记录】
实验操作 实验现象
1. 在盛有10 mL水的小烧杯中,加入5 g硝酸钾,充分搅拌。观察现象。
2. 将上述得到的液体静置后,取少量上层清液于试管中,加入少量硝酸钾固体,充分振荡,观察现象。然后将该试管加热,观察现象。待试管冷却后观察,又有什么现象?
3. 在步骤1的小烧杯中再加入10 mL水并充分搅拌。观察现象。
有部分未溶解
固体未溶解;
加热后固体溶解;
冷却后又有固体析出
固体全部溶解
[思考交流]
1.上述实验中,属于饱和溶液、不饱和溶液有哪些?
饱和溶液
不饱和溶液
操作1所得溶液
操作2取得上层清液
操作2加入硝酸钾后溶液
操作2加热后溶液
操作2冷却后溶液
操作3加水后溶液
2.本实验中采用哪些方法实现了饱和溶液与不饱和溶液的相互转化?你还能想到其他方法吗?
不饱和溶液
饱和溶液
增加溶质、蒸发溶剂、改变温度
增加溶剂、减少溶质、改变温度
(_______________________)
(_______________________)
1.100℃硝酸钾饱和溶液冷却至30℃,滤去晶体后,所得溶液是________溶液(饱和、不饱和)。
2.把60℃时的氯化铵饱和溶液冷却到10℃,有氯化铵晶体析出,剩余溶液是( )
A.浓溶液 B.稀溶液
C.饱和溶液 D. 不饱和溶液
饱和
C
3.20℃时,要使硝酸钾不饱和溶液,变为饱和溶液,可采取下列措施中的( )
A.温度升高至60℃ B.加入硝酸钾
C.加入水 D.加入20℃硝酸钾饱和溶液
B
4.室温时,在各盛有10ml水的两个小烧杯中,分别缓缓地加入氯化钠和硝酸钾的固体,边加入边搅拌,到烧杯里有剩余固体,不能再溶解为止。这个实验说明 。
在一定温度下物质不能无限制地溶解到一定量的溶剂中
3.饱和溶液与不饱和溶液的相互转化。
1.不能再继续溶解某种溶质的溶液叫做该溶质的饱和溶液
2.还能继续溶解某种溶质的溶液叫做该溶质的不饱和溶液
饱和溶液 不饱和溶液
增加溶剂,减少溶质,改变温度
增加溶质,蒸发溶剂,改变温度
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
