3.2 溶液组成的定量表示 课件(共20张PPT) 2023-2024学年鲁教版化学九年级上册
文档属性
| 名称 | 3.2 溶液组成的定量表示 课件(共20张PPT) 2023-2024学年鲁教版化学九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 32.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-19 00:00:00 | ||
图片预览








文档简介
(共20张PPT)
第二节 溶液组成的定量表示
配制浓度不同的硫酸铜溶液
两瓶都是硫酸铜溶液,为什么颜色上却差距这么大呢?
【实验现象】三个试管内溶液颜色分别为深蓝,蓝色,淡蓝。
【实验步骤】
1.在三支试管中各加入5mL、10 mL、15mL水。
2.分别加入约1 g固体硫酸铜,充分振荡。
3.比较三种溶液的颜色。
1.能说出溶质质量分数的概念和表示的含义。
2.能进行有关溶质质量分数的简单计算。
3.初步学会配制一定质量分数的溶液。
4.能解释导致实验结果产生误差的原因。
一、溶质组成的表示方法
1.溶质的质量分数= 。
溶液的质量= + 。
溶质的质量= × 。
溶液的体积= ÷ 。
溶质的质量
溶液的质量
×100%
溶质的质量
溶剂的质量
溶液的质量
溶质的质量分数
溶液的质量
溶液的密度
2.公式变形
二、托盘天平的使用
1.用托盘天平称量前,首先应该把游码放在 处,检查天平是否左右平衡。如果天平未达到平衡,可以调节 ,使天平平衡。
2.称量时,把称量物放在 盘,砝码放在 盘。如果称量物与砝码位置放反了,称量结果将会受到怎样的影响?
3.称量药品质量时,在托盘各放来一张质量相等的纸称量固体,为了 ,称量有腐蚀性、易潮解物应放在 中称量。
零刻度
平衡螺母
左
右
烧杯
保护托盘,也为了防止试剂污染
三、量筒的使用
1.量筒使用时,量筒必须放 ,视线要与量筒内 保持水平,快接近刻度线时,改用 加液体。
2.为了减小误差,选用量筒时应根据所取液体量选用,不能过大或过小,如量取45mL的水应用 的量筒。为了防止量筒破裂,量筒不可量取 溶液,也不可进行 ,不能用作 。
平
凹液面最低处
胶头滴管
热
加热
反应容器
50mL
10g白糖
糖水
50ml蒸馏水
②
8g白糖
糖水
40ml蒸馏水
①
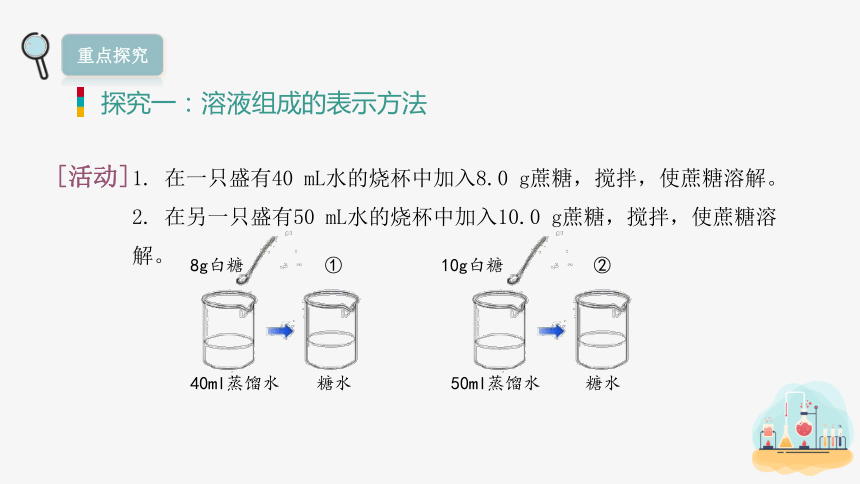
探究一:溶液组成的表示方法
[活动]
1. 在一只盛有40 mL水的烧杯中加入8.0 g蔗糖,搅拌,使蔗糖溶解。
2. 在另一只盛有50 mL水的烧杯中加入10.0 g蔗糖,搅拌,使蔗糖溶解。
[思考交流]
在上述两种溶液中,哪一种甜一些?你的依据是什么?
(1)溶质质量与溶剂的质量比
1.8g/(40mL×1g/mL)=1:5
2.10g/(50mL×1g/mL)=1:5
(2)溶质质量与溶液质量的比
1.8g/( 8g +40mL×1g/mL)=1:6
2.10g/(10g+50mL×1g/mL)=1:6
一样甜;因为溶质质量与溶剂的质量比值或溶质质量与溶液质量的比值都是相同的。
溶质质量分数的含义
5 % 的食盐溶液
①5g食盐溶于95g水形成的溶液。
②食盐的质量占整个食盐溶液的5%。
③将100g食盐溶液蒸干可以得到食盐5g。
④组成:M(食盐):M(水):M(食盐溶液) =5 : 95 : 100
溶质质量
溶液质量
讨论:5%表示的含义,你能说出多少个?
【例题1】 在农业生产上,常用质量分数为10%~20%的食盐溶液来选种。现要配制150kg质量分数为16%的食盐溶液,需要氯化钠和水的质量各是多少?
解:配制150kg16%的食盐溶液里需要氯化钠的质量为:
150kg×16% = 24kg
需要水的质量为: 150kg-24kg = 126kg
答:需要24kg氯化钠和126kg的水。
[溶质质量分数的相关计算]
【例题2】 化学实验室现有质量分数为98%的浓硫酸,但在实验中常需要用较稀的硫酸。要把50g上述浓硫酸稀释为质量为20%的硫酸,需要水的质量是多少?
解:设稀释时所加水的质量为x。
50g × 98% =(50g + x)× 20%
x = 195g
答:稀释时所用水的质量为195g。
计算原理:在溶液稀释过程中,溶质的质量不会发生变化。
【例题3】现有100g溶质质量分数为10%的氯化钠溶液,若是溶液的溶质质量分数增大一倍,应向此溶液中加入氯化钠_____g,或蒸发掉水_____g。
答:应加入的氯化钠12.5g,或蒸发掉水50g。
探究二:溶液的配制
【实验】
配制50g16%的氯化钠溶液
1.计算:需要食盐___克;需要水___克,即___mL。
2.称量:用_______称取食盐,用________量取水。
3.溶解:先将食盐放入烧杯中,然后将量取的水加入,并用______不断搅拌。
4.装瓶存放:将配好的溶液放入试剂瓶中,注意标签(注明药品的名称和溶质质量分数)向外。
【配制步骤】
8
42
42
托盘天平
50mL量筒
玻璃棒
【思考交流】
1.在配制过程中需要用到哪些实验仪器?
托盘天平
药匙
量筒
胶头滴管
烧杯
玻璃棒
该实验中,玻璃棒的作用是什么?
搅拌,加速溶解
2.本次试验中,有些小组的同学配制的溶液的溶质质量分数略大于或低于16%,你认为可能的原因是什么?
低于16%可能的原因:
大于16%可能的原因:
仰视读数;烧杯润湿;食盐不纯净;砝码缺损等。
俯视读数;水撒了;砝码生锈等。
1.家用食醋是含醋酸质量分数为10%的水溶液,其中的“10%”的含义是( )
A.100 g醋酸中含醋为10 g
B.100 g醋酸的水溶液中含醋酸10g
C.100 g水中含醋酸为10g
D.100 g醋酸的水溶液中含水10g
2.将80g质量分数为35%的浓盐酸,稀释成10%的稀盐酸,需加水的质量为( )
A.80g B.100g C.200g D.280g
B
C
3.用浓硫酸配制一定质量分数的稀硫酸,不需要用到的仪器是( )
A.托盘天平 B.烧杯 C.量筒 D.玻璃棒
4.在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是( )
A.用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码
B.用量筒量取蒸馏水读数时,仰视凹液面的最低处
C.将量筒中的水倒入烧杯时,有水洒出
D.将配好的氯化钠溶液转移到细口瓶时,不慎撒出部分溶液
A
B
5.现有200 g 溶质质量分数为10%的食盐溶液,若使溶液的溶质质量分数增加一倍,应蒸发掉多少水?
解:设应蒸发掉水的质量为x
答:应蒸发掉水100g水。
一、溶质的质量分数
1、概念:溶质质量与溶液质量之比。
2、计算公式:
溶质的质量分数=
溶质质量
溶液质量
×100%
二、配制一定溶质质量分数的溶液
计算
称量
溶解
装瓶存放
第二节 溶液组成的定量表示
配制浓度不同的硫酸铜溶液
两瓶都是硫酸铜溶液,为什么颜色上却差距这么大呢?
【实验现象】三个试管内溶液颜色分别为深蓝,蓝色,淡蓝。
【实验步骤】
1.在三支试管中各加入5mL、10 mL、15mL水。
2.分别加入约1 g固体硫酸铜,充分振荡。
3.比较三种溶液的颜色。
1.能说出溶质质量分数的概念和表示的含义。
2.能进行有关溶质质量分数的简单计算。
3.初步学会配制一定质量分数的溶液。
4.能解释导致实验结果产生误差的原因。
一、溶质组成的表示方法
1.溶质的质量分数= 。
溶液的质量= + 。
溶质的质量= × 。
溶液的体积= ÷ 。
溶质的质量
溶液的质量
×100%
溶质的质量
溶剂的质量
溶液的质量
溶质的质量分数
溶液的质量
溶液的密度
2.公式变形
二、托盘天平的使用
1.用托盘天平称量前,首先应该把游码放在 处,检查天平是否左右平衡。如果天平未达到平衡,可以调节 ,使天平平衡。
2.称量时,把称量物放在 盘,砝码放在 盘。如果称量物与砝码位置放反了,称量结果将会受到怎样的影响?
3.称量药品质量时,在托盘各放来一张质量相等的纸称量固体,为了 ,称量有腐蚀性、易潮解物应放在 中称量。
零刻度
平衡螺母
左
右
烧杯
保护托盘,也为了防止试剂污染
三、量筒的使用
1.量筒使用时,量筒必须放 ,视线要与量筒内 保持水平,快接近刻度线时,改用 加液体。
2.为了减小误差,选用量筒时应根据所取液体量选用,不能过大或过小,如量取45mL的水应用 的量筒。为了防止量筒破裂,量筒不可量取 溶液,也不可进行 ,不能用作 。
平
凹液面最低处
胶头滴管
热
加热
反应容器
50mL
10g白糖
糖水
50ml蒸馏水
②
8g白糖
糖水
40ml蒸馏水
①
探究一:溶液组成的表示方法
[活动]
1. 在一只盛有40 mL水的烧杯中加入8.0 g蔗糖,搅拌,使蔗糖溶解。
2. 在另一只盛有50 mL水的烧杯中加入10.0 g蔗糖,搅拌,使蔗糖溶解。
[思考交流]
在上述两种溶液中,哪一种甜一些?你的依据是什么?
(1)溶质质量与溶剂的质量比
1.8g/(40mL×1g/mL)=1:5
2.10g/(50mL×1g/mL)=1:5
(2)溶质质量与溶液质量的比
1.8g/( 8g +40mL×1g/mL)=1:6
2.10g/(10g+50mL×1g/mL)=1:6
一样甜;因为溶质质量与溶剂的质量比值或溶质质量与溶液质量的比值都是相同的。
溶质质量分数的含义
5 % 的食盐溶液
①5g食盐溶于95g水形成的溶液。
②食盐的质量占整个食盐溶液的5%。
③将100g食盐溶液蒸干可以得到食盐5g。
④组成:M(食盐):M(水):M(食盐溶液) =5 : 95 : 100
溶质质量
溶液质量
讨论:5%表示的含义,你能说出多少个?
【例题1】 在农业生产上,常用质量分数为10%~20%的食盐溶液来选种。现要配制150kg质量分数为16%的食盐溶液,需要氯化钠和水的质量各是多少?
解:配制150kg16%的食盐溶液里需要氯化钠的质量为:
150kg×16% = 24kg
需要水的质量为: 150kg-24kg = 126kg
答:需要24kg氯化钠和126kg的水。
[溶质质量分数的相关计算]
【例题2】 化学实验室现有质量分数为98%的浓硫酸,但在实验中常需要用较稀的硫酸。要把50g上述浓硫酸稀释为质量为20%的硫酸,需要水的质量是多少?
解:设稀释时所加水的质量为x。
50g × 98% =(50g + x)× 20%
x = 195g
答:稀释时所用水的质量为195g。
计算原理:在溶液稀释过程中,溶质的质量不会发生变化。
【例题3】现有100g溶质质量分数为10%的氯化钠溶液,若是溶液的溶质质量分数增大一倍,应向此溶液中加入氯化钠_____g,或蒸发掉水_____g。
答:应加入的氯化钠12.5g,或蒸发掉水50g。
探究二:溶液的配制
【实验】
配制50g16%的氯化钠溶液
1.计算:需要食盐___克;需要水___克,即___mL。
2.称量:用_______称取食盐,用________量取水。
3.溶解:先将食盐放入烧杯中,然后将量取的水加入,并用______不断搅拌。
4.装瓶存放:将配好的溶液放入试剂瓶中,注意标签(注明药品的名称和溶质质量分数)向外。
【配制步骤】
8
42
42
托盘天平
50mL量筒
玻璃棒
【思考交流】
1.在配制过程中需要用到哪些实验仪器?
托盘天平
药匙
量筒
胶头滴管
烧杯
玻璃棒
该实验中,玻璃棒的作用是什么?
搅拌,加速溶解
2.本次试验中,有些小组的同学配制的溶液的溶质质量分数略大于或低于16%,你认为可能的原因是什么?
低于16%可能的原因:
大于16%可能的原因:
仰视读数;烧杯润湿;食盐不纯净;砝码缺损等。
俯视读数;水撒了;砝码生锈等。
1.家用食醋是含醋酸质量分数为10%的水溶液,其中的“10%”的含义是( )
A.100 g醋酸中含醋为10 g
B.100 g醋酸的水溶液中含醋酸10g
C.100 g水中含醋酸为10g
D.100 g醋酸的水溶液中含水10g
2.将80g质量分数为35%的浓盐酸,稀释成10%的稀盐酸,需加水的质量为( )
A.80g B.100g C.200g D.280g
B
C
3.用浓硫酸配制一定质量分数的稀硫酸,不需要用到的仪器是( )
A.托盘天平 B.烧杯 C.量筒 D.玻璃棒
4.在配制一定质量分数的氯化钠溶液时,下列出现的操作失误,会引起所配溶液的溶质质量分数降低的是( )
A.用托盘天平称量氯化钠时,将砝码放在左盘,但未使用游码
B.用量筒量取蒸馏水读数时,仰视凹液面的最低处
C.将量筒中的水倒入烧杯时,有水洒出
D.将配好的氯化钠溶液转移到细口瓶时,不慎撒出部分溶液
A
B
5.现有200 g 溶质质量分数为10%的食盐溶液,若使溶液的溶质质量分数增加一倍,应蒸发掉多少水?
解:设应蒸发掉水的质量为x
答:应蒸发掉水100g水。
一、溶质的质量分数
1、概念:溶质质量与溶液质量之比。
2、计算公式:
溶质的质量分数=
溶质质量
溶液质量
×100%
二、配制一定溶质质量分数的溶液
计算
称量
溶解
装瓶存放
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
