山东省德州市2014-2015学年高二6月月考化学试题
文档属性
| 名称 | 山东省德州市2014-2015学年高二6月月考化学试题 |  | |
| 格式 | zip | ||
| 文件大小 | 96.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2015-07-01 16:45:41 | ||
图片预览


文档简介
本资料来自于资源最齐全的21世纪教育网www.21cnjy.com
高二阶段测试化学试题
2015年6月
一、选择题(每小题只有一个选项符合题意。每小题3分,共54分)
1.中学生应该能够正确认识一些与化学有关的问题。下列说法中,正确的是( )
A.用铝锅炒菜比用铁锅好
B.为防止身体发胖,炒菜时不放油
C.为了使火腿肠颜色更鲜红,可多加一些亚硝酸钠
D.碘盐中的碘是防止人体缺碘而加的营养强化剂,能预防地方性甲状腺肿
2.硅单质及其化合物在材料领域中一直扮演着主要角色。下列叙述中,不正确的是( )
A.石英可用来制作工艺品 B.硅酸盐是陶瓷的主要成分
C.硅单质是制造玻璃的主要原料 D.硅单质可用来制造太阳能电池
3.下列物质中,从化学键的角度看,有一种与其他三种明显不同,这种物质是( )
A.NaOH B.CH4 C.SO2 D.H2O
4.据报道,放射性同位素钬可用于治疗肝癌。原子核内中子数是( )
A.32 B.67 C.99 D.166 21·cn·jy·com
5.用固体NaOH配制一定物质的量浓度的NaOH溶液,下列操作正确的是( )
A.称量时,将固体NaOH直接放在天平左盘上
B.将称量好的固体NaOH放入容量瓶中,加蒸馏水溶解
C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分
D.在烧杯中溶解固体NaOH得到溶液,冷却到室温后再转移至容量瓶中
6.在一定条件下,对于密闭容器中进行的可逆反应:2SO2(g) + O2(g) 2SO3(g) 。
下列说法中,表明这一反应已经达到化学平衡状态的是( )
A.正、逆反应速率都等于零 B.SO2、O2、SO3的浓度相等
C.SO2、O2、SO3的浓度不再变化 D.SO2、O2、SO3在密闭容器中共存
7.下列各组物质中,互为同分异构体的是( )
A.红磷和白磷 B.C和 C
C.C2H4和C3H6 D. ( http: / / www.21cnjy.com ) 和
8.下列叙述中,指定粒子的数目约为6.02×1023的是( )
A.1.6 g CH4中含有的电子数
B.1 mol/L的稀硫酸100 mL中含有H+的数目
C.24 g金属镁与足量的盐酸反应转移的电子数
D.标准状况下,22.4 L H2和CO混合气体中的原子数
9.对于锌、铜和稀硫酸组成的原电池(如右图),下列有关说法不正确的是( )
A.Zn是负极
B.负极上发生氧化反应
C.负极发生的反应是 Zn - 2e- ==
D.正极发生的反应是+ 2e- == Cu
10.下列实验中,有白色沉淀产生且最终不会消失的是( )
A.向FeCl2溶液中逐滴滴入NaOH溶液
B.向硝酸银溶液中逐滴滴入氨水,直至过量
C.向澄清石灰水中通入二氧化碳,直至过量
D.向AlCl3溶液中逐滴滴入氨水,直至过量
11.下列陈述Ⅰ、Ⅱ均正确且有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A Fe3+有氧化性 FeCl3溶液可溶解废旧电路板中的铜
B SiO2有导电性 SiO2可用于制备光导纤维
C NH3有还原性 NH3可用H2SO4吸收
D 浓HNO3有酸性 浓HNO3不可用铁制容器盛放
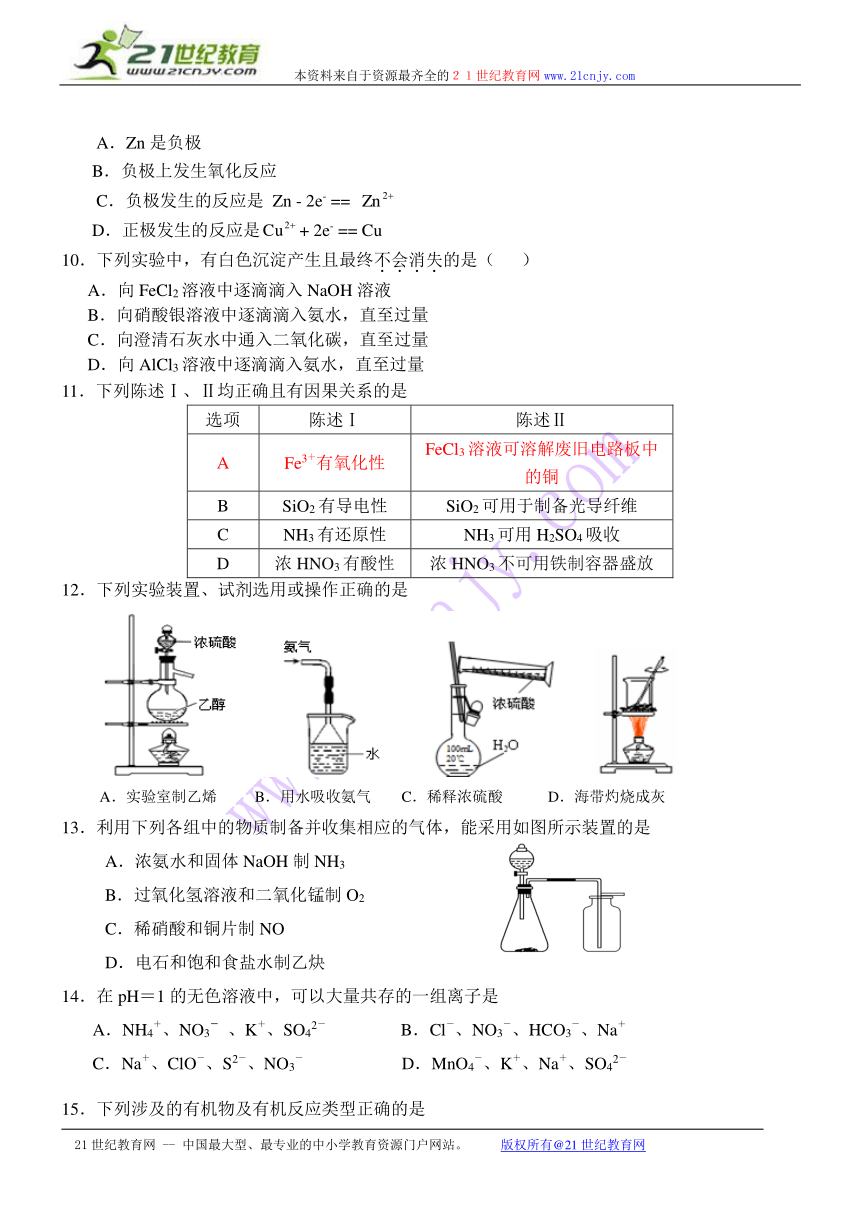
12.下列实验装置、试剂选用或操作正确的是
( http: / / www.21cnjy.com )
A.实验室制乙烯 B.用水吸收氨气 C.稀释浓硫酸 D.海带灼烧成灰
13.利用下列各组中的物质制备并收集相应的气体,能采用如图所示装置的是
A.浓氨水和固体NaOH制NH3
B.过氧化氢溶液和二氧化锰制O2
C.稀硝酸和铜片制NO
D.电石和饱和食盐水制乙炔
14.在pH=1的无色溶液中,可以大量共存的一组离子是
A.NH4+、NO3- 、K+、SO42- B.Cl-、NO3-、HCO3-、Na+21世纪教育网版权所有
C.Na+、ClO-、S2-、NO3- D.MnO4-、K+、Na+、SO42-21教育网
15.下列涉及的有机物及有机反应类型正确的是
A.苯与甲苯均可以使酸性高锰酸钾褪色
B.葡萄糖、蛋白质、纤维素都能发生水解反应
C.甲醛,氯乙烯,乙二醇均可做加聚反应的单体
D.乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应
16.将下表中的Y物质加入或通入X物质中,在反应所得溶液中一定只含一种溶质的是
选项 X物质 Y物质
A 蒸馏水 Na
B NaOH溶液 CO2
C NaOH溶液 Cl2
D 稀硝酸 Fe
17.下列反应中,离子方程式正确的是
A.大理石溶于盐酸中:CO32-+2H+= CO2↑+H2O
B.AlCl3溶液中加入过量氨水:Al3++3NH3 H2O = Al(OH)3↓+ 3NH4+
C.硫酸镁溶液与氢氧化钡溶液混合:SO42- + Ba2+ = BaSO4↓
D.氯化铁溶液中加入铜片:Fe3++Cu = Fe2++Cu2+
18.绿原酸是咖啡的热水提取液的成分之一,绿原酸结构简式如下:
( http: / / www.21cnjy.com )
下列关于绿原酸判断不正确的是
A.分子中所有的碳原子不可能在同一平面内
B.1mol绿原酸与足量溴水反应,最多消耗4molBr2
C.绿原酸既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.1mol绿原酸与足量NaOH溶液反应,最多消耗8mol NaOH
第Ⅱ卷(非选择题 共46分)
19. (12分)W.X.Y.Z是原子序数依次增大的同一短同期元素,W.X是金属元素,Y.Z是非金属元素。【来源:21·世纪·教育·网】
(1)W.X各自的最高价氧化物对应的水化 ( http: / / www.21cnjy.com )物可以反应生盐和水该反应的离子方程式为_______ 。21·世纪*教育网
(2)W与Y 可形成化合物W2Y,该化合物为 (填离子化合物或共价化合物)
(3)Y的低价氧化物通入Z单质的水溶液中, ( http: / / www.21cnjy.com )发生反应的离子方程式为__________ 。www-2-1-cnjy-com
(4)比较Y.Z气态氢化物的稳定性 > (用化学式表示)
(5)W.X.Y.Z四种元素简单离子的离子半径由大到小的顺序是:
> > > 。(用化学式表示)
(6)Z的最高价氧化物为无色液体,该物质与 ( http: / / www.21cnjy.com )一定量水混合得到一种稀溶液,试写出该反应的化学方程式:____________ ___________。www.21-cn-jy.com
20.(12分)已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中装置进行实验。2-1-c-n-j-y
( http: / / www.21cnjy.com )
主要实验步骤如下:①按图组装仪器,并检查装置的气密性
②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到bg
④从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为dg
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明
(2)装置中干燥管B的作用是
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的
结果 (填高、偏低或不变)
(4)步骤⑤的目的是 ( http: / / www.21cnjy.com )
(5)步骤⑦的目的是
(6)该试样中纯碱的质量分数的计算式为
21.(16分)以聚甲基丙烯酸羟乙基酯(HEMA)为材料,可制成软性隐形眼镜。其合成路线图如下:
( http: / / www.21cnjy.com )
已知:
回答以下问题:
(1)A的官能团的名称是
(2)反应①的反应类型是
(3)写出下列反应的化学方程式
反应② 2·1·c·n·j·y
反应③ 21*cnjy*com
(4)下列说法正确的是(选填字母)
a. G可以使酸性高锰酸钾褪色
b.F的核磁共振氢谱有三种峰,其峰面积之比为1:2:
c.D可以发生银镜反应
(5)F可以与氢气发生加成反应,加成后的产物有多种同分异构体,其中含-COO-的有
种,写出其中一种的结构简式 。
22. (6分)向V mL含0.2 ( http: / / www.21cnjy.com )6 mol HNO3的硝酸溶液中加入3.2 g Cu粉(HNO3的还原产物只有NO2和NO)。反应结束后,将所得溶液加水稀释至1000 mL,【出处:21教育名师】
测得c(NO3-)= 0.2 mol/L。则:
(1)稀释后的溶液中HNO3的物质的量浓度为________________。
(2)被还原的HNO3得到电子的物质的量为______________。
(3)生成NO气体的体积为 ______________mL(标准状况)。
化学答案及评分参考
选择题(每小题3分,共54分)
题号 1 2 3 4 5 6 7 8 9 10
答案 D C A C D C D A D D
题号 11 12 13 14 15 16 17 18
答案 A B B A D A B D
19.(12分) (1)OH-+Al(OH)3=[ Al(OH)4]-
(2) 离子化合物
(3)SO2+Cl2+2H2O=4H++SO42—+Cl—
(4) HCl>H2S21cnjy.com
(5) S2—>Cl—>Na+>Al3+
(6)Cl2O7+H2O=2HClO4
20、(12分)(1)样品重,砝码轻
(2)防止空气中的CO2和水气进入U型管中
(3)偏高
(4)把反应产生的CO2全部导入U型管中
(5)判断反应产生的CO2是否全部排出,并被U型管中的碱石灰吸收
(6)【来源:21cnj*y.co*m】
21.(16分)
(1)双键(2分)
(2)消去反应(2分)
(3) (3分)
(3分)
(4)b、c(2分)
(5)6(2分)
(写一种即可得2分)
22. (1)0.1 mol/L(2)0.1 mol(3)448
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
高二阶段测试化学试题
2015年6月
一、选择题(每小题只有一个选项符合题意。每小题3分,共54分)
1.中学生应该能够正确认识一些与化学有关的问题。下列说法中,正确的是( )
A.用铝锅炒菜比用铁锅好
B.为防止身体发胖,炒菜时不放油
C.为了使火腿肠颜色更鲜红,可多加一些亚硝酸钠
D.碘盐中的碘是防止人体缺碘而加的营养强化剂,能预防地方性甲状腺肿
2.硅单质及其化合物在材料领域中一直扮演着主要角色。下列叙述中,不正确的是( )
A.石英可用来制作工艺品 B.硅酸盐是陶瓷的主要成分
C.硅单质是制造玻璃的主要原料 D.硅单质可用来制造太阳能电池
3.下列物质中,从化学键的角度看,有一种与其他三种明显不同,这种物质是( )
A.NaOH B.CH4 C.SO2 D.H2O
4.据报道,放射性同位素钬可用于治疗肝癌。原子核内中子数是( )
A.32 B.67 C.99 D.166 21·cn·jy·com
5.用固体NaOH配制一定物质的量浓度的NaOH溶液,下列操作正确的是( )
A.称量时,将固体NaOH直接放在天平左盘上
B.将称量好的固体NaOH放入容量瓶中,加蒸馏水溶解
C.定容时如果加水超过了刻度线,用胶头滴管直接吸出多余部分
D.在烧杯中溶解固体NaOH得到溶液,冷却到室温后再转移至容量瓶中
6.在一定条件下,对于密闭容器中进行的可逆反应:2SO2(g) + O2(g) 2SO3(g) 。
下列说法中,表明这一反应已经达到化学平衡状态的是( )
A.正、逆反应速率都等于零 B.SO2、O2、SO3的浓度相等
C.SO2、O2、SO3的浓度不再变化 D.SO2、O2、SO3在密闭容器中共存
7.下列各组物质中,互为同分异构体的是( )
A.红磷和白磷 B.C和 C
C.C2H4和C3H6 D. ( http: / / www.21cnjy.com ) 和
8.下列叙述中,指定粒子的数目约为6.02×1023的是( )
A.1.6 g CH4中含有的电子数
B.1 mol/L的稀硫酸100 mL中含有H+的数目
C.24 g金属镁与足量的盐酸反应转移的电子数
D.标准状况下,22.4 L H2和CO混合气体中的原子数
9.对于锌、铜和稀硫酸组成的原电池(如右图),下列有关说法不正确的是( )
A.Zn是负极
B.负极上发生氧化反应
C.负极发生的反应是 Zn - 2e- ==
D.正极发生的反应是+ 2e- == Cu
10.下列实验中,有白色沉淀产生且最终不会消失的是( )
A.向FeCl2溶液中逐滴滴入NaOH溶液
B.向硝酸银溶液中逐滴滴入氨水,直至过量
C.向澄清石灰水中通入二氧化碳,直至过量
D.向AlCl3溶液中逐滴滴入氨水,直至过量
11.下列陈述Ⅰ、Ⅱ均正确且有因果关系的是
选项 陈述Ⅰ 陈述Ⅱ
A Fe3+有氧化性 FeCl3溶液可溶解废旧电路板中的铜
B SiO2有导电性 SiO2可用于制备光导纤维
C NH3有还原性 NH3可用H2SO4吸收
D 浓HNO3有酸性 浓HNO3不可用铁制容器盛放
12.下列实验装置、试剂选用或操作正确的是
( http: / / www.21cnjy.com )
A.实验室制乙烯 B.用水吸收氨气 C.稀释浓硫酸 D.海带灼烧成灰
13.利用下列各组中的物质制备并收集相应的气体,能采用如图所示装置的是
A.浓氨水和固体NaOH制NH3
B.过氧化氢溶液和二氧化锰制O2
C.稀硝酸和铜片制NO
D.电石和饱和食盐水制乙炔
14.在pH=1的无色溶液中,可以大量共存的一组离子是
A.NH4+、NO3- 、K+、SO42- B.Cl-、NO3-、HCO3-、Na+21世纪教育网版权所有
C.Na+、ClO-、S2-、NO3- D.MnO4-、K+、Na+、SO42-21教育网
15.下列涉及的有机物及有机反应类型正确的是
A.苯与甲苯均可以使酸性高锰酸钾褪色
B.葡萄糖、蛋白质、纤维素都能发生水解反应
C.甲醛,氯乙烯,乙二醇均可做加聚反应的单体
D.乙烯分子与苯分子中碳碳键不同,但二者都能发生加成反应
16.将下表中的Y物质加入或通入X物质中,在反应所得溶液中一定只含一种溶质的是
选项 X物质 Y物质
A 蒸馏水 Na
B NaOH溶液 CO2
C NaOH溶液 Cl2
D 稀硝酸 Fe
17.下列反应中,离子方程式正确的是
A.大理石溶于盐酸中:CO32-+2H+= CO2↑+H2O
B.AlCl3溶液中加入过量氨水:Al3++3NH3 H2O = Al(OH)3↓+ 3NH4+
C.硫酸镁溶液与氢氧化钡溶液混合:SO42- + Ba2+ = BaSO4↓
D.氯化铁溶液中加入铜片:Fe3++Cu = Fe2++Cu2+
18.绿原酸是咖啡的热水提取液的成分之一,绿原酸结构简式如下:
( http: / / www.21cnjy.com )
下列关于绿原酸判断不正确的是
A.分子中所有的碳原子不可能在同一平面内
B.1mol绿原酸与足量溴水反应,最多消耗4molBr2
C.绿原酸既可以催化加氢,又可以使酸性KMnO4溶液褪色
D.1mol绿原酸与足量NaOH溶液反应,最多消耗8mol NaOH
第Ⅱ卷(非选择题 共46分)
19. (12分)W.X.Y.Z是原子序数依次增大的同一短同期元素,W.X是金属元素,Y.Z是非金属元素。【来源:21·世纪·教育·网】
(1)W.X各自的最高价氧化物对应的水化 ( http: / / www.21cnjy.com )物可以反应生盐和水该反应的离子方程式为_______ 。21·世纪*教育网
(2)W与Y 可形成化合物W2Y,该化合物为 (填离子化合物或共价化合物)
(3)Y的低价氧化物通入Z单质的水溶液中, ( http: / / www.21cnjy.com )发生反应的离子方程式为__________ 。www-2-1-cnjy-com
(4)比较Y.Z气态氢化物的稳定性 > (用化学式表示)
(5)W.X.Y.Z四种元素简单离子的离子半径由大到小的顺序是:
> > > 。(用化学式表示)
(6)Z的最高价氧化物为无色液体,该物质与 ( http: / / www.21cnjy.com )一定量水混合得到一种稀溶液,试写出该反应的化学方程式:____________ ___________。www.21-cn-jy.com
20.(12分)已知某纯碱试样中含有NaCl杂质,为测定试样中纯碱的质量分数,可用下图中装置进行实验。2-1-c-n-j-y
( http: / / www.21cnjy.com )
主要实验步骤如下:①按图组装仪器,并检查装置的气密性
②将ag试样放入锥形瓶中,加适量蒸馏水溶解,得到试样溶液
③称量盛有碱石灰的U型管的质量,得到bg
④从分液漏斗滴入6mol·L-1的硫酸,直到不再产生气体时为止
⑤从导管A处缓缓鼓入一定量的空气
⑥再次称量盛有碱石灰的U型管的质量,得到cg
⑦重复步骤⑤和⑥的操作,直到U型管的质量基本不变,为dg
请填空和回答问题:
(1)在用托盘天平称量样品时,如果天平的指针向左偏转,说明
(2)装置中干燥管B的作用是
(3)如果将分液漏斗中的硫酸换成浓度相同的盐酸,测试的
结果 (填高、偏低或不变)
(4)步骤⑤的目的是 ( http: / / www.21cnjy.com )
(5)步骤⑦的目的是
(6)该试样中纯碱的质量分数的计算式为
21.(16分)以聚甲基丙烯酸羟乙基酯(HEMA)为材料,可制成软性隐形眼镜。其合成路线图如下:
( http: / / www.21cnjy.com )
已知:
回答以下问题:
(1)A的官能团的名称是
(2)反应①的反应类型是
(3)写出下列反应的化学方程式
反应② 2·1·c·n·j·y
反应③ 21*cnjy*com
(4)下列说法正确的是(选填字母)
a. G可以使酸性高锰酸钾褪色
b.F的核磁共振氢谱有三种峰,其峰面积之比为1:2:
c.D可以发生银镜反应
(5)F可以与氢气发生加成反应,加成后的产物有多种同分异构体,其中含-COO-的有
种,写出其中一种的结构简式 。
22. (6分)向V mL含0.2 ( http: / / www.21cnjy.com )6 mol HNO3的硝酸溶液中加入3.2 g Cu粉(HNO3的还原产物只有NO2和NO)。反应结束后,将所得溶液加水稀释至1000 mL,【出处:21教育名师】
测得c(NO3-)= 0.2 mol/L。则:
(1)稀释后的溶液中HNO3的物质的量浓度为________________。
(2)被还原的HNO3得到电子的物质的量为______________。
(3)生成NO气体的体积为 ______________mL(标准状况)。
化学答案及评分参考
选择题(每小题3分,共54分)
题号 1 2 3 4 5 6 7 8 9 10
答案 D C A C D C D A D D
题号 11 12 13 14 15 16 17 18
答案 A B B A D A B D
19.(12分) (1)OH-+Al(OH)3=[ Al(OH)4]-
(2) 离子化合物
(3)SO2+Cl2+2H2O=4H++SO42—+Cl—
(4) HCl>H2S21cnjy.com
(5) S2—>Cl—>Na+>Al3+
(6)Cl2O7+H2O=2HClO4
20、(12分)(1)样品重,砝码轻
(2)防止空气中的CO2和水气进入U型管中
(3)偏高
(4)把反应产生的CO2全部导入U型管中
(5)判断反应产生的CO2是否全部排出,并被U型管中的碱石灰吸收
(6)【来源:21cnj*y.co*m】
21.(16分)
(1)双键(2分)
(2)消去反应(2分)
(3) (3分)
(3分)
(4)b、c(2分)
(5)6(2分)
(写一种即可得2分)
22. (1)0.1 mol/L(2)0.1 mol(3)448
21世纪教育网 -- 中国最大型、最专业的中小学教育资源门户网站。 版权所有@21世纪教育网
