1.2.2离子反应导学案(含解析)2023-2024学年高一上学期化学人教版(2019)必修第一册
文档属性
| 名称 | 1.2.2离子反应导学案(含解析)2023-2024学年高一上学期化学人教版(2019)必修第一册 |

|
|
| 格式 | DOC | ||
| 文件大小 | 603.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-20 00:00:00 | ||
图片预览




文档简介
离子反应
【核心素养发展目标】
1.通过实验事实认识离子反应,并掌握离子反应发生的条件,增强化学核心素养中的变化观念意识
2.掌握离子方程式的书写方法及正误判断,能用离子方程式正确表示典型物质的主要化学性质,促进证据推理与模型认知化学核心素养的发展
【主干知识梳理】
一、离子反应与离子方程式书写
1.离子反应
(1)离子反应的实验探究
实验步骤 向盛有2ml Na2SO4稀溶液的试管中加入2ml BaCl2稀溶液,观察现象并分析
实验装置
实验现象 有白色沉淀生成
化学方程式 Na2SO4+BaCl2===BaSO4↓+2NaCl
微观分析 Na2SO4和BaCl2的电离方程式 混合前两种溶液中的离子 混合后溶液中的离子
BaCl2===Ba2++2Cl-Na2SO4===SO+2Na+ BaCl2溶液:Ba2+、Cl-Na2SO4溶液:Na+、SO Na+、Cl-
实验结论 当Na2SO4稀溶液与BaCl2溶稀溶液混合时,Na+与Cl-都没有发生化学反应;Ba2+而SO与发生了化学反应,生成难溶的BaSO4白色沉淀
反应本质 Ba2+、SO结合成BaSO4白色沉淀,即:Ba2++SO===BaSO4↓
(2)离子反应的定义:电解质在溶液中的反应实质上是离子之间的反应,这样的反应属于离子反应
(3)实质:
①从微观角度,酸、碱、盐在水溶液中发生的复分解反应,实质上是两种电解质在溶液中相互交换离子的反应②离子反应使溶液中某些离子的浓度减小
2.离子方程式
(1)定义:用实际参加反应的离子符号来表示反应的式子叫做离子方程式
(2)书写步骤——以Na2SO4溶液和BaCl2溶液反应为例
①写:正确书写反应的化学方程式:Na2SO4+BaCl2===BaSO4↓+2NaCl
②拆:把易溶于水且易电离的物质(如:强酸、强碱和大多数可溶性的盐)拆写成离子的形式,难溶的物质、气
体和水等仍用化学式表示:2Na++SO+Ba2++2Cl-===BaSO4↓+2Na++2Cl-
③删:等量删去方程式两边不参加反应的离子,并将化学计量数化为最简整数比:Ba2++SO===BaSO4↓
④查:检查方程式两边各元素的原子个数和电荷总数是否相等
【微点拨】
①书写步骤:写(是基础)拆(是关键)删(是途径)查(是保证)
②书写关键:单质、氧化物在离子方程式中一律写化学式;弱酸(如:HF、H2S、HClO、H2SO3等)、弱碱(如:NH3·H2O)、水等难电离的物质必须写化学式;难溶于水的物质(如:CaCO3、BaSO3、BaSO4,Fe(OH)3等)必须写化学式,气体、非电解质必须写化学式
【对点训练1】
1.写出下列反应的化学方程式并将其改写成离子方程式
(1)写:CuSO4 + NaOH —— _____________________ (2)写:Fe(OH)3 + H2SO4 —— ____________________
拆:______________________________________ 拆:______________________________________
删:______________________________________ 删:______________________________________
(3)写:CuO + HNO3—— ____________________ (4)写:Fe + HCl—— ______________________
拆:______________________________________ 拆:______________________________________
删:______________________________________ 删:______________________________________
(5)写:3Cu+8HNO3===3Cu(NO3)2+2NO↑+4H2O (6)写:CaCO3+2CH3COOH===(CH3COO)2Ca+CO2↑+H2O
拆:______________________________________ 拆:______________________________________
删:______________________________________ 删:______________________________________
2.写出下列反应的化学方程式和离子方程式,思考两种方程式在表示某一类反应时,表达的含义有什么不同
溶液中反应物 化学方程式 离子方程式
HCl+NaOH
HCl+KOH
H2SO4+NaOH
H2SO4+KOH
离子方程式的意义 离子方程式不仅可以表示某个具体的化学反应,还可以表示同一类型的离子反应
3.将下列化学方程式改写成离子方程式,并思考是否所有的酸碱中和反应都能用H++OH-===H2O来表示?
溶液中反应物 化学方程式 离子方程式
HCl+Cu(OH)2
HNO3+NH3 H2O
HF+NaOH
H2SO4+Ba(OH)2
结论 H++OH-===H2O表示强酸与强碱反应生成可溶性盐和H2O的一类反应
4.下列各组物质间的反应中,不属于离子反应的是( )
A.锌和稀硫酸反应 B.氯化钠溶液和硝酸银溶液反应
C.木炭和氧气反应 D.烧碱溶液和氯化铁溶液反应
5.离子方程式Ba2++SO===BaSO4↓可能表示( )
①可溶性钡盐溶液与可溶性硫酸盐溶液之间的反应 ②氢氧化钡溶液与可溶性硫酸盐溶液之间的反应
③稀硫酸与可溶性钡盐溶液之间的反应 ④氢氧化钡溶液与稀硫酸反应
A.①② B.①②④ C.②③ D.①②③
6.下列反应可用离子方程式H++OH-===H2O来表示的是( )
A.氢氧化钡和稀硫酸的反应 B.硫酸氢钠和氢氧化钾的反应
C.碳酸氢钠和氢氧化钾的反应 D.氢氧化钠溶液与醋酸的反应
7.下列反应①和②可以用同一离子方程式表示的是( )
A.①稀盐酸+碳酸钠溶液;②稀盐酸+碳酸氢钠溶液
B.①氢氧化钠溶液+稀盐酸;②氢氧化钡溶液+稀硫酸
C.①氯化钡溶液+稀硫酸;②氢氧化钡溶液+硫酸钠溶液
D.①稀盐酸+碳酸钙粉末;②稀硫酸+碳酸钠溶液
8.只能表示一个化学反应的离子方程式是( )
A.H++OH-===H2O B.2H++CO===H2O+CO2↑
C.Zn(OH)2+2H+===Zn2++2H2O D.Cu2++2OH-+Ba2++SO===BaSO4↓+Cu(OH)2↓
9.下列化学方程式对应的离子方程式正确的是( )
A.CuCO3+2NaOH===Cu(OH)2↓+Na2CO3 Cu2++2OH-===Cu(OH)2↓
B.Ba(OH)2+H2SO4===BaSO4↓+2H2O Ba2++SO===BaSO4↓
C.AgNO3+NaCl===AgCl↓+NaNO3 Ag++Cl-===AgCl↓
D.Cu(OH)2+H2SO4===CuSO4+2H2O OH-+H+===H2O
二、离子方程式的拆写原则
1.常见物质在离子方程式中的书写要求
书写要求 物质类型
需拆成离子的物质(写离子符号) ①强酸:HCl、H2SO4、HNO3等
②强碱:KOH、NaOH、Ba(OH)2等
③可溶性盐:NaCl、K2SO4、NaNO3等
不能拆成离子的物质(写化学式) ①单质;②气体;③氧化物
④难溶物:Cu(OH)2、BaSO4、AgCl等
⑤难电离的物质:CH3COOH、NH3·H2O、H2O等
⑥非电解质:乙醇等
⑦浓硫酸
2.对于微溶物的处理有三种情况
(1)生成物中有微溶物[Ag2SO4、CaSO4、Ca(OH)2、MgCO3]时,微溶物写化学式并标“↓”
如:Na2SO4溶液中加入AgNO3 溶液:2Ag++SO===Ag2SO4↓
(2)当反应物里有微溶物处于溶液状态(稀溶液),应写成离子的形式
如:CO2气体通入澄清石灰水中:CO2+Ca2++2OH-===CaCO3↓+H2O
(3)当反应物里有微溶物处于悬浊液或固态时,应写成化学式
如:用石灰乳制漂白粉的反应:2Ca(OH)2+2Cl2===2Ca2++2Cl-+2ClO-+H2O
3.对氨水的处理
(1)作反应物时用NH3 H2O
如:硫酸铝溶液中加入氨水:Al3++3NH3 H2O===Al(OH)3↓+3NH
(2)作生成物时,若加热或浓溶液时写成NH3↑+H2O;无特殊说明写NH3 H2O
如:浓NaOH溶液中加入硫酸铵固体:OH-+NH===NH3↑+H2O
(NH4)2SO4与NaOH两溶液混合加热:NH+OH-NH3↑+H2O
NH4Cl与NaOH两稀溶液混合:NH+OH-===NH3 H2O
4.固体与固体间反应不能写离子方程式,如:NH4Cl固体和Ca(OH)2固体混合加热,虽然也有离子和离子反应,但不能写成离子方程式,只能写化学方程式
5.浓H2SO4与固体反应不能写离子方程式,如:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
6.多元弱酸的酸式酸根离子,在离子方程式中不能拆写
如:NaHCO3与盐酸反应的离子方程式为HCO+H+===CO2↑+H2O。
【对点训练2】
1.能正确表示下列化学反应的离子方程式的是( )
A.氢氧化钡溶液与稀硝酸反应:OH-+H+===H2O
B.澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+===Ca2++2H2O
C.醋酸与氢氧化钠溶液反应:H++OH-===H2O
D.碳酸钡溶于稀盐酸中:CO+2H+===H2O+CO2↑
2.下列离子方程式书写错误的是( )
A.Ba(OH)2溶液与盐酸反应:OH-+H+===H2O
B.Al与CuSO4溶液反应:Al+Cu2+===Cu+Al3+
C.硫酸铵溶液和氢氧化钡溶液反应的离子方程式:2NH+SO+Ba2++2OH-===2NH3·H2O+BaSO4↓
D.向氯化钠溶液中滴加硝酸银溶液:Cl-+Ag+===AgCl↓
3.离子方程式BaCO3+2H+===CO2↑+H2O+Ba2+中的H+不能代表的物质是( )
①HCl ②H2SO4 ③HNO3 ④NaHSO4 ⑤CH3COOH
A.①③ B.①④⑤ C.②④⑤ D.①⑤
三、离子反应发生的条件
1.复分解型离子反应发生的条件
实验过程
实验现象 ① ② ③
生成蓝色沉淀 溶液红色消失 产生气泡
离子方程式 Cu2++2OH-===Cu(OH)2↓ H++OH-===H2O CO+2H+===CO2↑+H2O
酸、碱、盐在水溶液中发生的复分解反应,实质上就是两种电解质在溶液中相互交换离子的反应,这类离子反应发生的条件是:生成难溶物(沉淀)、生成挥发性的物质(气体)、生成难电离的物质(弱酸、弱碱和水),只要具备上述条件之一,反应就能发生
2.置换反应的条件:活泼金属与酸反应、活泼金属与盐反应等
如:Zn与稀H2SO4反应的离子方程式为Zn+2H+===Zn2++H2↑
Zn与CuSO4溶液反应的离子方程式为Zn+Cu2+===Cu+Zn2+
【对点训练3】
1.下列溶液混合后,不会发生离子反应的是( )
A.硝酸钡溶液和硫酸钠溶液 B.醋酸钠溶液和稀硫酸
C.碳酸钾溶液和硫酸氢钠溶液 D.硝酸钾溶液和氯化铜溶液
2.下列各组物质相互混合后,不会发生离子反应的是( )
A.NaOH溶液和CuCl2溶液 B.Na2CO3溶液和稀硫酸
C.Na2SO4溶液和MgCl2溶液 D.Ca(OH)2和盐酸
3.下列对于离子反应的表述正确的是( )
A.离子反应中一定有沉淀生成
B.反应中有气体生成的反应一定是离子反应
C.复分解型离子反应发生的条件之一可以是有难电离的物质生成
D.非电解质二氧化碳与足量烧碱溶液的反应不属于离子反应
4.NaHCO3和NaHSO4的溶液混合后,实际参加反应的离子是( )
A.H+和CO B.HCO和HSO
C.Na+、HCO和H+ D.HCO和H+
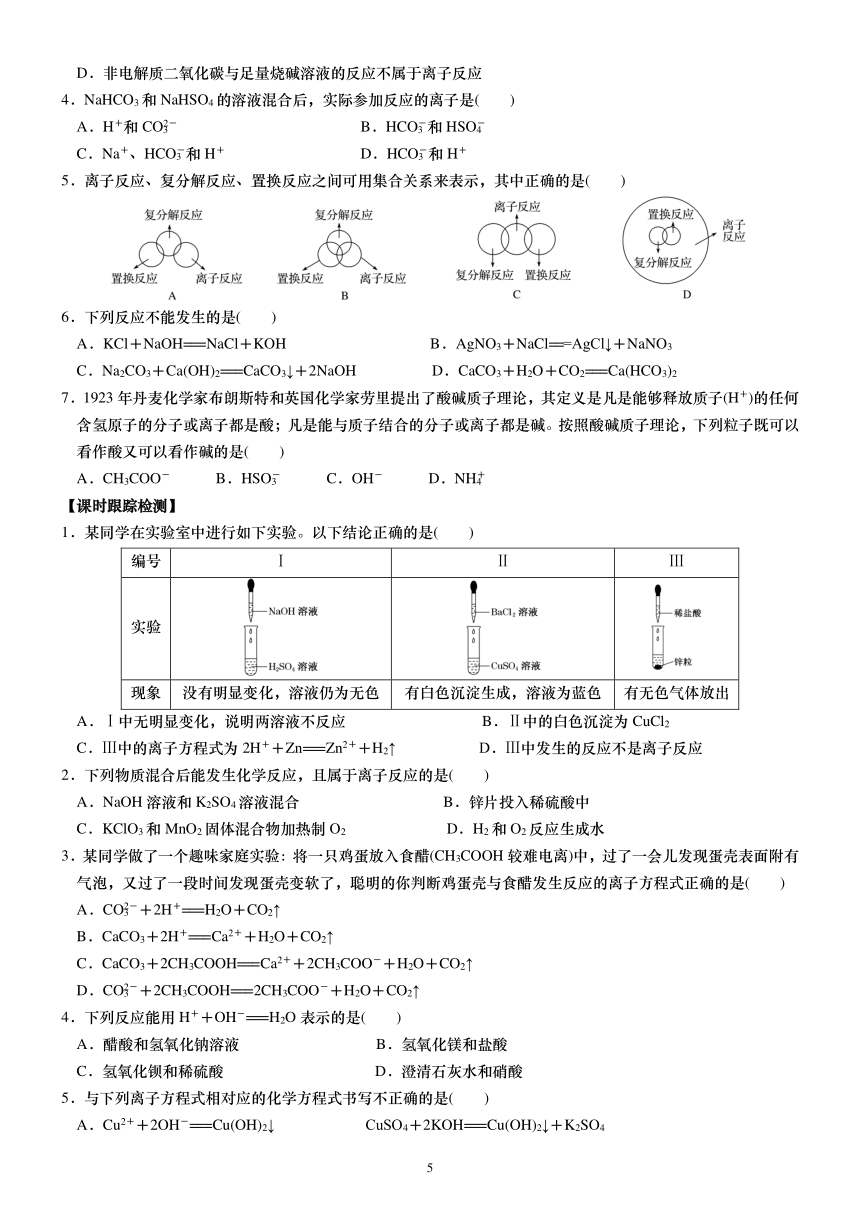
5.离子反应、复分解反应、置换反应之间可用集合关系来表示,其中正确的是( )
6.下列反应不能发生的是( )
A.KCl+NaOH===NaCl+KOH B.AgNO3+NaCl===AgCl↓+NaNO3
C.Na2CO3+Ca(OH)2===CaCO3↓+2NaOH D.CaCO3+H2O+CO2===Ca(HCO3)2
7.1923年丹麦化学家布朗斯特和英国化学家劳里提出了酸碱质子理论,其定义是凡是能够释放质子(H+)的任何含氢原子的分子或离子都是酸;凡是能与质子结合的分子或离子都是碱。按照酸碱质子理论,下列粒子既可以看作酸又可以看作碱的是( )
A.CH3COO- B.HSO C.OH- D.NH
【课时跟踪检测】
1.某同学在实验室中进行如下实验。以下结论正确的是( )
编号 Ⅰ Ⅱ Ⅲ
实验
现象 没有明显变化,溶液仍为无色 有白色沉淀生成,溶液为蓝色 有无色气体放出
A.Ⅰ中无明显变化,说明两溶液不反应 B.Ⅱ中的白色沉淀为CuCl2
C.Ⅲ中的离子方程式为2H++Zn===Zn2++H2↑ D.Ⅲ中发生的反应不是离子反应
2.下列物质混合后能发生化学反应,且属于离子反应的是( )
A.NaOH溶液和K2SO4溶液混合 B.锌片投入稀硫酸中
C.KClO3和MnO2固体混合物加热制O2 D.H2和O2反应生成水
3.某同学做了一个趣味家庭实验:将一只鸡蛋放入食醋(CH3COOH较难电离)中,过了一会儿发现蛋壳表面附有气泡,又过了一段时间发现蛋壳变软了,聪明的你判断鸡蛋壳与食醋发生反应的离子方程式正确的是( )
A.CO+2H+===H2O+CO2↑
B.CaCO3+2H+===Ca2++H2O+CO2↑
C.CaCO3+2CH3COOH===Ca2++2CH3COO-+H2O+CO2↑
D.CO+2CH3COOH===2CH3COO-+H2O+CO2↑
4.下列反应能用H++OH-===H2O表示的是( )
A.醋酸和氢氧化钠溶液 B.氢氧化镁和盐酸
C.氢氧化钡和稀硫酸 D.澄清石灰水和硝酸
5.与下列离子方程式相对应的化学方程式书写不正确的是( )
A.Cu2++2OH-===Cu(OH)2↓ CuSO4+2KOH===Cu(OH)2↓+K2SO4
B.CO+2H+===CO2↑+H2O BaCO3+2HCl===BaCl2+H2O+CO2↑
C.Ca2++CO===CaCO3↓ CaCl2+Na2CO3===CaCO3↓+2NaCl
D.H++OH-===H2O 2KOH+H2SO4===K2SO4+2H2O
6.下列离子方程式改写成化学方程式正确的是( )
A.Zn2++2OH-===Zn(OH)2↓ ZnCO3+2NaOH===Zn(OH)2↓+Na2CO3
B.Ba2++SO===BaSO4↓ Ba(OH)2+H2SO4===BaSO4↓+2H2O
C.Ag++Cl-===AgCl↓ AgNO3+NaCl===AgCl↓+NaNO3
D.Cu+2Ag+===Cu2++2Ag Cu+2AgCl===CuCl2+2Ag
7.铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
A.OH-+HCl===H2O+Cl- B.Ca(OH)2+Cu2+===Ca2++Cu(OH)2↓
C.Fe+Cu2+===Cu+Fe2+ D.Fe+2H+===Fe3++H2↑
8.下列离子方程式不正确的是( )
A.氢氧化钠与盐酸反应:OH-+H+===H2O
B.氧化镁与稀硫酸反应:O2-+2H+===H2O
C.碳酸钡与盐酸反应:BaCO3+2H+===Ba2++H2O+CO2↑
D.食盐水中滴加硝酸银溶液:Cl-+Ag+===AgCl↓
9.下列离子方程式不正确的是( )
A.氢氧化钡溶液与盐酸反应:OH-+H+===H2O
B.锌投入稀硫酸中:Zn+2H+===Zn2++H2↑
C.碳酸钠溶液与足量盐酸反应:2H++CO===H2O+CO2↑
D.氧化钠与水反应:O2-+H2O===2OH-
10.下列反应的离子方程式中,书写正确的是( )
A.碳酸钙跟盐酸反应:2H++CO===H2O+CO2↑
B.铁粉跟稀盐酸反应制备氢气:2Fe+6H+===2Fe3++3H2↑
C.硝酸银溶液跟铜反应:Cu+Ag+===Cu2++Ag
D.用小苏打治疗胃酸过多:HCO+H+===CO2↑+H2O
11.下列反应的离子方程式中,书写正确的是( )
A.铁粉与稀硫酸反应:2Fe+6H+===2Fe3++3H2↑
B.钠与水反应:Na+2H2O===Na++2OH-+H2↑
C.鸡蛋壳(主要成分为CaCO3)与醋酸反应:CaCO3+2H+===Ca2++CO2↑+H2O
D.小苏打与盐酸反应:HCO+H+===CO2↑+H2O
12.下列陈述正确的是( )
A.NaHSO4在水溶液中的电离方程式:NaHSO4===Na++HSO
B.氢氧化铁胶体的制备原理:FeCl3+3NaOH===Fe(OH)3↓+3NaCl
C.铜片插入硝酸银溶液中:Cu+2Ag+===Cu2++2Ag
D.将Ba(OH)2溶液滴入稀H2SO4溶液中:Ba2++OH-+H++SO===H2O+BaSO4↓
13.下列反应的离子方程式书写正确的是( )
A.金属镁与稀盐酸反应:Mg+2H++2Cl-===MgCl2+H2↑
B.氯化钡溶液与硫酸反应:Ba2++SO===BaSO4↓
C.碳酸钠溶液与盐酸反应:Na2CO3+2H+===2Na++H2O+CO2↑
D.氢氧化镁与硫酸溶液反应:OH-+H+===H2O
14.下列离子方程式书写正确的是( )
A.Ba(OH)2和H2SO4两溶液混合:Ba2++OH-+H++SO===BaSO4↓+H2O
B.氢氧化铜加到盐酸中:OH-+H+===H2O
C.锌和硝酸银溶液反应:Zn+Ag+===Ag+Zn2+
D.FeCl3和NaOH溶液反应:Fe3++3OH-===Fe(OH)3↓
15.下列离子方程式书写正确的是( )
A.实验室用铁和稀硫酸反应制氢气:Fe+2H+===Fe2++H2↑
B.向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2OFe(OH)3↓+3H+
C.实验室用大理石和稀盐酸反应制取CO2气体:CO+2H+===CO2↑+H2O
D.将铝片插入硝酸汞溶液中:Al+Hg2+===Al3++Hg
16.下列各组反应,前者与后者均可用同一离子方程式表示的是( )
A.HCl+Na2CO3,HCl+NaHCO3
B.HCl+Na2CO3,HNO3 +K2CO3
C.H2SO4+Ba(OH)2,H2SO4+KOH
D.BaCl2+Na2SO4,BaCO3+HCl
17.下列叙述正确的是( )
A.H++OH-===H2O表示所有强酸和强碱的反应 B.所有的离子方程式都可以表示一类反应
C.单质和氧化物在离子方程式中不能用离子符号表示 D.凡是易溶于水的化合物都可以写成离子形式
18.下列叙述正确的是( )
A.凡是强电解质,在离子方程式中都要以离子形式表示
B.复分解反应用离子方程式表示时总是向着溶液中反应物离子浓度减少的方向进行
C.酸碱中和反应的离子方程式都是H++OH-===H2O
D.凡是酸都可以在离子方程式中用H+表示
19.下列离子方程式书写正确的是( )
A.氢氧化钡与稀硫酸反应:Ba2++SO===BaSO4↓
B.Al2O3溶于盐酸中:O2-+2H+===H2O
C.铜和硝酸银溶液反应:Cu+Ag+===Cu2++Ag
D.Cu(OH)2中加入硝酸:Cu(OH)2+2H+===Cu2++2H2O
20.离子方程式CO+2H+===CO2↑+H2O表示( )
A.碳酸盐与盐酸之间的反应 B.一切碳酸盐与一切酸之间的反应
C.可溶性碳酸盐与强酸之间的反应 D.可溶性碳酸盐与一切酸之间的反应
21.有五瓶标签损坏的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如图所示。图中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做。
A
↓ B
C
↓ × D
↓ ↓ ↑ ↑ E
请回答下列问题:
(1)各试剂瓶中所盛试剂为(填溶质的化学式):A______,B______,C______,D______,E______
(2)写出下列反应的离子方程式
A与E:_______________________________________
B与E:_______________________________________
C与E:_______________________________________
22.某同学欲用离子方程式来表达两种物质相遇时发生的变化。请判断他写出的下列离子方程式是否正确表达了相应的操作和结果;对于不正确的,请帮他改正。
(1)向碳酸钙中加入稀盐酸:H++CO===H2O+CO2↑
______________________________________________________________________________
(2)向CuSO4溶液中滴加Ba(OH)2溶液:SO+Ba2+===BaSO4↓
______________________________________________________________________________
(3)向Na2SO4溶液中滴加CuCl2溶液:SO+Cu2+===CuSO4
______________________________________________________________________________
(4)向氢氧化铜悬浊液中滴加稀硫酸:H++OH-===H2O
______________________________________________________________________________
23.(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式是_______________________________;常用澄清石灰水检验CO2气体,该反应的离子方程式是___________________________________________
(2)表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是__________________________;反应片刻后,可观察到有气体产生,这时反应的离子方程式是_________________________________
(3)人体胃液中的胃酸(主要成分是盐酸),起杀菌、帮助消化等作用,但胃酸的量必须控制在一定范围内。当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用“小苏打片”(NaHCO3)治疗胃酸过多的离子方程式为__________________________________
②如果病人同时患有胃溃疡,此时最好服用“胃舒平”[主要成分是Al(OH)3],反应的离子方程式为_______________________________________________________
24.写出下列反应的离子方程式
(1)NaOH溶液与稀硝酸反应:_________________________________________________
(2)BaCl2溶液与K2SO4溶液反应:______________________________________________
(3)K2CO3溶液与足量稀硫酸反应:_____________________________________________
(4)AgNO3溶液与稀盐酸反应:______________________________________________
(5)碳酸钠溶液与氢氧化钙溶液反应:_________________________________________________
(6)碳酸钙与稀硝酸反应:_________________________________________________
(7)稀硫酸与Ba(OH)2溶液反应:___________________________________________
(8)氯化钠溶液与硝酸银溶液:___________________________________________
(9)氢氧化钡溶液和硫酸铜溶液:___________________________________________
(10)铜与硝酸银溶液反应:___________________________________________
(11)氧化镁溶于稀盐酸:___________________________________________
(12)用碳酸钙与稀盐酸反应制备二氧化碳:___________________________________________
(13)铁与稀硫酸反应生成氢气:___________________________________________
(14)二氧化碳与澄清石灰水反应生成沉淀:___________________________________________
(15)氢氧化铜溶于稀硫酸:___________________________________________
(16)碳酸氢钠与盐酸反应:___________________________________________
25.人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内。当胃酸过多时就会出现“咯酸水”“烧心”“胃部隐隐作痛”等症状。目前市场上的抗酸药主要有①吸收性抗酸药,如NaHCO3等。②非吸收性抗酸药,如CaCO3、MgO、Al(OH)3等
(1)上述所举抗酸药中有 个是电解质
(2)CaCO3作抗酸药时发生反应的离子方程式为_____________________________
(3) (填“可以”或“不可以”)服用BaCO3来治疗胃酸过多,理由是_____________________________
(4)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为_______________
26.某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示
请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有 (填字母)
a.天平 b.烧杯 c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为___________________________________________
(3)AB段反应的离子方程式为___________________________________________
27.用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
(1)BaCl2(HCl):试剂________,离子方程式为________________________________________
(2)O2(CO2):试剂______________,离子方程式为________________________________________
(3)SO(CO):试剂__________,离子方程式为__________________________________________
28.写出与下列离子方程式相对应的化学方程式 (各两个)
(1)2H++CaCO3===Ca2++H2O+CO2↑
________________________________________、___________________________________________
(2)2H++CO===H2O+CO2↑
________________________________________、___________________________________________
(3)Ba2++SO===BaSO4↓:
________________________________________、___________________________________________
【离子反应】答案
【对点训练1】
1.略
2.
溶液中反应物 化学方程式 离子方程式
HCl+NaOH HCl+NaOH===NaCl+H2O H++OH-===H2O
HCl+KOH HCl+KOH===KCl+H2O H++OH-===H2O
H2SO4+NaOH H2SO4+2NaOH===Na2SO4+2H2O H++OH-===H2O
H2SO4+KOH 2KOH+H2SO4===K2SO4+2H2O OH-+H+===H2O
3.
溶液中反应物 化学方程式 离子方程式
HCl+Cu(OH)2 2HCl+Cu(OH)2===CuCl2+2H2O 2H++Cu(OH)2===Cu2++2H2O
HNO3+NH3 H2O HNO3+NH3 H2O===NH4NO3+H2O H++NH3 H2O===NH+H2O
HF+NaOH HF+NaOH===NaF+H2O HF+OH-===F-+H2O
H2SO4+Ba(OH)2 H2SO4+Ba(OH)2===BaSO4↓+2H2O Ba2++2OH-+2H++SO===BaSO4↓+2H2O
4.C。解析:选项C中的反应不在溶液中进行且无离子参加或生成,不属于离子反应。
5.D。解析:氢氧化钡溶液与稀硫酸反应的离子方程式为Ba2++2OH-+2H++SO===BaSO4↓+2H2O,④不正确;①②③正确。
6.B。解析:易电离产生H+的化合物与易电离产生OH-的化合物反应,生成易溶、易电离的盐和水,都可用离子方程式H++OH-===H2O来表示。
7.C
8.D。解析:H++OH-===H2O可以代表强酸和强碱反应生成可溶于水的盐和水的反应,如盐酸和氢氧化钠、盐酸和氢氧化钡、硝酸和氢氧化钾等,故A错误;CO+2H+===CO2↑+H2O代表可溶性的碳酸盐和强酸之间的反应,如碳酸钠和盐酸、碳酸钠和硝酸等,故B错误;Zn(OH)2+2H+===Zn2++2H2O代表氢氧化锌和强酸之间的反应,如:氢氧化锌和盐酸、硝酸、硫酸等,故C错误;Ba2++2OH-+Cu2++SO===BaSO4↓+Cu(OH)2↓只能表示氢氧化钡和硫酸铜之间的反应,故D正确。
9.C。解析:CuCO3是难溶盐,在书写离子方程式时不能拆开,故A错误;有H2O生成,反应的离子方程式为Ba2++2H++2OH-+SO===BaSO4↓+2H2O,故B错误;AgNO3和NaCl反应的实质为Ag++Cl-===AgCl↓,化学方程式与离子方程式相对应,故C正确;Cu(OH)2不溶于水,不能拆成Cu2+和OH-,故D错误。
【对点训练2】
1.A。解析:澄清的石灰水是强碱溶液,应拆分为离子,B错误;醋酸是弱电解质不可拆,C错误;碳酸钡难溶于水,不能拆成离子形式,D错误。
2.B。解析:B项,违背电荷守恒,错误。
3.C。解析:BaSO4属于难溶性盐,在离子方程式中应写成化学式;CH3COOH属于弱电解质,在离子方程式中应写成化学式。则H+不能代表的物质是②④⑤。
【对点训练3】
1.D。解析:选项D中的溶液混合无沉淀、气体或水生成,不能发生离子反应。
2.C。解析:物质在溶液中是否能够发生化学反应,可根据是否生成难溶性物质,是否生成难电离的物质或是否生成易挥发性物质来进行判断。Na2SO4和MgCl2溶液混合后既没有难溶性物质,也没有难电离的物质和易挥发性物质生成,故不发生离子反应。
3.C。解析:离子反应不一定都有沉淀生成,有气体或难电离的物质生成的也是离子反应;有气体生成的不一定是离子反应,如碳酸钙加热分解生成二氧化碳气体的反应不是离子反应;二氧化碳与烧碱溶液反应有碳酸根离子和水生成,该反应属于离子反应。
4.D。解析:NaHCO3和NaHSO4的电离方程式分别为NaHCO3===Na++HCO、NaHSO4===Na++H++SO,故D项正确。
5.C。解析:置换反应与复分解反应没有相交的关系,离子反应与置换反应和复分解反应有相交的关系。
6.A。解析:NaOH是碱,KCl是盐,碱与盐的反应应为复分解反应,此反应不满足复分解反应发生的条件,所以不能发生。
7.B。解析:CH3COO-只能结合H+转化为CH3COOH,属于碱,A错误;HSO可以结合H+转化为H2SO3,属于碱,也可以释放H+转化为SO,属于酸,B正确;OH-只能结合H+转化为H2O,属于碱,C错误;NH只能释放H+转化为NH3,属于酸,D错误。
【课时跟踪检测】
1.C。解析:Ⅰ中虽无明显现象,但发生了离子反应:H++OH-===H2O,A项错误;Ⅱ中发生反应:Ba2++SO===BaSO4↓,白色沉淀为BaSO4,B项错误;Ⅲ中的反应是离子反应,离子方程式为Zn+2H+===Zn2++H2↑,C项正确、D项错误。
2.B。解析:A项,不具备复分解反应发生的条件;B项,离子反应是Zn+2H+===Zn2++H2↑;C项,不是在溶液中进行的反应;D项,不是离子反应。
3.C。解析:CaCO3难溶于水,CH3COOH难电离,在离子方程式中都要写成化学式。
4.D。解析:醋酸是弱酸,书写离子方程式时,应写成CH3COOH;氢氧化镁难溶于水,应写其化学式Mg(OH)2;C项反应生成的硫酸钡难溶于水,漏掉了另一个离子反应Ba2++SO===BaSO4↓。
5.B。解析:选项B中的碳酸钡不溶于水,不能写成离子的形式。
6.C。解析:A项中ZnCO3难溶于水;B项中OH-和H+生成H2O;D项中AgCl难溶于水。
7.C。解析:A项中HCl要拆写成离子形式,B项中Ca(OH)2应拆写成离子形式,D项中Fe与稀盐酸反应生成Fe2+。
8.B。解析:MgO不能拆开写。
9.D。解析:氧化物不能拆写。
10.D。解析:碳酸钙难溶,碳酸钙跟盐酸反应的离子方程式:2H++CaCO3===H2O+CO2↑+Ca2+,故A错误;铁粉跟稀盐酸反应生成氯化亚铁和氢气的离子方程式:Fe+2H+===Fe2++H2↑,故B错误;离子方程式要符合电荷守恒,硝酸银溶液跟铜反应的离子方程式:Cu+2Ag+===Cu2++2Ag,故C错误;用小苏打治疗胃酸过多生成氯化钠、水和二氧化碳的离子方程式:HCO+H+===CO2↑+H2O,故D正确。
11.D。解析:A项正确的离子方程式为Fe+2H+===Fe2++H2↑;B项正确的离子方程式为2Na+2H2O===2Na++2OH-+H2↑;C项正确的离子方程式为CaCO3+2CH3COOH===Ca2++2CH3COO-+CO2↑+H2O。
12.C。解析:NaHSO4在水溶液中的电离方程式:NaHSO4===Na++H++SO,A错误;氢氧化铁胶体的制备原理为向沸水中滴加饱和氯化铁溶液,化学方程式为:FeCl3+3H2OFe(OH)3(胶体)+3HCl,B错误;铜片插入硝酸银溶液中发生置换反应生成铜离子和银:Cu+2Ag+===Cu2++2Ag,C正确;将Ba(OH)2溶液滴入稀H2SO4溶液中,氢离子消耗完全:Ba2++2OH-+2H++SO===2H2O+BaSO4↓,D错误。
13.B。解析:MgCl2为可溶性电解质,应拆分为离子,正确的离子方程式为Mg+2H+===Mg2++H2↑,故A错误;Na2CO3为可溶性强电解质,应拆分为离子,正确的离子方程式为CO+2H+===H2O+CO2↑,故C错误;Mg(OH)2为难溶物,不可拆成离子形式,故D错误。
14.D。解析:A项,应写为Ba2++2OH-+2H++SO===BaSO4↓+2H2O;B项,应写为Cu(OH)2+2H+===Cu2++2H2O;C项,离子方程式中前后电荷不守恒,应写为Zn+2Ag+===2Ag+Zn2+。
15.A。解析:B项,Fe(OH)3胶体不是沉淀,不能标注“↓”,错误;C项,CaCO3为不溶于水的固体不能写成离子形式,错误;D项,电荷不守恒,错误。
16.B。解析:A项,前者:2H++CO===H2O+CO2↑或H++CO===HCO;后者:H++HCO===H2O+CO2↑。B项,前者:2H++CO===H2O+CO2↑;后者:2H++CO===H2O+CO2↑。C项,前者:2H++SO+Ba2++2OH-===BaSO4↓+2H2O;后者:H++OH-===H2O。D项,前者:Ba2++SO===BaSO4↓;后者:BaCO3+2H+===Ba2++CO2↑+H2O。
17.C
18.B
19.D。解析:反应过程中OH-与H+生成H2O,正确的离子方程式为Ba2++2OH-+2H++SO===BaSO4↓+2H2O,A项错误;氧化物不能拆分为离子,正确的离子方程式为Al2O3+6H+===2Al3++3H2O,B项错误;电荷不守恒,C项错误;Cu(OH)2是难溶碱,书写离子方程式时不可拆成离子,D项正确。
20.C。解析:CO只代表可溶性的碳酸盐,故选项A和选项B都是不正确的;H+只代表强酸而不是一切酸(如弱酸H2S、HF、CH3COOH等均不能用H+表示),故选项C正确,选项D不正确。
21.(1)BaCl2 AgNO3 HNO3 HCl K2CO3
(2)Ba2++CO===BaCO3↓ 2Ag++CO===Ag2CO3↓ CO+2H+===H2O+CO2↑
解析:根据题意,E与A、B反应分别产生沉淀,与C、D反应分别产生气体,可推知E为K2CO3溶液,A、B可能为AgNO3和BaCl2中的一种,C、D必为稀硝酸和盐酸中的一种,而B与D能产生沉淀,可确定B为AgNO3溶液,D为盐酸,因此A为BaCl2溶液,C为稀硝酸。
22.(1)错误,正确的是2H++CaCO3===Ca2++CO2↑+H2O
(2)错误,正确的是Cu2++SO+Ba2++2OH-===Cu(OH)2↓+BaSO4↓
(3)错误,两者不反应
(4)错误,正确的是Cu(OH)2+2H+===Cu2++2H2O
23.(1)CaCO3+2H+===Ca2++CO2↑+H2O Ca2++2OH-+CO2===CaCO3↓+H2O
(2)Fe2O3+6H+===2Fe3++3H2O Fe+2H+===Fe2++H2↑
(3)①HCO+H+===CO2↑+H2O
②Al(OH)3+3H+===Al3++3H2O
24.(1)OH-+H+===H2O
(2)Ba2++SO===BaSO4↓
(3)CO+2H+===H2O+CO2↑
(4)Ag++Cl-===AgCl↓
(5)Ca2++CO===CaCO3↓
(6)CaCO3+2H+===H2O+CO2↑+Ca2+
(7)2H++SO+Ba2++2OH-===BaSO4↓+2H2O
(8)Cl-+Ag+===AgCl↓
(9)Ba2++2OH-+SO+Cu2+===BaSO4↓+Cu(OH)2↓
(10)Cu+2Ag+===Cu2++2Ag
(11)MgO+2H+===Mg2++H2O
(12)CaCO3+2H+===Ca2++CO2↑+H2O
(13)Fe+2H+===Fe2++H2↑
(14)Ca2++2OH-+CO2===CaCO3↓+H2O
(15)Cu(OH)2+2H+===Cu2++2H2O
(16)HCO+H+===CO2↑+H2O
25.(1)4
(2)CaCO3+2H+===Ca2++CO2↑+H2O
(3)不可以 Ba2+是重金属离子,对人体有害
(4)Al(OH)3+3H+===Al3++3H2O
解析:(1)在水溶液里或熔融状态下能够导电的化合物是电解质,碳酸氢钠、碳酸钙、氧化镁和氢氧化铝均是电解质,则上述所举抗酸药中有4个是电解质。(2)CaCO3作抗酸药时与氢离子反应,则发生反应的离子方程式为CaCO3+2H+===Ca2++H2O+CO2↑。(3)碳酸钡与酸反应生成钡离子,Ba2+是重金属离子,对人体有害,因此不可以服用BaCO3来治疗胃酸过多。(4)胃舒平中的Al(OH)3难溶于水,作抗酸药时和胃酸中的H+反应的离子方程式为Al(OH)3+3H+===Al3++3H2O。
26.(1)bd
(2)H++OH-===H2O
(3)Mg2++2OH-===Mg(OH)2↓
解析:(1)溶解MgCl2固体所用的玻璃仪器有烧杯和玻璃棒。(2)OA段没有沉淀生成,说明是盐酸和氢氧化钠的反应。(3)AB段为氯化镁和氢氧化钠反应生成氢氧化镁沉淀。
27.(1)BaCO3 BaCO3+2H+===Ba2++H2O+CO2↑
(2)足量NaOH溶液 CO2+2OH-===CO+H2O
(3)适量稀硫酸 CO+2H+===H2O+CO2↑
28.略
PAGE
【核心素养发展目标】
1.通过实验事实认识离子反应,并掌握离子反应发生的条件,增强化学核心素养中的变化观念意识
2.掌握离子方程式的书写方法及正误判断,能用离子方程式正确表示典型物质的主要化学性质,促进证据推理与模型认知化学核心素养的发展
【主干知识梳理】
一、离子反应与离子方程式书写
1.离子反应
(1)离子反应的实验探究
实验步骤 向盛有2ml Na2SO4稀溶液的试管中加入2ml BaCl2稀溶液,观察现象并分析
实验装置
实验现象 有白色沉淀生成
化学方程式 Na2SO4+BaCl2===BaSO4↓+2NaCl
微观分析 Na2SO4和BaCl2的电离方程式 混合前两种溶液中的离子 混合后溶液中的离子
BaCl2===Ba2++2Cl-Na2SO4===SO+2Na+ BaCl2溶液:Ba2+、Cl-Na2SO4溶液:Na+、SO Na+、Cl-
实验结论 当Na2SO4稀溶液与BaCl2溶稀溶液混合时,Na+与Cl-都没有发生化学反应;Ba2+而SO与发生了化学反应,生成难溶的BaSO4白色沉淀
反应本质 Ba2+、SO结合成BaSO4白色沉淀,即:Ba2++SO===BaSO4↓
(2)离子反应的定义:电解质在溶液中的反应实质上是离子之间的反应,这样的反应属于离子反应
(3)实质:
①从微观角度,酸、碱、盐在水溶液中发生的复分解反应,实质上是两种电解质在溶液中相互交换离子的反应②离子反应使溶液中某些离子的浓度减小
2.离子方程式
(1)定义:用实际参加反应的离子符号来表示反应的式子叫做离子方程式
(2)书写步骤——以Na2SO4溶液和BaCl2溶液反应为例
①写:正确书写反应的化学方程式:Na2SO4+BaCl2===BaSO4↓+2NaCl
②拆:把易溶于水且易电离的物质(如:强酸、强碱和大多数可溶性的盐)拆写成离子的形式,难溶的物质、气
体和水等仍用化学式表示:2Na++SO+Ba2++2Cl-===BaSO4↓+2Na++2Cl-
③删:等量删去方程式两边不参加反应的离子,并将化学计量数化为最简整数比:Ba2++SO===BaSO4↓
④查:检查方程式两边各元素的原子个数和电荷总数是否相等
【微点拨】
①书写步骤:写(是基础)拆(是关键)删(是途径)查(是保证)
②书写关键:单质、氧化物在离子方程式中一律写化学式;弱酸(如:HF、H2S、HClO、H2SO3等)、弱碱(如:NH3·H2O)、水等难电离的物质必须写化学式;难溶于水的物质(如:CaCO3、BaSO3、BaSO4,Fe(OH)3等)必须写化学式,气体、非电解质必须写化学式
【对点训练1】
1.写出下列反应的化学方程式并将其改写成离子方程式
(1)写:CuSO4 + NaOH —— _____________________ (2)写:Fe(OH)3 + H2SO4 —— ____________________
拆:______________________________________ 拆:______________________________________
删:______________________________________ 删:______________________________________
(3)写:CuO + HNO3—— ____________________ (4)写:Fe + HCl—— ______________________
拆:______________________________________ 拆:______________________________________
删:______________________________________ 删:______________________________________
(5)写:3Cu+8HNO3===3Cu(NO3)2+2NO↑+4H2O (6)写:CaCO3+2CH3COOH===(CH3COO)2Ca+CO2↑+H2O
拆:______________________________________ 拆:______________________________________
删:______________________________________ 删:______________________________________
2.写出下列反应的化学方程式和离子方程式,思考两种方程式在表示某一类反应时,表达的含义有什么不同
溶液中反应物 化学方程式 离子方程式
HCl+NaOH
HCl+KOH
H2SO4+NaOH
H2SO4+KOH
离子方程式的意义 离子方程式不仅可以表示某个具体的化学反应,还可以表示同一类型的离子反应
3.将下列化学方程式改写成离子方程式,并思考是否所有的酸碱中和反应都能用H++OH-===H2O来表示?
溶液中反应物 化学方程式 离子方程式
HCl+Cu(OH)2
HNO3+NH3 H2O
HF+NaOH
H2SO4+Ba(OH)2
结论 H++OH-===H2O表示强酸与强碱反应生成可溶性盐和H2O的一类反应
4.下列各组物质间的反应中,不属于离子反应的是( )
A.锌和稀硫酸反应 B.氯化钠溶液和硝酸银溶液反应
C.木炭和氧气反应 D.烧碱溶液和氯化铁溶液反应
5.离子方程式Ba2++SO===BaSO4↓可能表示( )
①可溶性钡盐溶液与可溶性硫酸盐溶液之间的反应 ②氢氧化钡溶液与可溶性硫酸盐溶液之间的反应
③稀硫酸与可溶性钡盐溶液之间的反应 ④氢氧化钡溶液与稀硫酸反应
A.①② B.①②④ C.②③ D.①②③
6.下列反应可用离子方程式H++OH-===H2O来表示的是( )
A.氢氧化钡和稀硫酸的反应 B.硫酸氢钠和氢氧化钾的反应
C.碳酸氢钠和氢氧化钾的反应 D.氢氧化钠溶液与醋酸的反应
7.下列反应①和②可以用同一离子方程式表示的是( )
A.①稀盐酸+碳酸钠溶液;②稀盐酸+碳酸氢钠溶液
B.①氢氧化钠溶液+稀盐酸;②氢氧化钡溶液+稀硫酸
C.①氯化钡溶液+稀硫酸;②氢氧化钡溶液+硫酸钠溶液
D.①稀盐酸+碳酸钙粉末;②稀硫酸+碳酸钠溶液
8.只能表示一个化学反应的离子方程式是( )
A.H++OH-===H2O B.2H++CO===H2O+CO2↑
C.Zn(OH)2+2H+===Zn2++2H2O D.Cu2++2OH-+Ba2++SO===BaSO4↓+Cu(OH)2↓
9.下列化学方程式对应的离子方程式正确的是( )
A.CuCO3+2NaOH===Cu(OH)2↓+Na2CO3 Cu2++2OH-===Cu(OH)2↓
B.Ba(OH)2+H2SO4===BaSO4↓+2H2O Ba2++SO===BaSO4↓
C.AgNO3+NaCl===AgCl↓+NaNO3 Ag++Cl-===AgCl↓
D.Cu(OH)2+H2SO4===CuSO4+2H2O OH-+H+===H2O
二、离子方程式的拆写原则
1.常见物质在离子方程式中的书写要求
书写要求 物质类型
需拆成离子的物质(写离子符号) ①强酸:HCl、H2SO4、HNO3等
②强碱:KOH、NaOH、Ba(OH)2等
③可溶性盐:NaCl、K2SO4、NaNO3等
不能拆成离子的物质(写化学式) ①单质;②气体;③氧化物
④难溶物:Cu(OH)2、BaSO4、AgCl等
⑤难电离的物质:CH3COOH、NH3·H2O、H2O等
⑥非电解质:乙醇等
⑦浓硫酸
2.对于微溶物的处理有三种情况
(1)生成物中有微溶物[Ag2SO4、CaSO4、Ca(OH)2、MgCO3]时,微溶物写化学式并标“↓”
如:Na2SO4溶液中加入AgNO3 溶液:2Ag++SO===Ag2SO4↓
(2)当反应物里有微溶物处于溶液状态(稀溶液),应写成离子的形式
如:CO2气体通入澄清石灰水中:CO2+Ca2++2OH-===CaCO3↓+H2O
(3)当反应物里有微溶物处于悬浊液或固态时,应写成化学式
如:用石灰乳制漂白粉的反应:2Ca(OH)2+2Cl2===2Ca2++2Cl-+2ClO-+H2O
3.对氨水的处理
(1)作反应物时用NH3 H2O
如:硫酸铝溶液中加入氨水:Al3++3NH3 H2O===Al(OH)3↓+3NH
(2)作生成物时,若加热或浓溶液时写成NH3↑+H2O;无特殊说明写NH3 H2O
如:浓NaOH溶液中加入硫酸铵固体:OH-+NH===NH3↑+H2O
(NH4)2SO4与NaOH两溶液混合加热:NH+OH-NH3↑+H2O
NH4Cl与NaOH两稀溶液混合:NH+OH-===NH3 H2O
4.固体与固体间反应不能写离子方程式,如:NH4Cl固体和Ca(OH)2固体混合加热,虽然也有离子和离子反应,但不能写成离子方程式,只能写化学方程式
5.浓H2SO4与固体反应不能写离子方程式,如:Cu+2H2SO4(浓)CuSO4+SO2↑+2H2O
6.多元弱酸的酸式酸根离子,在离子方程式中不能拆写
如:NaHCO3与盐酸反应的离子方程式为HCO+H+===CO2↑+H2O。
【对点训练2】
1.能正确表示下列化学反应的离子方程式的是( )
A.氢氧化钡溶液与稀硝酸反应:OH-+H+===H2O
B.澄清的石灰水与稀盐酸反应:Ca(OH)2+2H+===Ca2++2H2O
C.醋酸与氢氧化钠溶液反应:H++OH-===H2O
D.碳酸钡溶于稀盐酸中:CO+2H+===H2O+CO2↑
2.下列离子方程式书写错误的是( )
A.Ba(OH)2溶液与盐酸反应:OH-+H+===H2O
B.Al与CuSO4溶液反应:Al+Cu2+===Cu+Al3+
C.硫酸铵溶液和氢氧化钡溶液反应的离子方程式:2NH+SO+Ba2++2OH-===2NH3·H2O+BaSO4↓
D.向氯化钠溶液中滴加硝酸银溶液:Cl-+Ag+===AgCl↓
3.离子方程式BaCO3+2H+===CO2↑+H2O+Ba2+中的H+不能代表的物质是( )
①HCl ②H2SO4 ③HNO3 ④NaHSO4 ⑤CH3COOH
A.①③ B.①④⑤ C.②④⑤ D.①⑤
三、离子反应发生的条件
1.复分解型离子反应发生的条件
实验过程
实验现象 ① ② ③
生成蓝色沉淀 溶液红色消失 产生气泡
离子方程式 Cu2++2OH-===Cu(OH)2↓ H++OH-===H2O CO+2H+===CO2↑+H2O
酸、碱、盐在水溶液中发生的复分解反应,实质上就是两种电解质在溶液中相互交换离子的反应,这类离子反应发生的条件是:生成难溶物(沉淀)、生成挥发性的物质(气体)、生成难电离的物质(弱酸、弱碱和水),只要具备上述条件之一,反应就能发生
2.置换反应的条件:活泼金属与酸反应、活泼金属与盐反应等
如:Zn与稀H2SO4反应的离子方程式为Zn+2H+===Zn2++H2↑
Zn与CuSO4溶液反应的离子方程式为Zn+Cu2+===Cu+Zn2+
【对点训练3】
1.下列溶液混合后,不会发生离子反应的是( )
A.硝酸钡溶液和硫酸钠溶液 B.醋酸钠溶液和稀硫酸
C.碳酸钾溶液和硫酸氢钠溶液 D.硝酸钾溶液和氯化铜溶液
2.下列各组物质相互混合后,不会发生离子反应的是( )
A.NaOH溶液和CuCl2溶液 B.Na2CO3溶液和稀硫酸
C.Na2SO4溶液和MgCl2溶液 D.Ca(OH)2和盐酸
3.下列对于离子反应的表述正确的是( )
A.离子反应中一定有沉淀生成
B.反应中有气体生成的反应一定是离子反应
C.复分解型离子反应发生的条件之一可以是有难电离的物质生成
D.非电解质二氧化碳与足量烧碱溶液的反应不属于离子反应
4.NaHCO3和NaHSO4的溶液混合后,实际参加反应的离子是( )
A.H+和CO B.HCO和HSO
C.Na+、HCO和H+ D.HCO和H+
5.离子反应、复分解反应、置换反应之间可用集合关系来表示,其中正确的是( )
6.下列反应不能发生的是( )
A.KCl+NaOH===NaCl+KOH B.AgNO3+NaCl===AgCl↓+NaNO3
C.Na2CO3+Ca(OH)2===CaCO3↓+2NaOH D.CaCO3+H2O+CO2===Ca(HCO3)2
7.1923年丹麦化学家布朗斯特和英国化学家劳里提出了酸碱质子理论,其定义是凡是能够释放质子(H+)的任何含氢原子的分子或离子都是酸;凡是能与质子结合的分子或离子都是碱。按照酸碱质子理论,下列粒子既可以看作酸又可以看作碱的是( )
A.CH3COO- B.HSO C.OH- D.NH
【课时跟踪检测】
1.某同学在实验室中进行如下实验。以下结论正确的是( )
编号 Ⅰ Ⅱ Ⅲ
实验
现象 没有明显变化,溶液仍为无色 有白色沉淀生成,溶液为蓝色 有无色气体放出
A.Ⅰ中无明显变化,说明两溶液不反应 B.Ⅱ中的白色沉淀为CuCl2
C.Ⅲ中的离子方程式为2H++Zn===Zn2++H2↑ D.Ⅲ中发生的反应不是离子反应
2.下列物质混合后能发生化学反应,且属于离子反应的是( )
A.NaOH溶液和K2SO4溶液混合 B.锌片投入稀硫酸中
C.KClO3和MnO2固体混合物加热制O2 D.H2和O2反应生成水
3.某同学做了一个趣味家庭实验:将一只鸡蛋放入食醋(CH3COOH较难电离)中,过了一会儿发现蛋壳表面附有气泡,又过了一段时间发现蛋壳变软了,聪明的你判断鸡蛋壳与食醋发生反应的离子方程式正确的是( )
A.CO+2H+===H2O+CO2↑
B.CaCO3+2H+===Ca2++H2O+CO2↑
C.CaCO3+2CH3COOH===Ca2++2CH3COO-+H2O+CO2↑
D.CO+2CH3COOH===2CH3COO-+H2O+CO2↑
4.下列反应能用H++OH-===H2O表示的是( )
A.醋酸和氢氧化钠溶液 B.氢氧化镁和盐酸
C.氢氧化钡和稀硫酸 D.澄清石灰水和硝酸
5.与下列离子方程式相对应的化学方程式书写不正确的是( )
A.Cu2++2OH-===Cu(OH)2↓ CuSO4+2KOH===Cu(OH)2↓+K2SO4
B.CO+2H+===CO2↑+H2O BaCO3+2HCl===BaCl2+H2O+CO2↑
C.Ca2++CO===CaCO3↓ CaCl2+Na2CO3===CaCO3↓+2NaCl
D.H++OH-===H2O 2KOH+H2SO4===K2SO4+2H2O
6.下列离子方程式改写成化学方程式正确的是( )
A.Zn2++2OH-===Zn(OH)2↓ ZnCO3+2NaOH===Zn(OH)2↓+Na2CO3
B.Ba2++SO===BaSO4↓ Ba(OH)2+H2SO4===BaSO4↓+2H2O
C.Ag++Cl-===AgCl↓ AgNO3+NaCl===AgCl↓+NaNO3
D.Cu+2Ag+===Cu2++2Ag Cu+2AgCl===CuCl2+2Ag
7.铁、稀盐酸、澄清石灰水、氯化铜溶液是中学化学中常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
A.OH-+HCl===H2O+Cl- B.Ca(OH)2+Cu2+===Ca2++Cu(OH)2↓
C.Fe+Cu2+===Cu+Fe2+ D.Fe+2H+===Fe3++H2↑
8.下列离子方程式不正确的是( )
A.氢氧化钠与盐酸反应:OH-+H+===H2O
B.氧化镁与稀硫酸反应:O2-+2H+===H2O
C.碳酸钡与盐酸反应:BaCO3+2H+===Ba2++H2O+CO2↑
D.食盐水中滴加硝酸银溶液:Cl-+Ag+===AgCl↓
9.下列离子方程式不正确的是( )
A.氢氧化钡溶液与盐酸反应:OH-+H+===H2O
B.锌投入稀硫酸中:Zn+2H+===Zn2++H2↑
C.碳酸钠溶液与足量盐酸反应:2H++CO===H2O+CO2↑
D.氧化钠与水反应:O2-+H2O===2OH-
10.下列反应的离子方程式中,书写正确的是( )
A.碳酸钙跟盐酸反应:2H++CO===H2O+CO2↑
B.铁粉跟稀盐酸反应制备氢气:2Fe+6H+===2Fe3++3H2↑
C.硝酸银溶液跟铜反应:Cu+Ag+===Cu2++Ag
D.用小苏打治疗胃酸过多:HCO+H+===CO2↑+H2O
11.下列反应的离子方程式中,书写正确的是( )
A.铁粉与稀硫酸反应:2Fe+6H+===2Fe3++3H2↑
B.钠与水反应:Na+2H2O===Na++2OH-+H2↑
C.鸡蛋壳(主要成分为CaCO3)与醋酸反应:CaCO3+2H+===Ca2++CO2↑+H2O
D.小苏打与盐酸反应:HCO+H+===CO2↑+H2O
12.下列陈述正确的是( )
A.NaHSO4在水溶液中的电离方程式:NaHSO4===Na++HSO
B.氢氧化铁胶体的制备原理:FeCl3+3NaOH===Fe(OH)3↓+3NaCl
C.铜片插入硝酸银溶液中:Cu+2Ag+===Cu2++2Ag
D.将Ba(OH)2溶液滴入稀H2SO4溶液中:Ba2++OH-+H++SO===H2O+BaSO4↓
13.下列反应的离子方程式书写正确的是( )
A.金属镁与稀盐酸反应:Mg+2H++2Cl-===MgCl2+H2↑
B.氯化钡溶液与硫酸反应:Ba2++SO===BaSO4↓
C.碳酸钠溶液与盐酸反应:Na2CO3+2H+===2Na++H2O+CO2↑
D.氢氧化镁与硫酸溶液反应:OH-+H+===H2O
14.下列离子方程式书写正确的是( )
A.Ba(OH)2和H2SO4两溶液混合:Ba2++OH-+H++SO===BaSO4↓+H2O
B.氢氧化铜加到盐酸中:OH-+H+===H2O
C.锌和硝酸银溶液反应:Zn+Ag+===Ag+Zn2+
D.FeCl3和NaOH溶液反应:Fe3++3OH-===Fe(OH)3↓
15.下列离子方程式书写正确的是( )
A.实验室用铁和稀硫酸反应制氢气:Fe+2H+===Fe2++H2↑
B.向沸水中滴加饱和FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2OFe(OH)3↓+3H+
C.实验室用大理石和稀盐酸反应制取CO2气体:CO+2H+===CO2↑+H2O
D.将铝片插入硝酸汞溶液中:Al+Hg2+===Al3++Hg
16.下列各组反应,前者与后者均可用同一离子方程式表示的是( )
A.HCl+Na2CO3,HCl+NaHCO3
B.HCl+Na2CO3,HNO3 +K2CO3
C.H2SO4+Ba(OH)2,H2SO4+KOH
D.BaCl2+Na2SO4,BaCO3+HCl
17.下列叙述正确的是( )
A.H++OH-===H2O表示所有强酸和强碱的反应 B.所有的离子方程式都可以表示一类反应
C.单质和氧化物在离子方程式中不能用离子符号表示 D.凡是易溶于水的化合物都可以写成离子形式
18.下列叙述正确的是( )
A.凡是强电解质,在离子方程式中都要以离子形式表示
B.复分解反应用离子方程式表示时总是向着溶液中反应物离子浓度减少的方向进行
C.酸碱中和反应的离子方程式都是H++OH-===H2O
D.凡是酸都可以在离子方程式中用H+表示
19.下列离子方程式书写正确的是( )
A.氢氧化钡与稀硫酸反应:Ba2++SO===BaSO4↓
B.Al2O3溶于盐酸中:O2-+2H+===H2O
C.铜和硝酸银溶液反应:Cu+Ag+===Cu2++Ag
D.Cu(OH)2中加入硝酸:Cu(OH)2+2H+===Cu2++2H2O
20.离子方程式CO+2H+===CO2↑+H2O表示( )
A.碳酸盐与盐酸之间的反应 B.一切碳酸盐与一切酸之间的反应
C.可溶性碳酸盐与强酸之间的反应 D.可溶性碳酸盐与一切酸之间的反应
21.有五瓶标签损坏的试剂,分别盛有AgNO3溶液、稀硝酸、盐酸、BaCl2溶液、K2CO3溶液,为了确定各瓶中是什么试剂,将它们任意编号为A、B、C、D、E,用小试管各取少量,多次进行两两混合反应,反应现象如图所示。图中“↓”表示生成沉淀,“↑”表示生成气体,“×”表示没有明显现象,空格表示实验未做。
A
↓ B
C
↓ × D
↓ ↓ ↑ ↑ E
请回答下列问题:
(1)各试剂瓶中所盛试剂为(填溶质的化学式):A______,B______,C______,D______,E______
(2)写出下列反应的离子方程式
A与E:_______________________________________
B与E:_______________________________________
C与E:_______________________________________
22.某同学欲用离子方程式来表达两种物质相遇时发生的变化。请判断他写出的下列离子方程式是否正确表达了相应的操作和结果;对于不正确的,请帮他改正。
(1)向碳酸钙中加入稀盐酸:H++CO===H2O+CO2↑
______________________________________________________________________________
(2)向CuSO4溶液中滴加Ba(OH)2溶液:SO+Ba2+===BaSO4↓
______________________________________________________________________________
(3)向Na2SO4溶液中滴加CuCl2溶液:SO+Cu2+===CuSO4
______________________________________________________________________________
(4)向氢氧化铜悬浊液中滴加稀硫酸:H++OH-===H2O
______________________________________________________________________________
23.(1)实验室用碳酸钙与盐酸反应制取CO2气体,反应的离子方程式是_______________________________;常用澄清石灰水检验CO2气体,该反应的离子方程式是___________________________________________
(2)表面附有铁锈(成分是Fe2O3)的铁钉放入稀硫酸中,开始反应的离子方程式是__________________________;反应片刻后,可观察到有气体产生,这时反应的离子方程式是_________________________________
(3)人体胃液中的胃酸(主要成分是盐酸),起杀菌、帮助消化等作用,但胃酸的量必须控制在一定范围内。当胃酸过多时,医生通常用“小苏打片”或“胃舒平”给病人治疗。
①用“小苏打片”(NaHCO3)治疗胃酸过多的离子方程式为__________________________________
②如果病人同时患有胃溃疡,此时最好服用“胃舒平”[主要成分是Al(OH)3],反应的离子方程式为_______________________________________________________
24.写出下列反应的离子方程式
(1)NaOH溶液与稀硝酸反应:_________________________________________________
(2)BaCl2溶液与K2SO4溶液反应:______________________________________________
(3)K2CO3溶液与足量稀硫酸反应:_____________________________________________
(4)AgNO3溶液与稀盐酸反应:______________________________________________
(5)碳酸钠溶液与氢氧化钙溶液反应:_________________________________________________
(6)碳酸钙与稀硝酸反应:_________________________________________________
(7)稀硫酸与Ba(OH)2溶液反应:___________________________________________
(8)氯化钠溶液与硝酸银溶液:___________________________________________
(9)氢氧化钡溶液和硫酸铜溶液:___________________________________________
(10)铜与硝酸银溶液反应:___________________________________________
(11)氧化镁溶于稀盐酸:___________________________________________
(12)用碳酸钙与稀盐酸反应制备二氧化碳:___________________________________________
(13)铁与稀硫酸反应生成氢气:___________________________________________
(14)二氧化碳与澄清石灰水反应生成沉淀:___________________________________________
(15)氢氧化铜溶于稀硫酸:___________________________________________
(16)碳酸氢钠与盐酸反应:___________________________________________
25.人体胃液中含有胃酸(0.2%~0.4%的盐酸),起杀菌、帮助消化等作用,但胃酸的量不能过多或过少,它必须控制在一定范围内。当胃酸过多时就会出现“咯酸水”“烧心”“胃部隐隐作痛”等症状。目前市场上的抗酸药主要有①吸收性抗酸药,如NaHCO3等。②非吸收性抗酸药,如CaCO3、MgO、Al(OH)3等
(1)上述所举抗酸药中有 个是电解质
(2)CaCO3作抗酸药时发生反应的离子方程式为_____________________________
(3) (填“可以”或“不可以”)服用BaCO3来治疗胃酸过多,理由是_____________________________
(4)如果病人同时患有胃溃疡,此时最好服用胃舒平[主要成分是Al(OH)3],反应的离子方程式为_______________
26.某同学称取一定质量的MgCl2固体配成溶液,在该溶液中加入一定量的稀盐酸,然后向此混合溶液中逐滴加入NaOH溶液(如图甲所示)。滴加过程中产生沉淀的质量与加入NaOH溶液的体积的关系如图乙所示
请回答下列问题:
(1)溶解MgCl2固体所用的玻璃仪器有 (填字母)
a.天平 b.烧杯 c.漏斗 d.玻璃棒
(2)OA段反应的离子方程式为___________________________________________
(3)AB段反应的离子方程式为___________________________________________
27.用一种试剂除去下列各物质中的杂质(括号内为杂质),并写出离子方程式。
(1)BaCl2(HCl):试剂________,离子方程式为________________________________________
(2)O2(CO2):试剂______________,离子方程式为________________________________________
(3)SO(CO):试剂__________,离子方程式为__________________________________________
28.写出与下列离子方程式相对应的化学方程式 (各两个)
(1)2H++CaCO3===Ca2++H2O+CO2↑
________________________________________、___________________________________________
(2)2H++CO===H2O+CO2↑
________________________________________、___________________________________________
(3)Ba2++SO===BaSO4↓:
________________________________________、___________________________________________
【离子反应】答案
【对点训练1】
1.略
2.
溶液中反应物 化学方程式 离子方程式
HCl+NaOH HCl+NaOH===NaCl+H2O H++OH-===H2O
HCl+KOH HCl+KOH===KCl+H2O H++OH-===H2O
H2SO4+NaOH H2SO4+2NaOH===Na2SO4+2H2O H++OH-===H2O
H2SO4+KOH 2KOH+H2SO4===K2SO4+2H2O OH-+H+===H2O
3.
溶液中反应物 化学方程式 离子方程式
HCl+Cu(OH)2 2HCl+Cu(OH)2===CuCl2+2H2O 2H++Cu(OH)2===Cu2++2H2O
HNO3+NH3 H2O HNO3+NH3 H2O===NH4NO3+H2O H++NH3 H2O===NH+H2O
HF+NaOH HF+NaOH===NaF+H2O HF+OH-===F-+H2O
H2SO4+Ba(OH)2 H2SO4+Ba(OH)2===BaSO4↓+2H2O Ba2++2OH-+2H++SO===BaSO4↓+2H2O
4.C。解析:选项C中的反应不在溶液中进行且无离子参加或生成,不属于离子反应。
5.D。解析:氢氧化钡溶液与稀硫酸反应的离子方程式为Ba2++2OH-+2H++SO===BaSO4↓+2H2O,④不正确;①②③正确。
6.B。解析:易电离产生H+的化合物与易电离产生OH-的化合物反应,生成易溶、易电离的盐和水,都可用离子方程式H++OH-===H2O来表示。
7.C
8.D。解析:H++OH-===H2O可以代表强酸和强碱反应生成可溶于水的盐和水的反应,如盐酸和氢氧化钠、盐酸和氢氧化钡、硝酸和氢氧化钾等,故A错误;CO+2H+===CO2↑+H2O代表可溶性的碳酸盐和强酸之间的反应,如碳酸钠和盐酸、碳酸钠和硝酸等,故B错误;Zn(OH)2+2H+===Zn2++2H2O代表氢氧化锌和强酸之间的反应,如:氢氧化锌和盐酸、硝酸、硫酸等,故C错误;Ba2++2OH-+Cu2++SO===BaSO4↓+Cu(OH)2↓只能表示氢氧化钡和硫酸铜之间的反应,故D正确。
9.C。解析:CuCO3是难溶盐,在书写离子方程式时不能拆开,故A错误;有H2O生成,反应的离子方程式为Ba2++2H++2OH-+SO===BaSO4↓+2H2O,故B错误;AgNO3和NaCl反应的实质为Ag++Cl-===AgCl↓,化学方程式与离子方程式相对应,故C正确;Cu(OH)2不溶于水,不能拆成Cu2+和OH-,故D错误。
【对点训练2】
1.A。解析:澄清的石灰水是强碱溶液,应拆分为离子,B错误;醋酸是弱电解质不可拆,C错误;碳酸钡难溶于水,不能拆成离子形式,D错误。
2.B。解析:B项,违背电荷守恒,错误。
3.C。解析:BaSO4属于难溶性盐,在离子方程式中应写成化学式;CH3COOH属于弱电解质,在离子方程式中应写成化学式。则H+不能代表的物质是②④⑤。
【对点训练3】
1.D。解析:选项D中的溶液混合无沉淀、气体或水生成,不能发生离子反应。
2.C。解析:物质在溶液中是否能够发生化学反应,可根据是否生成难溶性物质,是否生成难电离的物质或是否生成易挥发性物质来进行判断。Na2SO4和MgCl2溶液混合后既没有难溶性物质,也没有难电离的物质和易挥发性物质生成,故不发生离子反应。
3.C。解析:离子反应不一定都有沉淀生成,有气体或难电离的物质生成的也是离子反应;有气体生成的不一定是离子反应,如碳酸钙加热分解生成二氧化碳气体的反应不是离子反应;二氧化碳与烧碱溶液反应有碳酸根离子和水生成,该反应属于离子反应。
4.D。解析:NaHCO3和NaHSO4的电离方程式分别为NaHCO3===Na++HCO、NaHSO4===Na++H++SO,故D项正确。
5.C。解析:置换反应与复分解反应没有相交的关系,离子反应与置换反应和复分解反应有相交的关系。
6.A。解析:NaOH是碱,KCl是盐,碱与盐的反应应为复分解反应,此反应不满足复分解反应发生的条件,所以不能发生。
7.B。解析:CH3COO-只能结合H+转化为CH3COOH,属于碱,A错误;HSO可以结合H+转化为H2SO3,属于碱,也可以释放H+转化为SO,属于酸,B正确;OH-只能结合H+转化为H2O,属于碱,C错误;NH只能释放H+转化为NH3,属于酸,D错误。
【课时跟踪检测】
1.C。解析:Ⅰ中虽无明显现象,但发生了离子反应:H++OH-===H2O,A项错误;Ⅱ中发生反应:Ba2++SO===BaSO4↓,白色沉淀为BaSO4,B项错误;Ⅲ中的反应是离子反应,离子方程式为Zn+2H+===Zn2++H2↑,C项正确、D项错误。
2.B。解析:A项,不具备复分解反应发生的条件;B项,离子反应是Zn+2H+===Zn2++H2↑;C项,不是在溶液中进行的反应;D项,不是离子反应。
3.C。解析:CaCO3难溶于水,CH3COOH难电离,在离子方程式中都要写成化学式。
4.D。解析:醋酸是弱酸,书写离子方程式时,应写成CH3COOH;氢氧化镁难溶于水,应写其化学式Mg(OH)2;C项反应生成的硫酸钡难溶于水,漏掉了另一个离子反应Ba2++SO===BaSO4↓。
5.B。解析:选项B中的碳酸钡不溶于水,不能写成离子的形式。
6.C。解析:A项中ZnCO3难溶于水;B项中OH-和H+生成H2O;D项中AgCl难溶于水。
7.C。解析:A项中HCl要拆写成离子形式,B项中Ca(OH)2应拆写成离子形式,D项中Fe与稀盐酸反应生成Fe2+。
8.B。解析:MgO不能拆开写。
9.D。解析:氧化物不能拆写。
10.D。解析:碳酸钙难溶,碳酸钙跟盐酸反应的离子方程式:2H++CaCO3===H2O+CO2↑+Ca2+,故A错误;铁粉跟稀盐酸反应生成氯化亚铁和氢气的离子方程式:Fe+2H+===Fe2++H2↑,故B错误;离子方程式要符合电荷守恒,硝酸银溶液跟铜反应的离子方程式:Cu+2Ag+===Cu2++2Ag,故C错误;用小苏打治疗胃酸过多生成氯化钠、水和二氧化碳的离子方程式:HCO+H+===CO2↑+H2O,故D正确。
11.D。解析:A项正确的离子方程式为Fe+2H+===Fe2++H2↑;B项正确的离子方程式为2Na+2H2O===2Na++2OH-+H2↑;C项正确的离子方程式为CaCO3+2CH3COOH===Ca2++2CH3COO-+CO2↑+H2O。
12.C。解析:NaHSO4在水溶液中的电离方程式:NaHSO4===Na++H++SO,A错误;氢氧化铁胶体的制备原理为向沸水中滴加饱和氯化铁溶液,化学方程式为:FeCl3+3H2OFe(OH)3(胶体)+3HCl,B错误;铜片插入硝酸银溶液中发生置换反应生成铜离子和银:Cu+2Ag+===Cu2++2Ag,C正确;将Ba(OH)2溶液滴入稀H2SO4溶液中,氢离子消耗完全:Ba2++2OH-+2H++SO===2H2O+BaSO4↓,D错误。
13.B。解析:MgCl2为可溶性电解质,应拆分为离子,正确的离子方程式为Mg+2H+===Mg2++H2↑,故A错误;Na2CO3为可溶性强电解质,应拆分为离子,正确的离子方程式为CO+2H+===H2O+CO2↑,故C错误;Mg(OH)2为难溶物,不可拆成离子形式,故D错误。
14.D。解析:A项,应写为Ba2++2OH-+2H++SO===BaSO4↓+2H2O;B项,应写为Cu(OH)2+2H+===Cu2++2H2O;C项,离子方程式中前后电荷不守恒,应写为Zn+2Ag+===2Ag+Zn2+。
15.A。解析:B项,Fe(OH)3胶体不是沉淀,不能标注“↓”,错误;C项,CaCO3为不溶于水的固体不能写成离子形式,错误;D项,电荷不守恒,错误。
16.B。解析:A项,前者:2H++CO===H2O+CO2↑或H++CO===HCO;后者:H++HCO===H2O+CO2↑。B项,前者:2H++CO===H2O+CO2↑;后者:2H++CO===H2O+CO2↑。C项,前者:2H++SO+Ba2++2OH-===BaSO4↓+2H2O;后者:H++OH-===H2O。D项,前者:Ba2++SO===BaSO4↓;后者:BaCO3+2H+===Ba2++CO2↑+H2O。
17.C
18.B
19.D。解析:反应过程中OH-与H+生成H2O,正确的离子方程式为Ba2++2OH-+2H++SO===BaSO4↓+2H2O,A项错误;氧化物不能拆分为离子,正确的离子方程式为Al2O3+6H+===2Al3++3H2O,B项错误;电荷不守恒,C项错误;Cu(OH)2是难溶碱,书写离子方程式时不可拆成离子,D项正确。
20.C。解析:CO只代表可溶性的碳酸盐,故选项A和选项B都是不正确的;H+只代表强酸而不是一切酸(如弱酸H2S、HF、CH3COOH等均不能用H+表示),故选项C正确,选项D不正确。
21.(1)BaCl2 AgNO3 HNO3 HCl K2CO3
(2)Ba2++CO===BaCO3↓ 2Ag++CO===Ag2CO3↓ CO+2H+===H2O+CO2↑
解析:根据题意,E与A、B反应分别产生沉淀,与C、D反应分别产生气体,可推知E为K2CO3溶液,A、B可能为AgNO3和BaCl2中的一种,C、D必为稀硝酸和盐酸中的一种,而B与D能产生沉淀,可确定B为AgNO3溶液,D为盐酸,因此A为BaCl2溶液,C为稀硝酸。
22.(1)错误,正确的是2H++CaCO3===Ca2++CO2↑+H2O
(2)错误,正确的是Cu2++SO+Ba2++2OH-===Cu(OH)2↓+BaSO4↓
(3)错误,两者不反应
(4)错误,正确的是Cu(OH)2+2H+===Cu2++2H2O
23.(1)CaCO3+2H+===Ca2++CO2↑+H2O Ca2++2OH-+CO2===CaCO3↓+H2O
(2)Fe2O3+6H+===2Fe3++3H2O Fe+2H+===Fe2++H2↑
(3)①HCO+H+===CO2↑+H2O
②Al(OH)3+3H+===Al3++3H2O
24.(1)OH-+H+===H2O
(2)Ba2++SO===BaSO4↓
(3)CO+2H+===H2O+CO2↑
(4)Ag++Cl-===AgCl↓
(5)Ca2++CO===CaCO3↓
(6)CaCO3+2H+===H2O+CO2↑+Ca2+
(7)2H++SO+Ba2++2OH-===BaSO4↓+2H2O
(8)Cl-+Ag+===AgCl↓
(9)Ba2++2OH-+SO+Cu2+===BaSO4↓+Cu(OH)2↓
(10)Cu+2Ag+===Cu2++2Ag
(11)MgO+2H+===Mg2++H2O
(12)CaCO3+2H+===Ca2++CO2↑+H2O
(13)Fe+2H+===Fe2++H2↑
(14)Ca2++2OH-+CO2===CaCO3↓+H2O
(15)Cu(OH)2+2H+===Cu2++2H2O
(16)HCO+H+===CO2↑+H2O
25.(1)4
(2)CaCO3+2H+===Ca2++CO2↑+H2O
(3)不可以 Ba2+是重金属离子,对人体有害
(4)Al(OH)3+3H+===Al3++3H2O
解析:(1)在水溶液里或熔融状态下能够导电的化合物是电解质,碳酸氢钠、碳酸钙、氧化镁和氢氧化铝均是电解质,则上述所举抗酸药中有4个是电解质。(2)CaCO3作抗酸药时与氢离子反应,则发生反应的离子方程式为CaCO3+2H+===Ca2++H2O+CO2↑。(3)碳酸钡与酸反应生成钡离子,Ba2+是重金属离子,对人体有害,因此不可以服用BaCO3来治疗胃酸过多。(4)胃舒平中的Al(OH)3难溶于水,作抗酸药时和胃酸中的H+反应的离子方程式为Al(OH)3+3H+===Al3++3H2O。
26.(1)bd
(2)H++OH-===H2O
(3)Mg2++2OH-===Mg(OH)2↓
解析:(1)溶解MgCl2固体所用的玻璃仪器有烧杯和玻璃棒。(2)OA段没有沉淀生成,说明是盐酸和氢氧化钠的反应。(3)AB段为氯化镁和氢氧化钠反应生成氢氧化镁沉淀。
27.(1)BaCO3 BaCO3+2H+===Ba2++H2O+CO2↑
(2)足量NaOH溶液 CO2+2OH-===CO+H2O
(3)适量稀硫酸 CO+2H+===H2O+CO2↑
28.略
PAGE
