四川省达州市2023-2024学年高二上学期期末监测化学试题(含答案)
文档属性
| 名称 | 四川省达州市2023-2024学年高二上学期期末监测化学试题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 622.4KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-22 11:38:07 | ||
图片预览


文档简介
达州市2023年普通高中二年级秋季期末监测
化学试题
本试卷分选择题和非选择题两部分,第Ⅰ卷(选择题)部分1至4页,第Ⅱ卷(非选择题)部分4至6页,共6页,满分100分,考试时间75分钟.
注意事项:
1.答题前,考生务必将自己的姓名、考号用0.5毫米黑色字迹的签字笔或钢笔填写在答题卡上,将条形码贴在答题卡规定的位置上
2.选择题必须使用铅笔将答案标号填涂在答题卡上对应题目标号的位置上,非选择题用0.5毫米黑色字迹的签字笔或钢笔书写在答题卡的对应框内,超出答题区书写的答案无效;在草稿纸,试题卷上的答案无效.
3.考试结束后,将答题卡收回.
可能用到的相对原子质量:
第Ⅰ卷(选择题,共42分)
一、选择题(本大题共14个小题,每小题只有1个选项符合题意。每小题3分,共42分)
1.化学与生产、生活息息相关。下列有关说法错误的是
A.酒曲酿酒,利用了催化剂使平衡正向移动的原理
B.采用低温冷冻技术保存食物可减慢食物腐烂速率
C.海港码头的钢管桩,可利用“外加电流法”防腐蚀
D.盐碱地(含较多 等)可通过施加适量石膏 ,降低土壤的碱性
2.下列事实不能用勒夏特列原理解释的是
A.合成氨工业中将氨液化分离
B.夏天打开可乐瓶盖产生气泡
C.常用排饱和食盐水的方法收集
D.由 组成的平衡体系加压后颜色变深
3.设 为阿伏加德罗常数的值,下列说法正确的是
A.液中阴离子总数小于
B.的 液中,含有 数目为
C.与 在密闭容器中充分反应后分子的数目为
D.电解精炼铜时,阴极质量增加 电路中转移电子数为
4.下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明溶液中:
B.滴加石蕊试液显红色的溶液中:
C.与 反应产生 的溶液中:
D.溶液中:
5.下列指定反应的方程式正确的是
A.溶于水的离子方程式:
B.的燃烧热 ,则 时:
C.溶液中加入
D.溶液中加入足量澄清石灰水:
6.下列说法正确的是
A.使用催化剂可降低反应活化能,增大活化分子百分数,提高反应物的转化率
B.常温,反应 能自发进行,则该反应的
C.若 ,则含 的溶液与浓硫酸完全反应,放出的热量为
D.镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀
7.普通锌锰电池放电时发生的主要反应为:,碱性锌锰电池的总反应为:。下列说法正确的是
A.普通锌锰电池为一次电池,该废旧电池可反复充放电
B.普通锌锰电池正极反应式为:
C.碱性锌锰电池工作时 没有发挥作用
D.两种电池工作时电子均由 经外电路流向
8.下列实验操作、现象和结论(或目的)正确的是
选项 操作 现象 结论(或目的)
A 挤压碱式滴定管胶管内玻璃球 滴定管尖嘴部位有液体流出 赶碱式滴定管尖嘴 部位气泡
B 测同浓度和溶液的pH 的pH试 纸蓝色更深 酸性:
C 产生蓝色沉淀 溶液中有
D 浸泡在热水中的烧瓶气体颜色变深 为吸热反应
9.常温下,下列说法正确的是
A.加入 可除去 酸性溶液中的
B.相等的三种溶液① ② ③,其物质的量浓度:②①③
C.将 的 溶液和氨水各 分别稀释至 ,所得 溶液的 略大
D.将 的盐酸与 的 溶液混合后,若所得溶液的 则
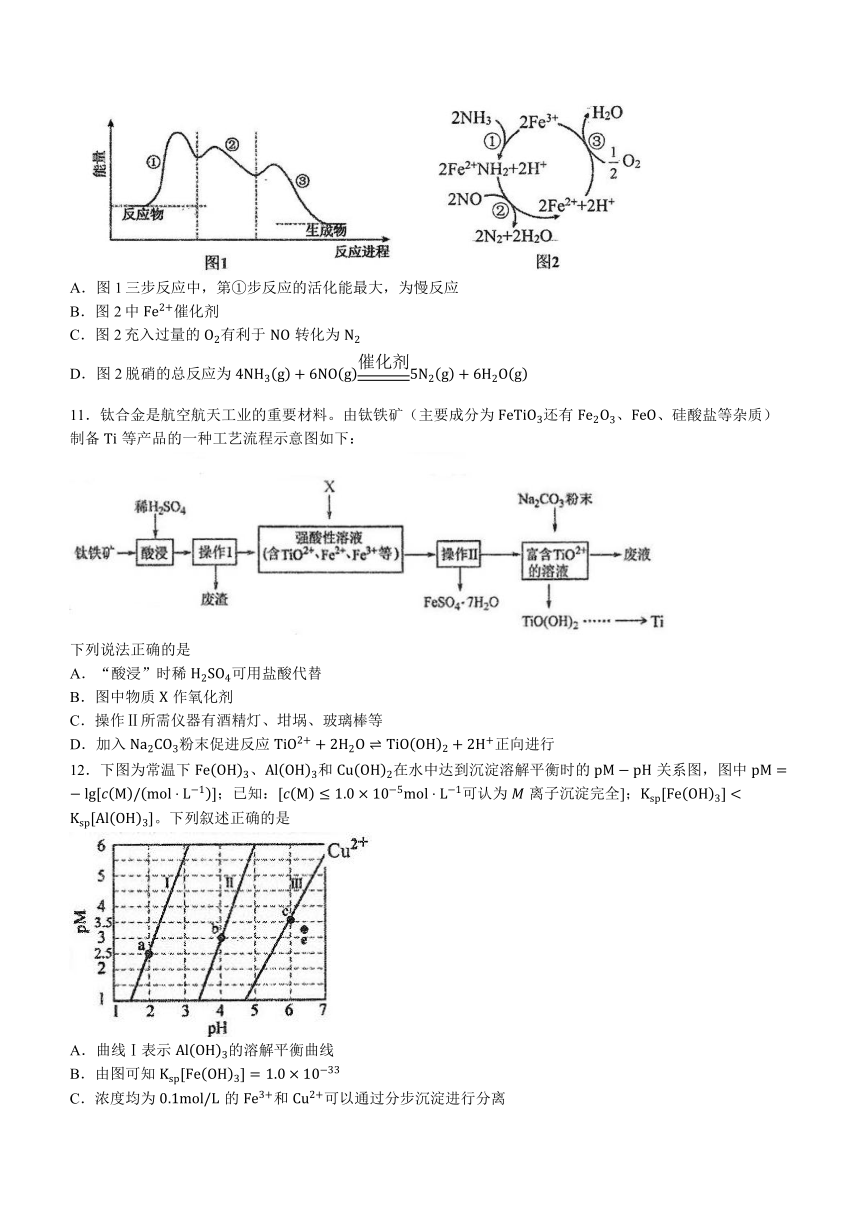
10.催化还原 是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现,在催化剂上可能发生的反应过程如图2所示。下列说法正确的是
A.图1三步反应中,第①步反应的活化能最大,为慢反应
B.图2中 催化剂
C.图2充入过量的 有利于 转化为
D.图2脱硝的总反应为
11.钛合金是航空航天工业的重要材料。由钛铁矿(主要成分为 还有 、硅酸盐等杂质)制备 等产品的一种工艺流程示意图如下:
下列说法正确的是
A.“酸浸”时稀 可用盐酸代替
B.图中物质 作氧化剂
C.操作Ⅱ所需仪器有酒精灯、坩埚、玻璃棒等
D.加入 粉末促进反应 正向进行
12.下图为常温下 和 在水中达到沉淀溶解平衡时的 关系图,图中 ;已知:可认为 离子沉淀完全];。下列叙述正确的是
A.曲线Ⅰ表示 的溶解平衡曲线
B.由图可知
C.浓度均为 的 和 可以通过分步沉淀进行分离
D.加入蒸馏水后,可使 点溶液变到 点
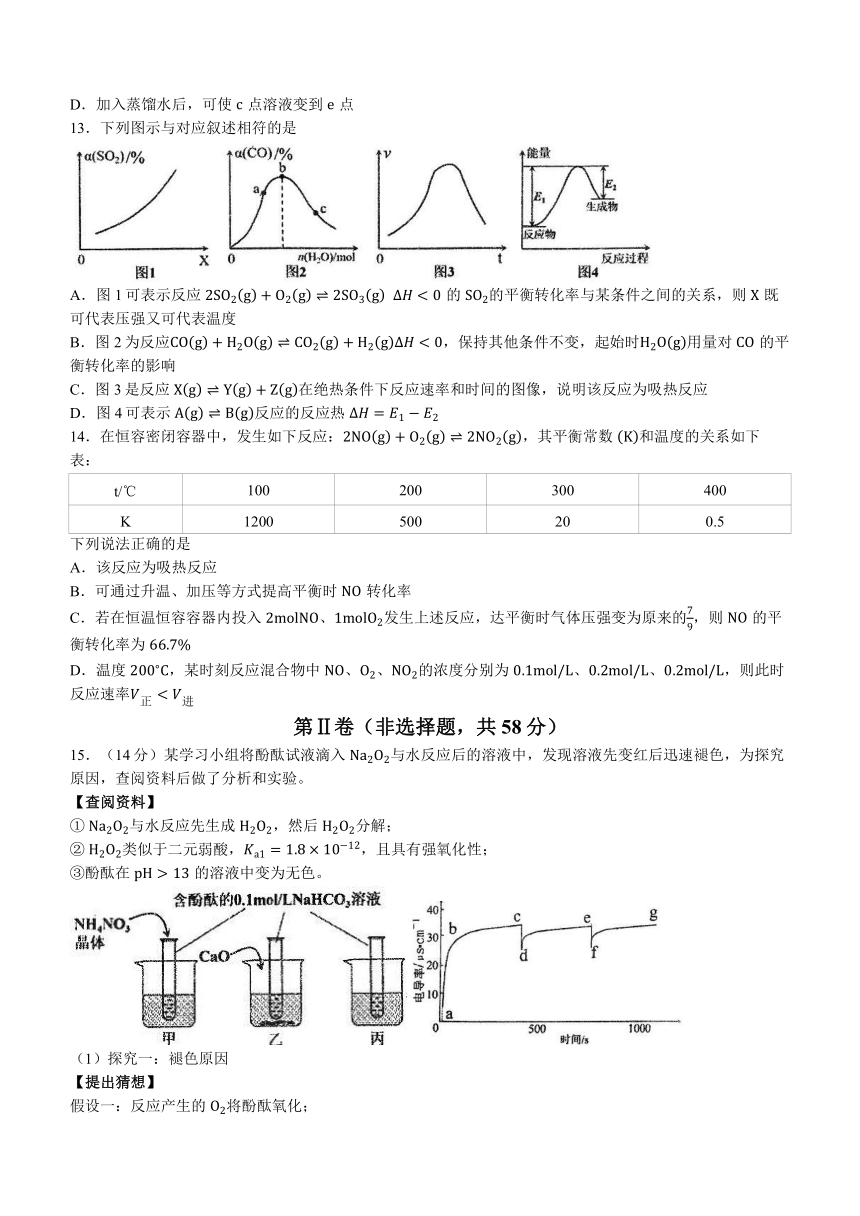
13.下列图示与对应叙述相符的是
A.图1可表示反应 的 的平衡转化率与某条件之间的关系,则 既可代表压强又可代表温度
B.图2为反应,保持其他条件不变,起始时用量对 的平衡转化率的影响
C.图3是反应 在绝热条件下反应速率和时间的图像,说明该反应为吸热反应
D.图4可表示 反应的反应热
14.在恒容密闭容器中,发生如下反应:,其平衡常数 和温度的关系如下表:
t/℃ 100 200 300 400
K 1200 500 20 0.5
下列说法正确的是
A.该反应为吸热反应
B.可通过升温、加压等方式提高平衡时 转化率
C.若在恒温恒容容器内投入 发生上述反应,达平衡时气体压强变为原来的,则 的平衡转化率为
D.温度 ,某时刻反应混合物中 的浓度分别为 、,则此时反应速率
第Ⅱ卷(非选择题,共58分)
15.(14分)某学习小组将酚酞试液滴入 与水反应后的溶液中,发现溶液先变红后迅速褪色,为探究原因,查阅资料后做了分析和实验。
【查阅资料】
① 与水反应先生成 ,然后 分解;
② 类似于二元弱酸,,且具有强氧化性;
③酚酞在的溶液中变为无色。
(1)探究一:褪色原因
【提出猜想】
假设一:反应产生的 将酚酞氧化;
假设二:反应产生的 将酚酞氧化;
假设三:溶液浓度过高导致酚酞试液褪色。
实验如下表,请填写空白:
实验编号 实验操作 实验现象 实验结论
① 在的溶液中滴加5滴酚酞试液,再通入足量 溶液变红后不褪色 假设一:
② 在的溶液中滴加5滴酚酞试液,再滴加 的溶液 假设二:成立
③ 在的溶液中滴加5滴酚酞试液 溶液先变红,后褪色 假设三:成立
【提出猜想】
(2)针对假设二,有同学提出还应补充实验才能证明 与水反应生成了 则补充的实验操作为:
(3)探究二:的性质及应用
①的酸性
用化学用语表示 显酸性的原因
②的还原性
某实验用量筒量取浓 溶液配制 溶液,所需玻璃仪器除量筒、烧杯、玻璃棒外,还有 。现用 酸性 液滴定所配 溶液,取 溶液于锥形瓶中,完成三次实验平均消耗 标准溶液 ,该反应的离子方程式为: ,标定的 溶液浓度为 。
③若滴定时出现以下情况,将导致测定结果偏高的是
A.装入标准酸性 溶液时,未润洗滴定管
B.滴入最后半滴标准液出现颜色变化就立即停止滴定
C.滴定前盛标准液的滴定管尖嘴处有气泡,滴定后气泡消失
D.记录标准液体积时,滴定前仰视读数,滴定后俯视读数
16.(14分)根据下列物质:① ② ③溶液 ④冰醋酸⑤ ⑥ ⑦ ⑧晶体,回答下列有关问题:
(1)以上物质中属于强电解质的是 (填编号)
(2)常温,测得 中 为 ,则 在该温度下的电离常数 约为 (结果保留一位小数)
(3)常温,,下列有关说法正确的是
A.向冰醋酸中加水,溶液的导电能力先增大后减小
B.向 溶液中加水稀释,增大
C.等温等浓度 混合溶液中,
D.为3的 溶液中,水电离的 为
(4)室温下,将三支装入含酚酞的 溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入 晶体,在乙烧杯中加入 。
写出 溶液中碳元素的守恒关系式: ;一段时间后,甲烧杯试管中溶液颜色 (填“变深”、“变浅”、“不变”);结合方程式解释乙烧杯中加 后其试管内颜色变化的原因:
(5)将 溶于 蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入 蒸馏水(加水过程,始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
则下列说法不正确的是
A.点电导率相等
B.点为饱和溶液
C.电导率基本不变的原因是 到溶解平衡
D.点再加 蒸馏水可重复 图像
17.(14分) 催化加氢制甲醇有利于减少 放,实现“碳达峰”,其总反应可表示为: ;
另有反应①:
反应②: 。
温度分别为 时,在 恒容密闭容器中充入 和一定量 按不同投料比发生总反应,绘制的 平衡转化率如图1。回答下列问题:
(1)由以上数据计算
(2)判定 填“”、“”或 “=”)
(3)若总反应进行到 点状态时耗时,则建立此状态过程中用 表示的平均反应速率 ,点的平衡常数 (保留2位小数)
(4)恒温恒容,能说明总反应达到平衡状态的是
A. B.混合气体的平均相对分子质量不变
C.混合气体的密度不变 D.容器内气体压强不变
(5)若将一定比例的 和 在装有催化剂的反应器中反应数小时。体系中甲醇的产率与温度的关系如图2所示。温度为 时,图中 点 (填“是”或“不是”)处于平衡状态。结合相关信息分析,如图 点之后,甲醇产率变化的原因可能是:①温度升高,生成的选择性降低;② ;③
18.(16分 是一种高效、安全消毒剂。目前已开发出多种电解法制取 气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取 ;方法二:如图丙,电极上通入 酸性溶液中电解 制取 。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
回答下:下列问题:
(1)图甲中,操作 为 ,试剂 Ⅱ为 (填化学式)
(2)图乙中,电解精制饱和食盐水产生 的电极反应式为 ;电解一段时间,若有 通过离子交换膜,在电极 上产生的气体体积(标准状况)为
(3)图丙中,阴极电极反应式为 ;电解一段时间后,阴极区(溶液体积变化忽略不计 溶液的 (填“变大”、“变小”、“不变”)
(4)若以图丁所示电池作图乙的电源,则 端与 相连(填 “”或 “”),图乙中阳极的另一产物可不断补充到图丁的正极区,该物质是 (填化学式)
(5)工业生产中,还可以用酸性 溶液还原 制得 ,则每生成 ,转移电子的数目为
【参考答案】
达州市2023年普通高中二年级秋季期末监测
化学试题
第Ⅰ卷(选择题,共42分)
一、选择题(本大题共14个小题,每小题只有1个选项符合题意。每小题3分,共42分)
1.A 2.D 3.D 4.A 5.C 6.B 7.B 8.C 9.D 10.A 11.D 12.C 13.D 14.C
第Ⅱ卷(非选择题,共58分)
15.(1) 不成立(1分); 溶液先变红,后褪色(1分)
(2) 向反应后的溶液中加入少量 ,若产生大量能使带火星的木条复燃的气体,则可证明 与水反应生成了
(3) ① (只写第一步不扣分)
② 容量瓶、胶头滴管; ;
③ AC
16.(1) ②⑦⑧
(2)
(3) AD
(4) (或 ); 变浅; 乙烧杯中加入 与水反应放热,使 的水解反应: 平衡正向移动,增大,溶液红色加深
(5) B
17.(1)
(2) (1分)
(3) ; 0.52
(4) BD
(5) 不是(1分); 温度升高催化剂活性降低;; 反应②为吸热反应,温度升高,反应②正向进行趋势大,使 产率降低(或总反应为放热反应,升温,平衡逆向进行,使 产率降低)
18.(1) 过滤(1分); (1分)
(2) (不写“↑”不扣分); 11.2
(3) ; 不变
(4) ;
(5) (写 不扣分)
化学试题
本试卷分选择题和非选择题两部分,第Ⅰ卷(选择题)部分1至4页,第Ⅱ卷(非选择题)部分4至6页,共6页,满分100分,考试时间75分钟.
注意事项:
1.答题前,考生务必将自己的姓名、考号用0.5毫米黑色字迹的签字笔或钢笔填写在答题卡上,将条形码贴在答题卡规定的位置上
2.选择题必须使用铅笔将答案标号填涂在答题卡上对应题目标号的位置上,非选择题用0.5毫米黑色字迹的签字笔或钢笔书写在答题卡的对应框内,超出答题区书写的答案无效;在草稿纸,试题卷上的答案无效.
3.考试结束后,将答题卡收回.
可能用到的相对原子质量:
第Ⅰ卷(选择题,共42分)
一、选择题(本大题共14个小题,每小题只有1个选项符合题意。每小题3分,共42分)
1.化学与生产、生活息息相关。下列有关说法错误的是
A.酒曲酿酒,利用了催化剂使平衡正向移动的原理
B.采用低温冷冻技术保存食物可减慢食物腐烂速率
C.海港码头的钢管桩,可利用“外加电流法”防腐蚀
D.盐碱地(含较多 等)可通过施加适量石膏 ,降低土壤的碱性
2.下列事实不能用勒夏特列原理解释的是
A.合成氨工业中将氨液化分离
B.夏天打开可乐瓶盖产生气泡
C.常用排饱和食盐水的方法收集
D.由 组成的平衡体系加压后颜色变深
3.设 为阿伏加德罗常数的值,下列说法正确的是
A.液中阴离子总数小于
B.的 液中,含有 数目为
C.与 在密闭容器中充分反应后分子的数目为
D.电解精炼铜时,阴极质量增加 电路中转移电子数为
4.下列各组离子在指定溶液中一定能大量共存的是
A.澄清透明溶液中:
B.滴加石蕊试液显红色的溶液中:
C.与 反应产生 的溶液中:
D.溶液中:
5.下列指定反应的方程式正确的是
A.溶于水的离子方程式:
B.的燃烧热 ,则 时:
C.溶液中加入
D.溶液中加入足量澄清石灰水:
6.下列说法正确的是
A.使用催化剂可降低反应活化能,增大活化分子百分数,提高反应物的转化率
B.常温,反应 能自发进行,则该反应的
C.若 ,则含 的溶液与浓硫酸完全反应,放出的热量为
D.镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易被腐蚀
7.普通锌锰电池放电时发生的主要反应为:,碱性锌锰电池的总反应为:。下列说法正确的是
A.普通锌锰电池为一次电池,该废旧电池可反复充放电
B.普通锌锰电池正极反应式为:
C.碱性锌锰电池工作时 没有发挥作用
D.两种电池工作时电子均由 经外电路流向
8.下列实验操作、现象和结论(或目的)正确的是
选项 操作 现象 结论(或目的)
A 挤压碱式滴定管胶管内玻璃球 滴定管尖嘴部位有液体流出 赶碱式滴定管尖嘴 部位气泡
B 测同浓度和溶液的pH 的pH试 纸蓝色更深 酸性:
C 产生蓝色沉淀 溶液中有
D 浸泡在热水中的烧瓶气体颜色变深 为吸热反应
9.常温下,下列说法正确的是
A.加入 可除去 酸性溶液中的
B.相等的三种溶液① ② ③,其物质的量浓度:②①③
C.将 的 溶液和氨水各 分别稀释至 ,所得 溶液的 略大
D.将 的盐酸与 的 溶液混合后,若所得溶液的 则
10.催化还原 是重要的烟气脱硝技术,其反应过程与能量关系如图1所示。研究发现,在催化剂上可能发生的反应过程如图2所示。下列说法正确的是
A.图1三步反应中,第①步反应的活化能最大,为慢反应
B.图2中 催化剂
C.图2充入过量的 有利于 转化为
D.图2脱硝的总反应为
11.钛合金是航空航天工业的重要材料。由钛铁矿(主要成分为 还有 、硅酸盐等杂质)制备 等产品的一种工艺流程示意图如下:
下列说法正确的是
A.“酸浸”时稀 可用盐酸代替
B.图中物质 作氧化剂
C.操作Ⅱ所需仪器有酒精灯、坩埚、玻璃棒等
D.加入 粉末促进反应 正向进行
12.下图为常温下 和 在水中达到沉淀溶解平衡时的 关系图,图中 ;已知:可认为 离子沉淀完全];。下列叙述正确的是
A.曲线Ⅰ表示 的溶解平衡曲线
B.由图可知
C.浓度均为 的 和 可以通过分步沉淀进行分离
D.加入蒸馏水后,可使 点溶液变到 点
13.下列图示与对应叙述相符的是
A.图1可表示反应 的 的平衡转化率与某条件之间的关系,则 既可代表压强又可代表温度
B.图2为反应,保持其他条件不变,起始时用量对 的平衡转化率的影响
C.图3是反应 在绝热条件下反应速率和时间的图像,说明该反应为吸热反应
D.图4可表示 反应的反应热
14.在恒容密闭容器中,发生如下反应:,其平衡常数 和温度的关系如下表:
t/℃ 100 200 300 400
K 1200 500 20 0.5
下列说法正确的是
A.该反应为吸热反应
B.可通过升温、加压等方式提高平衡时 转化率
C.若在恒温恒容容器内投入 发生上述反应,达平衡时气体压强变为原来的,则 的平衡转化率为
D.温度 ,某时刻反应混合物中 的浓度分别为 、,则此时反应速率
第Ⅱ卷(非选择题,共58分)
15.(14分)某学习小组将酚酞试液滴入 与水反应后的溶液中,发现溶液先变红后迅速褪色,为探究原因,查阅资料后做了分析和实验。
【查阅资料】
① 与水反应先生成 ,然后 分解;
② 类似于二元弱酸,,且具有强氧化性;
③酚酞在的溶液中变为无色。
(1)探究一:褪色原因
【提出猜想】
假设一:反应产生的 将酚酞氧化;
假设二:反应产生的 将酚酞氧化;
假设三:溶液浓度过高导致酚酞试液褪色。
实验如下表,请填写空白:
实验编号 实验操作 实验现象 实验结论
① 在的溶液中滴加5滴酚酞试液,再通入足量 溶液变红后不褪色 假设一:
② 在的溶液中滴加5滴酚酞试液,再滴加 的溶液 假设二:成立
③ 在的溶液中滴加5滴酚酞试液 溶液先变红,后褪色 假设三:成立
【提出猜想】
(2)针对假设二,有同学提出还应补充实验才能证明 与水反应生成了 则补充的实验操作为:
(3)探究二:的性质及应用
①的酸性
用化学用语表示 显酸性的原因
②的还原性
某实验用量筒量取浓 溶液配制 溶液,所需玻璃仪器除量筒、烧杯、玻璃棒外,还有 。现用 酸性 液滴定所配 溶液,取 溶液于锥形瓶中,完成三次实验平均消耗 标准溶液 ,该反应的离子方程式为: ,标定的 溶液浓度为 。
③若滴定时出现以下情况,将导致测定结果偏高的是
A.装入标准酸性 溶液时,未润洗滴定管
B.滴入最后半滴标准液出现颜色变化就立即停止滴定
C.滴定前盛标准液的滴定管尖嘴处有气泡,滴定后气泡消失
D.记录标准液体积时,滴定前仰视读数,滴定后俯视读数
16.(14分)根据下列物质:① ② ③溶液 ④冰醋酸⑤ ⑥ ⑦ ⑧晶体,回答下列有关问题:
(1)以上物质中属于强电解质的是 (填编号)
(2)常温,测得 中 为 ,则 在该温度下的电离常数 约为 (结果保留一位小数)
(3)常温,,下列有关说法正确的是
A.向冰醋酸中加水,溶液的导电能力先增大后减小
B.向 溶液中加水稀释,增大
C.等温等浓度 混合溶液中,
D.为3的 溶液中,水电离的 为
(4)室温下,将三支装入含酚酞的 溶液的试管分别放在盛水的烧杯中,然后在甲烧杯试管中加入 晶体,在乙烧杯中加入 。
写出 溶液中碳元素的守恒关系式: ;一段时间后,甲烧杯试管中溶液颜色 (填“变深”、“变浅”、“不变”);结合方程式解释乙烧杯中加 后其试管内颜色变化的原因:
(5)将 溶于 蒸馏水,测定电导率随时间的变化,当电导率不变时,再加入 蒸馏水(加水过程,始终未完全溶解),观察电导率的变化,重复操作,绘图如下:
则下列说法不正确的是
A.点电导率相等
B.点为饱和溶液
C.电导率基本不变的原因是 到溶解平衡
D.点再加 蒸馏水可重复 图像
17.(14分) 催化加氢制甲醇有利于减少 放,实现“碳达峰”,其总反应可表示为: ;
另有反应①:
反应②: 。
温度分别为 时,在 恒容密闭容器中充入 和一定量 按不同投料比发生总反应,绘制的 平衡转化率如图1。回答下列问题:
(1)由以上数据计算
(2)判定 填“”、“”或 “=”)
(3)若总反应进行到 点状态时耗时,则建立此状态过程中用 表示的平均反应速率 ,点的平衡常数 (保留2位小数)
(4)恒温恒容,能说明总反应达到平衡状态的是
A. B.混合气体的平均相对分子质量不变
C.混合气体的密度不变 D.容器内气体压强不变
(5)若将一定比例的 和 在装有催化剂的反应器中反应数小时。体系中甲醇的产率与温度的关系如图2所示。温度为 时,图中 点 (填“是”或“不是”)处于平衡状态。结合相关信息分析,如图 点之后,甲醇产率变化的原因可能是:①温度升高,生成的选择性降低;② ;③
18.(16分 是一种高效、安全消毒剂。目前已开发出多种电解法制取 气体的新工艺,方法一:如图乙,电解精制饱和食盐水制取 ;方法二:如图丙,电极上通入 酸性溶液中电解 制取 。某浓差电池的示意图如图丁,该电池既能提供电能,又能产生产生多种化学品。
回答下:下列问题:
(1)图甲中,操作 为 ,试剂 Ⅱ为 (填化学式)
(2)图乙中,电解精制饱和食盐水产生 的电极反应式为 ;电解一段时间,若有 通过离子交换膜,在电极 上产生的气体体积(标准状况)为
(3)图丙中,阴极电极反应式为 ;电解一段时间后,阴极区(溶液体积变化忽略不计 溶液的 (填“变大”、“变小”、“不变”)
(4)若以图丁所示电池作图乙的电源,则 端与 相连(填 “”或 “”),图乙中阳极的另一产物可不断补充到图丁的正极区,该物质是 (填化学式)
(5)工业生产中,还可以用酸性 溶液还原 制得 ,则每生成 ,转移电子的数目为
【参考答案】
达州市2023年普通高中二年级秋季期末监测
化学试题
第Ⅰ卷(选择题,共42分)
一、选择题(本大题共14个小题,每小题只有1个选项符合题意。每小题3分,共42分)
1.A 2.D 3.D 4.A 5.C 6.B 7.B 8.C 9.D 10.A 11.D 12.C 13.D 14.C
第Ⅱ卷(非选择题,共58分)
15.(1) 不成立(1分); 溶液先变红,后褪色(1分)
(2) 向反应后的溶液中加入少量 ,若产生大量能使带火星的木条复燃的气体,则可证明 与水反应生成了
(3) ① (只写第一步不扣分)
② 容量瓶、胶头滴管; ;
③ AC
16.(1) ②⑦⑧
(2)
(3) AD
(4) (或 ); 变浅; 乙烧杯中加入 与水反应放热,使 的水解反应: 平衡正向移动,增大,溶液红色加深
(5) B
17.(1)
(2) (1分)
(3) ; 0.52
(4) BD
(5) 不是(1分); 温度升高催化剂活性降低;; 反应②为吸热反应,温度升高,反应②正向进行趋势大,使 产率降低(或总反应为放热反应,升温,平衡逆向进行,使 产率降低)
18.(1) 过滤(1分); (1分)
(2) (不写“↑”不扣分); 11.2
(3) ; 不变
(4) ;
(5) (写 不扣分)
同课章节目录
