3.3.1物质燃烧的条件灭火原理课件(共42张PPT)2023-2024学年度科粤版化学九年级上册
文档属性
| 名称 | 3.3.1物质燃烧的条件灭火原理课件(共42张PPT)2023-2024学年度科粤版化学九年级上册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 69.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-22 00:00:00 | ||
图片预览










文档简介
(共42张PPT)
3.3.1 物质燃烧的条件 灭火原理
九上 化学
科粤版
学习目标
新课引入
新知学习
课堂小结
1
2
3
4
教学环节
1.了解燃烧和燃烧的条件、灭火原理;了解缓慢氧化和自然现象,知道它们与燃烧之间的区别和联系
2.了解物质燃烧条件的探究过程与方法
3.在学习了燃烧条件后,能应用到灭火方法的探讨上,从而培养学生分析问题、解决问题的能力,形成知识迁移
学习目标
难点
重点
新课引入
日常生活中有许多燃烧现象,如木柴、煤炭或煤气的燃烧。
煤气燃烧
篝火晚会
那么,你思考过燃烧需要哪些条件吗?
新知学习
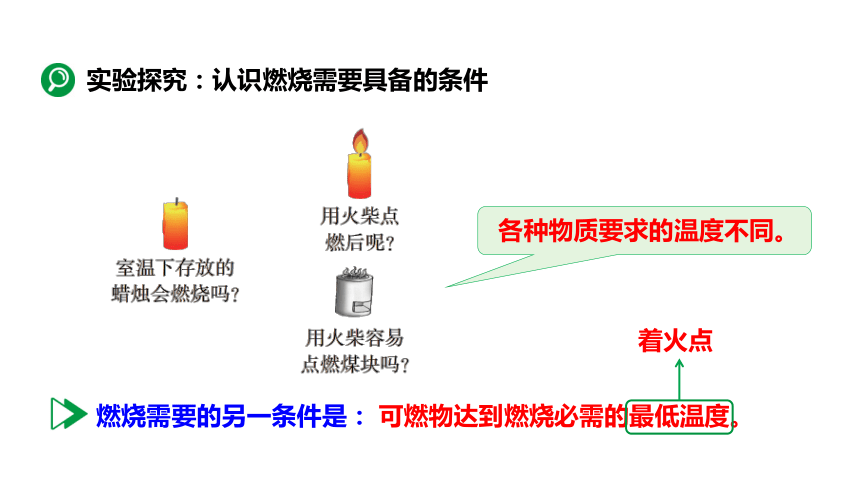
实验探究:认识燃烧需要具备的条件
蜡烛、煤块、火柴可燃吗?
沙子、石块、水泥砖可燃吗?
物质本身是可燃物。
燃烧首先需要的条件是:
Ⅰ 物质燃烧的条件
实验探究:认识燃烧需要具备的条件
点燃的蜡烛
用烧杯罩住被点燃的蜡烛
可燃物接触氧气或空气。
燃烧还必须具备的条件是:
实验探究:认识燃烧需要具备的条件
可燃物达到燃烧必需的最低温度。
燃烧需要的另一条件是:
各种物质要求的温度不同。
着火点
小结
1.物质本身是可燃物;
2.可燃物接触氧气或空气
3.温度达到着火点
同时具备,缺一不可
燃烧的条件
可燃物 + 氧气 生成物 + 能量
一定条件
温度
达到着火点
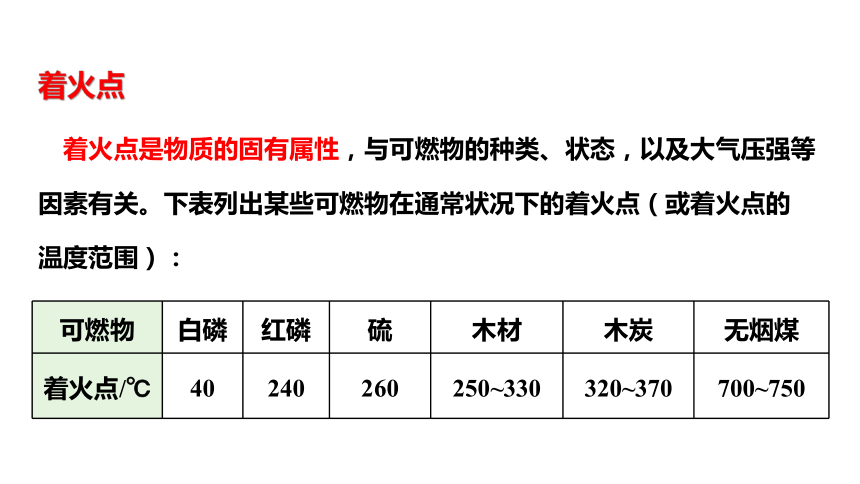
着火点
着火点是物质的固有属性,与可燃物的种类、状态,以及大气压强等
因素有关。下表列出某些可燃物在通常状况下的着火点(或着火点的
温度范围):
可燃物 白磷 红磷 硫 木材 木炭 无烟煤
着火点/℃ 40 240 260 250~330 320~370 700~750
可燃物虽然着火点各不相同,但其燃烧时都有共同的特征,那就是:发光、发热,而火焰则是可燃气体或可燃物汽化燃烧时的现象。
在通常情况下,燃烧是可燃物与氧气发生的一种发光、发热的剧烈氧化反应。
然而,有些氧化反应并不像燃烧那么剧烈,它们是缓慢氧化反应,这类反应也会放热。如果缓慢氧化的热量没有及时散开,造成热量积累,最终使温度达到可燃物的着火点时,便会发生自动燃烧。这种由缓慢氧化引起的自动燃烧叫做自燃。
稻草垛
落叶
煤堆
现代生活和生产中人类对火的应用
生活中用火烹饪食物
工业中用火炼钢
现代生活和生产中人类对火的应用
发射火箭
油是常见的可燃物,燃烧时会放出热量,向火中浇油会使燃烧更剧烈。
应用燃烧条件解决问题
1.火上浇油:
应用燃烧条件解决问题
2.室内起火时,如果打开门窗,火反而会烧的更旺。
在居室内起火时,由于居室是相对封闭的环境,室内的可燃物燃烧会消耗大量的氧气,若此时打开门窗,则会起到补充氧气的作用,会使火越烧越旺。
应用燃烧条件解决问题
3. “纸火锅”是用纸张代替金属材料做容器盛放汤料,当加热时纸张不会燃烧。
纸中盛放汤料、水等物质,水蒸发时能吸收燃烧产生的热量,使纸表面温度无法达到纸的着火点。
可燃物 + 氧气 生成物 + 能量
一定条件
温度
达到着火点
小结
控制变量
利用条件
1. 燃烧是人类最早利用的化学反应之一。下列说法正确的是( )
A. 物质与氧气发生的反应都是燃烧
B. 人类利用的能量都是通过燃烧获得的
C. 当温度达到可燃物的着火点即可燃烧
D. 燃烧一定伴随着发光、放热的现象
D
针对训练
如食物腐烂是食物与氧气发生缓慢氧化的结果,不属于燃烧
如太阳能、风能不是通过燃烧获得的
燃烧需同时满足三个条件
燃烧是可燃物与氧气发生的一种发光、放热的剧烈的氧化反应
火灾造成的巨大损失
如何有效地控制燃烧反应?
Ⅱ 灭火依据什么原理
思考
遇到下列情况应该怎么处理?
情 况 1
炒菜时油锅着火
隔绝氧气(空气)
将温度降到油的着火点以下
隔绝氧气(空气)
为什么隔绝氧气或降低温度就能使火熄灭呢?
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
通过模型看,氧气是反应物之一,温度是反应的条件,当缺少反应物,或使反应条件无法达到时,燃烧反应就终止了。
情 况 2
做实验时不慎打翻酒精灯,酒精在桌面上燃烧起来
隔绝氧气(空气)
湿抹布
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
情 况 3
纸张、纸箱着火
将温度降到纸的着火点以下
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
情 况 4
森林着火
清除可燃物
将温度降到可燃物着火点以下
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
小结
锅盖盖灭油锅着火 隔绝氧气
蔬菜熄灭油锅着火 降温到可燃物着火点以下
用水浇灭纸张着火 手持式风力灭火机吹灭森林着火 砍伐树木制造隔离带阻断森林大火 清除可燃物
归纳
灭火原理
破坏燃烧条件之一
清除可燃物
隔绝氧气(空气)
降温到可燃物着火点以下
【实验】蜡烛在不同条件下的燃烧
现象 分析
Ⅰ
Ⅱ
Ⅲ
火焰熄灭
正常燃烧
火焰熄灭
烧杯隔绝空气(氧气)
同时具备三个燃烧条件
碳酸钠与稀盐酸发生化学反应生成的二氧化碳气体不能燃烧且不支持燃烧,其密度比空气的大,可隔绝空气(氧气)。
【实验】设计灭火器
当装置倾斜倒置时,浓盐酸会与碳酸钠溶液接触,反应产生大量的二氧化碳气体,强大的气压使二氧化碳气体夹带液体一并从装置中溢出,喷射在可燃物的表面以达到隔绝空气及降温的作用。
认识常见灭火器
泡沫灭火器 灭火原理 喷射带水渍泡沫的 CO2 在燃烧物表面形成隔绝空气的水膜
适用范围 用于扑灭木材、棉布及可燃油的失火
认识常见灭火器
二氧化碳灭火器 灭火原理 压缩在瓶中的液态 CO2 喷出汽化 ,能降温和隔绝空气
适用范围 因灭火不会留痕迹 ,可用于扑灭图书 、档案 、贵重设备、 精密仪器发生的火灾
认识常见灭火器
干粉灭火器 灭火原理 由压缩的 CO2 吹出小苏打粉,受热分解出 CO2 而灭火
适用范围 其喷射率高 、不腐蚀容器和不易变质,可用于扑灭一般火灾及可燃性油、气的火灾
1. 用水可以熄灭着火的木材,这是因为( )
A.水蒸发吸热,降低了木材的着火点
B.水的密度比木材大
C.水蒸发吸热,提高了木材的着火点
D.水蒸发吸热,使温度降低到木材的着火点以下,而且水蒸气又起着使可燃物与空气隔绝的作用
D
针对训练
一般情况下,可燃物的着火点不会改变。
课堂小结
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
控制反应物
控制反应条件
清除可燃物
隔绝氧气
降温到着火点以下
控制接触面积、浓度等
1. 在一次家庭小实验中,当点燃装有半杯水的纸杯时,发现水面以下部分没有燃烧,其主要原因是( )
A. 纸杯着火点变低
B. 温度低于着火点
C. 与氧气接触面太小
D. 纸杯不是可燃物
B
新趋势 家庭实验
随堂检测
2. (2022成都)已知白磷的着火点是40 ℃,红磷的着火点是240 ℃。如图实验,三支试管里面充满氮气,初始温度25 ℃,升温至60 ℃后,用注射器同时向②③试管中迅速注入足量氧气。下列说法有误的是( )
A. 只有②中有燃烧现象
B. 由①②现象说明可燃物达着火点未必燃烧
C. 若继续水浴升温,则③中一定会燃烧
D. 该实验能总结出燃烧的条件
C
新趋势 创新实验
3. “灭火弹”是一种常见的灭火器材,主要分为沙石灭火弹和干粉灭火弹。 目前市场上的灭火弹主要以干粉为主。超细干粉灭火剂是目前国内外已查明的灭火剂中,灭火浓度最低,灭火效能最高,灭火速度最快的一种,且灭火时不会造成火场中人员中毒或窒息死亡。在扑灭森林大火时,可以选用引燃式超细干粉灭火弹。
根据内容回答下列问题:
(1)常见灭火弹主要分为沙石灭火弹和____________。
新趋势 科普阅读题
干粉灭火弹
(2)超细干粉灭火剂的特点有( )
A. 灭火浓度最低 B. 灭火效能最高
C. 灭火速度最快 D. 会造成人员伤亡
(3)某种干粉灭火剂的主要成分是NaHCO3,遇热时NaHCO3会分解生成Na2CO3并放出CO2气体,写出该反应的化学方程式____________________________________。
(4)“森林防火,人人有责”。请你对预防森林火灾提一条建设性意见_______________________________________________。
ABC
2NaHCO3 Na2CO3 + H2O + CO2↑
设置隔离带(或严禁携带火种进入林区等合理即可)
4. (2022泸州)燃烧与灭火紧密联系着我们的生活。请你依据下列实验探究,回答相关问题。
(1)在空气中点燃镁条,观察到镁条剧烈燃烧,发出耀眼白光,说明该反应______(填“放出”或“吸收”)能量,生成白色固体MgO,说明镁发生了______反应(填“氧化”或“还原”)。
放出
氧化
(2)CO2可用于灭火,是否也可熄灭燃着
的镁呢?某实验小组进行了如下探究:
①实验探究
取两块大小相同的干冰,在一块干
冰中央挖一个小穴,放入一些镁屑,用红热的铁棒点燃镁屑。(见图1)
迅速将另一块干冰盖上,镁在两块干冰间剧烈反应,发出耀眼的白光,像冰块中装入一个明亮的电灯泡一样。(见图2和图3)
取走上面一块干冰,观察到有白色固体产生(见图4),用铁片拨开图4产物的表面(见图5),还观察到的现象是________________,写出该反应的化学方程式___________________________。
②反思交流
小组实验后讨论,对初中教材中燃
烧的条件有了新的认识,请你代为表达__________________________________。
有黑色粉末出现
2Mg + CO2 2MgO + C
燃烧不一定需要氧气参与(合理即可)
实践与拓展
利用所给仪器和药品设计实验.
火柴头、火柴梗、蜡烛、镊子、薄铜片、三脚架、酒精灯、玻璃片、细沙、药匙
资料卡片
着火点:
火柴头 240~260 ℃
火柴梗 400~470 ℃
3.3.1 物质燃烧的条件 灭火原理
九上 化学
科粤版
学习目标
新课引入
新知学习
课堂小结
1
2
3
4
教学环节
1.了解燃烧和燃烧的条件、灭火原理;了解缓慢氧化和自然现象,知道它们与燃烧之间的区别和联系
2.了解物质燃烧条件的探究过程与方法
3.在学习了燃烧条件后,能应用到灭火方法的探讨上,从而培养学生分析问题、解决问题的能力,形成知识迁移
学习目标
难点
重点
新课引入
日常生活中有许多燃烧现象,如木柴、煤炭或煤气的燃烧。
煤气燃烧
篝火晚会
那么,你思考过燃烧需要哪些条件吗?
新知学习
实验探究:认识燃烧需要具备的条件
蜡烛、煤块、火柴可燃吗?
沙子、石块、水泥砖可燃吗?
物质本身是可燃物。
燃烧首先需要的条件是:
Ⅰ 物质燃烧的条件
实验探究:认识燃烧需要具备的条件
点燃的蜡烛
用烧杯罩住被点燃的蜡烛
可燃物接触氧气或空气。
燃烧还必须具备的条件是:
实验探究:认识燃烧需要具备的条件
可燃物达到燃烧必需的最低温度。
燃烧需要的另一条件是:
各种物质要求的温度不同。
着火点
小结
1.物质本身是可燃物;
2.可燃物接触氧气或空气
3.温度达到着火点
同时具备,缺一不可
燃烧的条件
可燃物 + 氧气 生成物 + 能量
一定条件
温度
达到着火点
着火点
着火点是物质的固有属性,与可燃物的种类、状态,以及大气压强等
因素有关。下表列出某些可燃物在通常状况下的着火点(或着火点的
温度范围):
可燃物 白磷 红磷 硫 木材 木炭 无烟煤
着火点/℃ 40 240 260 250~330 320~370 700~750
可燃物虽然着火点各不相同,但其燃烧时都有共同的特征,那就是:发光、发热,而火焰则是可燃气体或可燃物汽化燃烧时的现象。
在通常情况下,燃烧是可燃物与氧气发生的一种发光、发热的剧烈氧化反应。
然而,有些氧化反应并不像燃烧那么剧烈,它们是缓慢氧化反应,这类反应也会放热。如果缓慢氧化的热量没有及时散开,造成热量积累,最终使温度达到可燃物的着火点时,便会发生自动燃烧。这种由缓慢氧化引起的自动燃烧叫做自燃。
稻草垛
落叶
煤堆
现代生活和生产中人类对火的应用
生活中用火烹饪食物
工业中用火炼钢
现代生活和生产中人类对火的应用
发射火箭
油是常见的可燃物,燃烧时会放出热量,向火中浇油会使燃烧更剧烈。
应用燃烧条件解决问题
1.火上浇油:
应用燃烧条件解决问题
2.室内起火时,如果打开门窗,火反而会烧的更旺。
在居室内起火时,由于居室是相对封闭的环境,室内的可燃物燃烧会消耗大量的氧气,若此时打开门窗,则会起到补充氧气的作用,会使火越烧越旺。
应用燃烧条件解决问题
3. “纸火锅”是用纸张代替金属材料做容器盛放汤料,当加热时纸张不会燃烧。
纸中盛放汤料、水等物质,水蒸发时能吸收燃烧产生的热量,使纸表面温度无法达到纸的着火点。
可燃物 + 氧气 生成物 + 能量
一定条件
温度
达到着火点
小结
控制变量
利用条件
1. 燃烧是人类最早利用的化学反应之一。下列说法正确的是( )
A. 物质与氧气发生的反应都是燃烧
B. 人类利用的能量都是通过燃烧获得的
C. 当温度达到可燃物的着火点即可燃烧
D. 燃烧一定伴随着发光、放热的现象
D
针对训练
如食物腐烂是食物与氧气发生缓慢氧化的结果,不属于燃烧
如太阳能、风能不是通过燃烧获得的
燃烧需同时满足三个条件
燃烧是可燃物与氧气发生的一种发光、放热的剧烈的氧化反应
火灾造成的巨大损失
如何有效地控制燃烧反应?
Ⅱ 灭火依据什么原理
思考
遇到下列情况应该怎么处理?
情 况 1
炒菜时油锅着火
隔绝氧气(空气)
将温度降到油的着火点以下
隔绝氧气(空气)
为什么隔绝氧气或降低温度就能使火熄灭呢?
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
通过模型看,氧气是反应物之一,温度是反应的条件,当缺少反应物,或使反应条件无法达到时,燃烧反应就终止了。
情 况 2
做实验时不慎打翻酒精灯,酒精在桌面上燃烧起来
隔绝氧气(空气)
湿抹布
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
情 况 3
纸张、纸箱着火
将温度降到纸的着火点以下
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
情 况 4
森林着火
清除可燃物
将温度降到可燃物着火点以下
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
小结
锅盖盖灭油锅着火 隔绝氧气
蔬菜熄灭油锅着火 降温到可燃物着火点以下
用水浇灭纸张着火 手持式风力灭火机吹灭森林着火 砍伐树木制造隔离带阻断森林大火 清除可燃物
归纳
灭火原理
破坏燃烧条件之一
清除可燃物
隔绝氧气(空气)
降温到可燃物着火点以下
【实验】蜡烛在不同条件下的燃烧
现象 分析
Ⅰ
Ⅱ
Ⅲ
火焰熄灭
正常燃烧
火焰熄灭
烧杯隔绝空气(氧气)
同时具备三个燃烧条件
碳酸钠与稀盐酸发生化学反应生成的二氧化碳气体不能燃烧且不支持燃烧,其密度比空气的大,可隔绝空气(氧气)。
【实验】设计灭火器
当装置倾斜倒置时,浓盐酸会与碳酸钠溶液接触,反应产生大量的二氧化碳气体,强大的气压使二氧化碳气体夹带液体一并从装置中溢出,喷射在可燃物的表面以达到隔绝空气及降温的作用。
认识常见灭火器
泡沫灭火器 灭火原理 喷射带水渍泡沫的 CO2 在燃烧物表面形成隔绝空气的水膜
适用范围 用于扑灭木材、棉布及可燃油的失火
认识常见灭火器
二氧化碳灭火器 灭火原理 压缩在瓶中的液态 CO2 喷出汽化 ,能降温和隔绝空气
适用范围 因灭火不会留痕迹 ,可用于扑灭图书 、档案 、贵重设备、 精密仪器发生的火灾
认识常见灭火器
干粉灭火器 灭火原理 由压缩的 CO2 吹出小苏打粉,受热分解出 CO2 而灭火
适用范围 其喷射率高 、不腐蚀容器和不易变质,可用于扑灭一般火灾及可燃性油、气的火灾
1. 用水可以熄灭着火的木材,这是因为( )
A.水蒸发吸热,降低了木材的着火点
B.水的密度比木材大
C.水蒸发吸热,提高了木材的着火点
D.水蒸发吸热,使温度降低到木材的着火点以下,而且水蒸气又起着使可燃物与空气隔绝的作用
D
针对训练
一般情况下,可燃物的着火点不会改变。
课堂小结
温度
可燃物 + 氧气 生成物 + 能量
达到着火点
控制反应物
控制反应条件
清除可燃物
隔绝氧气
降温到着火点以下
控制接触面积、浓度等
1. 在一次家庭小实验中,当点燃装有半杯水的纸杯时,发现水面以下部分没有燃烧,其主要原因是( )
A. 纸杯着火点变低
B. 温度低于着火点
C. 与氧气接触面太小
D. 纸杯不是可燃物
B
新趋势 家庭实验
随堂检测
2. (2022成都)已知白磷的着火点是40 ℃,红磷的着火点是240 ℃。如图实验,三支试管里面充满氮气,初始温度25 ℃,升温至60 ℃后,用注射器同时向②③试管中迅速注入足量氧气。下列说法有误的是( )
A. 只有②中有燃烧现象
B. 由①②现象说明可燃物达着火点未必燃烧
C. 若继续水浴升温,则③中一定会燃烧
D. 该实验能总结出燃烧的条件
C
新趋势 创新实验
3. “灭火弹”是一种常见的灭火器材,主要分为沙石灭火弹和干粉灭火弹。 目前市场上的灭火弹主要以干粉为主。超细干粉灭火剂是目前国内外已查明的灭火剂中,灭火浓度最低,灭火效能最高,灭火速度最快的一种,且灭火时不会造成火场中人员中毒或窒息死亡。在扑灭森林大火时,可以选用引燃式超细干粉灭火弹。
根据内容回答下列问题:
(1)常见灭火弹主要分为沙石灭火弹和____________。
新趋势 科普阅读题
干粉灭火弹
(2)超细干粉灭火剂的特点有( )
A. 灭火浓度最低 B. 灭火效能最高
C. 灭火速度最快 D. 会造成人员伤亡
(3)某种干粉灭火剂的主要成分是NaHCO3,遇热时NaHCO3会分解生成Na2CO3并放出CO2气体,写出该反应的化学方程式____________________________________。
(4)“森林防火,人人有责”。请你对预防森林火灾提一条建设性意见_______________________________________________。
ABC
2NaHCO3 Na2CO3 + H2O + CO2↑
设置隔离带(或严禁携带火种进入林区等合理即可)
4. (2022泸州)燃烧与灭火紧密联系着我们的生活。请你依据下列实验探究,回答相关问题。
(1)在空气中点燃镁条,观察到镁条剧烈燃烧,发出耀眼白光,说明该反应______(填“放出”或“吸收”)能量,生成白色固体MgO,说明镁发生了______反应(填“氧化”或“还原”)。
放出
氧化
(2)CO2可用于灭火,是否也可熄灭燃着
的镁呢?某实验小组进行了如下探究:
①实验探究
取两块大小相同的干冰,在一块干
冰中央挖一个小穴,放入一些镁屑,用红热的铁棒点燃镁屑。(见图1)
迅速将另一块干冰盖上,镁在两块干冰间剧烈反应,发出耀眼的白光,像冰块中装入一个明亮的电灯泡一样。(见图2和图3)
取走上面一块干冰,观察到有白色固体产生(见图4),用铁片拨开图4产物的表面(见图5),还观察到的现象是________________,写出该反应的化学方程式___________________________。
②反思交流
小组实验后讨论,对初中教材中燃
烧的条件有了新的认识,请你代为表达__________________________________。
有黑色粉末出现
2Mg + CO2 2MgO + C
燃烧不一定需要氧气参与(合理即可)
实践与拓展
利用所给仪器和药品设计实验.
火柴头、火柴梗、蜡烛、镊子、薄铜片、三脚架、酒精灯、玻璃片、细沙、药匙
资料卡片
着火点:
火柴头 240~260 ℃
火柴梗 400~470 ℃
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
