浙江中考科学二轮复习提升讲义 08.水与溶液(含答案)
文档属性
| 名称 | 浙江中考科学二轮复习提升讲义 08.水与溶液(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 通用版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2024-01-26 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
第八讲:水与溶液
一、单选题
1.将少量的①面粉,②味精,③白糖,④泥土,⑤肥皂,⑥植物油分别加到入水中,充分振荡后,其中形成悬浊液的是( )
A.①④ B.③⑤ C.②⑥ D.⑤⑥
2.学习了溶液知识后,小可和小青两位同学得出了下列观点。其中正确的是( )
①冰放入水中融化后将形成溶液,冰是溶质。水是溶剂
②要将氢氧化钙饱和溶液转化为不饱和溶液,可采用加热溶液的方法
③硝酸钾饱和溶液一定要比硝酸钾不饱和溶液浓一点
④将食盐颗粒碾碎后、可以增大它的溶解度
A.② B.①④ C.①②④ D.①②③④
3.下列是有关科学问题中的因果关系,其中说法正确的是( )
A.浮在水面上的铁球一定是空心的,那么空心的铁球一定会浮在水面上
B.溶液是均一的,稳定的,那么均一的,稳定的物质一定是溶液
C.饱和溶液恒温蒸发后会有固体析出,那么能恒温蒸发析出固体的溶液一定是饱和溶液
D.密度比液体小的固体漂浮在液体中,那么漂浮在该液体中的实心固体的密度一定比液体小
4.如图所示是电解水的简易装置,下列分析正确的是( )
A.甲试管中产生的气体为氧气
B.甲、乙试管中产生的气体质量之比为2:1
C.实验说明水是由氢气和氧气组成的
D.a连接的是电源的正极,b连接的是负极
5.如图是水电解时的微观粒子模型,由该图可知( )
A.水是由氢气和氧气组成的 B.水是由氢原子和氧原子构成的
C.水分子含有氢分子和氧分子 D.水电解过程中产生了新的分子
6.概念图的建立有助于我们对知识理解和掌握。下列各项中的概念或结构,能分别代表图中X、Y、Z的是( )
A.饱和溶液、浓溶液、溶液 B.悬浊液、乳浊液、混合物
C.脑、中枢神经系统、神经系统 D.条件反射、非条件反射、反射
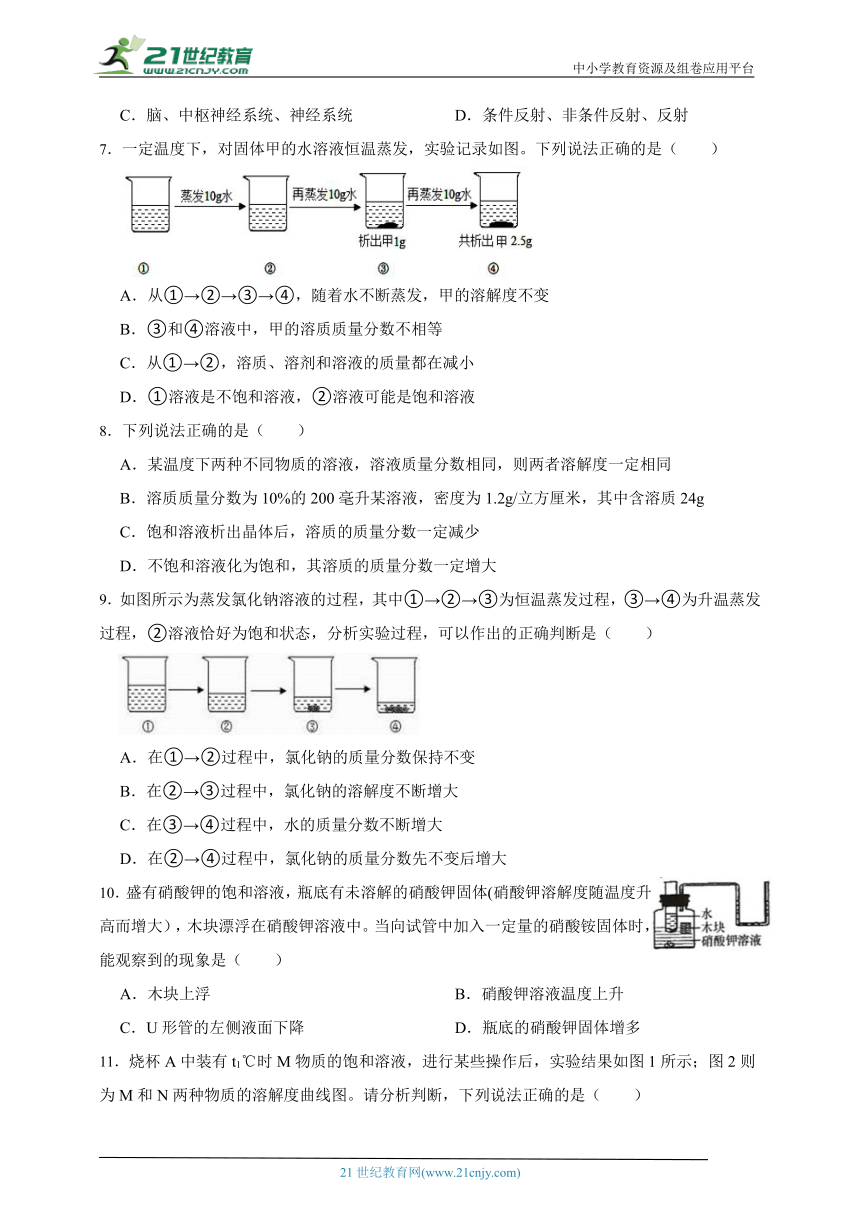
7.一定温度下,对固体甲的水溶液恒温蒸发,实验记录如图。下列说法正确的是( )
A.从①→②→③→④,随着水不断蒸发,甲的溶解度不变
B.③和④溶液中,甲的溶质质量分数不相等
C.从①→②,溶质、溶剂和溶液的质量都在减小
D.①溶液是不饱和溶液,②溶液可能是饱和溶液
8.下列说法正确的是( )
A.某温度下两种不同物质的溶液,溶液质量分数相同,则两者溶解度一定相同
B.溶质质量分数为10%的200毫升某溶液,密度为1.2g/立方厘米,其中含溶质24g
C.饱和溶液析出晶体后,溶质的质量分数一定减少
D.不饱和溶液化为饱和,其溶质的质量分数一定增大
9.如图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,可以作出的正确判断是( )
A.在①→②过程中,氯化钠的质量分数保持不变
B.在②→③过程中,氯化钠的溶解度不断增大
C.在③→④过程中,水的质量分数不断增大
D.在②→④过程中,氯化钠的质量分数先不变后增大
10.盛有硝酸钾的饱和溶液,瓶底有未溶解的硝酸钾固体(硝酸钾溶解度随温度升高而增大),木块漂浮在硝酸钾溶液中。当向试管中加入一定量的硝酸铵固体时,能观察到的现象是( )
A.木块上浮 B.硝酸钾溶液温度上升
C.U形管的左侧液面下降 D.瓶底的硝酸钾固体增多
11.烧杯A中装有t1℃时M物质的饱和溶液,进行某些操作后,实验结果如图1所示;图2则为M和N两种物质的溶解度曲线图。请分析判断,下列说法正确的是( )
A.M物质的溶解度曲线是a
B.烧杯B中的溶液一定是不饱和溶液
C.烧杯C到烧杯D的变化中,该物质的溶解度变小了
D.烧杯C到烧杯D的变化中,溶质的质量分数一定变大
12.现对某物质A的不饱和溶液进行恒温蒸发,若蒸发10g水析出ag固体,若蒸发20g水析出bg固体,若蒸发30g水析出cg固体,则下列关系是正确的是( )
A.c=a+b B.c=2b﹣a C.c=2b+a D.c=2a+b
13.甲、乙两物质的溶解度曲线如下图所示,下列叙述中正确的是( )
A.t1℃时,甲和乙的溶解度相等,都是30
B.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
C.温度从t2℃降至t1℃时,甲和乙的饱和溶液中析出晶体的质量甲大于乙
D.t1℃时,将甲、乙两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量一定相等
14.甲、乙两种固体物质的溶解度曲线如图所示,据图判断下列说法正确的是( )
A.甲物质的溶解度大于乙
B.60℃时,甲的饱和溶液的溶质质量分数为25%
C.20℃时,甲溶液质量分数一定小于乙溶液的质量分数
D.将60℃时甲、乙的饱和溶液降温至t℃,溶液的溶质质量分数:甲>乙
15.如图是 a、b、c 三种物质的溶解度曲线,下列说法不正确的是( )
A.P点表示t1℃时,a、c两种物质的溶解度相等
B.将c的饱和溶液变为不饱和溶液,可采用降温的方法
C.t2℃时,将30ga物质加入到50g水中充分搅拌,得到75ga的饱和溶液
D.将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,其溶质质量分数由大到小的顺序是a>b>c
二、填空题
16.读“水循环示意图”,回答问题:
(1)数字②在水循环中所代表的环节是 。
(2)目前, 人类修建水库主要是改造水循环中的 环节。
(3)不同的水循环中都包括的环节是 。
17.“美林”是为儿童开发设计的一款退烧药,主要成分是布洛芬,“美林”即使密封保存,放久了也会在底部看到白色沉淀,“美林”属于 (填(填“乳浊液”、“悬浊液”或“溶液”),将少量的下列物质分别加入到水中(①面粉②味精⑧白糖④泥土⑤肥皂⑥植物油),充分振荡后,其中形成的混合物与“美林”属于同类型的物质有
18.牛奶中掺水量越多,牛奶密度越小,品质越差。小丽想通过测定密度来比较二种牛奶品质的优劣,她用一根一端密封的空心玻璃管下端绕上一段细铁丝,制成一支自制密度计,如图所示。
(1)纯牛奶是 (选填“溶液”、“悬浊液”或“乳浊液”)
(2)分别将自制密度计浸入牛奶甲和牛奶乙中,静止后如图所示。由图可知品质较高的牛奶为 (选填“甲”、“乙”或“相同”)
(3)使用中,发现细铁丝容易滑落,于是他取下铁丝,置于玻璃管内,再次测量这一杯牛奶密度(过程中杯内液体总量不变),则测得密度与原来相比 (选填“偏大”、“偏小”或“不变”)。
19.某同学进行硫酸铜晶体(化学式为CuSO4·5H2O)的制备和生长实验,配制了某温度时的硫酸铜热饱和溶液,静置、冷却到室温,观察晶体的生长,如图。
(1)能判断原硫酸铜溶液已饱和的方法是____。
A.观察颜色,溶液蓝色较深
B.溶液冷却,有蓝色晶体析出
C.蒸发少量水,有蓝色晶体析出
D.加入硫酸铜晶体,晶体质量不变
(2)现称取49克无水硫酸铜溶于水,配成150克某温度时的热饱和溶液,再冷却到室温,共析出50克硫酸铜晶体,请计算该室温时硫酸铜饱和溶液的溶质质量分数。
三、实验探究题
20.下表是部分物质的溶解度数据。
温度(℃) 20 40 50 60 80
溶解度 (g/100g 水) 氯化铵 37.2 45.8 50.4 55.2 65.6
氯化钠 36.0 36.6 37.0 37.3 38.4
硝酸钾 31.6 63.9 85.5 110 169
(1)氯化铵溶于水,温度降低,说明该溶解过程 (选填“吸收 ”或“放 出 ”)热量。
(2)20℃时,20克的氯化钠加入50g水中,充分溶解后溶液质量 g。
(3)A是80℃含有120g水的硝酸钾(KNO3 )溶液。经过如下操作,得到102g硝酸钾固 体。
a、A溶液为 (选填“饱和 ”或“不饱和 ”)溶液。
b、下列对以上过程的分析中正确的是 (填数字)。
①.A到B的过程中,溶质质量分数没有改变 ②.B中溶质与溶剂的质量比为169:100
③.开始析出硝酸钾固体的温度在60℃至80℃之间 ④.A溶液的质量等于222g
21.如图所示为有关食盐的两个实验(天平使用时1克以下用游码):
(1)实验一:粗盐提纯并测定产率实验。
a.经过如图⑤蒸发结晶得到的精盐属于 (填“纯净物”或“混合物”);实验④中玻璃棒的作用 。
b.某同学所测得的产率与其他同学比较明显偏低,可能是以下哪些情况 (选填字母)。
A.溶解时将粗盐一次全部倒入水中,立即过滤 B.过滤时滤纸破损 C.提纯后的精盐尚未完全干燥就称其质量 D.蒸发时有一些液体、固体溅出
(2)实验二:用提纯得到的精盐配制13%的氯化钠溶液40克。
a.步骤如下:①计算:②称量和量取;③ ;④装瓶
b.经检测,所配制的氯化钠溶液的溶质质量分数偏小,其原因可能是 。
A.制得的食盐还不纯 B.量取水读数时俯视 C.称量时砝码与药品位置放反 D.盛装溶液的试剂瓶用蒸馏水润洗 E.配制结束后,不小心洒出一部分溶液 F.称量时,使用了生锈的砝码
22.由128克硝酸钾、60克氯化钠组成的混合物投入200g热水溶解,对该溶液进行如图实验(假设实验过程中无损耗)。
温度(℃) 10 20 30 40 60 80 100
溶解度 硝酸钾 20.9 31.6 45.8 64 110 169 248
氯化钠 35.8 36 36.3 35.4 37 38.4 39.8
(1)两种物质溶解在水中,用玻璃棒搅拌的目的是 。
(2)实验时温度t的范围为 。
(3)操作1用到的实验仪器有 。
A.酒精灯 B.铁架台 C.漏斗 D.玻璃棒 E.蒸发皿
(4)定量述晶体1的组成 。
(5)溶液2为 (填物质名称) 的饱和溶液。
(6)关于溶液中NaCl的质量分数:溶液1 溶液2(选填“>“、“<”或“=“)
(7)关于上述实验说法错误的是 。
A.晶体1与晶体2比较,晶体1中KNO3的纯度更高
B.溶液1中KNO3为饱和溶液,NaCl为不饱和溶液
C.溶液1恒温蒸发90g水后,与溶液2的成分相同
D.溶液2将水蒸干就可得到纯净的KNO3固体
23.小科同学暑期去宁波象山游玩,来到了花岙岛的盐场。据说这里是浙江省最后一块传统盐场,这里的晒盐技术已传承1300多年。爱探索的小科同学从盐场带回粗盐样品,进行粗盐提纯实验,如下图:
(1)图甲中的操作①②③分别对应图乙中的 (填图中字母);
(2)图乙a中,待到蒸发皿中 时,撤去酒精灯。
(3)下列哪些操作会使最终精盐的产量偏低的有______(多选)。
A.溶解粗盐时,加入的水量不足
B.过滤时滤纸破损,混合液流入滤液中
C.滤渣没有用蒸馏水冲洗
D.蒸发后,所得的精盐很潮湿
(4)假设图甲中的数据均通过正确合理的步骤得出,可计算氯化钠的产率=×100%=80%。请评价这样计算是否合理,并说明理由。
四、解答题
24.水对人类社会有着重要的作用,认识水是从宏观到微观的过程。
(1)图一是太空舱里拍下的地球景象,白色部分为云层,它属于 。(填大气分层的名称)
(2)图二是地球水体分布图,图一海洋水对应图二中的 。(填序号)
(3)如图三,对水进行电解研究时,a管中生成的气体为 。(填气体名称)
(4)下图是水电解过程的微观模型图,此过程的正确顺序是: .
(5)电解水时,向水中加入适量某物质可增加溶液导电性,从而加快水的电解。图四为水电解前溶质的分布情况,请在图五中画出电解一段时间后液面位置和溶质粒子的分布模型图。(为溶质粒子)
25.如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,阅读后计算:
浓硫酸(H2SO4)500毫升
浓度(质量分数) 98%
密度 1.84克/厘米3
相对分子质量 98
强腐蚀性,阴冷,密封贮藏
(1)这瓶浓硫酸的含溶质 g。
(2)欲配制600克溶质质量分数为19.6%的稀硫酸,需要这种硫酸多少毫升?
26.如图是硫酸的密度和浓度的对照表,阅读后计算:
硫酸的密度和硫酸溶液中溶质的质量分数对照表(20℃)
密度(克/厘米3) 1.01 1.07 1.14 1.22 1.30 1.40 1.50 1.61 1.73 1.81 1.84
质量分数(%) 1 10 20 30 40 50 60 70 80 90 98
(1)欲配制100克溶质质量分数为9.8%的稀硫酸,需要98%浓硫酸多少毫升 再加水多少毫升
(2)100毫升90%的硫酸与144.8毫升水混合后所得溶液的密度为多少
答案解析部分
1.【答案】A
2.【答案】D
3.【答案】D
4.【答案】D
5.【答案】D
6.【答案】C
7.【答案】A
8.【答案】B
9.【答案】D
10.【答案】D
11.【答案】B
12.【答案】B
13.【答案】D
14.【答案】D
15.【答案】D
16.【答案】(1)水汽输送
(2)地表径流
(3)蒸发和降水
17.【答案】悬浊物;①④
18.【答案】(1)乳浊液
(2)乙
(3)偏小
19.【答案】(1)D
(2)17%
20.【答案】(1)吸收
(2)68
(3)不饱和;③
21.【答案】(1)混合物;引流;AD
(2)溶解;ACD
22.【答案】(1)加快溶解
(2)≥40℃
(3)B;C;D
(4)32.4g 硝酸钾
(5)氯化钠和硝酸钾
(6)<
(7)C;D
23.【答案】(1)cba
(2)有大量晶体析出
(3)A;C
(4)不合理,最终得到的白色固体仍是混合物,不是纯净的氯化钠
24.【答案】(1)对流层
(2)①
(3)氢气
(4)丙甲乙
(5)
25.【答案】(1)901.6
(2)解:设需要这种浓硫酸的质量为x,
有600g×19.6%=98%x;解得:x=120g;
需要这种硫酸的体积为:V=m/ρ=120g/1.84g/cm3≈65.2cm3=65.2mL;
26.【答案】(1)54.3毫升|900毫升
(2)质量分数为:50.0%,所以密度为1.40克/厘米3
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
第八讲:水与溶液
一、单选题
1.将少量的①面粉,②味精,③白糖,④泥土,⑤肥皂,⑥植物油分别加到入水中,充分振荡后,其中形成悬浊液的是( )
A.①④ B.③⑤ C.②⑥ D.⑤⑥
2.学习了溶液知识后,小可和小青两位同学得出了下列观点。其中正确的是( )
①冰放入水中融化后将形成溶液,冰是溶质。水是溶剂
②要将氢氧化钙饱和溶液转化为不饱和溶液,可采用加热溶液的方法
③硝酸钾饱和溶液一定要比硝酸钾不饱和溶液浓一点
④将食盐颗粒碾碎后、可以增大它的溶解度
A.② B.①④ C.①②④ D.①②③④
3.下列是有关科学问题中的因果关系,其中说法正确的是( )
A.浮在水面上的铁球一定是空心的,那么空心的铁球一定会浮在水面上
B.溶液是均一的,稳定的,那么均一的,稳定的物质一定是溶液
C.饱和溶液恒温蒸发后会有固体析出,那么能恒温蒸发析出固体的溶液一定是饱和溶液
D.密度比液体小的固体漂浮在液体中,那么漂浮在该液体中的实心固体的密度一定比液体小
4.如图所示是电解水的简易装置,下列分析正确的是( )
A.甲试管中产生的气体为氧气
B.甲、乙试管中产生的气体质量之比为2:1
C.实验说明水是由氢气和氧气组成的
D.a连接的是电源的正极,b连接的是负极
5.如图是水电解时的微观粒子模型,由该图可知( )
A.水是由氢气和氧气组成的 B.水是由氢原子和氧原子构成的
C.水分子含有氢分子和氧分子 D.水电解过程中产生了新的分子
6.概念图的建立有助于我们对知识理解和掌握。下列各项中的概念或结构,能分别代表图中X、Y、Z的是( )
A.饱和溶液、浓溶液、溶液 B.悬浊液、乳浊液、混合物
C.脑、中枢神经系统、神经系统 D.条件反射、非条件反射、反射
7.一定温度下,对固体甲的水溶液恒温蒸发,实验记录如图。下列说法正确的是( )
A.从①→②→③→④,随着水不断蒸发,甲的溶解度不变
B.③和④溶液中,甲的溶质质量分数不相等
C.从①→②,溶质、溶剂和溶液的质量都在减小
D.①溶液是不饱和溶液,②溶液可能是饱和溶液
8.下列说法正确的是( )
A.某温度下两种不同物质的溶液,溶液质量分数相同,则两者溶解度一定相同
B.溶质质量分数为10%的200毫升某溶液,密度为1.2g/立方厘米,其中含溶质24g
C.饱和溶液析出晶体后,溶质的质量分数一定减少
D.不饱和溶液化为饱和,其溶质的质量分数一定增大
9.如图所示为蒸发氯化钠溶液的过程,其中①→②→③为恒温蒸发过程,③→④为升温蒸发过程,②溶液恰好为饱和状态,分析实验过程,可以作出的正确判断是( )
A.在①→②过程中,氯化钠的质量分数保持不变
B.在②→③过程中,氯化钠的溶解度不断增大
C.在③→④过程中,水的质量分数不断增大
D.在②→④过程中,氯化钠的质量分数先不变后增大
10.盛有硝酸钾的饱和溶液,瓶底有未溶解的硝酸钾固体(硝酸钾溶解度随温度升高而增大),木块漂浮在硝酸钾溶液中。当向试管中加入一定量的硝酸铵固体时,能观察到的现象是( )
A.木块上浮 B.硝酸钾溶液温度上升
C.U形管的左侧液面下降 D.瓶底的硝酸钾固体增多
11.烧杯A中装有t1℃时M物质的饱和溶液,进行某些操作后,实验结果如图1所示;图2则为M和N两种物质的溶解度曲线图。请分析判断,下列说法正确的是( )
A.M物质的溶解度曲线是a
B.烧杯B中的溶液一定是不饱和溶液
C.烧杯C到烧杯D的变化中,该物质的溶解度变小了
D.烧杯C到烧杯D的变化中,溶质的质量分数一定变大
12.现对某物质A的不饱和溶液进行恒温蒸发,若蒸发10g水析出ag固体,若蒸发20g水析出bg固体,若蒸发30g水析出cg固体,则下列关系是正确的是( )
A.c=a+b B.c=2b﹣a C.c=2b+a D.c=2a+b
13.甲、乙两物质的溶解度曲线如下图所示,下列叙述中正确的是( )
A.t1℃时,甲和乙的溶解度相等,都是30
B.t2℃时,甲溶液的溶质质量分数一定大于乙溶液的溶质质量分数
C.温度从t2℃降至t1℃时,甲和乙的饱和溶液中析出晶体的质量甲大于乙
D.t1℃时,将甲、乙两种物质的饱和溶液分别恒温蒸发等质量的水,析出晶体的质量一定相等
14.甲、乙两种固体物质的溶解度曲线如图所示,据图判断下列说法正确的是( )
A.甲物质的溶解度大于乙
B.60℃时,甲的饱和溶液的溶质质量分数为25%
C.20℃时,甲溶液质量分数一定小于乙溶液的质量分数
D.将60℃时甲、乙的饱和溶液降温至t℃,溶液的溶质质量分数:甲>乙
15.如图是 a、b、c 三种物质的溶解度曲线,下列说法不正确的是( )
A.P点表示t1℃时,a、c两种物质的溶解度相等
B.将c的饱和溶液变为不饱和溶液,可采用降温的方法
C.t2℃时,将30ga物质加入到50g水中充分搅拌,得到75ga的饱和溶液
D.将t1℃时a、b、c三种物质的饱和溶液升温至t2℃,其溶质质量分数由大到小的顺序是a>b>c
二、填空题
16.读“水循环示意图”,回答问题:
(1)数字②在水循环中所代表的环节是 。
(2)目前, 人类修建水库主要是改造水循环中的 环节。
(3)不同的水循环中都包括的环节是 。
17.“美林”是为儿童开发设计的一款退烧药,主要成分是布洛芬,“美林”即使密封保存,放久了也会在底部看到白色沉淀,“美林”属于 (填(填“乳浊液”、“悬浊液”或“溶液”),将少量的下列物质分别加入到水中(①面粉②味精⑧白糖④泥土⑤肥皂⑥植物油),充分振荡后,其中形成的混合物与“美林”属于同类型的物质有
18.牛奶中掺水量越多,牛奶密度越小,品质越差。小丽想通过测定密度来比较二种牛奶品质的优劣,她用一根一端密封的空心玻璃管下端绕上一段细铁丝,制成一支自制密度计,如图所示。
(1)纯牛奶是 (选填“溶液”、“悬浊液”或“乳浊液”)
(2)分别将自制密度计浸入牛奶甲和牛奶乙中,静止后如图所示。由图可知品质较高的牛奶为 (选填“甲”、“乙”或“相同”)
(3)使用中,发现细铁丝容易滑落,于是他取下铁丝,置于玻璃管内,再次测量这一杯牛奶密度(过程中杯内液体总量不变),则测得密度与原来相比 (选填“偏大”、“偏小”或“不变”)。
19.某同学进行硫酸铜晶体(化学式为CuSO4·5H2O)的制备和生长实验,配制了某温度时的硫酸铜热饱和溶液,静置、冷却到室温,观察晶体的生长,如图。
(1)能判断原硫酸铜溶液已饱和的方法是____。
A.观察颜色,溶液蓝色较深
B.溶液冷却,有蓝色晶体析出
C.蒸发少量水,有蓝色晶体析出
D.加入硫酸铜晶体,晶体质量不变
(2)现称取49克无水硫酸铜溶于水,配成150克某温度时的热饱和溶液,再冷却到室温,共析出50克硫酸铜晶体,请计算该室温时硫酸铜饱和溶液的溶质质量分数。
三、实验探究题
20.下表是部分物质的溶解度数据。
温度(℃) 20 40 50 60 80
溶解度 (g/100g 水) 氯化铵 37.2 45.8 50.4 55.2 65.6
氯化钠 36.0 36.6 37.0 37.3 38.4
硝酸钾 31.6 63.9 85.5 110 169
(1)氯化铵溶于水,温度降低,说明该溶解过程 (选填“吸收 ”或“放 出 ”)热量。
(2)20℃时,20克的氯化钠加入50g水中,充分溶解后溶液质量 g。
(3)A是80℃含有120g水的硝酸钾(KNO3 )溶液。经过如下操作,得到102g硝酸钾固 体。
a、A溶液为 (选填“饱和 ”或“不饱和 ”)溶液。
b、下列对以上过程的分析中正确的是 (填数字)。
①.A到B的过程中,溶质质量分数没有改变 ②.B中溶质与溶剂的质量比为169:100
③.开始析出硝酸钾固体的温度在60℃至80℃之间 ④.A溶液的质量等于222g
21.如图所示为有关食盐的两个实验(天平使用时1克以下用游码):
(1)实验一:粗盐提纯并测定产率实验。
a.经过如图⑤蒸发结晶得到的精盐属于 (填“纯净物”或“混合物”);实验④中玻璃棒的作用 。
b.某同学所测得的产率与其他同学比较明显偏低,可能是以下哪些情况 (选填字母)。
A.溶解时将粗盐一次全部倒入水中,立即过滤 B.过滤时滤纸破损 C.提纯后的精盐尚未完全干燥就称其质量 D.蒸发时有一些液体、固体溅出
(2)实验二:用提纯得到的精盐配制13%的氯化钠溶液40克。
a.步骤如下:①计算:②称量和量取;③ ;④装瓶
b.经检测,所配制的氯化钠溶液的溶质质量分数偏小,其原因可能是 。
A.制得的食盐还不纯 B.量取水读数时俯视 C.称量时砝码与药品位置放反 D.盛装溶液的试剂瓶用蒸馏水润洗 E.配制结束后,不小心洒出一部分溶液 F.称量时,使用了生锈的砝码
22.由128克硝酸钾、60克氯化钠组成的混合物投入200g热水溶解,对该溶液进行如图实验(假设实验过程中无损耗)。
温度(℃) 10 20 30 40 60 80 100
溶解度 硝酸钾 20.9 31.6 45.8 64 110 169 248
氯化钠 35.8 36 36.3 35.4 37 38.4 39.8
(1)两种物质溶解在水中,用玻璃棒搅拌的目的是 。
(2)实验时温度t的范围为 。
(3)操作1用到的实验仪器有 。
A.酒精灯 B.铁架台 C.漏斗 D.玻璃棒 E.蒸发皿
(4)定量述晶体1的组成 。
(5)溶液2为 (填物质名称) 的饱和溶液。
(6)关于溶液中NaCl的质量分数:溶液1 溶液2(选填“>“、“<”或“=“)
(7)关于上述实验说法错误的是 。
A.晶体1与晶体2比较,晶体1中KNO3的纯度更高
B.溶液1中KNO3为饱和溶液,NaCl为不饱和溶液
C.溶液1恒温蒸发90g水后,与溶液2的成分相同
D.溶液2将水蒸干就可得到纯净的KNO3固体
23.小科同学暑期去宁波象山游玩,来到了花岙岛的盐场。据说这里是浙江省最后一块传统盐场,这里的晒盐技术已传承1300多年。爱探索的小科同学从盐场带回粗盐样品,进行粗盐提纯实验,如下图:
(1)图甲中的操作①②③分别对应图乙中的 (填图中字母);
(2)图乙a中,待到蒸发皿中 时,撤去酒精灯。
(3)下列哪些操作会使最终精盐的产量偏低的有______(多选)。
A.溶解粗盐时,加入的水量不足
B.过滤时滤纸破损,混合液流入滤液中
C.滤渣没有用蒸馏水冲洗
D.蒸发后,所得的精盐很潮湿
(4)假设图甲中的数据均通过正确合理的步骤得出,可计算氯化钠的产率=×100%=80%。请评价这样计算是否合理,并说明理由。
四、解答题
24.水对人类社会有着重要的作用,认识水是从宏观到微观的过程。
(1)图一是太空舱里拍下的地球景象,白色部分为云层,它属于 。(填大气分层的名称)
(2)图二是地球水体分布图,图一海洋水对应图二中的 。(填序号)
(3)如图三,对水进行电解研究时,a管中生成的气体为 。(填气体名称)
(4)下图是水电解过程的微观模型图,此过程的正确顺序是: .
(5)电解水时,向水中加入适量某物质可增加溶液导电性,从而加快水的电解。图四为水电解前溶质的分布情况,请在图五中画出电解一段时间后液面位置和溶质粒子的分布模型图。(为溶质粒子)
25.如图是某学校实验室从化学试剂商店买回的硫酸试剂的标签上的部分内容,阅读后计算:
浓硫酸(H2SO4)500毫升
浓度(质量分数) 98%
密度 1.84克/厘米3
相对分子质量 98
强腐蚀性,阴冷,密封贮藏
(1)这瓶浓硫酸的含溶质 g。
(2)欲配制600克溶质质量分数为19.6%的稀硫酸,需要这种硫酸多少毫升?
26.如图是硫酸的密度和浓度的对照表,阅读后计算:
硫酸的密度和硫酸溶液中溶质的质量分数对照表(20℃)
密度(克/厘米3) 1.01 1.07 1.14 1.22 1.30 1.40 1.50 1.61 1.73 1.81 1.84
质量分数(%) 1 10 20 30 40 50 60 70 80 90 98
(1)欲配制100克溶质质量分数为9.8%的稀硫酸,需要98%浓硫酸多少毫升 再加水多少毫升
(2)100毫升90%的硫酸与144.8毫升水混合后所得溶液的密度为多少
答案解析部分
1.【答案】A
2.【答案】D
3.【答案】D
4.【答案】D
5.【答案】D
6.【答案】C
7.【答案】A
8.【答案】B
9.【答案】D
10.【答案】D
11.【答案】B
12.【答案】B
13.【答案】D
14.【答案】D
15.【答案】D
16.【答案】(1)水汽输送
(2)地表径流
(3)蒸发和降水
17.【答案】悬浊物;①④
18.【答案】(1)乳浊液
(2)乙
(3)偏小
19.【答案】(1)D
(2)17%
20.【答案】(1)吸收
(2)68
(3)不饱和;③
21.【答案】(1)混合物;引流;AD
(2)溶解;ACD
22.【答案】(1)加快溶解
(2)≥40℃
(3)B;C;D
(4)32.4g 硝酸钾
(5)氯化钠和硝酸钾
(6)<
(7)C;D
23.【答案】(1)cba
(2)有大量晶体析出
(3)A;C
(4)不合理,最终得到的白色固体仍是混合物,不是纯净的氯化钠
24.【答案】(1)对流层
(2)①
(3)氢气
(4)丙甲乙
(5)
25.【答案】(1)901.6
(2)解:设需要这种浓硫酸的质量为x,
有600g×19.6%=98%x;解得:x=120g;
需要这种硫酸的体积为:V=m/ρ=120g/1.84g/cm3≈65.2cm3=65.2mL;
26.【答案】(1)54.3毫升|900毫升
(2)质量分数为:50.0%,所以密度为1.40克/厘米3
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
