第二单元复习 课件 2023-2024学年初中化学人教版九年级上册(共24张PPT)
文档属性
| 名称 | 第二单元复习 课件 2023-2024学年初中化学人教版九年级上册(共24张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 365.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-01-31 00:00:00 | ||
图片预览








文档简介
(共24张PPT)
第二单元复习
我们周围的空气
1.能说出空气的成分、用途、污染和防治措施。
2.能说出测定氧气含量的实验原理、现象、结论。
3.能说出氧气的物理性质、化学性质。
4.能描述木炭、硫粉、铁丝与氧气反应的实验现象,并写出文字表达式。
5.能概述实验室制取氧气的原理、操作步骤、检验和验满方法。
6.能区分化合反应、分解反应和氧化反应。
7.能概括催化剂的特点。
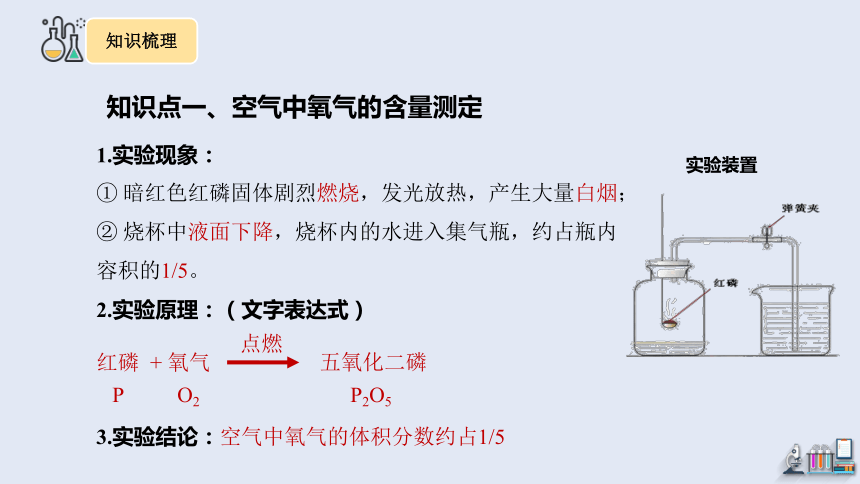
知识点一、空气中氧气的含量测定
1.实验现象:
① 暗红色红磷固体剧烈燃烧,发光放热,产生大量白烟;
② 烧杯中液面下降,烧杯内的水进入集气瓶,约占瓶内容积的1/5。
五氧化二磷
红磷 + 氧气
点燃
P O2 P2O5
实验装置
2.实验原理:(文字表达式)
3.实验结论:空气中氧气的体积分数约占1/5
知识点二、空气的组成
1.空气的成分按体积计算,大约是:
氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%。
3.纯净物:
只由一种物质组成的物质。
2.混合物:
由两种或两种以上的物质混合而成的物质。
纯净物可以用专门的
化学符号来表示
3.氧气的性质
物理性质:
通常情况下是一种无色无味气体,熔点-218.8℃,沸点-183.1℃,密度比空气大。
化学性质:
氧气具有助燃性,氧化性。化学符号:O2
用途:供给呼吸、支持燃烧、气焊等。
4.氮气的性质
物理性质:
在通常情况下是一种无色无味气体,熔点是-210 ℃ ,沸点是-195.8 ℃ ,大气中体积分数:78.08%(约78%)。
用途:制造硝酸和氮肥的重要原料、用作保护气等。
5.稀有气体的性质
物理性质:
无色无味气体,微溶于水,熔点和沸点都很低,低温时都可液化。
化学性质:
非常稳定,极少进行化学反应。
用途:制作霓虹灯,用作保护气等。
化学性质:
不活泼,常温下难与其他物质发生化学反应。
防治措施:
植树造林;减少化石燃料的燃烧;开发新能源等。
6.保护空气
污染物:
一氧化碳、二氧化硫、二氧化氮、臭氧、可吸入颗粒物
污染来源:
化石燃料的燃烧、汽车尾气的排放、工业废气等
危害:
形成酸雨、破环臭氧层、损害人体健康、影响农作物生长等
1.某班同学用如图装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管。然后点燃红磷,伸入瓶中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变 化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5。
下列对这两种现象解释合理的是( )。
①甲同学可能使用红磷的量不足,瓶内氧气没有消耗完
②甲同学可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
③乙同学可能没夹紧弹簧夹,红磷燃烧时瓶内部分空气受热从导管逸出
④乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出。
A. 只有①③ B. 只有②④ C. 只有①②③ D. ①②③④
D
2.空气是一种宝贵的自然资源。下列有关空气的说法不正确的是( )。
A. 氮气的化学性质不活泼,可用于食品的防腐
B. 燃烧法测定空气中氧气的含量,不能用硫代替红磷
C. 空气的成分按质量计算,氧气大约占21%
D. 禁止燃放烟花爆竹,可以减少空气污染
C
3.下列物质中,属于纯净物的是( )。
A 新鲜洁净的空气 B 冰水混合物 C 市售矿泉水 D 洁净的海水
B
4.下列关于空气的说法正确的是( )。
A.氮气可用于生产氮肥
B.二氧化碳是一种空气污染物
C.空气中氧气的质量分数约为21%
D.空气中的各成分在混合后,各自的化学性质改变
5.“人造空气”帮助人类实现了“太空漫步”的梦想,其中含有70%的N2、20%左右的O2、还有CO2等。下列说法正确的是( )。
A.带火星的木条放在“人造空气”中复燃
B.“人造空气”中的N2可用于生产氮肥
C.将澄清石灰水长期敞口放在“人造空气”中也不会变浑浊
D.利用木炭燃烧来测定“人造空气”中氧气的含量
A
B
知识点三、氧气
实验现象 文字表达式
硫在氧气中燃烧 (1)产生______________ 火焰 (2)生成_____________气味的气体 (3)放出热量
木炭氧气中燃烧 (1)发出_________光 (2)生成的气体可以使澄清石灰水________ (3)放出热量
铁丝氧气中燃烧 (1)_____________ (2)生成__________固体 (3)放出热量
铁+氧气 四氧化三铁
点燃
硫+氧气 二氧化硫
点燃
木炭+氧气 二氧化碳
点燃
明亮的蓝紫色
刺激性
白
变浑浊
火星四射
黑色
知识点四、化合反应和氧化反应
1.化合反应
概念:由两种或两种以上物质生成另一种物质的反应。
反应通式: A + B+···· = AB (多变一)
2.氧化反应
概念:物质与氧发生的反应叫做氧化反应。
强调是否有氧参加
1.下列关于氧气的说法正确的是( )。
A.氧气具有可燃性,可以支持燃烧
B.水生动物能在水中生存说明氧气易溶于水
C.工业上利用分离液态空气的方法制取氧气
D.氧气的化学性质比较活泼,能与所有的物质发生化学反应
C
2.下列化学变化不属于氧化反应的是( )。
A.燃气燃烧 B.铁生锈
C.光合作用 D.呼吸作用
C
2.现有①木炭 ②硫粉 ③红磷 ④镁带 ⑤铁丝,五种物质分别在氧气中燃烧,用序号回答下列问题:
(1)发出明亮的蓝紫色火焰的是________;
(2)产生大量白烟的是________;
(3)放出大量热,发出耀眼白光的是________;
(4)产生的气体能使澄清石灰水变浑浊的是________;
(5)生成的气体会污染空气的是________
(6)火星四射,生成一种黑色固体的是 。
③
②
④
①
②
⑤
知识点五、制取氧气
加热
高锰酸钾 锰酸钾+二氧化锰+氧气
加热
氯酸钾 氯化钾+氧气
二氧化锰
过氧化氢 水+氧气
二氧化锰
1.实验室制取氧气的方法
收集方法:排水法和向上排空气法
①分离液态空气法(利用沸点的不同)
②膜分离法(让空气通过具有富集氧气功能的薄膜,可得到含氧量较高的富氧空气)
氧气的工业制法是物理变化
氧气的实验室制法是化学变化
区别
2.工业制取氧气的方法
3.实验加热高锰酸钾制取氧气的实验步骤
①查:检查装置的气密性
②装:将药品平铺在试管底部
③定:将试管固定在铁架台上
④点:点燃酒精灯
⑤收:收集气体
⑥离:将导管移出水面
⑦熄:熄灭酒精灯
口诀:茶庄定点收利息
4.检验和验满
①检验:将带火星的木条插到集气瓶中,如果木条复燃,则证明是氧气。
②验满:用带火星的木条放在集气瓶口,木条复燃,表明集气瓶中已集满氧气。
知识点六、催化剂
能____化学反应的速率,而本身的______________在反应前后没有发生变化的物质叫做催化剂。催化剂在反应中的作用:________。
改变反应速率
本身质量、化学性质反应前后不改变
【催化剂特点】
催化作用
改变
质量和化学性质
不改变生成物的质量
知识点七、分解反应
1.概念
像这样都是由一种物质生成两种或两种以上其他的物质的反应,叫做分解反应。
即:A = B + C + · · ·
1.下列加热高锰酸钾制取氧气的部分操作示意图中,正确的是( )。
A
C
2.现有质量相等的两份氯酸钾固体,一份单独加热,一份与少量二氧化锰混合加热,当完全反应后,产生的氧气的质量(m)和反应时间(t)的关系图正确的是( )。
D
3.下列有关氧化反应、化合反应的说法中,正确的是( )。
A. 有两种物质参加的反应是化合反应
B. 只有物质与氧气之间发生的反应才叫做氧化反应
C. 化合反应一定是氧化反应,氧化反应不一定是化合反应
D. 有氧气参加,且由两种物质生成另一种物质的反应,既是化合反应,又是氧化反应
我们周围的空气
空气
氧气的含量的测定
氧气
催化剂
成分:氮气78%、氧气21%等
性质
制取
化合反应,分解反应、氧化反应
污染和防治
原理
装置
操作步骤
检验和验满
物理性质
化学性质
与木炭反应
与铁丝反应
与硫粉反应
第二单元复习
我们周围的空气
1.能说出空气的成分、用途、污染和防治措施。
2.能说出测定氧气含量的实验原理、现象、结论。
3.能说出氧气的物理性质、化学性质。
4.能描述木炭、硫粉、铁丝与氧气反应的实验现象,并写出文字表达式。
5.能概述实验室制取氧气的原理、操作步骤、检验和验满方法。
6.能区分化合反应、分解反应和氧化反应。
7.能概括催化剂的特点。
知识点一、空气中氧气的含量测定
1.实验现象:
① 暗红色红磷固体剧烈燃烧,发光放热,产生大量白烟;
② 烧杯中液面下降,烧杯内的水进入集气瓶,约占瓶内容积的1/5。
五氧化二磷
红磷 + 氧气
点燃
P O2 P2O5
实验装置
2.实验原理:(文字表达式)
3.实验结论:空气中氧气的体积分数约占1/5
知识点二、空气的组成
1.空气的成分按体积计算,大约是:
氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%、其他气体和杂质0.03%。
3.纯净物:
只由一种物质组成的物质。
2.混合物:
由两种或两种以上的物质混合而成的物质。
纯净物可以用专门的
化学符号来表示
3.氧气的性质
物理性质:
通常情况下是一种无色无味气体,熔点-218.8℃,沸点-183.1℃,密度比空气大。
化学性质:
氧气具有助燃性,氧化性。化学符号:O2
用途:供给呼吸、支持燃烧、气焊等。
4.氮气的性质
物理性质:
在通常情况下是一种无色无味气体,熔点是-210 ℃ ,沸点是-195.8 ℃ ,大气中体积分数:78.08%(约78%)。
用途:制造硝酸和氮肥的重要原料、用作保护气等。
5.稀有气体的性质
物理性质:
无色无味气体,微溶于水,熔点和沸点都很低,低温时都可液化。
化学性质:
非常稳定,极少进行化学反应。
用途:制作霓虹灯,用作保护气等。
化学性质:
不活泼,常温下难与其他物质发生化学反应。
防治措施:
植树造林;减少化石燃料的燃烧;开发新能源等。
6.保护空气
污染物:
一氧化碳、二氧化硫、二氧化氮、臭氧、可吸入颗粒物
污染来源:
化石燃料的燃烧、汽车尾气的排放、工业废气等
危害:
形成酸雨、破环臭氧层、损害人体健康、影响农作物生长等
1.某班同学用如图装置测定空气里氧气的含量。先用弹簧夹夹住乳胶管。然后点燃红磷,伸入瓶中并塞上瓶塞。待红磷熄灭并冷却后,打开弹簧夹,观察广口瓶内水面变 化情况。实验完毕,甲同学的广口瓶内水面上升明显小于瓶内空气体积的1/5,乙同学的广口瓶内水面上升明显大于瓶内空气体积的1/5。
下列对这两种现象解释合理的是( )。
①甲同学可能使用红磷的量不足,瓶内氧气没有消耗完
②甲同学可能未塞紧瓶塞,红磷熄灭冷却时外界空气进入瓶内
③乙同学可能没夹紧弹簧夹,红磷燃烧时瓶内部分空气受热从导管逸出
④乙同学可能插入燃烧匙太慢,塞紧瓶塞之前,瓶内部分空气受热逸出。
A. 只有①③ B. 只有②④ C. 只有①②③ D. ①②③④
D
2.空气是一种宝贵的自然资源。下列有关空气的说法不正确的是( )。
A. 氮气的化学性质不活泼,可用于食品的防腐
B. 燃烧法测定空气中氧气的含量,不能用硫代替红磷
C. 空气的成分按质量计算,氧气大约占21%
D. 禁止燃放烟花爆竹,可以减少空气污染
C
3.下列物质中,属于纯净物的是( )。
A 新鲜洁净的空气 B 冰水混合物 C 市售矿泉水 D 洁净的海水
B
4.下列关于空气的说法正确的是( )。
A.氮气可用于生产氮肥
B.二氧化碳是一种空气污染物
C.空气中氧气的质量分数约为21%
D.空气中的各成分在混合后,各自的化学性质改变
5.“人造空气”帮助人类实现了“太空漫步”的梦想,其中含有70%的N2、20%左右的O2、还有CO2等。下列说法正确的是( )。
A.带火星的木条放在“人造空气”中复燃
B.“人造空气”中的N2可用于生产氮肥
C.将澄清石灰水长期敞口放在“人造空气”中也不会变浑浊
D.利用木炭燃烧来测定“人造空气”中氧气的含量
A
B
知识点三、氧气
实验现象 文字表达式
硫在氧气中燃烧 (1)产生______________ 火焰 (2)生成_____________气味的气体 (3)放出热量
木炭氧气中燃烧 (1)发出_________光 (2)生成的气体可以使澄清石灰水________ (3)放出热量
铁丝氧气中燃烧 (1)_____________ (2)生成__________固体 (3)放出热量
铁+氧气 四氧化三铁
点燃
硫+氧气 二氧化硫
点燃
木炭+氧气 二氧化碳
点燃
明亮的蓝紫色
刺激性
白
变浑浊
火星四射
黑色
知识点四、化合反应和氧化反应
1.化合反应
概念:由两种或两种以上物质生成另一种物质的反应。
反应通式: A + B+···· = AB (多变一)
2.氧化反应
概念:物质与氧发生的反应叫做氧化反应。
强调是否有氧参加
1.下列关于氧气的说法正确的是( )。
A.氧气具有可燃性,可以支持燃烧
B.水生动物能在水中生存说明氧气易溶于水
C.工业上利用分离液态空气的方法制取氧气
D.氧气的化学性质比较活泼,能与所有的物质发生化学反应
C
2.下列化学变化不属于氧化反应的是( )。
A.燃气燃烧 B.铁生锈
C.光合作用 D.呼吸作用
C
2.现有①木炭 ②硫粉 ③红磷 ④镁带 ⑤铁丝,五种物质分别在氧气中燃烧,用序号回答下列问题:
(1)发出明亮的蓝紫色火焰的是________;
(2)产生大量白烟的是________;
(3)放出大量热,发出耀眼白光的是________;
(4)产生的气体能使澄清石灰水变浑浊的是________;
(5)生成的气体会污染空气的是________
(6)火星四射,生成一种黑色固体的是 。
③
②
④
①
②
⑤
知识点五、制取氧气
加热
高锰酸钾 锰酸钾+二氧化锰+氧气
加热
氯酸钾 氯化钾+氧气
二氧化锰
过氧化氢 水+氧气
二氧化锰
1.实验室制取氧气的方法
收集方法:排水法和向上排空气法
①分离液态空气法(利用沸点的不同)
②膜分离法(让空气通过具有富集氧气功能的薄膜,可得到含氧量较高的富氧空气)
氧气的工业制法是物理变化
氧气的实验室制法是化学变化
区别
2.工业制取氧气的方法
3.实验加热高锰酸钾制取氧气的实验步骤
①查:检查装置的气密性
②装:将药品平铺在试管底部
③定:将试管固定在铁架台上
④点:点燃酒精灯
⑤收:收集气体
⑥离:将导管移出水面
⑦熄:熄灭酒精灯
口诀:茶庄定点收利息
4.检验和验满
①检验:将带火星的木条插到集气瓶中,如果木条复燃,则证明是氧气。
②验满:用带火星的木条放在集气瓶口,木条复燃,表明集气瓶中已集满氧气。
知识点六、催化剂
能____化学反应的速率,而本身的______________在反应前后没有发生变化的物质叫做催化剂。催化剂在反应中的作用:________。
改变反应速率
本身质量、化学性质反应前后不改变
【催化剂特点】
催化作用
改变
质量和化学性质
不改变生成物的质量
知识点七、分解反应
1.概念
像这样都是由一种物质生成两种或两种以上其他的物质的反应,叫做分解反应。
即:A = B + C + · · ·
1.下列加热高锰酸钾制取氧气的部分操作示意图中,正确的是( )。
A
C
2.现有质量相等的两份氯酸钾固体,一份单独加热,一份与少量二氧化锰混合加热,当完全反应后,产生的氧气的质量(m)和反应时间(t)的关系图正确的是( )。
D
3.下列有关氧化反应、化合反应的说法中,正确的是( )。
A. 有两种物质参加的反应是化合反应
B. 只有物质与氧气之间发生的反应才叫做氧化反应
C. 化合反应一定是氧化反应,氧化反应不一定是化合反应
D. 有氧气参加,且由两种物质生成另一种物质的反应,既是化合反应,又是氧化反应
我们周围的空气
空气
氧气的含量的测定
氧气
催化剂
成分:氮气78%、氧气21%等
性质
制取
化合反应,分解反应、氧化反应
污染和防治
原理
装置
操作步骤
检验和验满
物理性质
化学性质
与木炭反应
与铁丝反应
与硫粉反应
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
