第一章 第一节 第3课时 泡利原理、洪特规则、能量最低原理 课件(共16张PPT) 2023-2024学年高二化学人教版(2019)选择性必修2
文档属性
| 名称 | 第一章 第一节 第3课时 泡利原理、洪特规则、能量最低原理 课件(共16张PPT) 2023-2024学年高二化学人教版(2019)选择性必修2 |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-01 00:00:00 | ||
图片预览





文档简介
(共16张PPT)
第一节 原子结构
第3课时 泡利原理、洪特规则、能量最低原理
第一章 原子结构与性质
利用STM观察原子
[学习目标]
1.能从原子微观层面理解原子的组成、结构。
2.能根据核外电子的排布规则熟知核外电子排布的表示方法(重点)。
知识回顾
能级 ns np nd nf
轨道数
最多容纳电子数
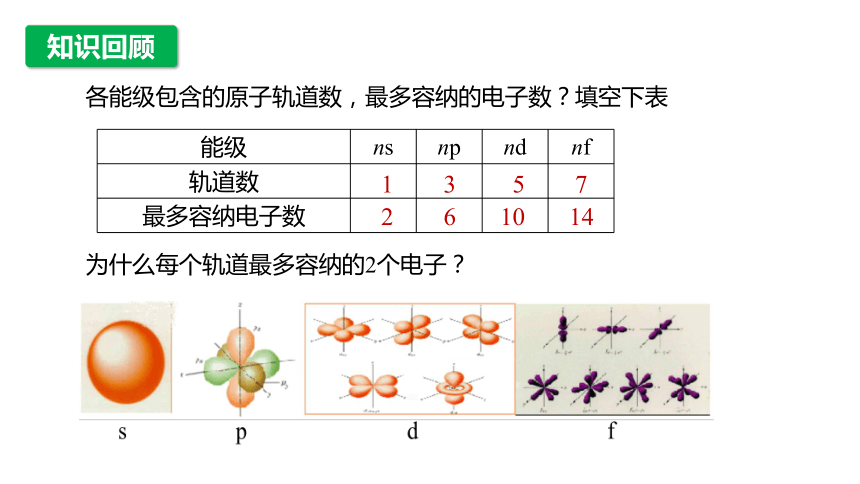
各能级包含的原子轨道数,最多容纳的电子数?填空下表
1 3 5 7
2 6 10 14
为什么每个轨道最多容纳的2个电子?
一、电子自旋与泡利原理
电子自旋——微观粒子普遍存在的一种内在属性
有顺时针和逆时针两种取向,简称自旋相反,常用“↑和↓”表示。
注意:能层、能级、原子轨道和自旋状态四个方面共同决定电子的运动状态。
一个原子中不可能存在运动状态完全相同的2个电子。
2.泡利原理
在一个原子轨道里,最多只能容纳2个电子,它们的自旋相反。
又称作泡利不相容原理。
二、电子排布的轨道表示式
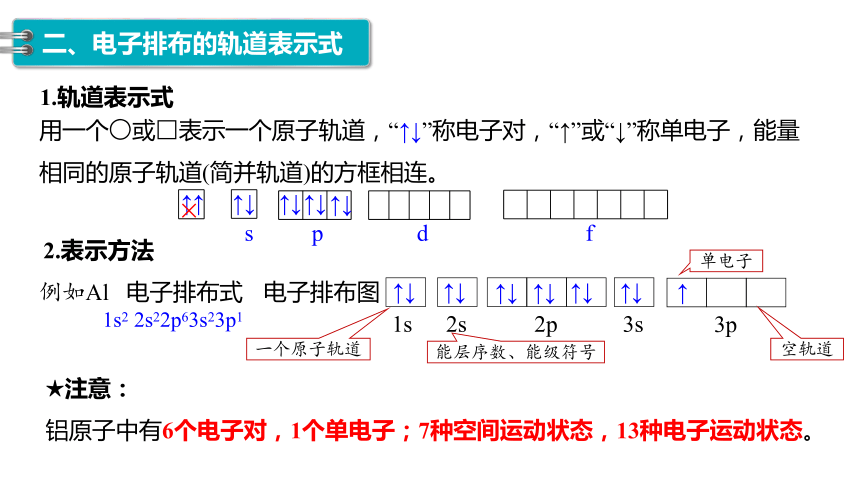
1.轨道表示式
用一个○或□表示一个原子轨道,“↑↓”称电子对,“↑”或“↓”称单电子,能量相同的原子轨道(简并轨道)的方框相连。
1s2 2s22p63s23p1
例如Al 电子排布式 电子排布图
s p d f
↑↓
↑↑
2.表示方法
1s
2s
2p
3s
3p
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑
↑↓
↑↓
↑↓
一个原子轨道
能层序数、能级符号
空轨道
单电子
★注意:
铝原子中有6个电子对,1个单电子;7种空间运动状态,13种电子运动状态。
×
三、洪特规则
↑↓
↑↓
1s
2s
2p
3s
3p
3d
4s
1.内容
基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行。
24Cr
1s
2s
2p
7N
↑
↑
↑
↑↓
↑↓
↓
1s
2s
2p
8O
↑
↑
↑
电子排布式:1s22s22p63s23p63d54s1
2.特例
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑ ↑ ↑ ↑
×
★全充满、全空、半充满状态时,具有较低的能量和较强的稳定性。
↑
↑ ↑ ↑ ↑ ↑
四、能量最低原理
结合构造原理分析Fe原子电子排布图,你能有何发现?
1.内容:
在构建基态原子时,电子将尽可能地占据能量最低的原子轨道,使整个原子的能量最低。
2.因素:
整个原子的能量由核电荷数、电子数和电子状态三个因素共同决定。
26Fe
↑↓
↑
↑
↑
↑
3d
↑↓
4s
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
1s
2s
2p
3s
↑↓
↑↓
↑↓
3p
思考交流
1.下列轨道表示式中哪个是氧的基态原子?为什么?
A. B. C.
洪特规则:基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行。
√
2.下列有关电子轨道表示式的表述正确的是
A. 可表示单核10电子粒子基态时的电子排布
B. 表示错误,违背了泡利原理
C. 表示基态N原子的价层电子排布
D. 表示处于激发态的B原子的核外电子轨道表示式
√
思考交流
3.(1)下列是一些原子的2p能级和3d能级电子排布的情况。试判断,违背了泡利原理的是____(填序号,下同),违背了洪特规则的是________。
② ③
④ ⑤ ⑥
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为______________;其最高价氧化物对应水化物的化学式______。
③
②④⑥
1s22s22p63s23p4
H2SO4
(3)现有下列多电子原子的原子轨道:①2s ②3d ③3s ④4p ⑤3p
轨道能量由低到高排列的顺序是____________(填序号)。
①③⑤②④
思考交流
4.(1)Mn元素与O元素中,基态原子核外未成对电子数较多的是______。
(2)基态Ge原子有____个未成对电子。
(3)镍元素基态原子的3d能级上的未成对电子数为____。
Mn
2
2
注意 书写轨道表示式时,常出现的错误及正确书写
归纳总结
自我测试
1.下列括号里对某些基态原子或离子的核外电子排布的评价正确的是
A.基态硫原子的3p电子轨道表示式: (错误,违背洪特规则)
B.基态Fe2+的价层电子轨道表示式: (正确,失去能量较低的3d电子)
C.基态碳原子的电子排布式:1s22s12p3(正确,半充满较稳定)
D.基态钪原子的电子排布式:1s22s22p63s23p63d14s2(正确,符合能量最低原理)
√
自我测试
2.下列有关电子排布式、原子结构示意图以及轨道表示式正确的是
A.钴(Co)的电子排布式为1s22s22p63s23p63d9
B.As的价层电子轨道表示式:
C.Fe的原子结构示意图:
D.Mn2+的价层电子轨道表示式:
√
自我测试
3.(2023·武汉高二期末)下列化学用语正确的是
A.Cl-的结构示意图:
B.基态镍原子(Ni)的电子排布式:[Ar]3d84s2
C.水的电子式:
D.基态氧原子的核外电子轨道表示式:
√
自我测试
4.(1)元素Y的原子最外层电子排布式为nsn-1npn+1,Y的元素符号为____,原子的核外电子排布式为_______________。
S
1s22s22p63s23p4
(2)下列轨道表示式中,能正确表示元素X的原子处于最低能量状态的是____(填字母)。
D
本节内容结束
第一节 原子结构
第3课时 泡利原理、洪特规则、能量最低原理
第一章 原子结构与性质
利用STM观察原子
[学习目标]
1.能从原子微观层面理解原子的组成、结构。
2.能根据核外电子的排布规则熟知核外电子排布的表示方法(重点)。
知识回顾
能级 ns np nd nf
轨道数
最多容纳电子数
各能级包含的原子轨道数,最多容纳的电子数?填空下表
1 3 5 7
2 6 10 14
为什么每个轨道最多容纳的2个电子?
一、电子自旋与泡利原理
电子自旋——微观粒子普遍存在的一种内在属性
有顺时针和逆时针两种取向,简称自旋相反,常用“↑和↓”表示。
注意:能层、能级、原子轨道和自旋状态四个方面共同决定电子的运动状态。
一个原子中不可能存在运动状态完全相同的2个电子。
2.泡利原理
在一个原子轨道里,最多只能容纳2个电子,它们的自旋相反。
又称作泡利不相容原理。
二、电子排布的轨道表示式
1.轨道表示式
用一个○或□表示一个原子轨道,“↑↓”称电子对,“↑”或“↓”称单电子,能量相同的原子轨道(简并轨道)的方框相连。
1s2 2s22p63s23p1
例如Al 电子排布式 电子排布图
s p d f
↑↓
↑↑
2.表示方法
1s
2s
2p
3s
3p
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑
↑↓
↑↓
↑↓
一个原子轨道
能层序数、能级符号
空轨道
单电子
★注意:
铝原子中有6个电子对,1个单电子;7种空间运动状态,13种电子运动状态。
×
三、洪特规则
↑↓
↑↓
1s
2s
2p
3s
3p
3d
4s
1.内容
基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行。
24Cr
1s
2s
2p
7N
↑
↑
↑
↑↓
↑↓
↓
1s
2s
2p
8O
↑
↑
↑
电子排布式:1s22s22p63s23p63d54s1
2.特例
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
↑ ↑ ↑ ↑
×
★全充满、全空、半充满状态时,具有较低的能量和较强的稳定性。
↑
↑ ↑ ↑ ↑ ↑
四、能量最低原理
结合构造原理分析Fe原子电子排布图,你能有何发现?
1.内容:
在构建基态原子时,电子将尽可能地占据能量最低的原子轨道,使整个原子的能量最低。
2.因素:
整个原子的能量由核电荷数、电子数和电子状态三个因素共同决定。
26Fe
↑↓
↑
↑
↑
↑
3d
↑↓
4s
↑↓
↑↓
↑↓
↑↓
↑↓
↑↓
1s
2s
2p
3s
↑↓
↑↓
↑↓
3p
思考交流
1.下列轨道表示式中哪个是氧的基态原子?为什么?
A. B. C.
洪特规则:基态原子中,填入简并轨道的电子总是先单独分占,且自旋平行。
√
2.下列有关电子轨道表示式的表述正确的是
A. 可表示单核10电子粒子基态时的电子排布
B. 表示错误,违背了泡利原理
C. 表示基态N原子的价层电子排布
D. 表示处于激发态的B原子的核外电子轨道表示式
√
思考交流
3.(1)下列是一些原子的2p能级和3d能级电子排布的情况。试判断,违背了泡利原理的是____(填序号,下同),违背了洪特规则的是________。
② ③
④ ⑤ ⑥
(2)某元素的激发态(不稳定状态)原子的电子排布式为1s22s22p63s13p33d2,则该元素基态原子的电子排布式为______________;其最高价氧化物对应水化物的化学式______。
③
②④⑥
1s22s22p63s23p4
H2SO4
(3)现有下列多电子原子的原子轨道:①2s ②3d ③3s ④4p ⑤3p
轨道能量由低到高排列的顺序是____________(填序号)。
①③⑤②④
思考交流
4.(1)Mn元素与O元素中,基态原子核外未成对电子数较多的是______。
(2)基态Ge原子有____个未成对电子。
(3)镍元素基态原子的3d能级上的未成对电子数为____。
Mn
2
2
注意 书写轨道表示式时,常出现的错误及正确书写
归纳总结
自我测试
1.下列括号里对某些基态原子或离子的核外电子排布的评价正确的是
A.基态硫原子的3p电子轨道表示式: (错误,违背洪特规则)
B.基态Fe2+的价层电子轨道表示式: (正确,失去能量较低的3d电子)
C.基态碳原子的电子排布式:1s22s12p3(正确,半充满较稳定)
D.基态钪原子的电子排布式:1s22s22p63s23p63d14s2(正确,符合能量最低原理)
√
自我测试
2.下列有关电子排布式、原子结构示意图以及轨道表示式正确的是
A.钴(Co)的电子排布式为1s22s22p63s23p63d9
B.As的价层电子轨道表示式:
C.Fe的原子结构示意图:
D.Mn2+的价层电子轨道表示式:
√
自我测试
3.(2023·武汉高二期末)下列化学用语正确的是
A.Cl-的结构示意图:
B.基态镍原子(Ni)的电子排布式:[Ar]3d84s2
C.水的电子式:
D.基态氧原子的核外电子轨道表示式:
√
自我测试
4.(1)元素Y的原子最外层电子排布式为nsn-1npn+1,Y的元素符号为____,原子的核外电子排布式为_______________。
S
1s22s22p63s23p4
(2)下列轨道表示式中,能正确表示元素X的原子处于最低能量状态的是____(填字母)。
D
本节内容结束
