湖南省衡阳市衡阳县2023-2024学年高二上学期1月期末考试化学试题(含解析)
文档属性
| 名称 | 湖南省衡阳市衡阳县2023-2024学年高二上学期1月期末考试化学试题(含解析) |  | |
| 格式 | docx | ||
| 文件大小 | 1009.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-03 23:32:44 | ||
图片预览



文档简介
衡阳县2023-2024学年高二上学期1月期末考试
化学
考生注意:
1.答题前,考生务必将自己的姓名、考生号填写在试卷和答题卡上,并将芳生号条形码粘贴在答题卡上的指定位置.
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑.如需改动,用橡皮擦干净后,再选涂其他答案标号.回答非选择题时,将答案写在答题卡上.写在本试卷上无效.
3.考试结束后,将本试卷和答题卡一并交回.
可能用到的相对原子质量:H 1 C 12 O 16 Cl 35.5 Fe 56 Cu 64
一、选择题:本题共14小题,每小题3分,共42分.每小题只有一个选项符合题目要求.
1.下列基态原子价层电子排布式对应元素的焰色呈黄色的是( )
A. B. C. D.
2.中国石化石油化工科学研究院最近从地沟油中提炼出航空燃油;我国航天科技集团六院自主成功开发500吨级液氧煤油发动机.下列叙述正确的是( )
A.航空燃油不完全燃烧不会对环境造成污染
B.液氧汽化过程是吸热反应
C.煤油燃烧反应是放热反应
D.航空燃油和煤油都是可再生能源
3.下列基态原子的未成对电子数最多的是( )
A.第二周期ⅦA族 B.第四周期ⅥB族
C.第四周期ⅡB族 D.第三周期ⅤA族
4.书写下列基态原子电子排布式时,最后一个电子进入$能级,但是不属于s区元素的是( )
A.锂 B.铁 C.钙 D.氦
5.主族元素X、Y、Z、R的原子序数依次增大,元素的某种性质递变规律如图所示.下列对应的元素和性质正确的是( )
A.原子半径: B.电负性:
C.第一电离能: D.最高正化合价:
6.下列化学用语错误的是( )
A.能层的能级:
B.基态锗()原子的电子排布式:
C.基态原子的价层电子轨道表示式:
D.p能级的电子云轮廓图:
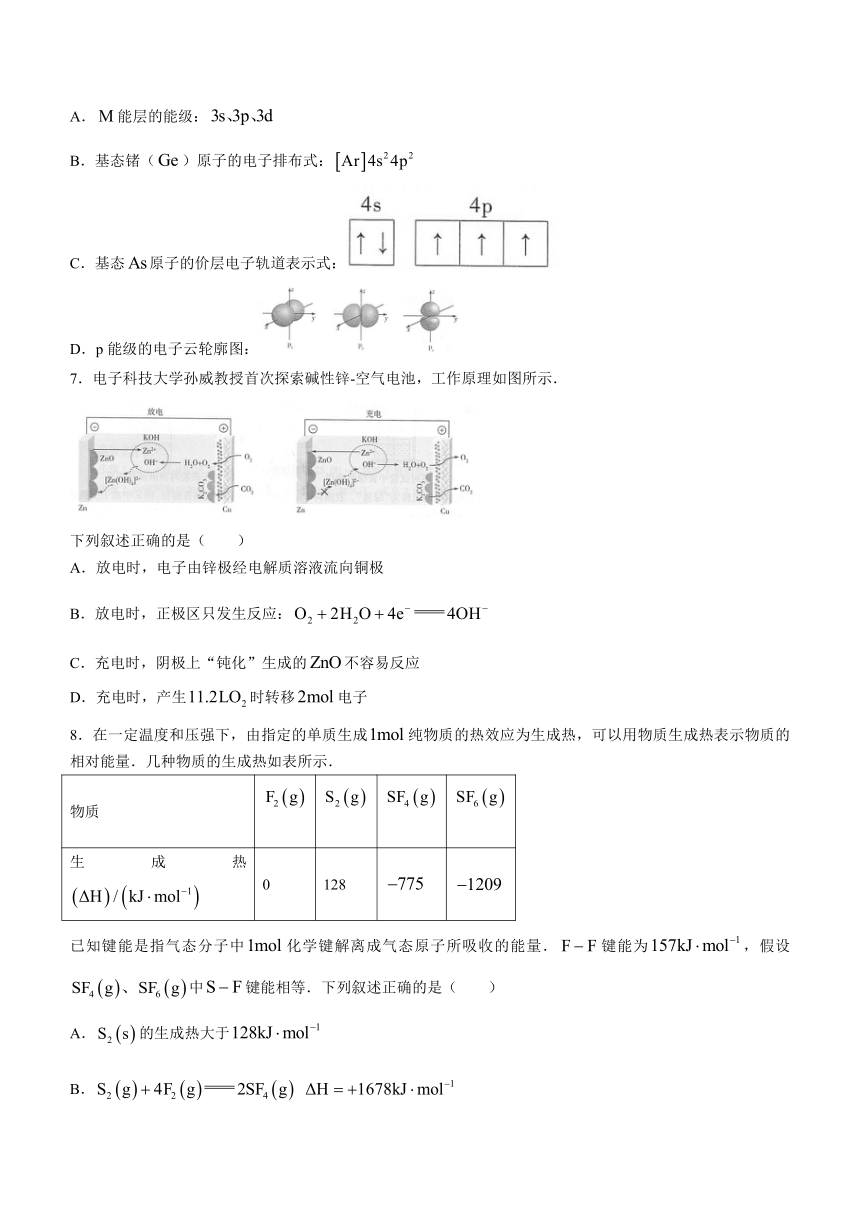
7.电子科技大学孙威教授首次探索碱性锌-空气电池,工作原理如图所示.
下列叙述正确的是( )
A.放电时,电子由锌极经电解质溶液流向铜极
B.放电时,正极区只发生反应:
C.充电时,阴极上“钝化”生成的不容易反应
D.充电时,产生时转移电子
8.在一定温度和压强下,由指定的单质生成纯物质的热效应为生成热,可以用物质生成热表示物质的相对能量.几种物质的生成热如表所示.
物质
生成热 0 128
已知键能是指气态分子中化学键解离成气态原子所吸收的能量.键能为,假设中键能相等.下列叙述正确的是( )
A.的生成热大于
B.
C.稳定性:
D.上述物质中,键能为
9.设为阿伏加德罗常数的值.下列叙述错误的是( )
A.电解法精炼铜时,阴极质量净增时,转移电子数为
B.时向密闭容器中充入,反应后体系中双原子分子总数为
C.溶液中阳离子总数小于
D.溶液中含粒子总数为
10.下列装置所示的过程与勒夏特列原理无关的是( )
A.加入时产生气泡速率加快 B.加入时乙烧瓶中气体颜色加深
C.光照时试管中黄绿色变浅 D.加入铁粉时溶液颜色变浅
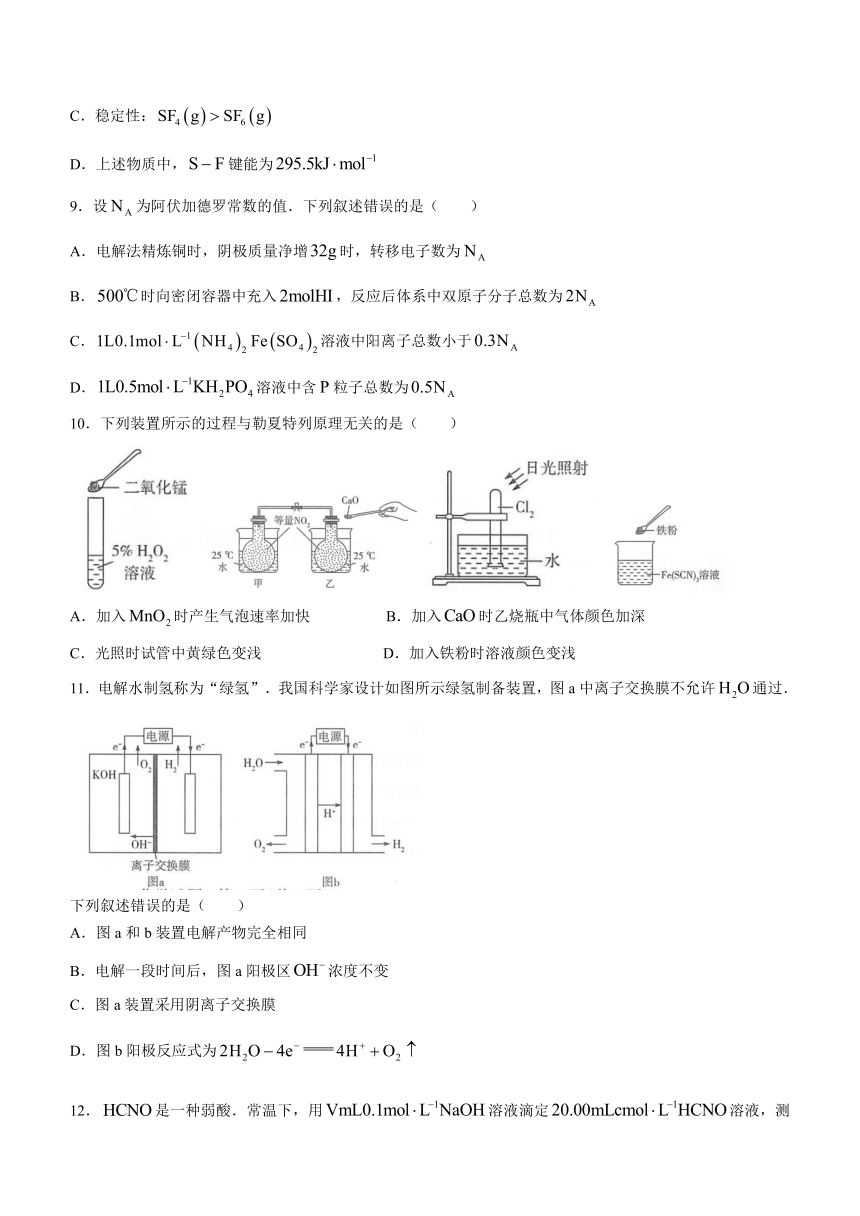
11.电解水制氢称为“绿氢”.我国科学家设计如图所示绿氢制备装置,图a中离子交换膜不允许通过.
下列叙述错误的是( )
A.图a和b装置电解产物完全相同
B.电解一段时间后,图a阳极区浓度不变
C.图a装置采用阴离子交换膜
D.图b阳极反应式为
12.是一种弱酸.常温下,用溶液滴定溶液,测定HCNO溶液的浓度.下列叙述正确的是( )
A.本实验可以选择甲基橙作指示剂
B.本实验需要的玻璃仪器为①②③
C.滴定过程中时,
D.若滴定终点时,则
13.某小组设计实验探究的性质,实验结果如下:
序号 操作及现象
① 向溶液中滴加溶液,产生白色沉淀,静置后,向上层清液中再滴加溶液,产生黑色沉淀
② 向溶液中滴加溶液,产生白色沉淀和臭鸡蛋气味气体
③ 向溶液中滴加溶液,产生乳白色浑浊
④ 向溶液中加入溶液,先产生乳白色浑浊,后产生黑色沉淀.分离黑色沉淀得到少量浅黄色固体和黑色固体;将黑色固体溶于稀硫酸,产生臭鸡蛋味气体和浅绿色溶液
下列推断错误的是( )
A.实验①证明溶解度:
B.实验②可知,产生的气体是
C.实验③中,产生乳白色浑浊发生的是复分解反应
D.实验③和④证明和相对量不同,产物不同
14.向三个体积均为的恒容绝热密闭容器中按不同方式投人反应物,起始温度为时发生反应:,测得达到平衡时的有关数据如下表.下列说法错误的是( )
容器 Ⅰ Ⅱ Ⅲ
反应物的投入量
平衡时正反应速率
平衡常数
平衡时的物质的量
反应物的转化率
A. B. C. D.
二、非选择题:本题共4小题,共58分.
15.(14分)前四周期元素的原子序数依次增大.基态原子核外电子的空间运动状态有4种,基态原子最外层电子数是内层电子数的3倍.元素对应的单质与酸或碱均能反应生成气体,基态核外有5个未成对电子.基态原子的部分电离能数据如下:
元素 电离能
738 1451 7733 10540
回答下列问题:
(1)W的元素符号为______________.
(2)基态原子最外层电子云轮廓图为______________(填名称).1个原子核外有______________种运动状态不同的电子.
(3)基态原子核外电子占据______________个原子轨道.基态原子核外能量最高的能层符号是______________.
(4)不稳定,易转化成的原因是______________(从结构角度分析).
(5)在水中剧烈反应生成一种碱和一种刺激性气味气体,该反应的化学方程式为______________.
16.(14分)是中学常用试剂,在化学实验中有广泛应用,请回答下列问题.
(1)溶于水,发生如下反应:
①
②
③
(用含的式子表示).
(2)利用制备无水氯化铁有如下三种方法.
①上述方法中的作用是______________.
②方法中制备的同时产生两种酸性气体,写出该反应的化学方程式:______________.
(3)为探究催化分解,设计如下实验方案:
实验 双氧水 加入试剂 温度 收集等质量所需时间
Ⅰ 10.0 蒸馏水 25
Ⅱ 10.0 溶液 25
Ⅲ 10.0 溶液 35
实验结果:.
①根据实验Ⅰ、Ⅱ可得出结论:______________.
②研究发现实验Ⅱ和Ⅲ中产生不同程度的红褐色沉淀,用必要的文字和化学用语解释产生红褐色沉淀的原因:______________.
(4)测定样品的纯度.
已知:(无色,稳定),易溶于水且完全电离.常温下,.
实验步骤如下:
步骤1:取样品配成溶液,准确量取溶液于锥形瓶中;
步骤2:向锥形瓶中加入足量溶液,充分反应后,加入溶液(过量)使完全沉淀;
步骤3:向其中加入硝基苯,用力振荡,使沉淀表面被有机物覆盖;
步骤4:加入3滴指示剂,用溶液滴定过量的至终点,消耗溶液.
测得样品中的质量分数为______________(用含和的代数式表示).若取消步骤3,则测定结果______________(填“偏大”“偏小”或“无影响”).
17.(14分)活性炭可用于处理气体,反应如下:
反应Ⅰ:
反应Ⅱ:
回答下列问题:
(1)______________.
(2)在恒温恒容密闭容器中投人足量的活性炭粉和.下列叙述正确的是______________(填字母).
A.容器中混合气体密度保持不变时达到平衡状态
B.达到平衡时,的体积分数等于
C.其他条件不变,增大活性炭粉质量,达到平衡时,的体积百分含量增大
D.平衡后再充入少量的平衡转化率降低
(3)在密闭容器中充入足量活性炭粉和气体,发生反应Ⅰ、Ⅱ.测得的平衡转化率与温度、压强的关系如图1所示.
图1 图2
______________(填“>”“<”或“=”),理由是______________.
(4)一定温度下,在甲、乙两个体积相同的密闭容器中均充入和足量活性炭粉的混合物,分别在恒温恒容、绝热恒容条件下仅发生反应Ⅱ,测得气体压强与时间的关系如图2所示.
①绝热恒容条件下的反应在______________(填“甲”或“乙”)容器中发生.
②点时转化率为,则内用表示的平均反应速率为______________.在该温度下,该反应的平衡常数______________(为用各气体的物质的量分数计算的平衡常数).
18.(16分)某课题组设计合成了负极材料,某简易流程如图所示(部分反应物、产物和条件省略):
已知:常温下,.
请回答下列问题:
(1)操作1前,反应物混合溶液要不断搅拌,其目的是______________.
(2)在实验室中完成操作1需要的玻璃仪器有______________(填名称).
(3)和表面吸附有等,检验固体是否洗净的操作是______________.
(4)操作3包括蒸发浓缩、______________、过滤、洗涤、干燥.利用如图所示装置除去固体中少量杂质,提纯氯化铵.
装置中棉花的作用是______________;
扎有小孔的滤纸的用途是______________.
(5)已知:离子浓度小于或等于时认为离子已沉淀完全.常温下,完全沉淀时溶液最小为______________.
(6)写出时发生反应的化学方程式:______________.
高二化学·答案
1~14题,每小题3分,共42分.
1.答案A
命题透析 本题以焰色试验为素材,考查常见元素焰色、基态原子价层电子排布式等知识,意在考查理解与辨析能力,宏观辨识与微观探析的核心素养.
思路点拨 对应的是钠元素,焰色试验呈黄色,A项符合题意;对应的是钾元素,焰色试验呈紫色(透过蓝色钴玻璃观察),B项不符合题意;对应的是铜元素,焰色试验呈绿色,C项不符合题意;对应的是元素,焰色试验呈砖红色,D项不符合题意.
2.答案 C
命题透析 本题以燃料为素材,考查热化学基本概念,意在考查判断能力,科学态度与社会责任的核心素养.
思路点拨 航空燃油不完全燃烧会产生等污染气体,A项错误;液氧汽化属于物理变化,由液态到气态,是吸热过程,不是吸热反应,B项错误;燃烧反应都是放热反应,C项正确;煤油是化石能源之一,是不可再生能源,D项错误.
3.答案 B
命题透析 本题以未成对电子数的判断为素材,考查核外电子排布、元素周期表结构等知识,意在考查分析与
推测能力,宏观辨识与微观探析的核心素养.
思路点拨 第二周期ⅦA族是F元素,价层电子排布式为有1个未成对电子;第四周期ⅥB族是元素,价层电子排布式为,有6个未成对电子;第四周期ⅡB族是元素,价层电子排布式为,无未成对电子;第三周期ⅤA族是P元素,价层电子排布式为,有3个未成对电子,B项符合题意.
4.答案 D
命题透析 本题以基态原子电子排布式为素材,考查元素分区等知识,意在考查分析与推测能力,证据推理与模型认知的核心素养.
思路点拨 基态锂原子的最后一个电子填充能级,属于s区元素,A项不符合题意;基态铁原子的最后一个电子填充能级,属于d区元素,B项不符合题意;基态钙原子的最后一个电子填充能级,属于s区元素,C项不符合题意;基态氮原子的最后一个电子填充1s能级,属于p区元素,D项符合题意.
5.答案 C
命题透析 本题以主族元素为素材,考查元素性质的递变规律等知识,意在考查分析与推测能力,宏观辨识与微观探析的核心素养.
思路点拨 根据图示,随着原子序数递增,元素性质总体呈增大趋势,但是Y元素出现“反常”.F、、、I的原子半径依次增大,A项不符合题意;O、S、、的电负性依次减小,B项不符合题意;、P、S、的第一电离能呈增大趋势,但P的能级电子排布是半充满的,比较稳定,电离能较高,C项符合题意;氧没有最高正化合价,氟没有正价,D项不符合题意.
6.答案 B
命题透析 本题以化学用语为素材,考查价层电子轨道表示式、电子云轮廓图等知识,意在考查理解与辨析能力,证据推理与模型认知的核心素养.
思路点拨 M能层为第三层,包括三个能级,A项正确;基态锗()原子的电子排布式为或,B项错误;基态As原子的价层电子排布式为,价层电子轨道表示式为,C项正确;p能级有3个相互垂直的电子云,电子云轮廓图为哑铃形,D项正确.
7.答案C
命题透析 本题以碱性锌-空气电池为素材,考查二次电池工作原理,意在考查推理与判断能力,证据推理与模型认知的核心素养.
思路点拨 放电时,电子由负极经外电路流向正极,不经过电解质溶液,A项错误;根据图像,放电时正极还有副产物产生,B项错误;充电时,阴极上氧化锌不容易得电子,C项正确;没有指明温度和压强,无法计算,D项错误.
8.答案D
命题透析 本题以硫的氟化物为素材,考查反应热、键能相关的计算,意在考查计算能力,宏观辨识与微观探析的核心素养.
思路点拨 是放热过程,的生成热小于,A项错误;反应热等于生成物的总能量与反应物的总能量之差,,B项错误;生成热越低,物质具有的能量越低,物质越稳定,故比稳定,C项错误;,反应热等于反应物总键能-生成物总键能,设S—F键能为x,则,解得:,D项正确.
9.答案 C
命题透析 本题以阿伏加德罗常数为素材,考查物质结构、性质和计算,意在考查推理与计算能力,宏观辨识与微观探析的核心素养.
思路点拨 电解法精炼铜中,阴极反应式为,A项正确;,混合气体中三种分子都是双原子分子且反应前后气体分子数相等,B项正确;硫酸亚铁铵溶液中阳离子包括,,阳离子总数增多,C项错误;由物料守恒得,D项正确.
10.答案 A
命题透析 本题以课本实验为情境,考查勤夏特列原理知识,意在考查实验探究的能力,科学探究与创新意识的核心素养.
思路点拨 作催化剂,加入时产生气泡速率加快,与勒夏特列原理无关,A项符合题意;,加入时,乙烧瓶中温度升高,平衡逆向移动,乙烧瓶中气体颜色加深,与勒夏特列原理有关,B项不符合题意;,光照使氯气与水反应的平衡正向移动,与勒夏特列原理有关,C项不符合题意;,,铁粉使铁离子与硫氰酸根离子反应的平衡逆向移动,与勒夏特列原理有关,D项不符合题意.
11.答案 B
命题透析 本题以电解水为情境,考查电解原理,意在考查理解与观察能力,证据推理与模型认知的核心素养.
思路点拨 上述装置实质是电解水,故电解产物都是氧气和氢气,A项正确;在图a阳极区添加了,阳极反应式为,消耗,但阴极区的会迁移至阳极区,故物质的量不变,但生成了水,溶液变稀,浓度下降,B项错误;根据图a知,阴极区的会迁移至阳极区,采用阴离子交换膜,C项正确;图b阳极上水参与反应,阳极反应式为,D项正确.
12.答案 D
命题透析 本题以和反应为素材,考查中和滴定实验,意在考查实验能力,科学探究与创新意识的核心素养.
思路点拨 是弱酸,恰好完全反应生成,溶液呈碱性,应选择酚酞作指示剂,A项错误;中和滴定实验需要锥形瓶,不需要烧杯,B项错误;时,由电荷守恒可得,中性溶液中,则,C项错误;,,D项正确.
13.答案 C
命题透析 本题以硫化钠为素材,考查化学反应,意在考查综合分析能力,科学探究与创新意识的核心素养.
思路点拨 实验①中,发生反应:、,氯化银转化成硫化银,则溶解度:,A项正确;实验②中,发生反应,产生的气体是,B项正确;根据实验③中现象可知,发生反应:,发生了氧化还原反应,C项错误;实验④中发生反应、,比较实验③、④,说明反应物相同,反应物的量不同,产物不同,D项正确.
14.答案 D
命题透析 本题以一氧化氮与臭氧的反应为情境,考查等效平衡知识,意在考查分析和解决问题的能力,变化观念与平衡思想的核心素养.
思路点拨 容器I中反应时会放热,容器Ⅲ中反应时逆向进行,会吸热,温度降低,平衡时容器I中温度大于容器Ⅲ中温度,所以,A项正确;反应时吸
热比反应时吸热少,平衡时容器Ⅱ中的温度比容器Ⅲ中的高,所以平衡常数,B项正确;容器I中反应时放热,温度升高平衡逆向移动,容器Ⅲ中反应时逆向进行会吸热,温度降低,平衡正向移动,所以容器Ⅲ中的物质的量小,即,C项正确;容器I中温度升高,平衡正向进行的程度小,容器Ⅲ中温度降低,平衡逆向进行的程度小,所以,D项错误.
15.答案(1)C (2)球形 13 (3)5 L
(4)基态的价层电子排布式分别为易再失去1个电子达到半充满稳定结构(合理即可,2分)
(5)
命题透析 本题以前四周期元素为素材,考查元素推断以及原子结构与性质等知识,意在考查分析与推测能力,宏观辨识与微观探析、证据推理与模型认知的核心素养.
思路点拨 基态W原子核外电子排布式为,W为碳元素;Y为氧元素,由Z原子的部分电离能数据可知,最外层只有2个电子,可能为镁元素或钙元素,再结合Q为铝元素可得,Z为镁元素,X为氮元素.基态M原子的价层电子排布式为,M为铁元素.
(2)镁的最外层电子在能级上,该能级的电子云轮廓图为球形.铝原子核外有13个电子,故有13种运动
状态不同的电子.
(3)基态氮原子核外电子排布式为,核外电子占据5个原子轨道.氧原子能量最高的能层为L层.
(4)从洪特规则特例角度分析离子稳定性.
(5)氮化镁与水反应类似盐类水解,生成氢氧化镁和氨气.
16.答案(1)
(2)①抑制氯化铁水解(合理即可,2分)
②
(3)①其他条件相同,能加快分解(合理即可,2分)
②铁离子水解过程吸热,分解放出热量,能促进平衡向右移动(合理即可,2分)
(4) 偏小
命题透析 本题以氯化铁为素材,考查水解平衡和影响速率的因素以及滴定计算,意在考查综合运用能力,变化观念与平衡思想的核心素养.
思路点拨 (1)由(①+②+③)得目标反应,则之积等于K.
(2)①在氯化氢气氛中加热氯化铁晶体,可以抑制氯化铁水解.②b中发生反应的化学方程式为.
(3)①由实验Ⅰ、Ⅱ可得出:其他条件相同,氯化铁催化分解;由实验Ⅱ、Ⅲ可得出,温度促进双氧水分解.②解是放热反应,氯化铁水解过程吸热,分解使温度升高,促进氯化铁水解.
(4)依题意,,根据氯化铁质量分数以及体积转化关系可得:.根据溶度积可知,氯化银易转化成硫氰化银.硝基苯的作用是防止氯化银转化成硫氰化银.如果氯化银部分转化成硫氰化银,消耗溶液体积偏大,测得氯化铁质量分数偏小.
17.答案(1) (2)AD
(3)< 反应Ⅰ是气体分子数增大的反应,反应Ⅱ是气体分子数相等的反应,减小压强,对反应Ⅱ无影响,反应Ⅰ平衡向正反应方向移动,的平衡转化率增大(合理即可,2分)
(4)①甲 ② 4
命题透析 本题以炭粉与氮的氧化物反应为素材,考查盖斯定律、反应速率与平衡知识,意在考查综合运用能力,变化观念与平衡思想的核心素养.
思路点拨 (1)根据盖斯定律,由(Ⅰ+Ⅱ)得目标反应.
(2)有固体参与反应,气体总质量发生了变化,当密度不变时达到平衡状态,A项正确;如果反应不可逆,完全反应时生成,混合气体中的体积分数为,而上述反应是可逆反应,不可能完全转化,故的体积分数小于,B项错误;炭粉是固体,改变固体质量不影响平衡移动,C项错误;通入,相当于原平衡体系加压,的平衡转化率降低,D项正确.
(3)反应Ⅰ是气体分子数增大的反应,反应Ⅱ是气体分子数相等的反应,减小压强,对反应Ⅱ无影响,反应Ⅰ平衡向正反应方向移动,的平衡转化率增大,故.
(4)①反应Ⅱ是反应前后气体分子数相等的可逆反应,在恒温恒容条件下反应,压强保持不变,故乙为恒温恒容条件.绝热恒容条件下,该反应是放热反应,温度升高,气体物质的量不变,压强增大,故甲为绝热恒容
条件.
②
起始/: 2 0 0
转化/: 1.6 0.8 0.8
平衡/: 0.4 0.8 0.8
内用表示的平均反应速率为..
18.答案(1)增大反应物接触面积,加快反应速率(合理即可,2分)
(2)烧杯、漏斗、玻璃棒
(3)取少量最后一次洗涤液于试管中,滴加溶液,若有白色沉淀产生,则固体没有洗净,否则已洗净(合理即可,2分)
(4)冷却(或降温)结晶防止氯化铵扩散到空气中(合理即可,2分)作承接的载体(合理即可,2分)
(5)1.25
(6)
命题透析 本题以合成电极材料为情境,考查化学反应及计算,意在考查综合运用能力,科学态度与社会责任的核心素养.
思路点拨 (1)搅拌的目的是增大反应物接触面积,加快反应速率.
(2)操作1为过滤,需要的玻璃仪器为烧杯、漏斗、玻璃棒.
(4)棉花能阻止氯化铵向空气中扩散.扎有小孔的滤纸的作用是承接氯化铵.
(5)根据溶度积计算:.
(6)氢氧化锡分解生成二氧化锡和水.
化学
考生注意:
1.答题前,考生务必将自己的姓名、考生号填写在试卷和答题卡上,并将芳生号条形码粘贴在答题卡上的指定位置.
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑.如需改动,用橡皮擦干净后,再选涂其他答案标号.回答非选择题时,将答案写在答题卡上.写在本试卷上无效.
3.考试结束后,将本试卷和答题卡一并交回.
可能用到的相对原子质量:H 1 C 12 O 16 Cl 35.5 Fe 56 Cu 64
一、选择题:本题共14小题,每小题3分,共42分.每小题只有一个选项符合题目要求.
1.下列基态原子价层电子排布式对应元素的焰色呈黄色的是( )
A. B. C. D.
2.中国石化石油化工科学研究院最近从地沟油中提炼出航空燃油;我国航天科技集团六院自主成功开发500吨级液氧煤油发动机.下列叙述正确的是( )
A.航空燃油不完全燃烧不会对环境造成污染
B.液氧汽化过程是吸热反应
C.煤油燃烧反应是放热反应
D.航空燃油和煤油都是可再生能源
3.下列基态原子的未成对电子数最多的是( )
A.第二周期ⅦA族 B.第四周期ⅥB族
C.第四周期ⅡB族 D.第三周期ⅤA族
4.书写下列基态原子电子排布式时,最后一个电子进入$能级,但是不属于s区元素的是( )
A.锂 B.铁 C.钙 D.氦
5.主族元素X、Y、Z、R的原子序数依次增大,元素的某种性质递变规律如图所示.下列对应的元素和性质正确的是( )
A.原子半径: B.电负性:
C.第一电离能: D.最高正化合价:
6.下列化学用语错误的是( )
A.能层的能级:
B.基态锗()原子的电子排布式:
C.基态原子的价层电子轨道表示式:
D.p能级的电子云轮廓图:
7.电子科技大学孙威教授首次探索碱性锌-空气电池,工作原理如图所示.
下列叙述正确的是( )
A.放电时,电子由锌极经电解质溶液流向铜极
B.放电时,正极区只发生反应:
C.充电时,阴极上“钝化”生成的不容易反应
D.充电时,产生时转移电子
8.在一定温度和压强下,由指定的单质生成纯物质的热效应为生成热,可以用物质生成热表示物质的相对能量.几种物质的生成热如表所示.
物质
生成热 0 128
已知键能是指气态分子中化学键解离成气态原子所吸收的能量.键能为,假设中键能相等.下列叙述正确的是( )
A.的生成热大于
B.
C.稳定性:
D.上述物质中,键能为
9.设为阿伏加德罗常数的值.下列叙述错误的是( )
A.电解法精炼铜时,阴极质量净增时,转移电子数为
B.时向密闭容器中充入,反应后体系中双原子分子总数为
C.溶液中阳离子总数小于
D.溶液中含粒子总数为
10.下列装置所示的过程与勒夏特列原理无关的是( )
A.加入时产生气泡速率加快 B.加入时乙烧瓶中气体颜色加深
C.光照时试管中黄绿色变浅 D.加入铁粉时溶液颜色变浅
11.电解水制氢称为“绿氢”.我国科学家设计如图所示绿氢制备装置,图a中离子交换膜不允许通过.
下列叙述错误的是( )
A.图a和b装置电解产物完全相同
B.电解一段时间后,图a阳极区浓度不变
C.图a装置采用阴离子交换膜
D.图b阳极反应式为
12.是一种弱酸.常温下,用溶液滴定溶液,测定HCNO溶液的浓度.下列叙述正确的是( )
A.本实验可以选择甲基橙作指示剂
B.本实验需要的玻璃仪器为①②③
C.滴定过程中时,
D.若滴定终点时,则
13.某小组设计实验探究的性质,实验结果如下:
序号 操作及现象
① 向溶液中滴加溶液,产生白色沉淀,静置后,向上层清液中再滴加溶液,产生黑色沉淀
② 向溶液中滴加溶液,产生白色沉淀和臭鸡蛋气味气体
③ 向溶液中滴加溶液,产生乳白色浑浊
④ 向溶液中加入溶液,先产生乳白色浑浊,后产生黑色沉淀.分离黑色沉淀得到少量浅黄色固体和黑色固体;将黑色固体溶于稀硫酸,产生臭鸡蛋味气体和浅绿色溶液
下列推断错误的是( )
A.实验①证明溶解度:
B.实验②可知,产生的气体是
C.实验③中,产生乳白色浑浊发生的是复分解反应
D.实验③和④证明和相对量不同,产物不同
14.向三个体积均为的恒容绝热密闭容器中按不同方式投人反应物,起始温度为时发生反应:,测得达到平衡时的有关数据如下表.下列说法错误的是( )
容器 Ⅰ Ⅱ Ⅲ
反应物的投入量
平衡时正反应速率
平衡常数
平衡时的物质的量
反应物的转化率
A. B. C. D.
二、非选择题:本题共4小题,共58分.
15.(14分)前四周期元素的原子序数依次增大.基态原子核外电子的空间运动状态有4种,基态原子最外层电子数是内层电子数的3倍.元素对应的单质与酸或碱均能反应生成气体,基态核外有5个未成对电子.基态原子的部分电离能数据如下:
元素 电离能
738 1451 7733 10540
回答下列问题:
(1)W的元素符号为______________.
(2)基态原子最外层电子云轮廓图为______________(填名称).1个原子核外有______________种运动状态不同的电子.
(3)基态原子核外电子占据______________个原子轨道.基态原子核外能量最高的能层符号是______________.
(4)不稳定,易转化成的原因是______________(从结构角度分析).
(5)在水中剧烈反应生成一种碱和一种刺激性气味气体,该反应的化学方程式为______________.
16.(14分)是中学常用试剂,在化学实验中有广泛应用,请回答下列问题.
(1)溶于水,发生如下反应:
①
②
③
(用含的式子表示).
(2)利用制备无水氯化铁有如下三种方法.
①上述方法中的作用是______________.
②方法中制备的同时产生两种酸性气体,写出该反应的化学方程式:______________.
(3)为探究催化分解,设计如下实验方案:
实验 双氧水 加入试剂 温度 收集等质量所需时间
Ⅰ 10.0 蒸馏水 25
Ⅱ 10.0 溶液 25
Ⅲ 10.0 溶液 35
实验结果:.
①根据实验Ⅰ、Ⅱ可得出结论:______________.
②研究发现实验Ⅱ和Ⅲ中产生不同程度的红褐色沉淀,用必要的文字和化学用语解释产生红褐色沉淀的原因:______________.
(4)测定样品的纯度.
已知:(无色,稳定),易溶于水且完全电离.常温下,.
实验步骤如下:
步骤1:取样品配成溶液,准确量取溶液于锥形瓶中;
步骤2:向锥形瓶中加入足量溶液,充分反应后,加入溶液(过量)使完全沉淀;
步骤3:向其中加入硝基苯,用力振荡,使沉淀表面被有机物覆盖;
步骤4:加入3滴指示剂,用溶液滴定过量的至终点,消耗溶液.
测得样品中的质量分数为______________(用含和的代数式表示).若取消步骤3,则测定结果______________(填“偏大”“偏小”或“无影响”).
17.(14分)活性炭可用于处理气体,反应如下:
反应Ⅰ:
反应Ⅱ:
回答下列问题:
(1)______________.
(2)在恒温恒容密闭容器中投人足量的活性炭粉和.下列叙述正确的是______________(填字母).
A.容器中混合气体密度保持不变时达到平衡状态
B.达到平衡时,的体积分数等于
C.其他条件不变,增大活性炭粉质量,达到平衡时,的体积百分含量增大
D.平衡后再充入少量的平衡转化率降低
(3)在密闭容器中充入足量活性炭粉和气体,发生反应Ⅰ、Ⅱ.测得的平衡转化率与温度、压强的关系如图1所示.
图1 图2
______________(填“>”“<”或“=”),理由是______________.
(4)一定温度下,在甲、乙两个体积相同的密闭容器中均充入和足量活性炭粉的混合物,分别在恒温恒容、绝热恒容条件下仅发生反应Ⅱ,测得气体压强与时间的关系如图2所示.
①绝热恒容条件下的反应在______________(填“甲”或“乙”)容器中发生.
②点时转化率为,则内用表示的平均反应速率为______________.在该温度下,该反应的平衡常数______________(为用各气体的物质的量分数计算的平衡常数).
18.(16分)某课题组设计合成了负极材料,某简易流程如图所示(部分反应物、产物和条件省略):
已知:常温下,.
请回答下列问题:
(1)操作1前,反应物混合溶液要不断搅拌,其目的是______________.
(2)在实验室中完成操作1需要的玻璃仪器有______________(填名称).
(3)和表面吸附有等,检验固体是否洗净的操作是______________.
(4)操作3包括蒸发浓缩、______________、过滤、洗涤、干燥.利用如图所示装置除去固体中少量杂质,提纯氯化铵.
装置中棉花的作用是______________;
扎有小孔的滤纸的用途是______________.
(5)已知:离子浓度小于或等于时认为离子已沉淀完全.常温下,完全沉淀时溶液最小为______________.
(6)写出时发生反应的化学方程式:______________.
高二化学·答案
1~14题,每小题3分,共42分.
1.答案A
命题透析 本题以焰色试验为素材,考查常见元素焰色、基态原子价层电子排布式等知识,意在考查理解与辨析能力,宏观辨识与微观探析的核心素养.
思路点拨 对应的是钠元素,焰色试验呈黄色,A项符合题意;对应的是钾元素,焰色试验呈紫色(透过蓝色钴玻璃观察),B项不符合题意;对应的是铜元素,焰色试验呈绿色,C项不符合题意;对应的是元素,焰色试验呈砖红色,D项不符合题意.
2.答案 C
命题透析 本题以燃料为素材,考查热化学基本概念,意在考查判断能力,科学态度与社会责任的核心素养.
思路点拨 航空燃油不完全燃烧会产生等污染气体,A项错误;液氧汽化属于物理变化,由液态到气态,是吸热过程,不是吸热反应,B项错误;燃烧反应都是放热反应,C项正确;煤油是化石能源之一,是不可再生能源,D项错误.
3.答案 B
命题透析 本题以未成对电子数的判断为素材,考查核外电子排布、元素周期表结构等知识,意在考查分析与
推测能力,宏观辨识与微观探析的核心素养.
思路点拨 第二周期ⅦA族是F元素,价层电子排布式为有1个未成对电子;第四周期ⅥB族是元素,价层电子排布式为,有6个未成对电子;第四周期ⅡB族是元素,价层电子排布式为,无未成对电子;第三周期ⅤA族是P元素,价层电子排布式为,有3个未成对电子,B项符合题意.
4.答案 D
命题透析 本题以基态原子电子排布式为素材,考查元素分区等知识,意在考查分析与推测能力,证据推理与模型认知的核心素养.
思路点拨 基态锂原子的最后一个电子填充能级,属于s区元素,A项不符合题意;基态铁原子的最后一个电子填充能级,属于d区元素,B项不符合题意;基态钙原子的最后一个电子填充能级,属于s区元素,C项不符合题意;基态氮原子的最后一个电子填充1s能级,属于p区元素,D项符合题意.
5.答案 C
命题透析 本题以主族元素为素材,考查元素性质的递变规律等知识,意在考查分析与推测能力,宏观辨识与微观探析的核心素养.
思路点拨 根据图示,随着原子序数递增,元素性质总体呈增大趋势,但是Y元素出现“反常”.F、、、I的原子半径依次增大,A项不符合题意;O、S、、的电负性依次减小,B项不符合题意;、P、S、的第一电离能呈增大趋势,但P的能级电子排布是半充满的,比较稳定,电离能较高,C项符合题意;氧没有最高正化合价,氟没有正价,D项不符合题意.
6.答案 B
命题透析 本题以化学用语为素材,考查价层电子轨道表示式、电子云轮廓图等知识,意在考查理解与辨析能力,证据推理与模型认知的核心素养.
思路点拨 M能层为第三层,包括三个能级,A项正确;基态锗()原子的电子排布式为或,B项错误;基态As原子的价层电子排布式为,价层电子轨道表示式为,C项正确;p能级有3个相互垂直的电子云,电子云轮廓图为哑铃形,D项正确.
7.答案C
命题透析 本题以碱性锌-空气电池为素材,考查二次电池工作原理,意在考查推理与判断能力,证据推理与模型认知的核心素养.
思路点拨 放电时,电子由负极经外电路流向正极,不经过电解质溶液,A项错误;根据图像,放电时正极还有副产物产生,B项错误;充电时,阴极上氧化锌不容易得电子,C项正确;没有指明温度和压强,无法计算,D项错误.
8.答案D
命题透析 本题以硫的氟化物为素材,考查反应热、键能相关的计算,意在考查计算能力,宏观辨识与微观探析的核心素养.
思路点拨 是放热过程,的生成热小于,A项错误;反应热等于生成物的总能量与反应物的总能量之差,,B项错误;生成热越低,物质具有的能量越低,物质越稳定,故比稳定,C项错误;,反应热等于反应物总键能-生成物总键能,设S—F键能为x,则,解得:,D项正确.
9.答案 C
命题透析 本题以阿伏加德罗常数为素材,考查物质结构、性质和计算,意在考查推理与计算能力,宏观辨识与微观探析的核心素养.
思路点拨 电解法精炼铜中,阴极反应式为,A项正确;,混合气体中三种分子都是双原子分子且反应前后气体分子数相等,B项正确;硫酸亚铁铵溶液中阳离子包括,,阳离子总数增多,C项错误;由物料守恒得,D项正确.
10.答案 A
命题透析 本题以课本实验为情境,考查勤夏特列原理知识,意在考查实验探究的能力,科学探究与创新意识的核心素养.
思路点拨 作催化剂,加入时产生气泡速率加快,与勒夏特列原理无关,A项符合题意;,加入时,乙烧瓶中温度升高,平衡逆向移动,乙烧瓶中气体颜色加深,与勒夏特列原理有关,B项不符合题意;,光照使氯气与水反应的平衡正向移动,与勒夏特列原理有关,C项不符合题意;,,铁粉使铁离子与硫氰酸根离子反应的平衡逆向移动,与勒夏特列原理有关,D项不符合题意.
11.答案 B
命题透析 本题以电解水为情境,考查电解原理,意在考查理解与观察能力,证据推理与模型认知的核心素养.
思路点拨 上述装置实质是电解水,故电解产物都是氧气和氢气,A项正确;在图a阳极区添加了,阳极反应式为,消耗,但阴极区的会迁移至阳极区,故物质的量不变,但生成了水,溶液变稀,浓度下降,B项错误;根据图a知,阴极区的会迁移至阳极区,采用阴离子交换膜,C项正确;图b阳极上水参与反应,阳极反应式为,D项正确.
12.答案 D
命题透析 本题以和反应为素材,考查中和滴定实验,意在考查实验能力,科学探究与创新意识的核心素养.
思路点拨 是弱酸,恰好完全反应生成,溶液呈碱性,应选择酚酞作指示剂,A项错误;中和滴定实验需要锥形瓶,不需要烧杯,B项错误;时,由电荷守恒可得,中性溶液中,则,C项错误;,,D项正确.
13.答案 C
命题透析 本题以硫化钠为素材,考查化学反应,意在考查综合分析能力,科学探究与创新意识的核心素养.
思路点拨 实验①中,发生反应:、,氯化银转化成硫化银,则溶解度:,A项正确;实验②中,发生反应,产生的气体是,B项正确;根据实验③中现象可知,发生反应:,发生了氧化还原反应,C项错误;实验④中发生反应、,比较实验③、④,说明反应物相同,反应物的量不同,产物不同,D项正确.
14.答案 D
命题透析 本题以一氧化氮与臭氧的反应为情境,考查等效平衡知识,意在考查分析和解决问题的能力,变化观念与平衡思想的核心素养.
思路点拨 容器I中反应时会放热,容器Ⅲ中反应时逆向进行,会吸热,温度降低,平衡时容器I中温度大于容器Ⅲ中温度,所以,A项正确;反应时吸
热比反应时吸热少,平衡时容器Ⅱ中的温度比容器Ⅲ中的高,所以平衡常数,B项正确;容器I中反应时放热,温度升高平衡逆向移动,容器Ⅲ中反应时逆向进行会吸热,温度降低,平衡正向移动,所以容器Ⅲ中的物质的量小,即,C项正确;容器I中温度升高,平衡正向进行的程度小,容器Ⅲ中温度降低,平衡逆向进行的程度小,所以,D项错误.
15.答案(1)C (2)球形 13 (3)5 L
(4)基态的价层电子排布式分别为易再失去1个电子达到半充满稳定结构(合理即可,2分)
(5)
命题透析 本题以前四周期元素为素材,考查元素推断以及原子结构与性质等知识,意在考查分析与推测能力,宏观辨识与微观探析、证据推理与模型认知的核心素养.
思路点拨 基态W原子核外电子排布式为,W为碳元素;Y为氧元素,由Z原子的部分电离能数据可知,最外层只有2个电子,可能为镁元素或钙元素,再结合Q为铝元素可得,Z为镁元素,X为氮元素.基态M原子的价层电子排布式为,M为铁元素.
(2)镁的最外层电子在能级上,该能级的电子云轮廓图为球形.铝原子核外有13个电子,故有13种运动
状态不同的电子.
(3)基态氮原子核外电子排布式为,核外电子占据5个原子轨道.氧原子能量最高的能层为L层.
(4)从洪特规则特例角度分析离子稳定性.
(5)氮化镁与水反应类似盐类水解,生成氢氧化镁和氨气.
16.答案(1)
(2)①抑制氯化铁水解(合理即可,2分)
②
(3)①其他条件相同,能加快分解(合理即可,2分)
②铁离子水解过程吸热,分解放出热量,能促进平衡向右移动(合理即可,2分)
(4) 偏小
命题透析 本题以氯化铁为素材,考查水解平衡和影响速率的因素以及滴定计算,意在考查综合运用能力,变化观念与平衡思想的核心素养.
思路点拨 (1)由(①+②+③)得目标反应,则之积等于K.
(2)①在氯化氢气氛中加热氯化铁晶体,可以抑制氯化铁水解.②b中发生反应的化学方程式为.
(3)①由实验Ⅰ、Ⅱ可得出:其他条件相同,氯化铁催化分解;由实验Ⅱ、Ⅲ可得出,温度促进双氧水分解.②解是放热反应,氯化铁水解过程吸热,分解使温度升高,促进氯化铁水解.
(4)依题意,,根据氯化铁质量分数以及体积转化关系可得:.根据溶度积可知,氯化银易转化成硫氰化银.硝基苯的作用是防止氯化银转化成硫氰化银.如果氯化银部分转化成硫氰化银,消耗溶液体积偏大,测得氯化铁质量分数偏小.
17.答案(1) (2)AD
(3)< 反应Ⅰ是气体分子数增大的反应,反应Ⅱ是气体分子数相等的反应,减小压强,对反应Ⅱ无影响,反应Ⅰ平衡向正反应方向移动,的平衡转化率增大(合理即可,2分)
(4)①甲 ② 4
命题透析 本题以炭粉与氮的氧化物反应为素材,考查盖斯定律、反应速率与平衡知识,意在考查综合运用能力,变化观念与平衡思想的核心素养.
思路点拨 (1)根据盖斯定律,由(Ⅰ+Ⅱ)得目标反应.
(2)有固体参与反应,气体总质量发生了变化,当密度不变时达到平衡状态,A项正确;如果反应不可逆,完全反应时生成,混合气体中的体积分数为,而上述反应是可逆反应,不可能完全转化,故的体积分数小于,B项错误;炭粉是固体,改变固体质量不影响平衡移动,C项错误;通入,相当于原平衡体系加压,的平衡转化率降低,D项正确.
(3)反应Ⅰ是气体分子数增大的反应,反应Ⅱ是气体分子数相等的反应,减小压强,对反应Ⅱ无影响,反应Ⅰ平衡向正反应方向移动,的平衡转化率增大,故.
(4)①反应Ⅱ是反应前后气体分子数相等的可逆反应,在恒温恒容条件下反应,压强保持不变,故乙为恒温恒容条件.绝热恒容条件下,该反应是放热反应,温度升高,气体物质的量不变,压强增大,故甲为绝热恒容
条件.
②
起始/: 2 0 0
转化/: 1.6 0.8 0.8
平衡/: 0.4 0.8 0.8
内用表示的平均反应速率为..
18.答案(1)增大反应物接触面积,加快反应速率(合理即可,2分)
(2)烧杯、漏斗、玻璃棒
(3)取少量最后一次洗涤液于试管中,滴加溶液,若有白色沉淀产生,则固体没有洗净,否则已洗净(合理即可,2分)
(4)冷却(或降温)结晶防止氯化铵扩散到空气中(合理即可,2分)作承接的载体(合理即可,2分)
(5)1.25
(6)
命题透析 本题以合成电极材料为情境,考查化学反应及计算,意在考查综合运用能力,科学态度与社会责任的核心素养.
思路点拨 (1)搅拌的目的是增大反应物接触面积,加快反应速率.
(2)操作1为过滤,需要的玻璃仪器为烧杯、漏斗、玻璃棒.
(4)棉花能阻止氯化铵向空气中扩散.扎有小孔的滤纸的作用是承接氯化铵.
(5)根据溶度积计算:.
(6)氢氧化锡分解生成二氧化锡和水.
同课章节目录
