8.1溶液的酸碱性同步练习(含解析) 科粤版化学九年级下册
文档属性
| 名称 | 8.1溶液的酸碱性同步练习(含解析) 科粤版化学九年级下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 854.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-05 00:00:00 | ||
图片预览

文档简介
8.1溶液的酸碱性
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.实验过程中要注意安全,下列实验操作安全的是( )
A.为了快捷可直接把pH试纸放入待测液测溶液的pH
B.点燃氢气前先检验其纯度
C.给试管内液体加热时试管口对着人
D.将鼻孔凑到容器口去闻药品的气味
2.下列对实验现象的分析合理的是( )
A.某无色气体混入空气后点燃爆炸,可证明该气体一定是H2
B.氧化钙放入水中使液体温度升高,可证明氧化钙溶于水吸热
C.某气体在空气中燃烧产生蓝色火焰,可证明该气体一定是一氧化碳
D.煤燃烧产生二氧化硫等有害气体,可证明该物质中一定含有硫元素
3.规范的操作是实验成功的基本保证,下列实验操作正确的是
A.溶解固体 B.测溶液pH
C.添加锌粒 D.连接仪器
4.下列实验操作正确的是( )
A. 熄灭酒精灯 B. 滴加液体
C. 测溶液pH D. 蒸发食盐水
5.下列实验操作正确的是
A.熄灭酒精灯 B.滴加液体
C.检查装置的气密性 D.测定溶液的pH
6.下列图示实验操作中,正确的是( )
A. B.
C. D.
7.下列实验操作错误的是
A.氢气还原氧化铜 B.称量药品 C.测定溶液pH D.检查气密性
8.下表列出了生活中某些饮品在常温下pH范围,下列说法中不正确的是
饮品名称 橙汁 西瓜汁 牛奶 豆浆
pH范围 3.0~4.0 5.3~6.2 6.3~6.6 7.4~7.9
A.橙汁和西瓜汁均显酸性 B.胃酸过多的人应少喝橙汁和西瓜汁
C.西瓜汁没有橙汁的酸性强 D.豆浆和牛奶均是碱性饮品
9.下列有关化学与生活的说法中,正确的是
A.胃酸过多的人应少饮葡萄汁(葡萄汁的pH为3.5-4.5)
B.纯乙醇是均一稳定的液体,纯乙醇是溶液。
C.饮用水要干净,因此长时间喝蒸馏水更有利于人体健康
D.金属、酸、碱和盐等都是重要的化合物
10.下列图像能正确反应其对应操作中各量变化关系的是( )
A.①表示利用二氧化锰分解过氧化氢制氧气
B.②表示向一定量不饱和的硝酸钾溶液中加入硝酸钾固体
C.③表示向pH=1的酸溶液中不断加水
D.④向一定质量的稀盐酸中加入氧化铁
二、判断题
11.蒸馏水润湿pH试纸测定溶液的pH,结果一定偏小( )
12.碱溶液的pH>7,pH>7的溶液不一定是碱溶液( )
13.用pH试纸测定白醋的酸碱度时,先将试纸用蒸馏水润湿,再把白醋滴在试纸上。( )
14.用润湿的pH试纸测定氢氧化钠的pH会使结果偏小( )
15.用pH试纸测定溶液的pH时,应先用蒸馏水将试纸润湿( )
三、综合应用题
16.碱式碳酸铜〔Cu2(OH)2CO3〕是孔雀石的主要成分,主要用于生产油漆、颜料等。兴趣小组探究碱式碳酸铜制备的最佳实验条件。
【查阅资料】碱式碳酸铜是翠绿色、难溶于水的固体,酸性条件下不稳定。
【进行实验】按下表中的数据进行图示实验,记录实验结果。
序号 CuSO4溶液体积/mL Na2CO3溶液体积/mL 水浴温度/℃ 固体颜色
i 50 60 60 蓝绿
ii 50 60 70 翠绿
iii 50 60 80 暗绿
iv 50 70 70 蓝绿
v 50 50 x 蓝绿
【解释与结论】
(1)为了使生成的碱式碳酸铜稳定,实验过程中需保持反应体系的pH 7(填“<”或“>”)。
(2)ii、iv、v的目的是探究制备碱式碳酸铜时CuSO4溶液与Na2CO3溶液最佳配比,x= 。
(3)设计i~iii的目的为 。
(4)由表中数据知,制备碱式碳酸铜的最佳实验条件是 。
【反思与评价】
(5)iii中所得固体颜色偏暗。查阅资料知碱式碳酸铜受热分解会生成CuO,猜想颜色变暗的原因与该反应有关。
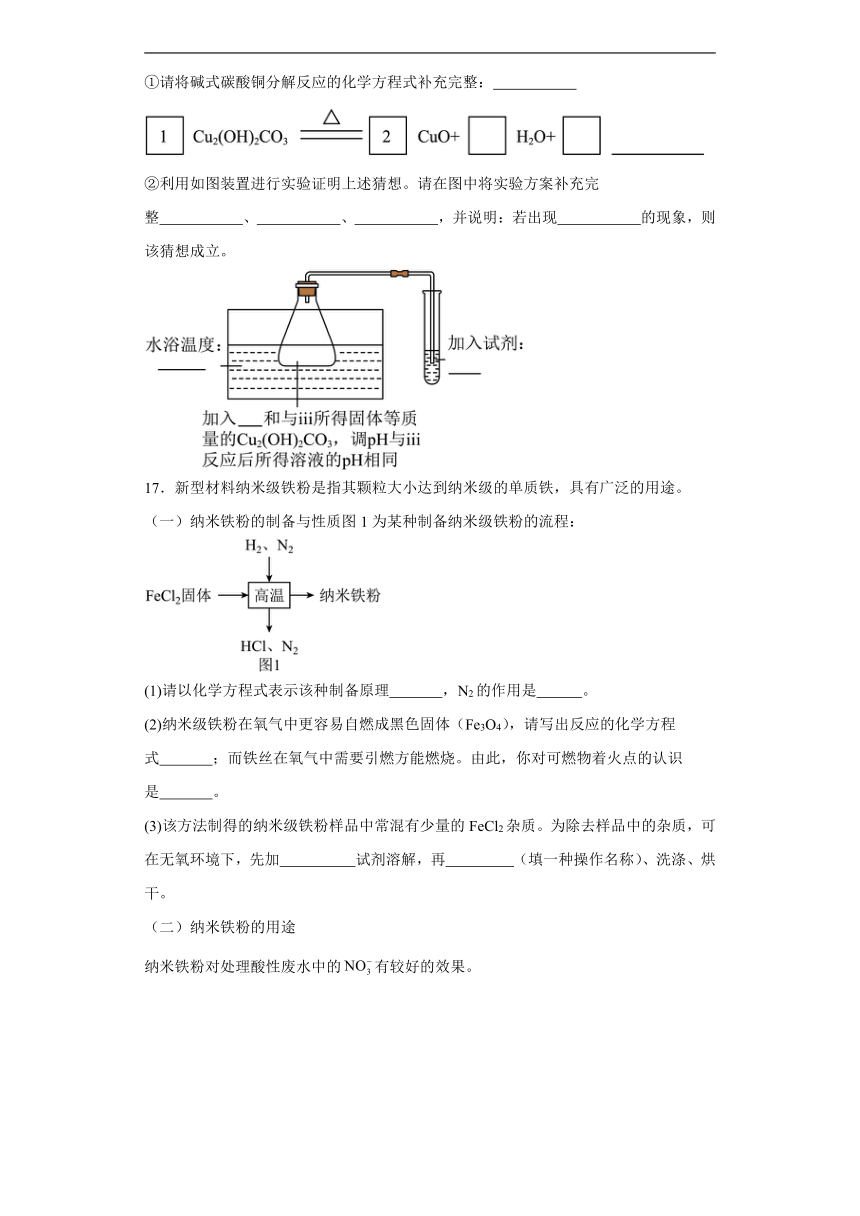
①请将碱式碳酸铜分解反应的化学方程式补充完整:
②利用如图装置进行实验证明上述猜想。请在图中将实验方案补充完整 、 、 ,并说明:若出现 的现象,则该猜想成立。
17.新型材料纳米级铁粉是指其颗粒大小达到纳米级的单质铁,具有广泛的用途。
(一)纳米铁粉的制备与性质图1为某种制备纳米级铁粉的流程:
(1)请以化学方程式表示该种制备原理 ,N2的作用是 。
(2)纳米级铁粉在氧气中更容易自燃成黑色固体(Fe3O4),请写出反应的化学方程式 ;而铁丝在氧气中需要引燃方能燃烧。由此,你对可燃物着火点的认识是 。
(3)该方法制得的纳米级铁粉样品中常混有少量的FeCl2杂质。为除去样品中的杂质,可在无氧环境下,先加 试剂溶解,再 (填一种操作名称)、洗涤、烘干。
(二)纳米铁粉的用途
纳米铁粉对处理酸性废水中的有较好的效果。
(4)废水中的在含纳米铁粉的水处理剂表面的变化如图2,上述变化过程中,化合价降低的元素是 。
(5)研究发现:
①纳米铁粉较普通铁粉去除的速率快得多,其原因是 。
②已知当溶液的pH为7.6时,Fe2+开始沉淀。纳米铁粉在酸性条件下对的去除效果要好于中性和碱性条件,其原因是 。
③废水中溶解氧会对的去除产生一定影响。在其它条件相同情况下,有氧与无氧条件下的去除率随反应时间的变化如图3所示。1~3h时,有氧条件下去除率低于无氧条件下,其可能原因是 。
参考答案:
1.B
【详解】A、用pH试纸测定溶液的酸碱度时,不能将pH试纸放入待测液中蘸取,污染试剂,实验操作不安全,不符合题意;
B、氢气具有可燃性,为防止氢气与空气混合点燃时可能发生爆炸,点燃氢气前先检验其纯度,实验操作安全,符合题意;
C、给试管内液体加热时试管口不能对着人,否则液体沸腾时喷出会伤人,实验操作不安全,不符合题意;
D、闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,实验操作不安全,不符合题意。故选B 。
2.D
【详解】A、可燃性气体与空气混合遇明火可能会发生爆炸,某无色气体混入空气后点燃爆炸,不能证明该气体一定是H2,也可能是一氧化碳等气体,故选项说法错误。
B、氧化钙放入水中使液体温度升高,不能证明氧化钙溶于水吸热,氧化钙能与水反应生成氢氧化钙,该反应放出热量,故选项说法错误。
C、某气体在空气中燃烧产生蓝色火焰,不能证明该气体一定是一氧化碳,也可能是甲烷等,故选项说法错误。
D、煤燃烧产生二氧化硫等有害气体,二氧化硫中含有硫、氧两种元素,根据质量守恒定律,反应前后,元素种类不变,反应物氧气中只含有氧元素,则煤中一定含有硫元素,故选项说法正确。
故选:D。
3.D
【详解】A、量筒不能溶解固体,不符合题意;
B、pH试纸不能直接浸入待测液,不符合题意;
C、固液反应一般先添加固体,再加入液体,不符合题意;
D、连接玻璃管和胶皮管用水润湿能起到润滑作用,使两部分更容易连接,符合题意。
故选D。
4.A
【详解】A、使用酒精灯时要注意“两查、两禁、一不可”,熄灭酒精灯时,不能用嘴吹灭酒精灯,应用灯帽盖灭,图中所示操作正确。
B、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误。
C、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能将pH试纸伸入待测液中,以免污染待测液,图中所示操作错误。
D、蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,图中所示操作错误。
故选A。
5.C
【详解】A、熄灭酒精灯应用灯帽盖灭,不能用嘴吹灭,图示操作错误;
B、用胶头滴管滴加少量液体时,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图示操作错误;
C、检查装置气密性的操作是把导管放入装有水的烧杯,用手握住试管,若导管口有气泡冒出,则装置气密性良好,图示操作正确;
D、用pH试纸测定溶液的pH时,正确的操作方法为在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH。不能将pH试纸伸入待测液中,以免污染待测液,图示操作错误;
故选C。
6.C
【详解】A、闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,图中所示操作错误。
B、使用酒精灯时要注意“两查、两禁、一不可”,禁止用一酒精灯去引燃另一酒精灯,图中所示操作错误。
C、用pH试纸测定未知溶液的pH时,正确的操作方法为取一片pH试纸放在玻璃片或白瓷板上,用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,图中所示操作正确。
D、正在加热的蒸发皿温度较高,为防止烫伤手,不能用手直接拿热的蒸发皿,应用坩埚钳夹取,图中所示操作错误。
故选C。
7.B
【详解】A、氢气还原氧化铜时,导管应伸入试管的底部,图中所示装置正确;B、托盘天平的使用要遵循“左物右码”的原则,且氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,图中所示操作错误;C、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,图中所示装置正确;D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确。故选B。
8.D
【详解】A、pH<7的溶解显酸性,故橙汁和西瓜汁均显酸性,故A正确;
B、橙汁和西瓜汁显酸性,所以胃酸过多的人应少喝橙汁和西瓜汁,故B正确;
C、西瓜汁的pH大于橙汁的pH,pH越大,酸性越弱,故C正确;
D、豆浆的pH>7是碱性饮品,牛奶的pH<7显酸性,故D错误。
故选D。
9.A
【详解】A、葡萄汁的pH为3.5-4.5,小于7呈酸性,所以胃酸过多的人应少饮葡萄汁,故A选项正确;
B、溶液是均一、稳定的混合物,纯乙醇均一稳定,但不是混合物,所以纯乙醇不是溶液,故B选项错误;
C、蒸馏水是纯水,不含人体所需的其它矿物质,因此常时间喝蒸馏水不利于人体健康,故C选项错误;
D、酸、碱、盐是重要的化合物,金属是不是化合物,是单质,故D选项错误。
故选A。
10.C
【详解】A.由于二氧化锰是催化剂,在反应前后二氧化锰的质量不变,故A错误;
B.一定温度时,向一定量不饱和的硝酸钾溶液中不断加入硝酸钾固体,溶质质量逐渐增大,至达到饱和状态,溶质质量不再发生改变,故B错误;
C.稀释酸性溶液时,溶液的pH值逐渐增大,但是酸性溶液无论如何稀释都是酸性溶液,溶液的pH都不会等于7,更不会大于7,故C正确;
D.氧化铁和盐酸反应生成氯化铁和水,溶液的质量不断增大,直至盐酸反应溶液质量不再增大,故D错误。
故选:C。
11.错误
【详解】蒸馏水润湿pH试纸测定溶液的pH,如果溶液显酸性,溶液被稀释,酸性减弱,pH偏大,如果溶液显中性,pH不变,如果溶液显碱性,碱性减弱,pH偏小,错误。
12.正确
【详解】pH>7的溶液可以是碱溶液,还可以是某些显碱性的盐溶液,比如碳酸钠溶液。
故题干说法正确。
13.错误
【详解】用pH试纸测定白醋的酸碱度时,先将试纸用蒸馏水润湿,实际上是对白醋进行稀释,则溶液的酸性会减弱,对于酸性溶液来说酸性越弱pH数值越大,故实际的白醋pH会偏大,故错误。
14.正确
【详解】用湿润的pH试纸测顶氢氧化钠的pH,相当于对氢氧化钠溶液进行稀释后再测定,稀释后的氢氧化钠溶液碱性减小,所以测定的pH偏小,故说法正确
故答案为正确
15.错误
【详解】用pH试纸测定溶液的pH时,先用蒸馏水将试纸润湿,会稀释溶液,如果溶液显酸性或碱性,会影响实验结果,错误。
16.(1)>
(2)70
(3)探究碱式碳酸铜制备的最佳水浴温度
(4)CuSO4溶液与Na2CO3溶液最佳体积比为5:6,水浴温度为70℃
(5) 1 Cu2(OH)2CO3 2CuO +1 H2O+ 1CO2↑ 80℃ 澄清石灰水 110 mL水 固体颜色变暗,澄清石灰水变浑浊
【详解】(1)由题文可知,碱式碳酸铜在酸性条件下不稳定,所以为了使生成的碱式碳酸铜稳定,实验过程中需保持反应体系的pH>7,保障反应体系不呈酸性,故填>。
(2)由控制变量法可知,变量只有一个,ii、iv、v的目的是探究制备碱式碳酸铜时CuSO4溶液与Na2CO3溶液最佳配比,其中的变量是Na2CO3溶液体积,则水浴温度应该相同,即x为70,故填70。
(3)由题文可知,实验i~iii的变量是水浴的温度,其它的量相同,则实验目的为探究碱式碳酸铜制备的最佳水浴温度,故填探究碱式碳酸铜制备的最佳水浴温度。
(4)碱式碳酸铜是翠绿色、难溶于水的固体,由图可知,生成碱式碳酸铜的最佳条件是实验ii,即CuSO4溶液与Na2CO3溶液最佳体积比为5:6,水浴温度为70℃,故填CuSO4溶液与Na2CO3溶液最佳体积比为5:6,水浴温度为70℃。
(5)①由质量守恒定律可知,碱式碳酸铜在加热的条件下反应生成氧化铜、二氧化碳和水,故反应的完整的化学方程式写为:1 Cu2(OH)2CO3 2CuO +1 H2O+ 1CO2↑。
②由题文可知,实验iii是水浴的温度为80℃,所以该实验中水浴的温度也应为80℃,故填80℃;
碱式碳酸铜受热分解会生成CuO,同时生成二氧化碳,检验二氧化碳的生成应选择澄清石灰水,故填澄清石灰水;
实验iii中的反应体系中含有50mLCuSO4溶液和60mLNa2CO3溶液,所以该实验的反应体系也应该含有110mL液体,可以加入110mL水,故填110 mL水;
碱式碳酸铜受热分解会生成CuO,猜想颜色变暗的原因与该反应有关,如果固体颜色真的与该变化有关,即猜想成立,则出现的现象是固体颜色变暗,澄清石灰水变浑浊,故填固体颜色变暗,澄清石灰水变浑浊。
17.(1) FeCl2+H2Fe+2HCl 保护气,防止铁粉被氧化
(2) 3Fe+2O2Fe3O4 可燃物着火点与物质间的接触面积大小有关
(3) 水 过滤
(4)氮元素
(5) 增大了接触面积 沉淀附着在铁粉表面阻止反应进行 纳米铁粉优先和水中溶解的氧发生反应,导致硝酸根的去除率降低
【详解】(1)由图可知,氯化亚铁和氢气在高温条件下生成纳米铁粉和氯化氢,化学方程式FeCl2+H2Fe+2HCl,氮气化学性质稳定作用是保护气,防止铁粉被氧化,故填:FeCl2+H2Fe+2HCl;保护气,防止铁粉被氧化。
(2)铁粉燃烧生成四氧化三铁,化学方程式3Fe+2O2Fe3O4,铁丝在氧气中需要引燃方能燃烧。纳米铁粉可以自燃,纳米铁粉与氧气的接触面积增大,故可知可燃物着火点与物质间的接触面积大小有关,故填:3Fe+2O2Fe3O4;可燃物着火点与物质间的接触面积大小有关。
(3)氯化亚铁溶于水,铁粉不溶,除去样品中的杂质氯化亚铁,可在无氧环境下,先加水溶解,再过滤,洗涤、烘干,故填:水;过滤。
(4)硝酸根中氮元素+5价,铵根中氮元素-3价,上述变化过程中,化合价降低的元素是氮元素,故填:氮元素。
(5)①纳米铁粉较普通铁粉去除的速率快得多,其原因是颗粒小,增大了接触面积,故填:增大了接触面积。
②pH为7.6时,Fe2+开始沉淀。纳米铁粉在酸性条件下对的去除效果要好于中性和碱性条件,其原因是碱性条件下,亚铁离子生成沉淀,沉淀附着在铁粉表面阻止反应进行,故填:沉淀附着在铁粉表面阻止反应进行。
③1~3h时,有氧条件下去除率低于无氧条件下,其可能原因是纳米铁粉优先和水中溶解的氧发生反应,导致硝酸根的去除率降低,故填:纳米铁粉优先和水中溶解的氧发生反应,导致硝酸根的去除率降低。
学校:___________姓名:___________班级:___________考号:___________
一、选择题
1.实验过程中要注意安全,下列实验操作安全的是( )
A.为了快捷可直接把pH试纸放入待测液测溶液的pH
B.点燃氢气前先检验其纯度
C.给试管内液体加热时试管口对着人
D.将鼻孔凑到容器口去闻药品的气味
2.下列对实验现象的分析合理的是( )
A.某无色气体混入空气后点燃爆炸,可证明该气体一定是H2
B.氧化钙放入水中使液体温度升高,可证明氧化钙溶于水吸热
C.某气体在空气中燃烧产生蓝色火焰,可证明该气体一定是一氧化碳
D.煤燃烧产生二氧化硫等有害气体,可证明该物质中一定含有硫元素
3.规范的操作是实验成功的基本保证,下列实验操作正确的是
A.溶解固体 B.测溶液pH
C.添加锌粒 D.连接仪器
4.下列实验操作正确的是( )
A. 熄灭酒精灯 B. 滴加液体
C. 测溶液pH D. 蒸发食盐水
5.下列实验操作正确的是
A.熄灭酒精灯 B.滴加液体
C.检查装置的气密性 D.测定溶液的pH
6.下列图示实验操作中,正确的是( )
A. B.
C. D.
7.下列实验操作错误的是
A.氢气还原氧化铜 B.称量药品 C.测定溶液pH D.检查气密性
8.下表列出了生活中某些饮品在常温下pH范围,下列说法中不正确的是
饮品名称 橙汁 西瓜汁 牛奶 豆浆
pH范围 3.0~4.0 5.3~6.2 6.3~6.6 7.4~7.9
A.橙汁和西瓜汁均显酸性 B.胃酸过多的人应少喝橙汁和西瓜汁
C.西瓜汁没有橙汁的酸性强 D.豆浆和牛奶均是碱性饮品
9.下列有关化学与生活的说法中,正确的是
A.胃酸过多的人应少饮葡萄汁(葡萄汁的pH为3.5-4.5)
B.纯乙醇是均一稳定的液体,纯乙醇是溶液。
C.饮用水要干净,因此长时间喝蒸馏水更有利于人体健康
D.金属、酸、碱和盐等都是重要的化合物
10.下列图像能正确反应其对应操作中各量变化关系的是( )
A.①表示利用二氧化锰分解过氧化氢制氧气
B.②表示向一定量不饱和的硝酸钾溶液中加入硝酸钾固体
C.③表示向pH=1的酸溶液中不断加水
D.④向一定质量的稀盐酸中加入氧化铁
二、判断题
11.蒸馏水润湿pH试纸测定溶液的pH,结果一定偏小( )
12.碱溶液的pH>7,pH>7的溶液不一定是碱溶液( )
13.用pH试纸测定白醋的酸碱度时,先将试纸用蒸馏水润湿,再把白醋滴在试纸上。( )
14.用润湿的pH试纸测定氢氧化钠的pH会使结果偏小( )
15.用pH试纸测定溶液的pH时,应先用蒸馏水将试纸润湿( )
三、综合应用题
16.碱式碳酸铜〔Cu2(OH)2CO3〕是孔雀石的主要成分,主要用于生产油漆、颜料等。兴趣小组探究碱式碳酸铜制备的最佳实验条件。
【查阅资料】碱式碳酸铜是翠绿色、难溶于水的固体,酸性条件下不稳定。
【进行实验】按下表中的数据进行图示实验,记录实验结果。
序号 CuSO4溶液体积/mL Na2CO3溶液体积/mL 水浴温度/℃ 固体颜色
i 50 60 60 蓝绿
ii 50 60 70 翠绿
iii 50 60 80 暗绿
iv 50 70 70 蓝绿
v 50 50 x 蓝绿
【解释与结论】
(1)为了使生成的碱式碳酸铜稳定,实验过程中需保持反应体系的pH 7(填“<”或“>”)。
(2)ii、iv、v的目的是探究制备碱式碳酸铜时CuSO4溶液与Na2CO3溶液最佳配比,x= 。
(3)设计i~iii的目的为 。
(4)由表中数据知,制备碱式碳酸铜的最佳实验条件是 。
【反思与评价】
(5)iii中所得固体颜色偏暗。查阅资料知碱式碳酸铜受热分解会生成CuO,猜想颜色变暗的原因与该反应有关。
①请将碱式碳酸铜分解反应的化学方程式补充完整:
②利用如图装置进行实验证明上述猜想。请在图中将实验方案补充完整 、 、 ,并说明:若出现 的现象,则该猜想成立。
17.新型材料纳米级铁粉是指其颗粒大小达到纳米级的单质铁,具有广泛的用途。
(一)纳米铁粉的制备与性质图1为某种制备纳米级铁粉的流程:
(1)请以化学方程式表示该种制备原理 ,N2的作用是 。
(2)纳米级铁粉在氧气中更容易自燃成黑色固体(Fe3O4),请写出反应的化学方程式 ;而铁丝在氧气中需要引燃方能燃烧。由此,你对可燃物着火点的认识是 。
(3)该方法制得的纳米级铁粉样品中常混有少量的FeCl2杂质。为除去样品中的杂质,可在无氧环境下,先加 试剂溶解,再 (填一种操作名称)、洗涤、烘干。
(二)纳米铁粉的用途
纳米铁粉对处理酸性废水中的有较好的效果。
(4)废水中的在含纳米铁粉的水处理剂表面的变化如图2,上述变化过程中,化合价降低的元素是 。
(5)研究发现:
①纳米铁粉较普通铁粉去除的速率快得多,其原因是 。
②已知当溶液的pH为7.6时,Fe2+开始沉淀。纳米铁粉在酸性条件下对的去除效果要好于中性和碱性条件,其原因是 。
③废水中溶解氧会对的去除产生一定影响。在其它条件相同情况下,有氧与无氧条件下的去除率随反应时间的变化如图3所示。1~3h时,有氧条件下去除率低于无氧条件下,其可能原因是 。
参考答案:
1.B
【详解】A、用pH试纸测定溶液的酸碱度时,不能将pH试纸放入待测液中蘸取,污染试剂,实验操作不安全,不符合题意;
B、氢气具有可燃性,为防止氢气与空气混合点燃时可能发生爆炸,点燃氢气前先检验其纯度,实验操作安全,符合题意;
C、给试管内液体加热时试管口不能对着人,否则液体沸腾时喷出会伤人,实验操作不安全,不符合题意;
D、闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,实验操作不安全,不符合题意。故选B 。
2.D
【详解】A、可燃性气体与空气混合遇明火可能会发生爆炸,某无色气体混入空气后点燃爆炸,不能证明该气体一定是H2,也可能是一氧化碳等气体,故选项说法错误。
B、氧化钙放入水中使液体温度升高,不能证明氧化钙溶于水吸热,氧化钙能与水反应生成氢氧化钙,该反应放出热量,故选项说法错误。
C、某气体在空气中燃烧产生蓝色火焰,不能证明该气体一定是一氧化碳,也可能是甲烷等,故选项说法错误。
D、煤燃烧产生二氧化硫等有害气体,二氧化硫中含有硫、氧两种元素,根据质量守恒定律,反应前后,元素种类不变,反应物氧气中只含有氧元素,则煤中一定含有硫元素,故选项说法正确。
故选:D。
3.D
【详解】A、量筒不能溶解固体,不符合题意;
B、pH试纸不能直接浸入待测液,不符合题意;
C、固液反应一般先添加固体,再加入液体,不符合题意;
D、连接玻璃管和胶皮管用水润湿能起到润滑作用,使两部分更容易连接,符合题意。
故选D。
4.A
【详解】A、使用酒精灯时要注意“两查、两禁、一不可”,熄灭酒精灯时,不能用嘴吹灭酒精灯,应用灯帽盖灭,图中所示操作正确。
B、使用胶头滴管滴加少量液体的操作,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图中所示操作错误。
C、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH.不能将pH试纸伸入待测液中,以免污染待测液,图中所示操作错误。
D、蒸发时,应用玻璃棒不断搅拌,以防止局部温度过高,造成液体飞溅,图中所示操作错误。
故选A。
5.C
【详解】A、熄灭酒精灯应用灯帽盖灭,不能用嘴吹灭,图示操作错误;
B、用胶头滴管滴加少量液体时,注意胶头滴管不能伸入到试管内或接触试管内壁,应垂直悬空在试管口上方滴加液体,防止污染胶头滴管,图示操作错误;
C、检查装置气密性的操作是把导管放入装有水的烧杯,用手握住试管,若导管口有气泡冒出,则装置气密性良好,图示操作正确;
D、用pH试纸测定溶液的pH时,正确的操作方法为在白瓷板或玻璃片上放一小片pH试纸,用玻璃棒蘸取待测液滴到pH试纸上,把试纸显示的颜色与标准比色卡比较,读出pH。不能将pH试纸伸入待测液中,以免污染待测液,图示操作错误;
故选C。
6.C
【详解】A、闻气体的气味时,应用手在瓶口轻轻的扇动,使极少量的气体飘进鼻子中,不能将鼻子凑到集气瓶口去闻气体的气味,图中所示操作错误。
B、使用酒精灯时要注意“两查、两禁、一不可”,禁止用一酒精灯去引燃另一酒精灯,图中所示操作错误。
C、用pH试纸测定未知溶液的pH时,正确的操作方法为取一片pH试纸放在玻璃片或白瓷板上,用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,图中所示操作正确。
D、正在加热的蒸发皿温度较高,为防止烫伤手,不能用手直接拿热的蒸发皿,应用坩埚钳夹取,图中所示操作错误。
故选C。
7.B
【详解】A、氢气还原氧化铜时,导管应伸入试管的底部,图中所示装置正确;B、托盘天平的使用要遵循“左物右码”的原则,且氢氧化钠具有腐蚀性,应放在玻璃器皿中称量,图中所示操作错误;C、用pH试纸测定未知溶液的pH时,正确的操作方法为用玻璃棒蘸取少量待测液滴在干燥的pH试纸上,与标准比色卡对比来确定pH,图中所示装置正确;D、检查装置气密性的方法:把导管的一端浸没在水里,双手紧贴容器外壁,若导管口有气泡冒出,装置不漏气;图中所示操作正确。故选B。
8.D
【详解】A、pH<7的溶解显酸性,故橙汁和西瓜汁均显酸性,故A正确;
B、橙汁和西瓜汁显酸性,所以胃酸过多的人应少喝橙汁和西瓜汁,故B正确;
C、西瓜汁的pH大于橙汁的pH,pH越大,酸性越弱,故C正确;
D、豆浆的pH>7是碱性饮品,牛奶的pH<7显酸性,故D错误。
故选D。
9.A
【详解】A、葡萄汁的pH为3.5-4.5,小于7呈酸性,所以胃酸过多的人应少饮葡萄汁,故A选项正确;
B、溶液是均一、稳定的混合物,纯乙醇均一稳定,但不是混合物,所以纯乙醇不是溶液,故B选项错误;
C、蒸馏水是纯水,不含人体所需的其它矿物质,因此常时间喝蒸馏水不利于人体健康,故C选项错误;
D、酸、碱、盐是重要的化合物,金属是不是化合物,是单质,故D选项错误。
故选A。
10.C
【详解】A.由于二氧化锰是催化剂,在反应前后二氧化锰的质量不变,故A错误;
B.一定温度时,向一定量不饱和的硝酸钾溶液中不断加入硝酸钾固体,溶质质量逐渐增大,至达到饱和状态,溶质质量不再发生改变,故B错误;
C.稀释酸性溶液时,溶液的pH值逐渐增大,但是酸性溶液无论如何稀释都是酸性溶液,溶液的pH都不会等于7,更不会大于7,故C正确;
D.氧化铁和盐酸反应生成氯化铁和水,溶液的质量不断增大,直至盐酸反应溶液质量不再增大,故D错误。
故选:C。
11.错误
【详解】蒸馏水润湿pH试纸测定溶液的pH,如果溶液显酸性,溶液被稀释,酸性减弱,pH偏大,如果溶液显中性,pH不变,如果溶液显碱性,碱性减弱,pH偏小,错误。
12.正确
【详解】pH>7的溶液可以是碱溶液,还可以是某些显碱性的盐溶液,比如碳酸钠溶液。
故题干说法正确。
13.错误
【详解】用pH试纸测定白醋的酸碱度时,先将试纸用蒸馏水润湿,实际上是对白醋进行稀释,则溶液的酸性会减弱,对于酸性溶液来说酸性越弱pH数值越大,故实际的白醋pH会偏大,故错误。
14.正确
【详解】用湿润的pH试纸测顶氢氧化钠的pH,相当于对氢氧化钠溶液进行稀释后再测定,稀释后的氢氧化钠溶液碱性减小,所以测定的pH偏小,故说法正确
故答案为正确
15.错误
【详解】用pH试纸测定溶液的pH时,先用蒸馏水将试纸润湿,会稀释溶液,如果溶液显酸性或碱性,会影响实验结果,错误。
16.(1)>
(2)70
(3)探究碱式碳酸铜制备的最佳水浴温度
(4)CuSO4溶液与Na2CO3溶液最佳体积比为5:6,水浴温度为70℃
(5) 1 Cu2(OH)2CO3 2CuO +1 H2O+ 1CO2↑ 80℃ 澄清石灰水 110 mL水 固体颜色变暗,澄清石灰水变浑浊
【详解】(1)由题文可知,碱式碳酸铜在酸性条件下不稳定,所以为了使生成的碱式碳酸铜稳定,实验过程中需保持反应体系的pH>7,保障反应体系不呈酸性,故填>。
(2)由控制变量法可知,变量只有一个,ii、iv、v的目的是探究制备碱式碳酸铜时CuSO4溶液与Na2CO3溶液最佳配比,其中的变量是Na2CO3溶液体积,则水浴温度应该相同,即x为70,故填70。
(3)由题文可知,实验i~iii的变量是水浴的温度,其它的量相同,则实验目的为探究碱式碳酸铜制备的最佳水浴温度,故填探究碱式碳酸铜制备的最佳水浴温度。
(4)碱式碳酸铜是翠绿色、难溶于水的固体,由图可知,生成碱式碳酸铜的最佳条件是实验ii,即CuSO4溶液与Na2CO3溶液最佳体积比为5:6,水浴温度为70℃,故填CuSO4溶液与Na2CO3溶液最佳体积比为5:6,水浴温度为70℃。
(5)①由质量守恒定律可知,碱式碳酸铜在加热的条件下反应生成氧化铜、二氧化碳和水,故反应的完整的化学方程式写为:1 Cu2(OH)2CO3 2CuO +1 H2O+ 1CO2↑。
②由题文可知,实验iii是水浴的温度为80℃,所以该实验中水浴的温度也应为80℃,故填80℃;
碱式碳酸铜受热分解会生成CuO,同时生成二氧化碳,检验二氧化碳的生成应选择澄清石灰水,故填澄清石灰水;
实验iii中的反应体系中含有50mLCuSO4溶液和60mLNa2CO3溶液,所以该实验的反应体系也应该含有110mL液体,可以加入110mL水,故填110 mL水;
碱式碳酸铜受热分解会生成CuO,猜想颜色变暗的原因与该反应有关,如果固体颜色真的与该变化有关,即猜想成立,则出现的现象是固体颜色变暗,澄清石灰水变浑浊,故填固体颜色变暗,澄清石灰水变浑浊。
17.(1) FeCl2+H2Fe+2HCl 保护气,防止铁粉被氧化
(2) 3Fe+2O2Fe3O4 可燃物着火点与物质间的接触面积大小有关
(3) 水 过滤
(4)氮元素
(5) 增大了接触面积 沉淀附着在铁粉表面阻止反应进行 纳米铁粉优先和水中溶解的氧发生反应,导致硝酸根的去除率降低
【详解】(1)由图可知,氯化亚铁和氢气在高温条件下生成纳米铁粉和氯化氢,化学方程式FeCl2+H2Fe+2HCl,氮气化学性质稳定作用是保护气,防止铁粉被氧化,故填:FeCl2+H2Fe+2HCl;保护气,防止铁粉被氧化。
(2)铁粉燃烧生成四氧化三铁,化学方程式3Fe+2O2Fe3O4,铁丝在氧气中需要引燃方能燃烧。纳米铁粉可以自燃,纳米铁粉与氧气的接触面积增大,故可知可燃物着火点与物质间的接触面积大小有关,故填:3Fe+2O2Fe3O4;可燃物着火点与物质间的接触面积大小有关。
(3)氯化亚铁溶于水,铁粉不溶,除去样品中的杂质氯化亚铁,可在无氧环境下,先加水溶解,再过滤,洗涤、烘干,故填:水;过滤。
(4)硝酸根中氮元素+5价,铵根中氮元素-3价,上述变化过程中,化合价降低的元素是氮元素,故填:氮元素。
(5)①纳米铁粉较普通铁粉去除的速率快得多,其原因是颗粒小,增大了接触面积,故填:增大了接触面积。
②pH为7.6时,Fe2+开始沉淀。纳米铁粉在酸性条件下对的去除效果要好于中性和碱性条件,其原因是碱性条件下,亚铁离子生成沉淀,沉淀附着在铁粉表面阻止反应进行,故填:沉淀附着在铁粉表面阻止反应进行。
③1~3h时,有氧条件下去除率低于无氧条件下,其可能原因是纳米铁粉优先和水中溶解的氧发生反应,导致硝酸根的去除率降低,故填:纳米铁粉优先和水中溶解的氧发生反应,导致硝酸根的去除率降低。
