化学人教版(2019)选择性必修3 3.4羧酸 羧酸衍生物(共29张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修3 3.4羧酸 羧酸衍生物(共29张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 51.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-12 00:00:00 | ||
图片预览







文档简介
(共29张PPT)
走进奇妙的化学世界
选择性必修3
第三章 烃的衍生物
第四节 羧酸
羧酸衍生物--酯
目录
1.概念
2.结构
3.命名
4.物理性质
5.化学性质
6.用途
自制“青苹果汁”
是什么让这杯“饮品”味道这么香?
经检测,苹果香精香气成分主要成分就是酯类,如丁酸乙酯、乙酸丁酯、乙酸异戊酯、2-甲基丁酸乙酯等
生活中的酯
乙酸异戊酯
丁酸乙酯
γ-癸酸内酯
硬脂酸甘油酯
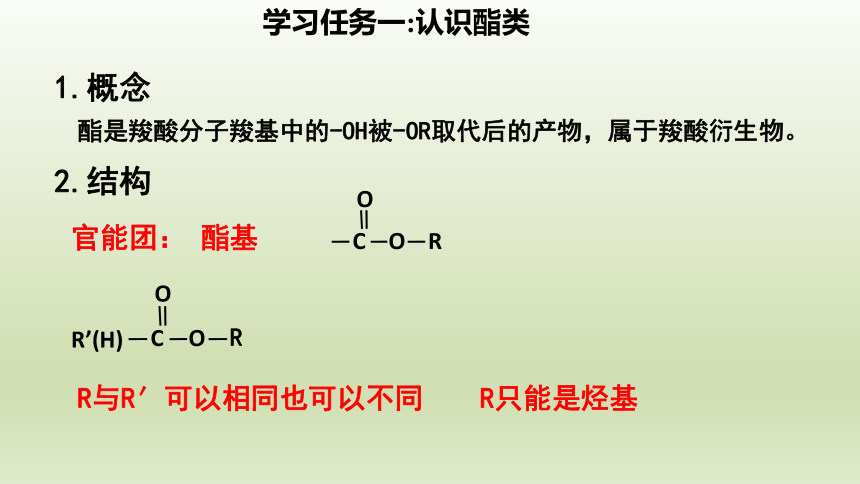
1.概念
酯是羧酸分子羧基中的-OH被-OR取代后的产物,属于羧酸衍生物。
2.结构
R与R′可以相同也可以不同 R只能是烃基
R’(H)
C
O
R
O
学习任务一:认识酯类
官能团: 酯基
C
O
R
O
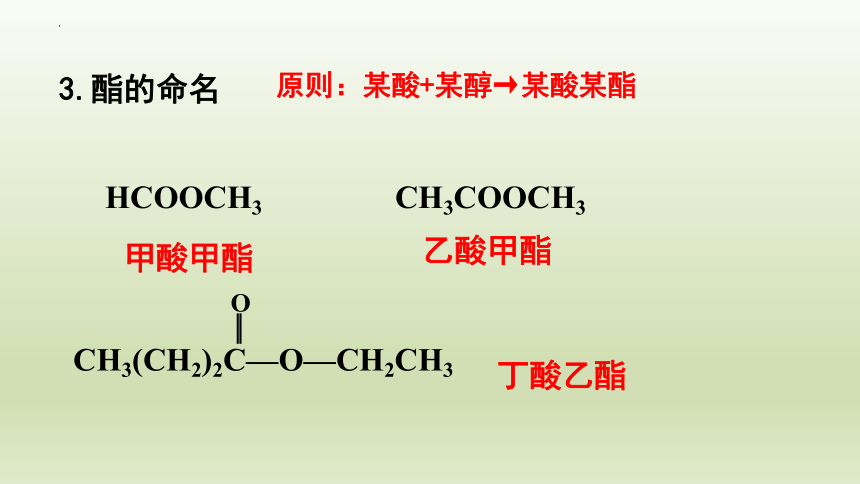
HCOOCH3
CH3COOCH3
甲酸甲酯
乙酸甲酯
3.酯的命名
原则:某酸+某醇→某酸某酯
CH3(CH2)2C—O—CH2CH3
O
丁酸乙酯
③难溶于水,易溶于乙醇和乙醚 等有机溶剂
②密度比水小
①低级酯是具有芳香气味的液体。
4.物理性质
学习任务二:探究酯的物理性质
5.酯的化学性质
CH3COOC2H5 +H2O
浓硫酸
△
CH3COOH + C2H5OH
根据该反应的特点,预测乙酸乙酯可能发生的化学反应。
CH3COOC2H5 +H2O
△
CH3COOH + C2H5OH
在酸或碱存在条件下,酯能发生水解反应生成相应的羧酸和醇,酯的水解反应是酯化反应的逆反应。
水解反应
5.酯的化学性质
稀硫酸
△
CH3C—O—C2H5+H2O CH3COOH+C2H5OH
=
O
酯的水解反应也是取代反应
稀硫酸
△
CH3C—O—C2H5+H2O CH3COOH+C2H5OH
=
O
学习任务三:探究酯的水解
思考1:如何提高乙酸乙酯的水解速率?
升温、催化剂、增大反应的接触面积等
思考3:如何比较水解速率的大小?
相同时间内酯层的消失量
思考2:什么条件下有利于提高酯水解的程度?
碱性条件
请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶液及不同温度下的水解速率
已知:①乙酸乙酯在常温下水解速率很慢
②乙酸乙酯的沸点为76.5—77.5℃
可供选择的试剂:经染色的乙酸乙酯、饱和食盐水、3mol/L稀硫酸、6 mol/L NaOH溶液、
实验仪器:微型带刻度玻璃瓶、酒精灯、烧杯等
学习任务三:探究酯的水解
学习任务三:探究酯的水解
实验方案设计
实验编号 饱和食盐水的体积(mL) 3mol/L 稀硫酸的体积(mL) 6mol/L的氢氧化钠溶液的体积(mL) 乙酸乙酯的体积(mL) 是否加热 其他
①
② ③ ④ 加热方式应为水浴加热
振荡
a
/
/
b
/
a
a
/
/
/
b
b
b
加热
加热
加热
不加热
/加热
/不加热
/不加热
/不加热
a/0/0
0/a/0
0/0/a
以上溶液体积用字母a、b、c等代替
思考1:为什么使用经染色的乙酸乙酯进行实验?
学习任务三:探究酯的水解
思考2:为什么酸性条件下选用稀硫酸而不用浓硫酸进行实验?
便于观察酯层的变化
浓硫酸有吸水性,不利于酯与水反应正向进行
学习任务三:探究酯的水解
将2ml经染色的乙酸乙酯同时加入下列溶液中
小组实验
5mL饱和食盐水
5mL 3mol/L 稀硫酸
5mL 6mol/L的氢氧化钠溶液
同时振荡相同的时间(振荡力度要一致),静置,待溶液澄清后比较相同时间内酯层的高度
5mL 3mol/L 稀硫酸
5mL 3mol/L 稀硫酸
水浴加热
中性条件分层,酯层基本不变,未水解
酸性条件,
酯层消失慢
碱性条件
酯层和香味消失很快
实验现象
学习任务三:探究酯的水解
加热条件下酯层消失比不加热快
加热
未加热
⑴酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解;且在碱性条件下酯水解趋于完全
⑵温度越高,酯水解速率越大。
酯的水解规律:
归纳小结
学习任务三:探究酯的水解
思考与讨论(用化学方程式解释):
1、为什么乙酸乙酯在酸性和碱性溶液中的水解速率大于中性溶液的水解速率?
CH3COOC2H5 +H2O
稀硫酸
△
CH3COOH + C2H5OH
无机酸、碱作催化剂,加快反应速率
2、为什么乙酸乙酯在碱性溶液中水解比酸性条件下快且能够水解完全?
碱能与水解生成的羧酸发生中和反应,使平衡右移,水解程度增大,同时中和反应放热,反应速率加快,直至完全反应。
学习任务三:探究酯的水解
水解反应
5.酯的化学性质
CH3COOC2H5+H2O CH3COOH+C2H5OH
H+
△
CH3COOC2H5+NaOH CH3COONa+C2H5OH
△
生成了羧酸盐,使水解反应不可逆,用“→”
酸性水解可逆
对点训练
1.(双选)下列说法不正确的是( )
A.可通过测相同时间内乙醇浓度的增加量比较不同条件下乙 酸乙酯的水解速率
B.可通过用PH计测乙酸浓度在相同时间内的改变值比较不同条件下乙酸乙酯的水解速率
C.为加快乙酸乙酯的水解速率,温度越高越好
D.热碱去油污涉及的化学原理包含酯的水解
BC
利用手持技术精确定量测定电导率,探究水解速率的影响因素
实验仪器:数据采集器、电导率传感器、计算机、恒温磁力搅拌器、搅拌磁子、烧杯 、量筒 、胶头滴管等。
实验药品:乙酸乙酯 、氢氧化钠溶液、酸溶液、蒸馏水。
酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解
思想提升
1、探究实验中,一定要控制变量;
2、有机反应反应原理复杂,不同条件产物不同;
3、多角度看问题,为解决问题提供新的思路。
6、酯的用途
作溶剂
作制备饮料、糖果和糕点的酯类香料
化学与职业——调香师
调香师,就是用各种天然或人工合成的化学成分调制气味的专业人员。 设计调合香料配方的人叫调香师,设计食品香精配方的人也叫调香师。
及时反馈
1.同位素在化学反应机理的研究中有着重要的作用.下列有关乙酸乙酯水解的化学方程式不正确的是( )
A.CH3COOCH2CH3+HOD→CH3COOD+CH3CH2OH
B.CH3COOCH2CH3+HOD→CH3COOH+CH3CH2OD
C.CH3CO18OCH2CH3+H2O→CH3CO18OH+CH3CH2OH
D.CH3C18OOCH2CH3+H2O→CH3C18OOH+CH3CH2OH
C
CH3OH+HCOOH
HCOOCH3 +H2O
1.
稀硫酸
△
CH3COOCH3 +NaOH
2.
CH3OH+CH3COONa
△
写出下列酯的水解方程式
及时反馈
CH2OOCCH3
CH2OOCCH3
+ H2O
3.
CH2OH
CH2OH
+ CH3COOH
2
稀硫酸
△
2
课堂小结
酯的概念
酯的结构、命名
酯的物理性质
酯的化学性质
酯的用途
谢谢大家
走进奇妙的化学世界
选择性必修3
第三章 烃的衍生物
第四节 羧酸
羧酸衍生物--酯
目录
1.概念
2.结构
3.命名
4.物理性质
5.化学性质
6.用途
自制“青苹果汁”
是什么让这杯“饮品”味道这么香?
经检测,苹果香精香气成分主要成分就是酯类,如丁酸乙酯、乙酸丁酯、乙酸异戊酯、2-甲基丁酸乙酯等
生活中的酯
乙酸异戊酯
丁酸乙酯
γ-癸酸内酯
硬脂酸甘油酯
1.概念
酯是羧酸分子羧基中的-OH被-OR取代后的产物,属于羧酸衍生物。
2.结构
R与R′可以相同也可以不同 R只能是烃基
R’(H)
C
O
R
O
学习任务一:认识酯类
官能团: 酯基
C
O
R
O
HCOOCH3
CH3COOCH3
甲酸甲酯
乙酸甲酯
3.酯的命名
原则:某酸+某醇→某酸某酯
CH3(CH2)2C—O—CH2CH3
O
丁酸乙酯
③难溶于水,易溶于乙醇和乙醚 等有机溶剂
②密度比水小
①低级酯是具有芳香气味的液体。
4.物理性质
学习任务二:探究酯的物理性质
5.酯的化学性质
CH3COOC2H5 +H2O
浓硫酸
△
CH3COOH + C2H5OH
根据该反应的特点,预测乙酸乙酯可能发生的化学反应。
CH3COOC2H5 +H2O
△
CH3COOH + C2H5OH
在酸或碱存在条件下,酯能发生水解反应生成相应的羧酸和醇,酯的水解反应是酯化反应的逆反应。
水解反应
5.酯的化学性质
稀硫酸
△
CH3C—O—C2H5+H2O CH3COOH+C2H5OH
=
O
酯的水解反应也是取代反应
稀硫酸
△
CH3C—O—C2H5+H2O CH3COOH+C2H5OH
=
O
学习任务三:探究酯的水解
思考1:如何提高乙酸乙酯的水解速率?
升温、催化剂、增大反应的接触面积等
思考3:如何比较水解速率的大小?
相同时间内酯层的消失量
思考2:什么条件下有利于提高酯水解的程度?
碱性条件
请你设计实验,探讨乙酸乙酯在中性、酸性和碱性溶液及不同温度下的水解速率
已知:①乙酸乙酯在常温下水解速率很慢
②乙酸乙酯的沸点为76.5—77.5℃
可供选择的试剂:经染色的乙酸乙酯、饱和食盐水、3mol/L稀硫酸、6 mol/L NaOH溶液、
实验仪器:微型带刻度玻璃瓶、酒精灯、烧杯等
学习任务三:探究酯的水解
学习任务三:探究酯的水解
实验方案设计
实验编号 饱和食盐水的体积(mL) 3mol/L 稀硫酸的体积(mL) 6mol/L的氢氧化钠溶液的体积(mL) 乙酸乙酯的体积(mL) 是否加热 其他
①
② ③ ④ 加热方式应为水浴加热
振荡
a
/
/
b
/
a
a
/
/
/
b
b
b
加热
加热
加热
不加热
/加热
/不加热
/不加热
/不加热
a/0/0
0/a/0
0/0/a
以上溶液体积用字母a、b、c等代替
思考1:为什么使用经染色的乙酸乙酯进行实验?
学习任务三:探究酯的水解
思考2:为什么酸性条件下选用稀硫酸而不用浓硫酸进行实验?
便于观察酯层的变化
浓硫酸有吸水性,不利于酯与水反应正向进行
学习任务三:探究酯的水解
将2ml经染色的乙酸乙酯同时加入下列溶液中
小组实验
5mL饱和食盐水
5mL 3mol/L 稀硫酸
5mL 6mol/L的氢氧化钠溶液
同时振荡相同的时间(振荡力度要一致),静置,待溶液澄清后比较相同时间内酯层的高度
5mL 3mol/L 稀硫酸
5mL 3mol/L 稀硫酸
水浴加热
中性条件分层,酯层基本不变,未水解
酸性条件,
酯层消失慢
碱性条件
酯层和香味消失很快
实验现象
学习任务三:探究酯的水解
加热条件下酯层消失比不加热快
加热
未加热
⑴酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解;且在碱性条件下酯水解趋于完全
⑵温度越高,酯水解速率越大。
酯的水解规律:
归纳小结
学习任务三:探究酯的水解
思考与讨论(用化学方程式解释):
1、为什么乙酸乙酯在酸性和碱性溶液中的水解速率大于中性溶液的水解速率?
CH3COOC2H5 +H2O
稀硫酸
△
CH3COOH + C2H5OH
无机酸、碱作催化剂,加快反应速率
2、为什么乙酸乙酯在碱性溶液中水解比酸性条件下快且能够水解完全?
碱能与水解生成的羧酸发生中和反应,使平衡右移,水解程度增大,同时中和反应放热,反应速率加快,直至完全反应。
学习任务三:探究酯的水解
水解反应
5.酯的化学性质
CH3COOC2H5+H2O CH3COOH+C2H5OH
H+
△
CH3COOC2H5+NaOH CH3COONa+C2H5OH
△
生成了羧酸盐,使水解反应不可逆,用“→”
酸性水解可逆
对点训练
1.(双选)下列说法不正确的是( )
A.可通过测相同时间内乙醇浓度的增加量比较不同条件下乙 酸乙酯的水解速率
B.可通过用PH计测乙酸浓度在相同时间内的改变值比较不同条件下乙酸乙酯的水解速率
C.为加快乙酸乙酯的水解速率,温度越高越好
D.热碱去油污涉及的化学原理包含酯的水解
BC
利用手持技术精确定量测定电导率,探究水解速率的影响因素
实验仪器:数据采集器、电导率传感器、计算机、恒温磁力搅拌器、搅拌磁子、烧杯 、量筒 、胶头滴管等。
实验药品:乙酸乙酯 、氢氧化钠溶液、酸溶液、蒸馏水。
酯在碱性条件下水解速率最快,其次是酸性条件,中性条件下几乎不水解
思想提升
1、探究实验中,一定要控制变量;
2、有机反应反应原理复杂,不同条件产物不同;
3、多角度看问题,为解决问题提供新的思路。
6、酯的用途
作溶剂
作制备饮料、糖果和糕点的酯类香料
化学与职业——调香师
调香师,就是用各种天然或人工合成的化学成分调制气味的专业人员。 设计调合香料配方的人叫调香师,设计食品香精配方的人也叫调香师。
及时反馈
1.同位素在化学反应机理的研究中有着重要的作用.下列有关乙酸乙酯水解的化学方程式不正确的是( )
A.CH3COOCH2CH3+HOD→CH3COOD+CH3CH2OH
B.CH3COOCH2CH3+HOD→CH3COOH+CH3CH2OD
C.CH3CO18OCH2CH3+H2O→CH3CO18OH+CH3CH2OH
D.CH3C18OOCH2CH3+H2O→CH3C18OOH+CH3CH2OH
C
CH3OH+HCOOH
HCOOCH3 +H2O
1.
稀硫酸
△
CH3COOCH3 +NaOH
2.
CH3OH+CH3COONa
△
写出下列酯的水解方程式
及时反馈
CH2OOCCH3
CH2OOCCH3
+ H2O
3.
CH2OH
CH2OH
+ CH3COOH
2
稀硫酸
△
2
课堂小结
酯的概念
酯的结构、命名
酯的物理性质
酯的化学性质
酯的用途
谢谢大家
