难点5 水-2023-2024学年沪教版九年级化学上册期中期末难点突破(含解析)
文档属性
| 名称 | 难点5 水-2023-2024学年沪教版九年级化学上册期中期末难点突破(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 471.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-15 00:00:00 | ||
图片预览



文档简介
九年级化学上册期中期末难点突破
第5关水
知识点回顾
【知识点1】水的性质
1.水是由氢、氧两种元素组成的无机物
2.在常温常压下为无色无味的透明液体
3.三态变化:固态、液态、气态
4.沸点:100oC
【知识点练习】
【例1】以下有关水的说法,正确的是( )
A.受热蒸发时水分子的体积逐渐变大,水由液态变为气态
B.降温结冰时水分子静止不动,水的物理性质发生了变化
C.水的天然循环是通过其三态变化实现的,发生的是物理变化
D.天然水经过自来水厂净化后得到的水是纯净物
【知识点2】水的组成
【实验】水的电解
【注意】为增强水的导电性,可在水中加入少量稀硫酸或氢氧化钠溶液。
【现象】
正极:有气泡产生,气体体积是负极的一半
【检验】将带火星的木条伸入,木条复燃,说明正极产生氧气
负极:有气泡产生,气体体积是正极的2倍
【检验】气体能在空气中燃烧,产生淡蓝色火焰,说明负极产生氢气
【结论】水在通电的条件下能发生分解反应,生成氢气和氧气,说明水是由氢元素和氧元素组成的。
【知识点练习】
【例2】下列是两个关于水的实验。
(1)该实验说明水由____________________组成。
(2)下列说法正确的是 _________(填字母序号)。
A.实验1中b管产生的气体能使带火星的木条复燃
B.实验1中原子的种类、个数均不改变
C.实验2中发生的是物理变化
D.实验2中水分子大小改变
【知识点3】水的净化
1.硬水:水中溶有较多含钙、镁的可溶性物质,这种水称为硬水
2.软水:水中不溶或有含少量钙、镁的可溶性物质,这种水称为软水
【注意】分别用两只烧杯取等量水样。向两只烧杯中分别滴加等量肥皂水。泡沫多、浮渣少的为软水。反之,泡沫少、浮渣多的为硬水
3.水的软化:过滤和蒸馏
(1)过滤:将不溶于液体的固体物质与液体分离的一种方法
【装置】
【操作要点】
①一贴:滤纸紧贴漏斗内壁。紧贴时用水润湿,使漏斗内壁和滤纸间不留气泡。
②二低:a.滤纸边缘低于漏斗边缘,b.漏斗内液面略低于滤纸边缘。(以防滤液从滤纸与器壁间渗出)。
③三靠:a.烧杯口紧靠玻璃棒_(防止液滴飞溅);
b.玻璃棒末端轻靠三层滤纸处;
c.漏斗末端紧靠烧杯内壁(起引流作用)。
【引申】如果用具有吸附作用的固体(如活性炭)过滤液体,可以滤去液体中的不溶性杂质,还可以吸附掉一些溶解的杂质,除去异味。
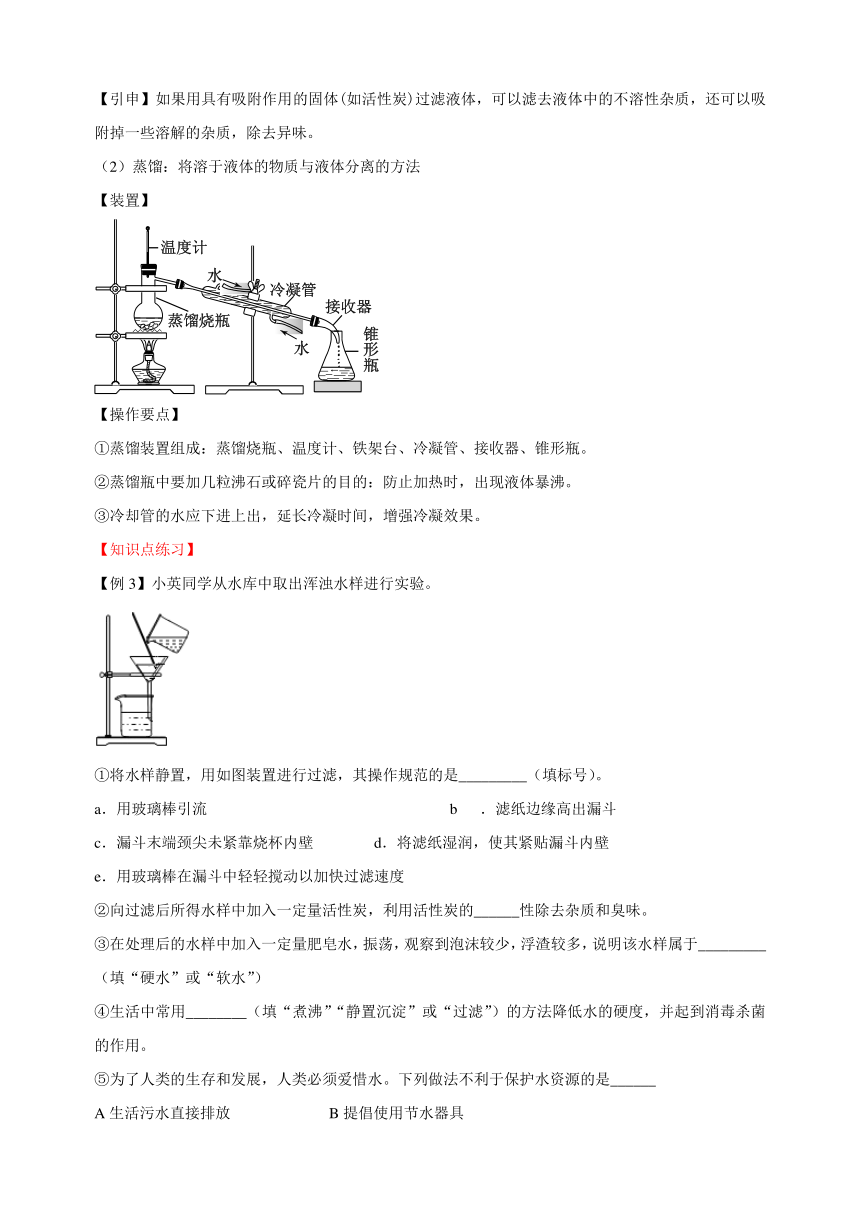
(2)蒸馏:将溶于液体的物质与液体分离的方法
【装置】
【操作要点】
①蒸馏装置组成:蒸馏烧瓶、温度计、铁架台、冷凝管、接收器、锥形瓶。
②蒸馏瓶中要加几粒沸石或碎瓷片的目的:防止加热时,出现液体暴沸。
③冷却管的水应下进上出,延长冷凝时间,增强冷凝效果。
【知识点练习】
【例3】小英同学从水库中取出浑浊水样进行实验。
①将水样静置,用如图装置进行过滤,其操作规范的是_________(填标号)。
a.用玻璃棒引流 b .滤纸边缘高出漏斗
c.漏斗末端颈尖未紧靠烧杯内壁 d.将滤纸湿润,使其紧贴漏斗内壁
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
②向过滤后所得水样中加入一定量活性炭,利用活性炭的______性除去杂质和臭味。
③在处理后的水样中加入一定量肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该水样属于_________(填“硬水”或“软水”)
④生活中常用________(填“煮沸”“静置沉淀”或“过滤”)的方法降低水的硬度,并起到消毒杀菌的作用。
⑤为了人类的生存和发展,人类必须爱惜水。下列做法不利于保护水资源的是______
A生活污水直接排放 B提倡使用节水器具
C工业上冷却水重复利用 D园林浇灌用滴灌、喷灌
【知识点4】水资源的利用
1.海水资源丰富,淡水资源紧缺
2.我国现阶段农业用水逐渐降低;工业用水逐渐提高;生活用水日益提高。
3.我国的人均水资源占有量仅为世界人均水平的四分之一,有超过一半地区处于严重缺水状态。
难点练习
1.水是重要的资源。下列说法正确的是( )
A.过滤能使硬水转化为软水 B.自然界中的水都是纯净物
C.杀菌能使海水转化为淡水 D.水是由氢、氧元素组成的
2.水是生产生活中不可缺少的物质。下列关于水的说法中不正确的是( )
A.肥皂水可以区分硬水和软水
B.在自来水厂净化水的过程中,发生的变化都是物理变化
C.水净化过程中加入明矾使悬浮物凝聚
D.生活中常通过煮沸来达到硬水软化的目的
3.国家游泳中心“水立方”的设计灵感于一个“方盆子”,许多“水泡泡”、许多“水分子”。下列关于水分子的说法正确的是( )
A.水分子是极小的水滴 B.水分子不能再分
C.水分子由氢元素和氧元素组成 D.1个水分子由2个氢原子和一个氧原子构成
4.下列混合物可以用过滤法分离的是( )
①含泥沙的粗盐②浑浊的河水③含有沙子的大米④食盐和白糖
A.①② B.①②③ C.①②④ D.②
5.下列有关说法正确的是( )
①市场上出售的某些净水器中的活性炭能吸附、过滤水中的杂质
②不同的纯净物可能由相同的元素组成
③由一种反应物生成其他物质的反应叫做分解反应
④分子是保持物质性质的最小粒子
⑤化学反应前后元素的种类不变
⑥混合物的组成中含有两种或两种以上的元素
A.③④⑥ B.①②③⑤ C.①②⑤ D.②③⑤
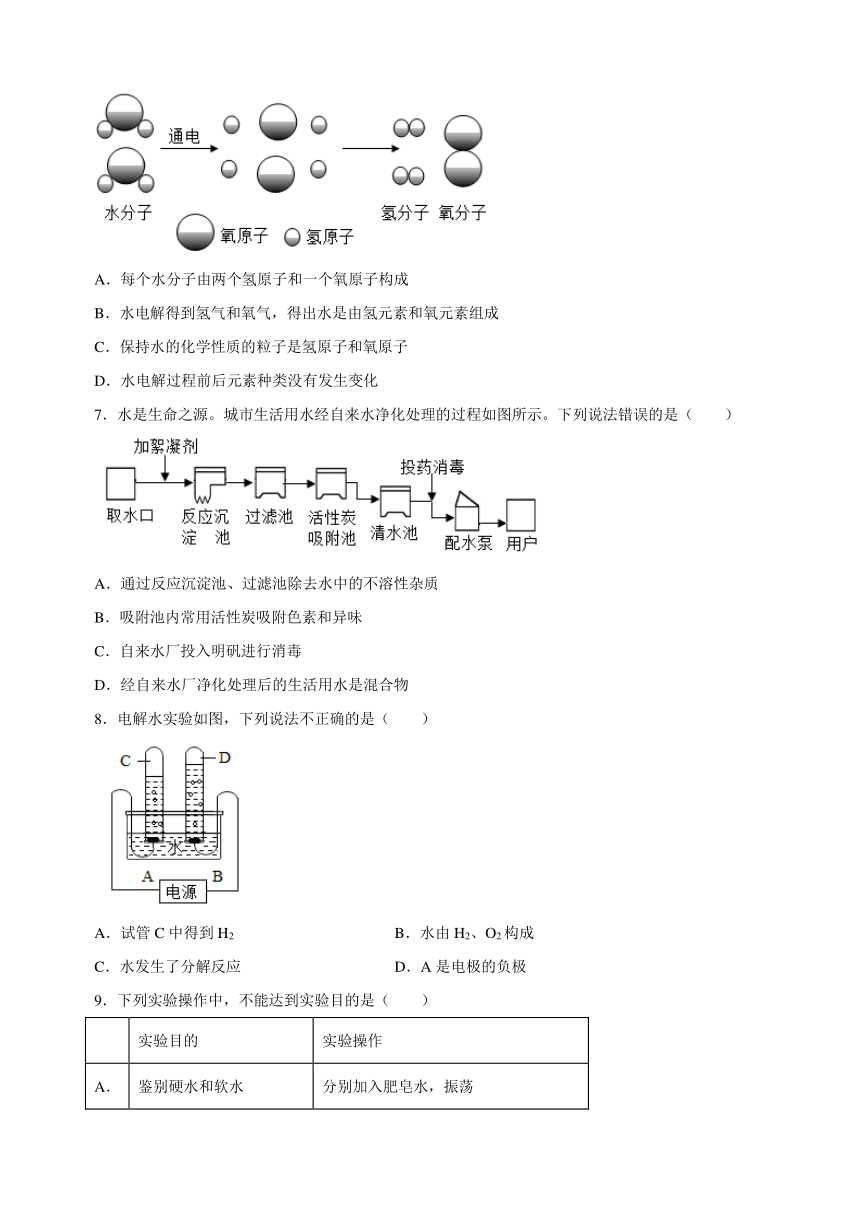
6.对水组成的研究,可采用对水电解的方法,下列有关叙述错误的是( )
A.每个水分子由两个氢原子和一个氧原子构成
B.水电解得到氢气和氧气,得出水是由氢元素和氧元素组成
C.保持水的化学性质的粒子是氢原子和氧原子
D.水电解过程前后元素种类没有发生变化
7.水是生命之源。城市生活用水经自来水净化处理的过程如图所示。下列说法错误的是( )
A.通过反应沉淀池、过滤池除去水中的不溶性杂质
B.吸附池内常用活性炭吸附色素和异味
C.自来水厂投入明矾进行消毒
D.经自来水厂净化处理后的生活用水是混合物
8.电解水实验如图,下列说法不正确的是( )
A.试管C中得到H2 B.水由H2、O2构成
C.水发生了分解反应 D.A是电极的负极
9.下列实验操作中,不能达到实验目的是( )
实验目的 实验操作
A. 鉴别硬水和软水 分别加入肥皂水,振荡
B. 提纯粗盐(含少量泥沙) 将粗盐加适量水溶解、过滤、蒸发结晶
C. 除去水中悬浮的小颗粒 加活性炭
D. 增强水的导电性 加入少量稀硫酸
A.A B.B C.C D.D
10.某同学对前面学过的内容进行了梳理,归纳了以下知识点:
①比较人体吸入空气和呼出气体中氧气含量时,应该用带火星的小木条来探究实验
②若两种粒子的质子数相等,则它们一定属于同种元素
③爱护水资源包括节约用水和防止水体污染
④加热高锰酸钾制氧气,在试管口放一团棉花可以防止加热时试管内的粉末状物质进入导管
⑤氦可用于制造低温环境
⑥镁在氧气中燃烧生成氧化镁,镁在氮气中燃烧生成氮化镁,又因为空气中氮气含量大于氧气的含量,所以镁条在空气中燃烧主要应该生成氮化镁
其中说法正确的有( )
A.1个 B.2个 C.3个 D.4个
11.化学是一门以实验为基础的科学,明明同学对化学非常感兴趣,国庆假期将至,明明同学准备从护城河中带回一瓶浑浊的河水,模拟天然水的净水过程,根据化学知识回答:
(1)净化水是可以通过加入絮凝剂凝聚、沉降,然后通过 ___(填实验操作名称)而实现。明明制作了图1所示的简易净水器,其中活性炭的主要作用是 ___。图2还缺少的一种仪器是 ___;其作用是 ___。
(2)经过简易净化后的水澄清透明,取其少量于小烧杯中,加入 ___搅拌,发现烧杯中没有泡沫,却有大量的浮渣,则说明该河水是 ___(填“硬水”或者“软水”)。该河水中含有较多的钙离子和镁离子,两种离子符号表示为 ___和 ___;家庭生活中除去水中较多的钙镁离子的方法是 ___。
12.2022年3月22日是第三十届“世界水日”,其主题为“珍惜地下水,珍视隐藏的资源”。
(1)地下水属于__________(填“混合物”或“纯净物”)。地下水也参与了水的天然循环,下列关于水的天然循环说法正确的是__________(填选项)。
①水在天然循环过程中实现了水的自身净化
②水的天然循环是通过水的三态变化实现的
③太阳为水的天然循环提供了能量
④水的天然循环完成了水资源的重新分配
A.只有①②③ B.只有①② C.只有③④ D.①②③④
(2)实验室制取蒸馏水时,发生了__________(填“化学”或“物理”)变化。实验结束,可加入__________比较水蒸馏前后的硬度变化。
(3)如图1是电解水的实验示意图,通电一段时间后,a玻璃管中收集到10mL气体,b玻璃管中收集到___mL气体。水中通直流电的文字表达式____________________,属于__________(填“分解反应”或“化合反应”)。电解水中玻璃管__________(填“a”或“b”)中的气体能使带火星的木条复燃。该实验说明水是由____________________组成的。
(4)我校教学楼中安装的直饮水机,能将自来水进一步净化处理得到可直接饮用水,其处理水的过程如图2所示。
吸附罐中固体颗粒的主要作用是吸附杂质,固体颗粒可选用__________。
13.如图所示,在空气中点燃纯净的氢气,并在火焰上方罩一只凉烧杯,观察到现象是______,用手轻轻触摸烧杯外壁,感觉到______。该反应的文字表达式是______,该反应的基本类型是______。请画出氢气燃烧过程的微观示意图:______。
。
14.回答下列与水有关的问题。
(1)保持水化学性质的最小粒子是____________。
(2)实验室常用来区别硬水和软水的物质是____________。
(3)电解水的实验中,证明水中含有氧元素的实验方法是____________。
(4)工业生产自来水的过程中,可用____________方法除去水中不溶性的固体杂质。
15.下图为测定水的组成实验装置,根据到的实验现象回答:
(1)上面实验中发生反应的文字表达式为______。
(2)电源正极为______填(“A”或“B”)。
(3)电解水的过程中,发生改变的微粒是(请注意,写名称)______。
(4)水是生命之源。下列行为,不利于保护水资源的是______(填字母)
A.工业上可以循环利用水
B.用喷灌、滴灌等方法给农作物浇水
C.农业上可以大量使用农药业和化肥以提高粮食产量
D.水体有一定的自净能力,未经处理的生活污水可以任意排放
16.根据所学知识回答问题:
(1)小明自制了如图所示的实验装置,对水通电进行实验探究。
①与A量筒中的电极相连接的是电池的______极A量筒中产生的气体是______,检验此气体的方法是______。说明此气体的化学性质是______,该反应的文字表达式是______,反应类型是______。从能量转化角度分析,电解水是将______能转化为______能。
②若在正极上产生了20mL的气体,则在负极上约产生______mL气体。
(2)水的微观结构:构成水的粒子可表示为______(填下图中的字母代号,下同),该变化中,最小的微粒符号为______,保持氢气化学性质的最小微粒可表示为______。上述实验证明化学反应的实质是:______。
(3)水的性质:
①人体发烧时,常用冰块来降温,这是利用了水的______(填“物理”或“化学”)性质。
②常温下,水能与氧化钠反应生成氢氧化钠。请写出其文字表达式及反应类型是______,______。
(4)水的净化。兴趣小组的同学取学校附近河水样品,利用下图所示的实验过程对该水样进行了净化处理。请回答下列问题:
①加入的物质A是______,其作用是______,为除去水样2中的一些异味和色素,加入的物质B是______,其作用是______。
②取少量水样3于试管中,加入少量肥皂水并振荡,发现______,说明水样3是硬水,其中含较多的______。生活中,可通过______的方法,将其转化为软水。
③操作②是采用紫外线灯照射,发生______变化。水样4因为含有______,所以不是纯水,但可通过______的方法获得纯水。
(5)保护水环境,珍爱水资源,是每个公民应尽的责任和义务。为了防止水的污染,下列做法有利于保护水资源的是(填序号)______。
①抑制水中所有动、植物的生长
②不任意排放工业废水
③大量使用化肥农药
④生活污水经过净化处理后再排放
参考答案
1.D
【详解】A.过滤能除去不溶性杂质,煮沸使硬水转化为软水,故选项说法错误;
B.自然界中的水中含有多种物质不是纯净物,故选项说法错误;
C.杀菌能除去水中的微生物等不能使海水转化为淡水,故选项说法错误;
D.水是由氢、氧元素组成的,说法正确,故选项说法正确;故选:D。
2.B
【详解】A、向水中加入肥皂水时,如果产生的泡沫较多,是软水,如果产生大量浮渣,是硬水,因此可以用肥皂水区分硬水和软水,该选项说法正确;
B、在自来水厂净化水的过程中,发生的变化不都是物理变化,例如杀菌消毒,有新物质生成,发生的是化学变化,故选项说法错误;
C、水净化过程中加入明矾,明矾溶于水形成的胶状物具有吸附性,能够吸附悬浮杂质,使悬浮物凝聚,加速沉降,故选项说法正确;
D、生活中常通过煮沸,使水中的钙镁离子形成沉淀,从而达到软化水的目的,故选项说法正确。
故选B。
3.D
【详解】A、分子是微观概念,分子的质量和体积都很小,一个水分子的质量约是3×10-26kg,而水滴是宏观物质,故不正确;
B、分子是由原子构成的,所以分子可以再分成原子,故不正确;
C、分子是微观粒子,分子构成物质,元素是宏观概念,元素组成物质,可以说水分子是由氢原子和氧原子构成,或者说水是由氢元素和氧元素组成,故不正确;
D、由电解水实验可知一个水分子是由2个氢原子和一个氧原子构成,故正确。
4.A
【详解】①含泥沙的粗盐,氯化钠易溶于水,泥沙不溶于水,可以通过过滤的方法进行分离;
②浑浊的河水中泥沙不溶于水,可以通过过滤的方法进行分离;
③沙子和大米都不溶于水,不能用过滤的方法进行分离;
④食盐和白糖均易溶于水,不能用过滤的方法进行分离;
故①②可用过滤法分离;故选A。
5.C
【详解】①活性炭具有吸附作用,市场上出售的某些净水器中的活性炭能吸附、过滤水中的杂质,说法正确;
②不同的纯净物可能由相同的元素组成,如氧气与臭氧都是由氧元素组成的,说法正确;
③由一种反应物生成两种或两种以上其他物质的反应叫做分解反应,说法错误;
④分子是保持物质化学性质的最小粒子,不能保持物质的物理性质,说法错误;
⑤由质量守恒定律可知,化学反应前后元素的种类不变,说法正确;
⑥混合物是由两种或两种以上的物质组成的,其组成中含有两种或两种以上的元素,也可能是含有一种元素,如氧气与臭氧组成的混合物中只含一种元素,说法错误。
故①②⑤正确,选C。
6.C
【详解】A、由水分子的模型图可知,每个水分子由两个氢原子和一个氧原子构成,故A叙述正确;
B、水电解得到氢气和氧气,氢气由氢元素组成,氧气由氧元素组成,根据质量守恒定律,反应前后元素种类不变,得出水是由氢元素和氧元素组成,故B叙述正确;
C、保持水的化学性质的粒子是水分子,故C叙述错误;
D、由质量守恒定律可知,水电解过程前后元素种类没有发生变化,故D叙述正确。故选C。
7.C
【详解】A、反应沉淀池中加入絮凝剂,吸附水中悬浮杂质而加速其沉淀,过滤把不溶于水的固体与液体分离,除去水中不溶性杂质,故A正确;
B、活性炭具有吸附性,吸附池内常用活性炭吸附色素和异味,故B正确;
C、明矾没有强氧化性,不能消毒;明矾水解生成氢氧化铝胶体能吸附水中的悬浮物从而加速沉降,而不能起到消毒的作用,故C错误;
D、经自来水厂净化处理后的生活用水仍含有多种物质,属于混合物,故D正确;故选C。
8.B
【详解】A、在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,试管C生成的气体较少,故试管C中得到H2,故A正确;
B、水是由水分子构成的,故 B错误;
C、水通电生成氢气和氧气,反应符合“一变多”,则水发生了分解反应,故C正确;
D、电解水正极生成氧气,负极生成氢气,氢气与氧气体积比2:1,A是电极的负极,故D正确。
故选B。
9.C
【详解】A、通常用肥皂水来区分硬水和软水,肥皂水在硬水中浮渣多,在软水中泡沫较多,不符合题意;
B、粗盐提纯,可采取溶解、过滤、蒸发的方法,不符合题意;
C、活性炭结构疏松多孔,具有吸附性,可以吸附水中的色素和异味,不能除去水中悬浮的小颗粒,符合题意;
D、纯水不导电,水中加入少量的稀硫酸,可以增强水的导电性,不符合题意。故选C。
10.B
【详解】①比较人体吸入空气和呼出气体中氧气含量时,应该用燃着的小木条来探究实验;①错;
②若两种粒子的质子数相等,则它们不一定属于同种元素;水分子和氖原子质子数相等,它们不属于同种元素;②错;
③爱护水资源包括节约用水和防治水体污染。③错;
④加热高锰酸钾制氧气,在试管口放一团棉花可以防止加热时试管内的粉末状物质进入导管;④正确;
⑤氦可用于制造低温环境;⑤正确;
⑥氧气相对于氮气,其对单质镁的氧化能力远远强于氮气,氮气相对来说是不活泼的。显然,镁自然更容易与氧气发生反应而不容易与氮气发生反应,生成的氧化镁的质量大于氮化镁,所以镁条在空气中燃烧主要应该生成氧化镁。⑥错。
综上所述:④⑤正确;选择B。
11.(1) 过滤 吸附色素和异味 玻璃棒 引流(2) 肥皂水 硬水 Ca2+ Mg2+ 煮沸
【解析】(1)净化水是可以通过加入絮凝剂凝聚、沉降,然后通过过滤而实现。明明制作了图1所示的简易净水器,其中活性炭具有吸附性,能够吸附色素和异味;图2还缺少的一种仪器是玻璃棒;其作用是引流;
(2)经过简易净化后的水澄清透明,取其少量于小烧杯中,加入肥皂水搅拌,发现烧杯中没有泡沫,却有大量的浮渣,则说明该河水是硬水,反之产生泡沫较多,浮渣较少的是软水;
该河水中含有较多的钙离子和镁离子,根据离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,则钙离子和镁离子的符号为:Ca2+和Mg2+;
家庭生活中除去水中较多的钙镁离子的方法是煮沸,煮沸可以将硬水中的钙镁化合物转化为水垢除去从而降低水的硬度。
12.(1) 混合物 D(2) 物理 肥皂水(3) 5 分解反应 b 氢元素和氧元素(4)活性炭
【解析】(1)
地下水中含有水和可溶性杂质等物质,属于混合物;
①水在天然循环过程中实现了水的自身净化,正确;
②水的天然循环是通过水的三态变化实现的,正确;
③太阳为水的天然循环提供了能量,正确;
④水的天然循环完成了水资源的重新分配,正确;
故选D;
(2)实验室制取蒸馏水时,只是水的形态发生改变,未产生新的物质,属于物理变化;实验结束可加入肥皂水来比较水蒸馏前后的硬度变化;
(3)由电解水实验结论:“正氧负氢,氧一氢二”和图1实验示意图可知,a玻璃管中产生的气体体积是b玻璃管中产生的气体体积的两倍,a玻璃管中收集到的气体为氢气,体积为10mL,b玻璃管中收集到的为氧气,体积应为5mL;电解水生成氢气和氧气,反应的文字表达式为;该反应符合“一变多”的特点,属于分解反应;能使带火星的木条复燃的是氧气,b玻璃管中产生的气体为氧气,故玻璃管b中的气体能使带火星的木条复燃;该实验说明水是由氢元素和氧元素组成的;
(4)活性炭具有吸附性,可以除去水中的异味和杂质,吸附罐中固体颗粒的主要作用是吸附杂质,固体颗粒可选用活性炭。
13.产生淡蓝色火焰,烧杯内壁出现水雾 发烫 氢气+氧气水 化合反应
【详解】氢气燃烧产生淡蓝色火焰,生成水,水蒸气遇到凉烧杯,在烧杯内壁写出水雾,故填烧杯内壁出现水雾;
氢气燃烧时放出热量,将烧杯罩在火焰上方,用手轻轻触摸烧杯外壁,感觉到发烫,故填发烫;
氢气与氧气在点燃的条件下反应生成水,故反应的文字表达式写为:氢气+氧气水;
由文字表达式可知,该反应是两种物质生成一种新物质的反应,符合化合反应的特点,属于化合反应,故填化合反应;
氢气与氧气发生燃烧时,氢分子被破坏成氢原子,同时氧分子被破坏成氧原子,然后每2个氢原子与1个氧原子构成1个水分子,故氢气燃烧过程的微观示意图画为。
14.(1)水分子##H2O(2)肥皂水
(3)用带火星的木条检验与电源正极相连(或产生气体较少)的玻璃管内产生的气体(4)过滤
【解析】(1)水是由水分子构成的,保持水化学性质的最小粒子是水分子;
(2)肥皂水在软水中泡沫较多,在硬水中泡沫较少,所以生活中区别硬水和软水最简便的方法可采用肥皂水;
(3)通电分解水,用带火星的木条验证正极收集的气体,带火星的木条复燃,说明生成了氧气,氧气是由氧元素组成的,说明水中含有氧元素;
(4)过滤能将固液分开,除去水中难溶性杂质的操作是过滤。
15.(1)(2)B(3)水分子(4)CD
【解析】(1)电解水生成氢气和氧气,则实验中发生反应的文字表达式为。
(2)电解水正极生成氧气,负极生成氢气,氧气和氢气的体积比为1:2,则与乙试管相连的B端为正极,故电源正极为B。
(3)水电解生成氢气和氧气,水分子破裂成氢原子和氧原子,氧原子重新组合成氧分子,氢原子重新组合成氢分子,故电解水的过程中,发生改变的微粒是水分子。
(4)A、工业上可以循环利用水,可以节约水资源,有利于保护水资源,故A正确;B、用喷灌、滴灌等方法给农作物浇水,可以节约水资源,有利于保护水资源,故B正确;C、农业上要合理使用农药业和化肥以提高粮食产量,大量使用污染土壤,化肥随雨水等流入河流,污染水资源,故C不正确;D、水体有一定的自净能力,未经处理的生活污水不能任意排放,超过水体的自净能力,会造成水体污染,故D不正确。故选CD。
16.(1) 负 氢气##H2 用燃着的木条接触该气体,气体被点燃,且产生淡蓝色的火焰,证明是氢气; 具有可燃性 化合反应 电 化学 40
(2) C EF##FE B 在化学变化中,分子分为原子,原子重新组合为新的分子
(3) 物理 化合反应
(4) 明矾 吸附水中悬浮的杂质,加速其沉降 活性炭 吸附水中色素和异味 泡沫较少 可溶性钙镁化合物 煮沸 化学 可溶性杂质 蒸馏
(5)②④
【解析】(1)①在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,A量筒中产生的气体较多,是氢气,与电池的负极相连;
氢气具有可燃性,检验氢气的方法是:用燃着的木条接触该气体,气体被点燃,且产生淡蓝色的火焰,证明是氢气;说明氢气具有可燃性;
氢气燃烧生成水,该反应的文字表达式为:;
该反应符合“多变一”的特点,属于化合反应;
电解水过程中,消耗电能产生氢气和氧气,电能转化为化学能;
②在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,若在正极上产生了20mL的气体,则在负极上约产生40mL气体;
(2)水由水分子构成,每个水分子由2个氢原子和1个氧原子构成,故表示为C;
原子是化学变化中的最小粒子,该变化中,最小的微粒符号为氢原子和氧原子,故填:EF;
氢气由氢分子构成,保持氢气化学性质的最小微粒为氢分子,每个氢分子由2个氢原子构成,表示为:B;
该实验证明化学反应的实质是:在化学变化中,分子分为原子,原子重新组合为新的分子;
(3)①人体发热时,常用冰块来降温,是因为冰融化吸热,不需要通过化学变化就能表现出来,这是利用了水的物理性质;
②常温下,水能与氧化钠反应生成氢氧化钠,该反应的文字表达式为:;
该反应符合“多变一”的特点,属于化合反应;
(4)①加入的物质A是明矾,明矾溶于水形成的胶状物具有吸附性,可以吸附水中悬浮的杂质。加速其沉降;
为除去水样2中的一些异味和色素,加入的物质B是活性炭,活性炭具有吸附性,可以吸附水中的色素和异味;
②通常用肥皂水来区分硬水和软水,肥皂水在硬水中易起浮渣,在软水中泡沫较多,故取少量水样3于试管中,加入少量肥皂水并振荡,发现浮渣多、泡沫少,说明水样3是硬水,其中含较多的可溶性钙、镁化合物;
可溶性钙、镁化合物在加热时,能形成沉淀,故生活中,可通过煮沸的方法将其转化为软水;
③操作②是采用紫外线灯照射,发生了蛋白质变性,有新物质生成,属于化学变化;
水样4中因为含有可溶性杂质,不是纯水,属于混合物,可通过蒸馏的方法获得纯水,蒸馏可除去所有杂质。
(5)①抑制水中所有动、植物的生长的做法不现实也不利于保护水资源,错误;
②不任意排放工业废水,可减少水体污染物,利于水体保护,正确;
③大量使用化肥农药,残留化肥、农药进入水体,不利于水体保护,错误;
④生活污水经过净化处理后再排放,利于水体保护,正确;
故选②④。
第5关水
知识点回顾
【知识点1】水的性质
1.水是由氢、氧两种元素组成的无机物
2.在常温常压下为无色无味的透明液体
3.三态变化:固态、液态、气态
4.沸点:100oC
【知识点练习】
【例1】以下有关水的说法,正确的是( )
A.受热蒸发时水分子的体积逐渐变大,水由液态变为气态
B.降温结冰时水分子静止不动,水的物理性质发生了变化
C.水的天然循环是通过其三态变化实现的,发生的是物理变化
D.天然水经过自来水厂净化后得到的水是纯净物
【知识点2】水的组成
【实验】水的电解
【注意】为增强水的导电性,可在水中加入少量稀硫酸或氢氧化钠溶液。
【现象】
正极:有气泡产生,气体体积是负极的一半
【检验】将带火星的木条伸入,木条复燃,说明正极产生氧气
负极:有气泡产生,气体体积是正极的2倍
【检验】气体能在空气中燃烧,产生淡蓝色火焰,说明负极产生氢气
【结论】水在通电的条件下能发生分解反应,生成氢气和氧气,说明水是由氢元素和氧元素组成的。
【知识点练习】
【例2】下列是两个关于水的实验。
(1)该实验说明水由____________________组成。
(2)下列说法正确的是 _________(填字母序号)。
A.实验1中b管产生的气体能使带火星的木条复燃
B.实验1中原子的种类、个数均不改变
C.实验2中发生的是物理变化
D.实验2中水分子大小改变
【知识点3】水的净化
1.硬水:水中溶有较多含钙、镁的可溶性物质,这种水称为硬水
2.软水:水中不溶或有含少量钙、镁的可溶性物质,这种水称为软水
【注意】分别用两只烧杯取等量水样。向两只烧杯中分别滴加等量肥皂水。泡沫多、浮渣少的为软水。反之,泡沫少、浮渣多的为硬水
3.水的软化:过滤和蒸馏
(1)过滤:将不溶于液体的固体物质与液体分离的一种方法
【装置】
【操作要点】
①一贴:滤纸紧贴漏斗内壁。紧贴时用水润湿,使漏斗内壁和滤纸间不留气泡。
②二低:a.滤纸边缘低于漏斗边缘,b.漏斗内液面略低于滤纸边缘。(以防滤液从滤纸与器壁间渗出)。
③三靠:a.烧杯口紧靠玻璃棒_(防止液滴飞溅);
b.玻璃棒末端轻靠三层滤纸处;
c.漏斗末端紧靠烧杯内壁(起引流作用)。
【引申】如果用具有吸附作用的固体(如活性炭)过滤液体,可以滤去液体中的不溶性杂质,还可以吸附掉一些溶解的杂质,除去异味。
(2)蒸馏:将溶于液体的物质与液体分离的方法
【装置】
【操作要点】
①蒸馏装置组成:蒸馏烧瓶、温度计、铁架台、冷凝管、接收器、锥形瓶。
②蒸馏瓶中要加几粒沸石或碎瓷片的目的:防止加热时,出现液体暴沸。
③冷却管的水应下进上出,延长冷凝时间,增强冷凝效果。
【知识点练习】
【例3】小英同学从水库中取出浑浊水样进行实验。
①将水样静置,用如图装置进行过滤,其操作规范的是_________(填标号)。
a.用玻璃棒引流 b .滤纸边缘高出漏斗
c.漏斗末端颈尖未紧靠烧杯内壁 d.将滤纸湿润,使其紧贴漏斗内壁
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
②向过滤后所得水样中加入一定量活性炭,利用活性炭的______性除去杂质和臭味。
③在处理后的水样中加入一定量肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该水样属于_________(填“硬水”或“软水”)
④生活中常用________(填“煮沸”“静置沉淀”或“过滤”)的方法降低水的硬度,并起到消毒杀菌的作用。
⑤为了人类的生存和发展,人类必须爱惜水。下列做法不利于保护水资源的是______
A生活污水直接排放 B提倡使用节水器具
C工业上冷却水重复利用 D园林浇灌用滴灌、喷灌
【知识点4】水资源的利用
1.海水资源丰富,淡水资源紧缺
2.我国现阶段农业用水逐渐降低;工业用水逐渐提高;生活用水日益提高。
3.我国的人均水资源占有量仅为世界人均水平的四分之一,有超过一半地区处于严重缺水状态。
难点练习
1.水是重要的资源。下列说法正确的是( )
A.过滤能使硬水转化为软水 B.自然界中的水都是纯净物
C.杀菌能使海水转化为淡水 D.水是由氢、氧元素组成的
2.水是生产生活中不可缺少的物质。下列关于水的说法中不正确的是( )
A.肥皂水可以区分硬水和软水
B.在自来水厂净化水的过程中,发生的变化都是物理变化
C.水净化过程中加入明矾使悬浮物凝聚
D.生活中常通过煮沸来达到硬水软化的目的
3.国家游泳中心“水立方”的设计灵感于一个“方盆子”,许多“水泡泡”、许多“水分子”。下列关于水分子的说法正确的是( )
A.水分子是极小的水滴 B.水分子不能再分
C.水分子由氢元素和氧元素组成 D.1个水分子由2个氢原子和一个氧原子构成
4.下列混合物可以用过滤法分离的是( )
①含泥沙的粗盐②浑浊的河水③含有沙子的大米④食盐和白糖
A.①② B.①②③ C.①②④ D.②
5.下列有关说法正确的是( )
①市场上出售的某些净水器中的活性炭能吸附、过滤水中的杂质
②不同的纯净物可能由相同的元素组成
③由一种反应物生成其他物质的反应叫做分解反应
④分子是保持物质性质的最小粒子
⑤化学反应前后元素的种类不变
⑥混合物的组成中含有两种或两种以上的元素
A.③④⑥ B.①②③⑤ C.①②⑤ D.②③⑤
6.对水组成的研究,可采用对水电解的方法,下列有关叙述错误的是( )
A.每个水分子由两个氢原子和一个氧原子构成
B.水电解得到氢气和氧气,得出水是由氢元素和氧元素组成
C.保持水的化学性质的粒子是氢原子和氧原子
D.水电解过程前后元素种类没有发生变化
7.水是生命之源。城市生活用水经自来水净化处理的过程如图所示。下列说法错误的是( )
A.通过反应沉淀池、过滤池除去水中的不溶性杂质
B.吸附池内常用活性炭吸附色素和异味
C.自来水厂投入明矾进行消毒
D.经自来水厂净化处理后的生活用水是混合物
8.电解水实验如图,下列说法不正确的是( )
A.试管C中得到H2 B.水由H2、O2构成
C.水发生了分解反应 D.A是电极的负极
9.下列实验操作中,不能达到实验目的是( )
实验目的 实验操作
A. 鉴别硬水和软水 分别加入肥皂水,振荡
B. 提纯粗盐(含少量泥沙) 将粗盐加适量水溶解、过滤、蒸发结晶
C. 除去水中悬浮的小颗粒 加活性炭
D. 增强水的导电性 加入少量稀硫酸
A.A B.B C.C D.D
10.某同学对前面学过的内容进行了梳理,归纳了以下知识点:
①比较人体吸入空气和呼出气体中氧气含量时,应该用带火星的小木条来探究实验
②若两种粒子的质子数相等,则它们一定属于同种元素
③爱护水资源包括节约用水和防止水体污染
④加热高锰酸钾制氧气,在试管口放一团棉花可以防止加热时试管内的粉末状物质进入导管
⑤氦可用于制造低温环境
⑥镁在氧气中燃烧生成氧化镁,镁在氮气中燃烧生成氮化镁,又因为空气中氮气含量大于氧气的含量,所以镁条在空气中燃烧主要应该生成氮化镁
其中说法正确的有( )
A.1个 B.2个 C.3个 D.4个
11.化学是一门以实验为基础的科学,明明同学对化学非常感兴趣,国庆假期将至,明明同学准备从护城河中带回一瓶浑浊的河水,模拟天然水的净水过程,根据化学知识回答:
(1)净化水是可以通过加入絮凝剂凝聚、沉降,然后通过 ___(填实验操作名称)而实现。明明制作了图1所示的简易净水器,其中活性炭的主要作用是 ___。图2还缺少的一种仪器是 ___;其作用是 ___。
(2)经过简易净化后的水澄清透明,取其少量于小烧杯中,加入 ___搅拌,发现烧杯中没有泡沫,却有大量的浮渣,则说明该河水是 ___(填“硬水”或者“软水”)。该河水中含有较多的钙离子和镁离子,两种离子符号表示为 ___和 ___;家庭生活中除去水中较多的钙镁离子的方法是 ___。
12.2022年3月22日是第三十届“世界水日”,其主题为“珍惜地下水,珍视隐藏的资源”。
(1)地下水属于__________(填“混合物”或“纯净物”)。地下水也参与了水的天然循环,下列关于水的天然循环说法正确的是__________(填选项)。
①水在天然循环过程中实现了水的自身净化
②水的天然循环是通过水的三态变化实现的
③太阳为水的天然循环提供了能量
④水的天然循环完成了水资源的重新分配
A.只有①②③ B.只有①② C.只有③④ D.①②③④
(2)实验室制取蒸馏水时,发生了__________(填“化学”或“物理”)变化。实验结束,可加入__________比较水蒸馏前后的硬度变化。
(3)如图1是电解水的实验示意图,通电一段时间后,a玻璃管中收集到10mL气体,b玻璃管中收集到___mL气体。水中通直流电的文字表达式____________________,属于__________(填“分解反应”或“化合反应”)。电解水中玻璃管__________(填“a”或“b”)中的气体能使带火星的木条复燃。该实验说明水是由____________________组成的。
(4)我校教学楼中安装的直饮水机,能将自来水进一步净化处理得到可直接饮用水,其处理水的过程如图2所示。
吸附罐中固体颗粒的主要作用是吸附杂质,固体颗粒可选用__________。
13.如图所示,在空气中点燃纯净的氢气,并在火焰上方罩一只凉烧杯,观察到现象是______,用手轻轻触摸烧杯外壁,感觉到______。该反应的文字表达式是______,该反应的基本类型是______。请画出氢气燃烧过程的微观示意图:______。
。
14.回答下列与水有关的问题。
(1)保持水化学性质的最小粒子是____________。
(2)实验室常用来区别硬水和软水的物质是____________。
(3)电解水的实验中,证明水中含有氧元素的实验方法是____________。
(4)工业生产自来水的过程中,可用____________方法除去水中不溶性的固体杂质。
15.下图为测定水的组成实验装置,根据到的实验现象回答:
(1)上面实验中发生反应的文字表达式为______。
(2)电源正极为______填(“A”或“B”)。
(3)电解水的过程中,发生改变的微粒是(请注意,写名称)______。
(4)水是生命之源。下列行为,不利于保护水资源的是______(填字母)
A.工业上可以循环利用水
B.用喷灌、滴灌等方法给农作物浇水
C.农业上可以大量使用农药业和化肥以提高粮食产量
D.水体有一定的自净能力,未经处理的生活污水可以任意排放
16.根据所学知识回答问题:
(1)小明自制了如图所示的实验装置,对水通电进行实验探究。
①与A量筒中的电极相连接的是电池的______极A量筒中产生的气体是______,检验此气体的方法是______。说明此气体的化学性质是______,该反应的文字表达式是______,反应类型是______。从能量转化角度分析,电解水是将______能转化为______能。
②若在正极上产生了20mL的气体,则在负极上约产生______mL气体。
(2)水的微观结构:构成水的粒子可表示为______(填下图中的字母代号,下同),该变化中,最小的微粒符号为______,保持氢气化学性质的最小微粒可表示为______。上述实验证明化学反应的实质是:______。
(3)水的性质:
①人体发烧时,常用冰块来降温,这是利用了水的______(填“物理”或“化学”)性质。
②常温下,水能与氧化钠反应生成氢氧化钠。请写出其文字表达式及反应类型是______,______。
(4)水的净化。兴趣小组的同学取学校附近河水样品,利用下图所示的实验过程对该水样进行了净化处理。请回答下列问题:
①加入的物质A是______,其作用是______,为除去水样2中的一些异味和色素,加入的物质B是______,其作用是______。
②取少量水样3于试管中,加入少量肥皂水并振荡,发现______,说明水样3是硬水,其中含较多的______。生活中,可通过______的方法,将其转化为软水。
③操作②是采用紫外线灯照射,发生______变化。水样4因为含有______,所以不是纯水,但可通过______的方法获得纯水。
(5)保护水环境,珍爱水资源,是每个公民应尽的责任和义务。为了防止水的污染,下列做法有利于保护水资源的是(填序号)______。
①抑制水中所有动、植物的生长
②不任意排放工业废水
③大量使用化肥农药
④生活污水经过净化处理后再排放
参考答案
1.D
【详解】A.过滤能除去不溶性杂质,煮沸使硬水转化为软水,故选项说法错误;
B.自然界中的水中含有多种物质不是纯净物,故选项说法错误;
C.杀菌能除去水中的微生物等不能使海水转化为淡水,故选项说法错误;
D.水是由氢、氧元素组成的,说法正确,故选项说法正确;故选:D。
2.B
【详解】A、向水中加入肥皂水时,如果产生的泡沫较多,是软水,如果产生大量浮渣,是硬水,因此可以用肥皂水区分硬水和软水,该选项说法正确;
B、在自来水厂净化水的过程中,发生的变化不都是物理变化,例如杀菌消毒,有新物质生成,发生的是化学变化,故选项说法错误;
C、水净化过程中加入明矾,明矾溶于水形成的胶状物具有吸附性,能够吸附悬浮杂质,使悬浮物凝聚,加速沉降,故选项说法正确;
D、生活中常通过煮沸,使水中的钙镁离子形成沉淀,从而达到软化水的目的,故选项说法正确。
故选B。
3.D
【详解】A、分子是微观概念,分子的质量和体积都很小,一个水分子的质量约是3×10-26kg,而水滴是宏观物质,故不正确;
B、分子是由原子构成的,所以分子可以再分成原子,故不正确;
C、分子是微观粒子,分子构成物质,元素是宏观概念,元素组成物质,可以说水分子是由氢原子和氧原子构成,或者说水是由氢元素和氧元素组成,故不正确;
D、由电解水实验可知一个水分子是由2个氢原子和一个氧原子构成,故正确。
4.A
【详解】①含泥沙的粗盐,氯化钠易溶于水,泥沙不溶于水,可以通过过滤的方法进行分离;
②浑浊的河水中泥沙不溶于水,可以通过过滤的方法进行分离;
③沙子和大米都不溶于水,不能用过滤的方法进行分离;
④食盐和白糖均易溶于水,不能用过滤的方法进行分离;
故①②可用过滤法分离;故选A。
5.C
【详解】①活性炭具有吸附作用,市场上出售的某些净水器中的活性炭能吸附、过滤水中的杂质,说法正确;
②不同的纯净物可能由相同的元素组成,如氧气与臭氧都是由氧元素组成的,说法正确;
③由一种反应物生成两种或两种以上其他物质的反应叫做分解反应,说法错误;
④分子是保持物质化学性质的最小粒子,不能保持物质的物理性质,说法错误;
⑤由质量守恒定律可知,化学反应前后元素的种类不变,说法正确;
⑥混合物是由两种或两种以上的物质组成的,其组成中含有两种或两种以上的元素,也可能是含有一种元素,如氧气与臭氧组成的混合物中只含一种元素,说法错误。
故①②⑤正确,选C。
6.C
【详解】A、由水分子的模型图可知,每个水分子由两个氢原子和一个氧原子构成,故A叙述正确;
B、水电解得到氢气和氧气,氢气由氢元素组成,氧气由氧元素组成,根据质量守恒定律,反应前后元素种类不变,得出水是由氢元素和氧元素组成,故B叙述正确;
C、保持水的化学性质的粒子是水分子,故C叙述错误;
D、由质量守恒定律可知,水电解过程前后元素种类没有发生变化,故D叙述正确。故选C。
7.C
【详解】A、反应沉淀池中加入絮凝剂,吸附水中悬浮杂质而加速其沉淀,过滤把不溶于水的固体与液体分离,除去水中不溶性杂质,故A正确;
B、活性炭具有吸附性,吸附池内常用活性炭吸附色素和异味,故B正确;
C、明矾没有强氧化性,不能消毒;明矾水解生成氢氧化铝胶体能吸附水中的悬浮物从而加速沉降,而不能起到消毒的作用,故C错误;
D、经自来水厂净化处理后的生活用水仍含有多种物质,属于混合物,故D正确;故选C。
8.B
【详解】A、在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,试管C生成的气体较少,故试管C中得到H2,故A正确;
B、水是由水分子构成的,故 B错误;
C、水通电生成氢气和氧气,反应符合“一变多”,则水发生了分解反应,故C正确;
D、电解水正极生成氧气,负极生成氢气,氢气与氧气体积比2:1,A是电极的负极,故D正确。
故选B。
9.C
【详解】A、通常用肥皂水来区分硬水和软水,肥皂水在硬水中浮渣多,在软水中泡沫较多,不符合题意;
B、粗盐提纯,可采取溶解、过滤、蒸发的方法,不符合题意;
C、活性炭结构疏松多孔,具有吸附性,可以吸附水中的色素和异味,不能除去水中悬浮的小颗粒,符合题意;
D、纯水不导电,水中加入少量的稀硫酸,可以增强水的导电性,不符合题意。故选C。
10.B
【详解】①比较人体吸入空气和呼出气体中氧气含量时,应该用燃着的小木条来探究实验;①错;
②若两种粒子的质子数相等,则它们不一定属于同种元素;水分子和氖原子质子数相等,它们不属于同种元素;②错;
③爱护水资源包括节约用水和防治水体污染。③错;
④加热高锰酸钾制氧气,在试管口放一团棉花可以防止加热时试管内的粉末状物质进入导管;④正确;
⑤氦可用于制造低温环境;⑤正确;
⑥氧气相对于氮气,其对单质镁的氧化能力远远强于氮气,氮气相对来说是不活泼的。显然,镁自然更容易与氧气发生反应而不容易与氮气发生反应,生成的氧化镁的质量大于氮化镁,所以镁条在空气中燃烧主要应该生成氧化镁。⑥错。
综上所述:④⑤正确;选择B。
11.(1) 过滤 吸附色素和异味 玻璃棒 引流(2) 肥皂水 硬水 Ca2+ Mg2+ 煮沸
【解析】(1)净化水是可以通过加入絮凝剂凝聚、沉降,然后通过过滤而实现。明明制作了图1所示的简易净水器,其中活性炭具有吸附性,能够吸附色素和异味;图2还缺少的一种仪器是玻璃棒;其作用是引流;
(2)经过简易净化后的水澄清透明,取其少量于小烧杯中,加入肥皂水搅拌,发现烧杯中没有泡沫,却有大量的浮渣,则说明该河水是硬水,反之产生泡沫较多,浮渣较少的是软水;
该河水中含有较多的钙离子和镁离子,根据离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负符号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,则钙离子和镁离子的符号为:Ca2+和Mg2+;
家庭生活中除去水中较多的钙镁离子的方法是煮沸,煮沸可以将硬水中的钙镁化合物转化为水垢除去从而降低水的硬度。
12.(1) 混合物 D(2) 物理 肥皂水(3) 5 分解反应 b 氢元素和氧元素(4)活性炭
【解析】(1)
地下水中含有水和可溶性杂质等物质,属于混合物;
①水在天然循环过程中实现了水的自身净化,正确;
②水的天然循环是通过水的三态变化实现的,正确;
③太阳为水的天然循环提供了能量,正确;
④水的天然循环完成了水资源的重新分配,正确;
故选D;
(2)实验室制取蒸馏水时,只是水的形态发生改变,未产生新的物质,属于物理变化;实验结束可加入肥皂水来比较水蒸馏前后的硬度变化;
(3)由电解水实验结论:“正氧负氢,氧一氢二”和图1实验示意图可知,a玻璃管中产生的气体体积是b玻璃管中产生的气体体积的两倍,a玻璃管中收集到的气体为氢气,体积为10mL,b玻璃管中收集到的为氧气,体积应为5mL;电解水生成氢气和氧气,反应的文字表达式为;该反应符合“一变多”的特点,属于分解反应;能使带火星的木条复燃的是氧气,b玻璃管中产生的气体为氧气,故玻璃管b中的气体能使带火星的木条复燃;该实验说明水是由氢元素和氧元素组成的;
(4)活性炭具有吸附性,可以除去水中的异味和杂质,吸附罐中固体颗粒的主要作用是吸附杂质,固体颗粒可选用活性炭。
13.产生淡蓝色火焰,烧杯内壁出现水雾 发烫 氢气+氧气水 化合反应
【详解】氢气燃烧产生淡蓝色火焰,生成水,水蒸气遇到凉烧杯,在烧杯内壁写出水雾,故填烧杯内壁出现水雾;
氢气燃烧时放出热量,将烧杯罩在火焰上方,用手轻轻触摸烧杯外壁,感觉到发烫,故填发烫;
氢气与氧气在点燃的条件下反应生成水,故反应的文字表达式写为:氢气+氧气水;
由文字表达式可知,该反应是两种物质生成一种新物质的反应,符合化合反应的特点,属于化合反应,故填化合反应;
氢气与氧气发生燃烧时,氢分子被破坏成氢原子,同时氧分子被破坏成氧原子,然后每2个氢原子与1个氧原子构成1个水分子,故氢气燃烧过程的微观示意图画为。
14.(1)水分子##H2O(2)肥皂水
(3)用带火星的木条检验与电源正极相连(或产生气体较少)的玻璃管内产生的气体(4)过滤
【解析】(1)水是由水分子构成的,保持水化学性质的最小粒子是水分子;
(2)肥皂水在软水中泡沫较多,在硬水中泡沫较少,所以生活中区别硬水和软水最简便的方法可采用肥皂水;
(3)通电分解水,用带火星的木条验证正极收集的气体,带火星的木条复燃,说明生成了氧气,氧气是由氧元素组成的,说明水中含有氧元素;
(4)过滤能将固液分开,除去水中难溶性杂质的操作是过滤。
15.(1)(2)B(3)水分子(4)CD
【解析】(1)电解水生成氢气和氧气,则实验中发生反应的文字表达式为。
(2)电解水正极生成氧气,负极生成氢气,氧气和氢气的体积比为1:2,则与乙试管相连的B端为正极,故电源正极为B。
(3)水电解生成氢气和氧气,水分子破裂成氢原子和氧原子,氧原子重新组合成氧分子,氢原子重新组合成氢分子,故电解水的过程中,发生改变的微粒是水分子。
(4)A、工业上可以循环利用水,可以节约水资源,有利于保护水资源,故A正确;B、用喷灌、滴灌等方法给农作物浇水,可以节约水资源,有利于保护水资源,故B正确;C、农业上要合理使用农药业和化肥以提高粮食产量,大量使用污染土壤,化肥随雨水等流入河流,污染水资源,故C不正确;D、水体有一定的自净能力,未经处理的生活污水不能任意排放,超过水体的自净能力,会造成水体污染,故D不正确。故选CD。
16.(1) 负 氢气##H2 用燃着的木条接触该气体,气体被点燃,且产生淡蓝色的火焰,证明是氢气; 具有可燃性 化合反应 电 化学 40
(2) C EF##FE B 在化学变化中,分子分为原子,原子重新组合为新的分子
(3) 物理 化合反应
(4) 明矾 吸附水中悬浮的杂质,加速其沉降 活性炭 吸附水中色素和异味 泡沫较少 可溶性钙镁化合物 煮沸 化学 可溶性杂质 蒸馏
(5)②④
【解析】(1)①在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,A量筒中产生的气体较多,是氢气,与电池的负极相连;
氢气具有可燃性,检验氢气的方法是:用燃着的木条接触该气体,气体被点燃,且产生淡蓝色的火焰,证明是氢气;说明氢气具有可燃性;
氢气燃烧生成水,该反应的文字表达式为:;
该反应符合“多变一”的特点,属于化合反应;
电解水过程中,消耗电能产生氢气和氧气,电能转化为化学能;
②在电解水实验中,“正氧负氢”,生成氢气和氧气的体积比约为2:1,若在正极上产生了20mL的气体,则在负极上约产生40mL气体;
(2)水由水分子构成,每个水分子由2个氢原子和1个氧原子构成,故表示为C;
原子是化学变化中的最小粒子,该变化中,最小的微粒符号为氢原子和氧原子,故填:EF;
氢气由氢分子构成,保持氢气化学性质的最小微粒为氢分子,每个氢分子由2个氢原子构成,表示为:B;
该实验证明化学反应的实质是:在化学变化中,分子分为原子,原子重新组合为新的分子;
(3)①人体发热时,常用冰块来降温,是因为冰融化吸热,不需要通过化学变化就能表现出来,这是利用了水的物理性质;
②常温下,水能与氧化钠反应生成氢氧化钠,该反应的文字表达式为:;
该反应符合“多变一”的特点,属于化合反应;
(4)①加入的物质A是明矾,明矾溶于水形成的胶状物具有吸附性,可以吸附水中悬浮的杂质。加速其沉降;
为除去水样2中的一些异味和色素,加入的物质B是活性炭,活性炭具有吸附性,可以吸附水中的色素和异味;
②通常用肥皂水来区分硬水和软水,肥皂水在硬水中易起浮渣,在软水中泡沫较多,故取少量水样3于试管中,加入少量肥皂水并振荡,发现浮渣多、泡沫少,说明水样3是硬水,其中含较多的可溶性钙、镁化合物;
可溶性钙、镁化合物在加热时,能形成沉淀,故生活中,可通过煮沸的方法将其转化为软水;
③操作②是采用紫外线灯照射,发生了蛋白质变性,有新物质生成,属于化学变化;
水样4中因为含有可溶性杂质,不是纯水,属于混合物,可通过蒸馏的方法获得纯水,蒸馏可除去所有杂质。
(5)①抑制水中所有动、植物的生长的做法不现实也不利于保护水资源,错误;
②不任意排放工业废水,可减少水体污染物,利于水体保护,正确;
③大量使用化肥农药,残留化肥、农药进入水体,不利于水体保护,错误;
④生活污水经过净化处理后再排放,利于水体保护,正确;
故选②④。
同课章节目录
