第十单元 酸和碱 单元检测试题——2023-2024学年九年级化学人教版下册(无答案)
文档属性
| 名称 | 第十单元 酸和碱 单元检测试题——2023-2024学年九年级化学人教版下册(无答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 310.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-18 00:00:00 | ||
图片预览


文档简介
【单元检测】
第十单元《酸和碱》单元检测试题
湖北省石首市文峰初级中学
说明:1.全卷满分50分,考试时间42分钟。
2.请将答案写在答题卡上,否则不给分。
3.本卷可能用到的相对原子质量:H﹣1、C﹣12、O﹣16、Na﹣23、Mg﹣24、Ca﹣40。
一、选择题(共13个题,共18分,1~8题每题1分,9~13题每题2分,在每题有四个选项,只有一项符合题目要求)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13
答案
1.硫酸是一种非常重要化工原料。下列关于硫酸的说法中正确的是( )
A.实验室用稀硫酸和石灰石制取二氧化碳
B.常温下,可用铁制容器存放稀硫酸
C.用稀硫酸制备氯化锌
D.稀硫酸可用于金属除锈
2.在做有关酸的性质实验中,下列操作规范的是( )
A.滴加盐酸 B.稀释浓硫酸 C.倾倒盐酸 D.测盐酸的pH
3.下列有关常见酸与碱的说法中不正确的是( )
A.碱溶液中都含有氢氧根离子,因此有相似的化学性质
B.炉具清洁剂中含有氢氧化钠,是利用氢氧化钠具有的乳化作用
C.酸、碱在水溶液中都可解离出带电的粒子,因此酸、碱溶液能导电
D.在实验室,常用氢氧化钠固体来干燥某些气体
4. 使用酸、碱等腐蚀性药品时,必须按照操作规程进行。下列处理方法中有错误的是( )
A.有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓洒
B.稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的小苏打溶液
C.配制稀硫酸时,可先在量筒中加入一定量的浓硫酸,再慢慢注入水并不断搅拌
D.氢氧化钠溶液洒在衣服上,先用水冲洗后,再涂上硼酸溶液
5.中和反应在生活中有广泛应用。下列应用不属于中和反应的是( )
A.用盐酸除铁锈
B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤
D.用硫酸处理印染厂含碱废水
6.碱溶液中都含有OH-,因此不同的碱表现出一些共同的性质。下列关于Ba((OH)2性质的描述中不属于碱的共同性质的是( )
A.能使无色酚酞溶液变红色 B.能与盐酸反应生成水
C.能与Na2SO4溶液反应生成BaSO4沉淀 D.能与CO2反应生成水
7.下列物质敞口放置一段时间后,质量增加但溶质成分没有改变的是( )
A.氢氧化钠溶液 B.石灰水 C.浓硫酸 D.浓盐酸
8.下表是部分常见物质的pH,在这些物质中,能使紫色石蕊溶液变蓝的是( )
物质 厕所清洁剂 橘汁 草木灰水 柠檬汁
pH 1.7 3.5 10.6 2.5
A.厕所清洁剂 B.草木灰水 C.柠檬汁 D.橘汁
9.胃舒平治疗胃酸过多的化学反应为:Al(OH)3+3HCl=AlCl3+3H2O,其中未涉及的物质类别是( )
A.酸 B.碱 C.单质 D.氧化物
10.下列各组物质间的反应,由于现象不明显需要借助酸碱指示剂才能判断出反应发生的是( )
A.锌与稀盐酸
B.烧碱溶液与稀硫酸
C.氧化铁与稀硫酸
D.硫酸铜溶液与氢氧化钠溶液
11. 如图是稀HCl和NaOH溶液反应的pH变化曲线图,据图分析能得出的结论正确的是( )
A.该反应是NaOH溶液滴入稀盐酸
B.a克是指加入NaOH溶液的质量
C.A点时,溶液的溶质为NaOH、NaCl
D.B点表示稀盐酸和加入的NaOH溶液质量一定相同
12.下列试剂能将稀硫酸、氯化钠溶液、澄清石灰水三种溶液一步鉴别出来的是( )
A.稀盐酸 B.二氧化碳 C.碳酸钙 D.石蕊溶液
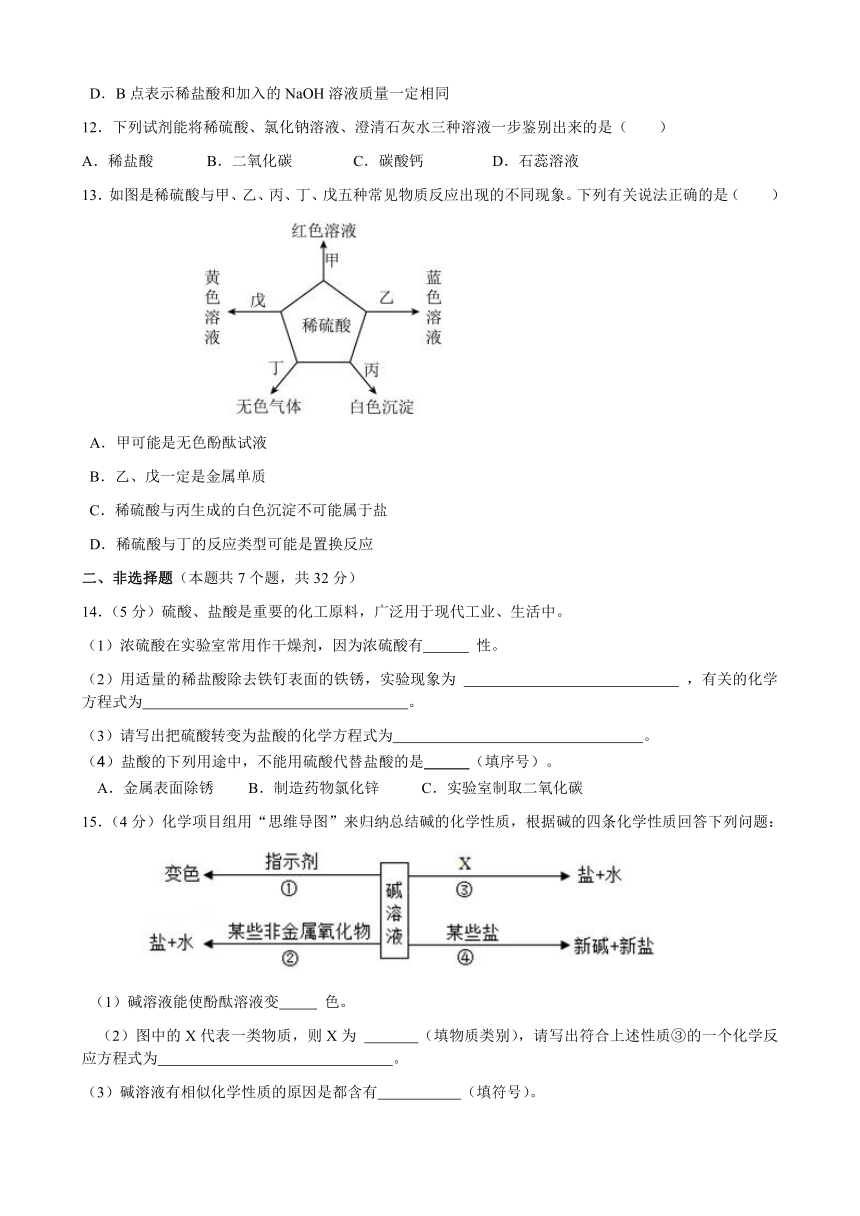
13.如图是稀硫酸与甲、乙、丙、丁、戊五种常见物质反应出现的不同现象。下列有关说法正确的是( )
A.甲可能是无色酚酞试液
B.乙、戊一定是金属单质
C.稀硫酸与丙生成的白色沉淀不可能属于盐
D.稀硫酸与丁的反应类型可能是置换反应
二、非选择题(本题共7个题,共32分)
14.(5分)硫酸、盐酸是重要的化工原料,广泛用于现代工业、生活中。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)用适量的稀盐酸除去铁钉表面的铁锈,实验现象为 ,有关的化学方程式为 。
(3)请写出把硫酸转变为盐酸的化学方程式为 。
(4)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填序号)。
A.金属表面除锈 B.制造药物氯化锌 C.实验室制取二氧化碳
15.(4分)化学项目组用“思维导图”来归纳总结碱的化学性质,根据碱的四条化学性质回答下列问题:
(1)碱溶液能使酚酞溶液变 色。
(2)图中的X代表一类物质,则X为 (填物质类别),请写出符合上述性质③的一个化学反应方程式为 。
(3)碱溶液有相似化学性质的原因是都含有 (填符号)。
16.(4分)某校化学课外活动小组在一次活动中,取刚降到地面的雨水水样,每隔5分钟用pH计测定一次pH,其数据如下表:
测定时刻 6︰05 6︰10 6︰15 6︰20 6︰25 6︰30
pH 4.95 4.94 4.94 4.88 4.86 4.85
已知:正常雨水的pH约为5.6,酸雨的pH小于5.6。
⑴所取的雨水是否属于酸雨 (填“属于”或“不属于”);在测定的期间,雨水水样的酸性随着时间的变化逐渐 (填“减弱”“无影响”或“增强”)。
⑵经调查,这一地区有一座燃煤发电厂,用火碱来吸收生产过程中产生的SO2,将其转化成亚硫酸钠。该反应的化学方程式 。
⑶若用pH试纸测定雨水的酸碱度,其中使用玻璃棒的作用是 。
17.(5分)化工产品是NaCl和NaOH组成的混合物。课外活动小组为测定该产品中NaCl的质量分数,进行了以下实验。取10.0g该固体样品置于锥形瓶中,加入适量的水配成溶液,逐滴加入溶质质量分数为10%的稀盐酸,用pH传感器等电子设备测得滴加过程中溶液的pH与加入稀盐酸的质量关系如图所示。请回答下列问题:
(1)恰好完全反应时,消耗稀盐酸中溶质的质量为 g。
(2)计算样品中NaCl的质量分数(写出计算过程)。
18.(4分) 如下图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。
(1)单质A不可能是 (填序号)。
A.Mg B.Fe C.Ag D.Zn
(2)若B为黑色的氧化铜,B与盐酸反应的化学方程式为 。
(3)若C为碳酸钠,C与足量的盐酸反应的化学方程式为 。
(4)若甲+乙→盐+水,根据“化学拼图”判断,一定符合条件的组合是 (填序号)。
①盐酸+A ②盐酸+B ③盐酸+C ④盐酸+D ⑤B+D
19.(5分)某兴趣小组同学开展跨学科实践活动,进行了“无形变有形”的创新实验。(装置气密性良好、部分仪器省略)。
(1)图1中,打开塑料瓶瓶盖,同时打开氧气传感器开关,得到了氧气体积分数随时间变化的曲线。AB段氧气体积分数逐渐降低,从微观角度解释其原因是 ,BC段氧气体积分数快速下册降,BC段对应的实验操作是 (写一种)。
(2)图2中,打开弹簧夹,向试管Ⅰ中加入一定量稀盐酸,关闭弹簧夹(保持导管口在液面以下)。观察到试管Ⅰ中有大量气泡产生且有液体流入试管Ⅱ中,产生此现象的原因是 。
(3)反应结束后,试管Ⅱ中的溶液由红色变为无色且无沉淀生成,试管Ⅱ中发生反应的化学方程式为 ,试管Ⅱ的溶液中一定含有的溶质是 (除酚酞以外)。
20.(5分)微型化学实验,因节能环保备受青睐,某化学兴趣小组设计了图1、图2两个微型实验,据图回答下列问题。
(1)如图1所示:在直径约为1.5cm的水滴两边,同时放少量硫酸铜晶体、氢氧化钠固体。已知:相对分子质量越大,微粒运动越慢,反之越快。实验中在 (填“A”或“B”)区域会先出现沉淀,反应的化学方程式为 。
(2)如图2所示:探究紫色石蕊溶液变色规律。
步骤1:向点滴板1~6号的孔穴中先加入如图2所示的试剂,再分别滴入2滴紫色石蕊溶液。6号孔穴中水的作用是 。
步骤2:将步骤1中所得的1号溶液和4号溶液互滴后溶液颜色发生明显变化,选出下列组合中互滴后溶液颜色有明显变化的是 (填序号)。
A.1号、5号 B.1号、3号 C.3号、4号 D.4号、5号
步骤3:重复步骤1,用吸管向5号孔穴吹入人呼出的气体,溶液表面出现白膜,写出反应的化学方程式为 。
第十单元《酸和碱》单元检测试题
湖北省石首市文峰初级中学
说明:1.全卷满分50分,考试时间42分钟。
2.请将答案写在答题卡上,否则不给分。
3.本卷可能用到的相对原子质量:H﹣1、C﹣12、O﹣16、Na﹣23、Mg﹣24、Ca﹣40。
一、选择题(共13个题,共18分,1~8题每题1分,9~13题每题2分,在每题有四个选项,只有一项符合题目要求)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13
答案
1.硫酸是一种非常重要化工原料。下列关于硫酸的说法中正确的是( )
A.实验室用稀硫酸和石灰石制取二氧化碳
B.常温下,可用铁制容器存放稀硫酸
C.用稀硫酸制备氯化锌
D.稀硫酸可用于金属除锈
2.在做有关酸的性质实验中,下列操作规范的是( )
A.滴加盐酸 B.稀释浓硫酸 C.倾倒盐酸 D.测盐酸的pH
3.下列有关常见酸与碱的说法中不正确的是( )
A.碱溶液中都含有氢氧根离子,因此有相似的化学性质
B.炉具清洁剂中含有氢氧化钠,是利用氢氧化钠具有的乳化作用
C.酸、碱在水溶液中都可解离出带电的粒子,因此酸、碱溶液能导电
D.在实验室,常用氢氧化钠固体来干燥某些气体
4. 使用酸、碱等腐蚀性药品时,必须按照操作规程进行。下列处理方法中有错误的是( )
A.有腐蚀性的药液溅入眼睛内,要立即用水冲洗,切不可用手揉搓洒
B.稀酸飞溅到皮肤上,立即用大量的水冲洗,再涂上3%~5%的小苏打溶液
C.配制稀硫酸时,可先在量筒中加入一定量的浓硫酸,再慢慢注入水并不断搅拌
D.氢氧化钠溶液洒在衣服上,先用水冲洗后,再涂上硼酸溶液
5.中和反应在生活中有广泛应用。下列应用不属于中和反应的是( )
A.用盐酸除铁锈
B.服用含有氢氧化镁的药物治疗胃酸过多
C.用熟石灰改良酸性土壤
D.用硫酸处理印染厂含碱废水
6.碱溶液中都含有OH-,因此不同的碱表现出一些共同的性质。下列关于Ba((OH)2性质的描述中不属于碱的共同性质的是( )
A.能使无色酚酞溶液变红色 B.能与盐酸反应生成水
C.能与Na2SO4溶液反应生成BaSO4沉淀 D.能与CO2反应生成水
7.下列物质敞口放置一段时间后,质量增加但溶质成分没有改变的是( )
A.氢氧化钠溶液 B.石灰水 C.浓硫酸 D.浓盐酸
8.下表是部分常见物质的pH,在这些物质中,能使紫色石蕊溶液变蓝的是( )
物质 厕所清洁剂 橘汁 草木灰水 柠檬汁
pH 1.7 3.5 10.6 2.5
A.厕所清洁剂 B.草木灰水 C.柠檬汁 D.橘汁
9.胃舒平治疗胃酸过多的化学反应为:Al(OH)3+3HCl=AlCl3+3H2O,其中未涉及的物质类别是( )
A.酸 B.碱 C.单质 D.氧化物
10.下列各组物质间的反应,由于现象不明显需要借助酸碱指示剂才能判断出反应发生的是( )
A.锌与稀盐酸
B.烧碱溶液与稀硫酸
C.氧化铁与稀硫酸
D.硫酸铜溶液与氢氧化钠溶液
11. 如图是稀HCl和NaOH溶液反应的pH变化曲线图,据图分析能得出的结论正确的是( )
A.该反应是NaOH溶液滴入稀盐酸
B.a克是指加入NaOH溶液的质量
C.A点时,溶液的溶质为NaOH、NaCl
D.B点表示稀盐酸和加入的NaOH溶液质量一定相同
12.下列试剂能将稀硫酸、氯化钠溶液、澄清石灰水三种溶液一步鉴别出来的是( )
A.稀盐酸 B.二氧化碳 C.碳酸钙 D.石蕊溶液
13.如图是稀硫酸与甲、乙、丙、丁、戊五种常见物质反应出现的不同现象。下列有关说法正确的是( )
A.甲可能是无色酚酞试液
B.乙、戊一定是金属单质
C.稀硫酸与丙生成的白色沉淀不可能属于盐
D.稀硫酸与丁的反应类型可能是置换反应
二、非选择题(本题共7个题,共32分)
14.(5分)硫酸、盐酸是重要的化工原料,广泛用于现代工业、生活中。
(1)浓硫酸在实验室常用作干燥剂,因为浓硫酸有 性。
(2)用适量的稀盐酸除去铁钉表面的铁锈,实验现象为 ,有关的化学方程式为 。
(3)请写出把硫酸转变为盐酸的化学方程式为 。
(4)盐酸的下列用途中,不能用硫酸代替盐酸的是 (填序号)。
A.金属表面除锈 B.制造药物氯化锌 C.实验室制取二氧化碳
15.(4分)化学项目组用“思维导图”来归纳总结碱的化学性质,根据碱的四条化学性质回答下列问题:
(1)碱溶液能使酚酞溶液变 色。
(2)图中的X代表一类物质,则X为 (填物质类别),请写出符合上述性质③的一个化学反应方程式为 。
(3)碱溶液有相似化学性质的原因是都含有 (填符号)。
16.(4分)某校化学课外活动小组在一次活动中,取刚降到地面的雨水水样,每隔5分钟用pH计测定一次pH,其数据如下表:
测定时刻 6︰05 6︰10 6︰15 6︰20 6︰25 6︰30
pH 4.95 4.94 4.94 4.88 4.86 4.85
已知:正常雨水的pH约为5.6,酸雨的pH小于5.6。
⑴所取的雨水是否属于酸雨 (填“属于”或“不属于”);在测定的期间,雨水水样的酸性随着时间的变化逐渐 (填“减弱”“无影响”或“增强”)。
⑵经调查,这一地区有一座燃煤发电厂,用火碱来吸收生产过程中产生的SO2,将其转化成亚硫酸钠。该反应的化学方程式 。
⑶若用pH试纸测定雨水的酸碱度,其中使用玻璃棒的作用是 。
17.(5分)化工产品是NaCl和NaOH组成的混合物。课外活动小组为测定该产品中NaCl的质量分数,进行了以下实验。取10.0g该固体样品置于锥形瓶中,加入适量的水配成溶液,逐滴加入溶质质量分数为10%的稀盐酸,用pH传感器等电子设备测得滴加过程中溶液的pH与加入稀盐酸的质量关系如图所示。请回答下列问题:
(1)恰好完全反应时,消耗稀盐酸中溶质的质量为 g。
(2)计算样品中NaCl的质量分数(写出计算过程)。
18.(4分) 如下图是包含物质A、B、C、D和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生反应。
(1)单质A不可能是 (填序号)。
A.Mg B.Fe C.Ag D.Zn
(2)若B为黑色的氧化铜,B与盐酸反应的化学方程式为 。
(3)若C为碳酸钠,C与足量的盐酸反应的化学方程式为 。
(4)若甲+乙→盐+水,根据“化学拼图”判断,一定符合条件的组合是 (填序号)。
①盐酸+A ②盐酸+B ③盐酸+C ④盐酸+D ⑤B+D
19.(5分)某兴趣小组同学开展跨学科实践活动,进行了“无形变有形”的创新实验。(装置气密性良好、部分仪器省略)。
(1)图1中,打开塑料瓶瓶盖,同时打开氧气传感器开关,得到了氧气体积分数随时间变化的曲线。AB段氧气体积分数逐渐降低,从微观角度解释其原因是 ,BC段氧气体积分数快速下册降,BC段对应的实验操作是 (写一种)。
(2)图2中,打开弹簧夹,向试管Ⅰ中加入一定量稀盐酸,关闭弹簧夹(保持导管口在液面以下)。观察到试管Ⅰ中有大量气泡产生且有液体流入试管Ⅱ中,产生此现象的原因是 。
(3)反应结束后,试管Ⅱ中的溶液由红色变为无色且无沉淀生成,试管Ⅱ中发生反应的化学方程式为 ,试管Ⅱ的溶液中一定含有的溶质是 (除酚酞以外)。
20.(5分)微型化学实验,因节能环保备受青睐,某化学兴趣小组设计了图1、图2两个微型实验,据图回答下列问题。
(1)如图1所示:在直径约为1.5cm的水滴两边,同时放少量硫酸铜晶体、氢氧化钠固体。已知:相对分子质量越大,微粒运动越慢,反之越快。实验中在 (填“A”或“B”)区域会先出现沉淀,反应的化学方程式为 。
(2)如图2所示:探究紫色石蕊溶液变色规律。
步骤1:向点滴板1~6号的孔穴中先加入如图2所示的试剂,再分别滴入2滴紫色石蕊溶液。6号孔穴中水的作用是 。
步骤2:将步骤1中所得的1号溶液和4号溶液互滴后溶液颜色发生明显变化,选出下列组合中互滴后溶液颜色有明显变化的是 (填序号)。
A.1号、5号 B.1号、3号 C.3号、4号 D.4号、5号
步骤3:重复步骤1,用吸管向5号孔穴吹入人呼出的气体,溶液表面出现白膜,写出反应的化学方程式为 。
同课章节目录
