第八章 常见的酸、碱、盐同步练习(含答案)---2023-2024学年九年级化学科粤版(2012)下册
文档属性
| 名称 | 第八章 常见的酸、碱、盐同步练习(含答案)---2023-2024学年九年级化学科粤版(2012)下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 337.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-19 00:00:00 | ||
图片预览


文档简介
第八章 常见的酸、碱、盐同步练习附答案2023—2024学年科粤版(2012)化学九年级下册
一、选择题。
1、某同学测定了生活中常见物质的pH,部分数据如下,其中酸性最强的是( )
A.洁厕剂:1 B.白醋:3 C.牙膏:9 D.洗发水:10
2、关于酸和碱的描述正确的是( )
A.紫色石蕊溶液遇碱溶液变蓝色 B.生石灰和熟石灰都属于碱
C.酸就是有酸味的物质 D.碱就是有腐蚀性的物质
3、若将100g10%的氢氧化钠溶液和100g10%稀盐酸混合,下列叙述正确的是( )
A.混合后溶液的pH =7
B.混合前后溶液的温度不变
C.混合后溶液的质量为200g
D.混合后溶液中溶质的质量分数仍为10%
4、下列各组物质的溶液,不用其他试剂就能鉴别的是( )
A.KCl、Ba(NO3)2、AgNO3、HCl
B.MgSO4、H2SO4、BaCl2、NaOH
C.FeCl3、NaOH、K2SO4、Ba(NO3) 2
D.MgCl2、BaCl2、NaOH、H2SO4
5、下列属于钾肥的是( )
A.NH4Cl B.K2CO3 C.NH4H2PO4 D.Ca3 (PO4)2
6、下列物质的化学式、俗名及所属类别的对应关系正确的是( )
A.NaOH 烧碱 盐 B.CO2固体 干冰 氧化物
C.NaHCO3 小苏打 酸 D.Hg 水银 非金属
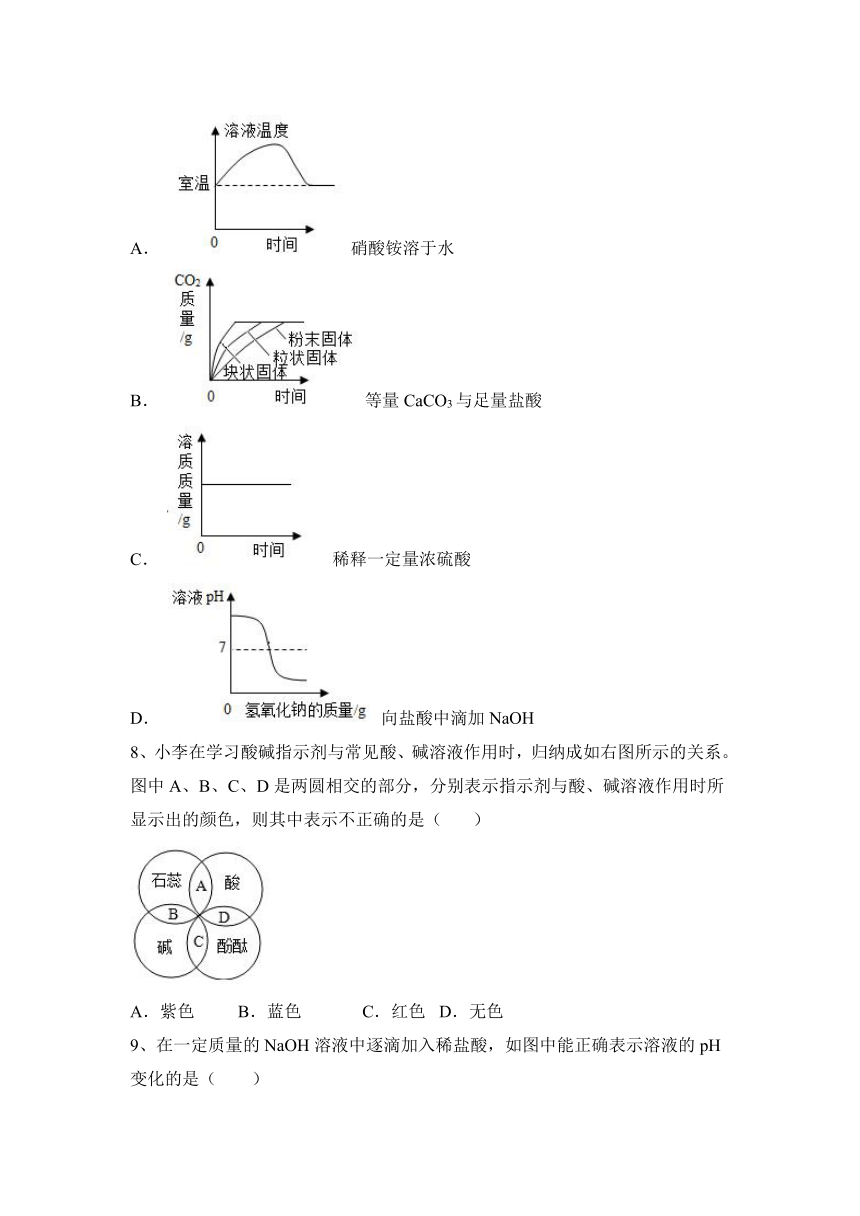
7、下列实验所示的图像中,其纵坐标随横坐标变化关系合理的是( )
A. 硝酸铵溶于水
B. 等量CaCO3与足量盐酸
C. 稀释一定量浓硫酸
D. 向盐酸中滴加NaOH
8、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
9、在一定质量的NaOH溶液中逐滴加入稀盐酸,如图中能正确表示溶液的pH变化的是( )
(横坐标表示加入稀盐酸的质量,纵坐标表示溶液的pH)
A. B.
C. D.
10、一包不纯的氯化钾粉末,所含杂质可能是氯化钠、硝酸钾、氯化钙、硝酸铜、碳酸钠中的一种或几种。为确定其成分,某兴趣小组的同学们进行如下实验:
(1)取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得无色澄清溶液。
(2)取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成。
(3)另称取149g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后生成28.7g白色沉淀。
根据上述实验判断,下列说法正确的是( )
A.杂质中可能含有硝酸钾、氯化钠
B.杂质中肯定不含硝酸钾、硝酸铜、碳酸钠
C.杂质中肯定含有碳酸钠,可能含有氯化钠
D.杂质中肯定含有氯化钠、碳酸钠,可能含有硝酸钾
11、下列化肥中,属于氮肥的是( )
A.氯化钾(KCl) B.碳酸钾(K2CO3)
C.尿素[CO(NH2)2] D.磷酸二氢钙[Ca(H2PO4)]
12、化学基本概念和原理对学习化学有重要的指导作用。下列说法中,错误的是( )
A.水通电发生分解反应,是破坏旧分子、形成新分子的过程
B.氧化物是指含有氧元素的化合物
C.化合物一定含有两种或两种以上元素
D.盐酸、硫酸有相似的化学性质,是因为它们的溶液中都存在H+
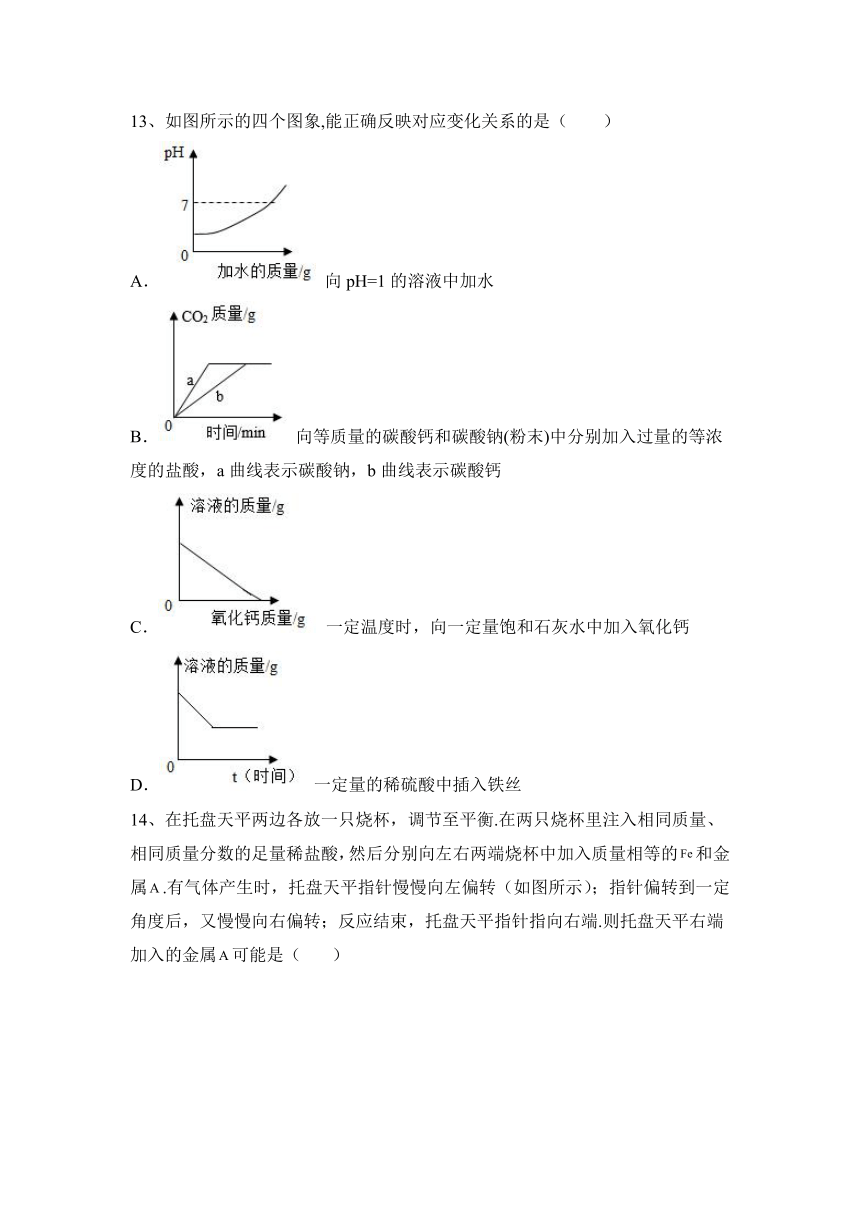
13、如图所示的四个图象,能正确反映对应变化关系的是( )
A. 向pH=1的溶液中加水
B. 向等质量的碳酸钙和碳酸钠(粉末)中分别加入过量的等浓度的盐酸,a曲线表示碳酸钠,b曲线表示碳酸钙
C. 一定温度时,向一定量饱和石灰水中加入氧化钙
D. 一定量的稀硫酸中插入铁丝
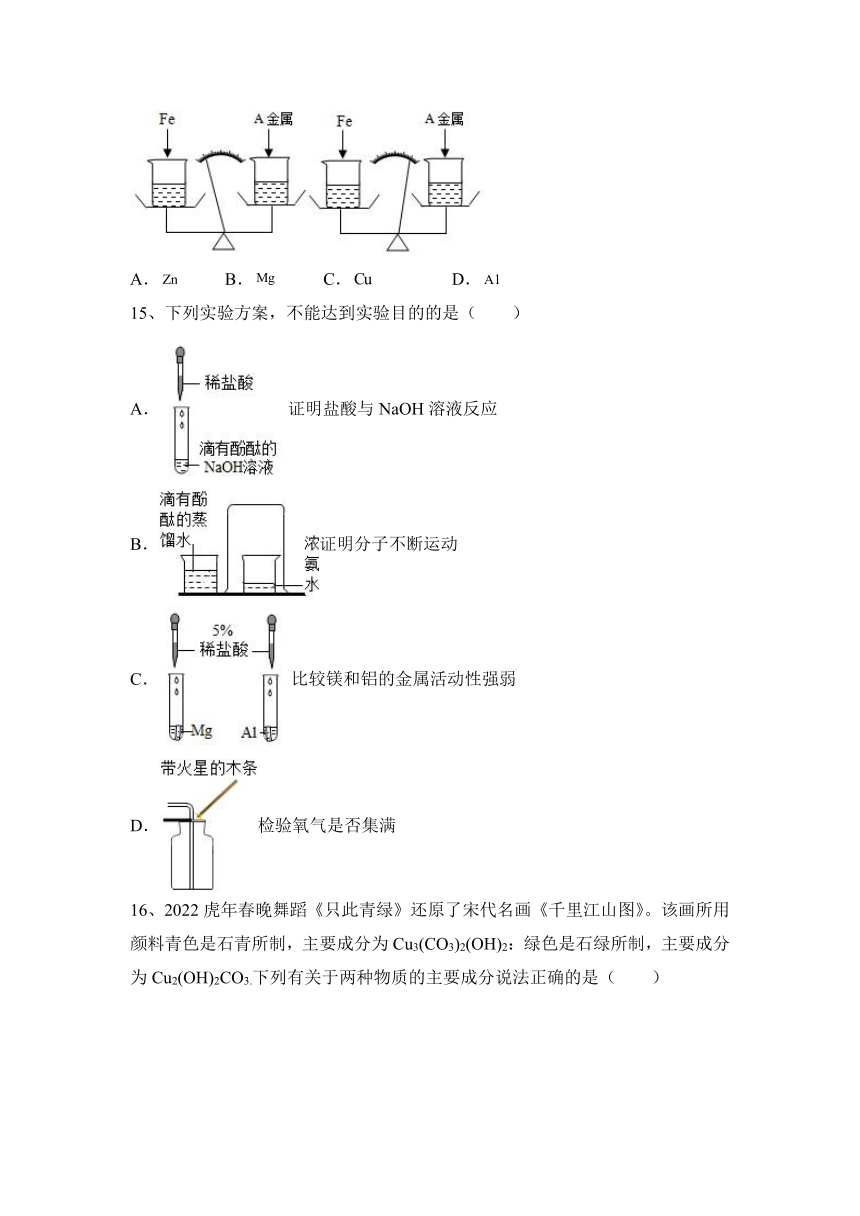
14、在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的和金属.有气体产生时,托盘天平指针慢慢向左偏转(如图所示);指针偏转到一定角度后,又慢慢向右偏转;反应结束,托盘天平指针指向右端.则托盘天平右端加入的金属可能是( )
A. B. C. D.
15、下列实验方案,不能达到实验目的的是( )
A.证明盐酸与NaOH溶液反应
B.证明分子不断运动
C.比较镁和铝的金属活动性强弱
D.检验氧气是否集满
16、2022虎年春晚舞蹈《只此青绿》还原了宋代名画《千里江山图》。该画所用颜料青色是石青所制,主要成分为Cu3(CO3)2(OH)2:绿色是石绿所制,主要成分为Cu2(OH)2CO3.下列有关于两种物质的主要成分说法正确的是( )
A.都属于碱 B.都由五种元素组成
C.都可以与盐酸反应 D.Cu元素的化合价不相同
二、填空题。
17、铅蓄电池在生产、生活中使用广泛,其构造如图所示,回答下列问题。
(1)铅蓄电池充电时是将电能转化为 ______ (填序号)。
A 机械能 B 热能 C 化学能
(2)铅蓄电池放电过程中,反应的化学方程式为:
,据此可知,铅蓄电池在放电时,溶液的pH不断 ______ (选填“增大”“减小”或“不变”)。
18、某实验小组探究酸的化学性质,在做盐酸除铁锈的实验时发现:
(1)将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为 ,待铁锈消失后又看到 现象。
(2)课后清洗仪器时,一同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为 溶液。
19、向盐酸中滴加氢氧化钠溶液时,当溶液的pH=5时,溶液显____性,溶液中的溶质是__________,(填化学式)当溶液的pH=7时,溶液显____性,溶液中的溶质是__________(填化学式),当溶液的pH=13时,溶液显____性,溶液中的溶质是_________(填化学式)。
20、Ba2+是有毒性的物质。
(1)对胃作X光造影时,BaSO4可用作钡餐而不造成中毒,这是因为________。
(2)若用BaCO3代替BaSO4,将导致中毒,这是因为________ 。
21、家用干粉灭火器,是利用压缩的二氧化碳吹干粉(主要含有磷酸二氢铵)来灭火的,灭火器的罐体有铝合金和铁质的,前者的使用年限约是后者的6倍。回答下列问题:
(1)二氧化碳可利用空气中含量最多的气体来代替,该气体是______(填化学式);
(2)磷酸二氢铵(NH4H2PO4)溶于水时与NH4NO3相似,会出现明显的______(填“升温”或“降温”)现象;
(3)NH4H2PO4在灭火时的作用之一是:它受热分解后在可燃物表面形成一层玻璃状的覆盖层。其灭火原理是______;
(4)为了变废为宝,报废灭火器中的NH4H2PO4可作为______(填写字母标号)使用。
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
(5)用化学知识解释,两种罐体的使用年限为什么不同?
______
______ 。
22、水是生命之源,也是工农业生产不可缺少的物质,合理利用和保护水资源是我们义不容辞的责任。
(1)利用如图所示的简易装置可把海水转化为淡水。下列说法错误的是 (填序号)。
a 小容器中的水为淡水
b 大容器中得到的溶液一定是氯化钠的饱和溶液
c 获得淡水的快慢与温度有关
(2)市售“自热米饭”的加热原理:饭盒夹层中的水与生石灰接触,反应发出大量热。该反应的化学方程式为 。
(3)自来水厂生产自来水的过程中,常加入 ,用来吸附水中一些溶解性的杂质,除去臭味。
三、实验与探究题。
23、实验是科学探究的重要方式,请结合图示回答下列问题:
(1)实验一可用于实验室检验二氧化碳气体,烧杯中应盛放的试剂是______,通入二氧化碳气体后,现象是_______。
(2)实验二是向一定量的水中不断通入二氧化碳气体,利用pH传感器采集到的数据如下图所示,可推测出混合后溶液显_______(填“酸性”或“碱性”),t1时刻后,溶液pH几乎无变化,其原因是__________(填字母序号)。
A.二氧化碳难溶于水
B.二氧化碳与水不能发生化学反应
C.二氧化碳在水中已经达饱和状态
(3)实验三可用于探究二氧化碳与氢氧化钠溶液的反应,该反应的化学方程式是_______,反应过程中利用pH传感器采集到的数据如下图所示,可推测出反应后减少的物质是_______。
(4)综上所述,对于有明显现象的化学反应,可借助生成沉淀或________等现象(写一条即可)判断化学反应是否发生:对于没有明显现象的化学反应,可以从验证反应物的减少或验证_______等角度来判断化学反应是否发生。
四、计算题。
24、侯德榜是我国著名的化学家,由他发明的侯氏制碱法制得的纯碱中可能含有少量杂质氯化钠,现取仅含氯化钠杂质的纯碱样品11g,加入93.4g 稀盐酸中,恰好完全反应,得氯化钠溶液100g。请计算:
(1)该纯碱样品中 Na2CO3的质量为 g。
(2)反应后所得溶液的溶质质量分数 。
第八章 常见的酸、碱、盐同步练习附答案2023—2024学年科粤版(2012)化学九年级下册
一、选择题。
1、某同学测定了生活中常见物质的pH,部分数据如下,其中酸性最强的是( )
A.洁厕剂:1 B.白醋:3 C.牙膏:9 D.洗发水:10
【答案】A
2、关于酸和碱的描述正确的是( )
A.紫色石蕊溶液遇碱溶液变蓝色 B.生石灰和熟石灰都属于碱
C.酸就是有酸味的物质 D.碱就是有腐蚀性的物质
【答案】A
3、若将100g10%的氢氧化钠溶液和100g10%稀盐酸混合,下列叙述正确的是( )
A.混合后溶液的pH =7
B.混合前后溶液的温度不变
C.混合后溶液的质量为200g
D.混合后溶液中溶质的质量分数仍为10%
【答案】C
4、下列各组物质的溶液,不用其他试剂就能鉴别的是( )
A.KCl、Ba(NO3)2、AgNO3、HCl
B.MgSO4、H2SO4、BaCl2、NaOH
C.FeCl3、NaOH、K2SO4、Ba(NO3) 2
D.MgCl2、BaCl2、NaOH、H2SO4
【答案】B
5、下列属于钾肥的是( )
A.NH4Cl B.K2CO3 C.NH4H2PO4 D.Ca3 (PO4)2
【答案】B
6、下列物质的化学式、俗名及所属类别的对应关系正确的是( )
A.NaOH 烧碱 盐 B.CO2固体 干冰 氧化物
C.NaHCO3 小苏打 酸 D.Hg 水银 非金属
【答案】B
7、下列实验所示的图像中,其纵坐标随横坐标变化关系合理的是( )
A. 硝酸铵溶于水
B. 等量CaCO3与足量盐酸
C. 稀释一定量浓硫酸
D. 向盐酸中滴加NaOH
【答案】C
8、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
【答案】A
9、在一定质量的NaOH溶液中逐滴加入稀盐酸,如图中能正确表示溶液的pH变化的是( )
(横坐标表示加入稀盐酸的质量,纵坐标表示溶液的pH)
A. B.
C. D.
【答案】B
10、一包不纯的氯化钾粉末,所含杂质可能是氯化钠、硝酸钾、氯化钙、硝酸铜、碳酸钠中的一种或几种。为确定其成分,某兴趣小组的同学们进行如下实验:
(1)取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得无色澄清溶液。
(2)取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成。
(3)另称取149g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后生成28.7g白色沉淀。
根据上述实验判断,下列说法正确的是( )
A.杂质中可能含有硝酸钾、氯化钠
B.杂质中肯定不含硝酸钾、硝酸铜、碳酸钠
C.杂质中肯定含有碳酸钠,可能含有氯化钠
D.杂质中肯定含有氯化钠、碳酸钠,可能含有硝酸钾
【答案】D
11、下列化肥中,属于氮肥的是( )
A.氯化钾(KCl) B.碳酸钾(K2CO3)
C.尿素[CO(NH2)2] D.磷酸二氢钙[Ca(H2PO4)]
【答案】C
12、化学基本概念和原理对学习化学有重要的指导作用。下列说法中,错误的是( )
A.水通电发生分解反应,是破坏旧分子、形成新分子的过程
B.氧化物是指含有氧元素的化合物
C.化合物一定含有两种或两种以上元素
D.盐酸、硫酸有相似的化学性质,是因为它们的溶液中都存在H+
【答案】B
13、如图所示的四个图象,能正确反映对应变化关系的是( )
A. 向pH=1的溶液中加水
B. 向等质量的碳酸钙和碳酸钠(粉末)中分别加入过量的等浓度的盐酸,a曲线表示碳酸钠,b曲线表示碳酸钙
C. 一定温度时,向一定量饱和石灰水中加入氧化钙
D. 一定量的稀硫酸中插入铁丝
【答案】C
14、在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的和金属.有气体产生时,托盘天平指针慢慢向左偏转(如图所示);指针偏转到一定角度后,又慢慢向右偏转;反应结束,托盘天平指针指向右端.则托盘天平右端加入的金属可能是( )
A. B. C. D.
【答案】A
15、下列实验方案,不能达到实验目的的是( )
A.证明盐酸与NaOH溶液反应
B.证明分子不断运动
C.比较镁和铝的金属活动性强弱
D.检验氧气是否集满
【答案】B
16、2022虎年春晚舞蹈《只此青绿》还原了宋代名画《千里江山图》。该画所用颜料青色是石青所制,主要成分为Cu3(CO3)2(OH)2:绿色是石绿所制,主要成分为Cu2(OH)2CO3.下列有关于两种物质的主要成分说法正确的是( )
A.都属于碱 B.都由五种元素组成
C.都可以与盐酸反应 D.Cu元素的化合价不相同
【答案】C
二、填空题。
17、铅蓄电池在生产、生活中使用广泛,其构造如图所示,回答下列问题。
(1)铅蓄电池充电时是将电能转化为 ______ (填序号)。
A 机械能 B 热能 C 化学能
(2)铅蓄电池放电过程中,反应的化学方程式为:
,据此可知,铅蓄电池在放电时,溶液的pH不断 ______ (选填“增大”“减小”或“不变”)。
【答案】C 增大
18、某实验小组探究酸的化学性质,在做盐酸除铁锈的实验时发现:
(1)将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为 ,待铁锈消失后又看到 现象。
(2)课后清洗仪器时,一同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为 溶液。
【答案】;有气泡产生;氯化亚铁
19、向盐酸中滴加氢氧化钠溶液时,当溶液的pH=5时,溶液显____性,溶液中的溶质是__________,(填化学式)当溶液的pH=7时,溶液显____性,溶液中的溶质是__________(填化学式),当溶液的pH=13时,溶液显____性,溶液中的溶质是_________(填化学式)。
【答案】酸 HCl和NaCl 中 NaCl 碱 NaCl和NaOH
20、Ba2+是有毒性的物质。
(1)对胃作X光造影时,BaSO4可用作钡餐而不造成中毒,这是因为________。
(2)若用BaCO3代替BaSO4,将导致中毒,这是因为________ 。
【答案】硫酸钡不溶解. 碳酸钡溶于胃酸
21、家用干粉灭火器,是利用压缩的二氧化碳吹干粉(主要含有磷酸二氢铵)来灭火的,灭火器的罐体有铝合金和铁质的,前者的使用年限约是后者的6倍。回答下列问题:
(1)二氧化碳可利用空气中含量最多的气体来代替,该气体是______(填化学式);
(2)磷酸二氢铵(NH4H2PO4)溶于水时与NH4NO3相似,会出现明显的______(填“升温”或“降温”)现象;
(3)NH4H2PO4在灭火时的作用之一是:它受热分解后在可燃物表面形成一层玻璃状的覆盖层。其灭火原理是______;
(4)为了变废为宝,报废灭火器中的NH4H2PO4可作为______(填写字母标号)使用。
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
(5)用化学知识解释,两种罐体的使用年限为什么不同?
______
______ 。
【答案】(1)N2 (2)降温 (3)隔绝空气(或隔绝氧气) (4)D
(5)合金的硬度大,耐腐蚀,而铁易生锈。铁在空气中容易生锈,铝在空气中能被氧气氧化成一层致密而坚硬的氧化物薄膜,对铝起保护作用
22、水是生命之源,也是工农业生产不可缺少的物质,合理利用和保护水资源是我们义不容辞的责任。
(1)利用如图所示的简易装置可把海水转化为淡水。下列说法错误的是 (填序号)。
a 小容器中的水为淡水
b 大容器中得到的溶液一定是氯化钠的饱和溶液
c 获得淡水的快慢与温度有关
(2)市售“自热米饭”的加热原理:饭盒夹层中的水与生石灰接触,反应发出大量热。该反应的化学方程式为 。
(3)自来水厂生产自来水的过程中,常加入 ,用来吸附水中一些溶解性的杂质,除去臭味。
【答案】b 活性炭
三、实验与探究题。
23、实验是科学探究的重要方式,请结合图示回答下列问题:
(1)实验一可用于实验室检验二氧化碳气体,烧杯中应盛放的试剂是______,通入二氧化碳气体后,现象是_______。
(2)实验二是向一定量的水中不断通入二氧化碳气体,利用pH传感器采集到的数据如下图所示,可推测出混合后溶液显_______(填“酸性”或“碱性”),t1时刻后,溶液pH几乎无变化,其原因是__________(填字母序号)。
A.二氧化碳难溶于水
B.二氧化碳与水不能发生化学反应
C.二氧化碳在水中已经达饱和状态
(3)实验三可用于探究二氧化碳与氢氧化钠溶液的反应,该反应的化学方程式是_______,反应过程中利用pH传感器采集到的数据如下图所示,可推测出反应后减少的物质是_______。
(4)综上所述,对于有明显现象的化学反应,可借助生成沉淀或________等现象(写一条即可)判断化学反应是否发生:对于没有明显现象的化学反应,可以从验证反应物的减少或验证_______等角度来判断化学反应是否发生。
【答案】(1) 澄清石灰水 澄清石灰水变浑浊 (2)酸性 C
(3) 氢氧化钠【NaOH】
(4) 气体(或颜色等合理即可) 生成物的生成
四、计算题。
24、侯德榜是我国著名的化学家,由他发明的侯氏制碱法制得的纯碱中可能含有少量杂质氯化钠,现取仅含氯化钠杂质的纯碱样品11g,加入93.4g 稀盐酸中,恰好完全反应,得氯化钠溶液100g。请计算:
(1)该纯碱样品中 Na2CO3的质量为 g。
(2)反应后所得溶液的溶质质量分数 。
【答案】(1)10.6 (2)12.1%。
【详解】(2)设生成的氯化钠质量为y,则
由(1)可知,样品中含有的氯化钠质量为
故反应后所得溶液的溶质质量分数为
答:反应后所得溶液的溶质质量分数为12.1%。
一、选择题。
1、某同学测定了生活中常见物质的pH,部分数据如下,其中酸性最强的是( )
A.洁厕剂:1 B.白醋:3 C.牙膏:9 D.洗发水:10
2、关于酸和碱的描述正确的是( )
A.紫色石蕊溶液遇碱溶液变蓝色 B.生石灰和熟石灰都属于碱
C.酸就是有酸味的物质 D.碱就是有腐蚀性的物质
3、若将100g10%的氢氧化钠溶液和100g10%稀盐酸混合,下列叙述正确的是( )
A.混合后溶液的pH =7
B.混合前后溶液的温度不变
C.混合后溶液的质量为200g
D.混合后溶液中溶质的质量分数仍为10%
4、下列各组物质的溶液,不用其他试剂就能鉴别的是( )
A.KCl、Ba(NO3)2、AgNO3、HCl
B.MgSO4、H2SO4、BaCl2、NaOH
C.FeCl3、NaOH、K2SO4、Ba(NO3) 2
D.MgCl2、BaCl2、NaOH、H2SO4
5、下列属于钾肥的是( )
A.NH4Cl B.K2CO3 C.NH4H2PO4 D.Ca3 (PO4)2
6、下列物质的化学式、俗名及所属类别的对应关系正确的是( )
A.NaOH 烧碱 盐 B.CO2固体 干冰 氧化物
C.NaHCO3 小苏打 酸 D.Hg 水银 非金属
7、下列实验所示的图像中,其纵坐标随横坐标变化关系合理的是( )
A. 硝酸铵溶于水
B. 等量CaCO3与足量盐酸
C. 稀释一定量浓硫酸
D. 向盐酸中滴加NaOH
8、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
9、在一定质量的NaOH溶液中逐滴加入稀盐酸,如图中能正确表示溶液的pH变化的是( )
(横坐标表示加入稀盐酸的质量,纵坐标表示溶液的pH)
A. B.
C. D.
10、一包不纯的氯化钾粉末,所含杂质可能是氯化钠、硝酸钾、氯化钙、硝酸铜、碳酸钠中的一种或几种。为确定其成分,某兴趣小组的同学们进行如下实验:
(1)取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得无色澄清溶液。
(2)取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成。
(3)另称取149g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后生成28.7g白色沉淀。
根据上述实验判断,下列说法正确的是( )
A.杂质中可能含有硝酸钾、氯化钠
B.杂质中肯定不含硝酸钾、硝酸铜、碳酸钠
C.杂质中肯定含有碳酸钠,可能含有氯化钠
D.杂质中肯定含有氯化钠、碳酸钠,可能含有硝酸钾
11、下列化肥中,属于氮肥的是( )
A.氯化钾(KCl) B.碳酸钾(K2CO3)
C.尿素[CO(NH2)2] D.磷酸二氢钙[Ca(H2PO4)]
12、化学基本概念和原理对学习化学有重要的指导作用。下列说法中,错误的是( )
A.水通电发生分解反应,是破坏旧分子、形成新分子的过程
B.氧化物是指含有氧元素的化合物
C.化合物一定含有两种或两种以上元素
D.盐酸、硫酸有相似的化学性质,是因为它们的溶液中都存在H+
13、如图所示的四个图象,能正确反映对应变化关系的是( )
A. 向pH=1的溶液中加水
B. 向等质量的碳酸钙和碳酸钠(粉末)中分别加入过量的等浓度的盐酸,a曲线表示碳酸钠,b曲线表示碳酸钙
C. 一定温度时,向一定量饱和石灰水中加入氧化钙
D. 一定量的稀硫酸中插入铁丝
14、在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的和金属.有气体产生时,托盘天平指针慢慢向左偏转(如图所示);指针偏转到一定角度后,又慢慢向右偏转;反应结束,托盘天平指针指向右端.则托盘天平右端加入的金属可能是( )
A. B. C. D.
15、下列实验方案,不能达到实验目的的是( )
A.证明盐酸与NaOH溶液反应
B.证明分子不断运动
C.比较镁和铝的金属活动性强弱
D.检验氧气是否集满
16、2022虎年春晚舞蹈《只此青绿》还原了宋代名画《千里江山图》。该画所用颜料青色是石青所制,主要成分为Cu3(CO3)2(OH)2:绿色是石绿所制,主要成分为Cu2(OH)2CO3.下列有关于两种物质的主要成分说法正确的是( )
A.都属于碱 B.都由五种元素组成
C.都可以与盐酸反应 D.Cu元素的化合价不相同
二、填空题。
17、铅蓄电池在生产、生活中使用广泛,其构造如图所示,回答下列问题。
(1)铅蓄电池充电时是将电能转化为 ______ (填序号)。
A 机械能 B 热能 C 化学能
(2)铅蓄电池放电过程中,反应的化学方程式为:
,据此可知,铅蓄电池在放电时,溶液的pH不断 ______ (选填“增大”“减小”或“不变”)。
18、某实验小组探究酸的化学性质,在做盐酸除铁锈的实验时发现:
(1)将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为 ,待铁锈消失后又看到 现象。
(2)课后清洗仪器时,一同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为 溶液。
19、向盐酸中滴加氢氧化钠溶液时,当溶液的pH=5时,溶液显____性,溶液中的溶质是__________,(填化学式)当溶液的pH=7时,溶液显____性,溶液中的溶质是__________(填化学式),当溶液的pH=13时,溶液显____性,溶液中的溶质是_________(填化学式)。
20、Ba2+是有毒性的物质。
(1)对胃作X光造影时,BaSO4可用作钡餐而不造成中毒,这是因为________。
(2)若用BaCO3代替BaSO4,将导致中毒,这是因为________ 。
21、家用干粉灭火器,是利用压缩的二氧化碳吹干粉(主要含有磷酸二氢铵)来灭火的,灭火器的罐体有铝合金和铁质的,前者的使用年限约是后者的6倍。回答下列问题:
(1)二氧化碳可利用空气中含量最多的气体来代替,该气体是______(填化学式);
(2)磷酸二氢铵(NH4H2PO4)溶于水时与NH4NO3相似,会出现明显的______(填“升温”或“降温”)现象;
(3)NH4H2PO4在灭火时的作用之一是:它受热分解后在可燃物表面形成一层玻璃状的覆盖层。其灭火原理是______;
(4)为了变废为宝,报废灭火器中的NH4H2PO4可作为______(填写字母标号)使用。
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
(5)用化学知识解释,两种罐体的使用年限为什么不同?
______
______ 。
22、水是生命之源,也是工农业生产不可缺少的物质,合理利用和保护水资源是我们义不容辞的责任。
(1)利用如图所示的简易装置可把海水转化为淡水。下列说法错误的是 (填序号)。
a 小容器中的水为淡水
b 大容器中得到的溶液一定是氯化钠的饱和溶液
c 获得淡水的快慢与温度有关
(2)市售“自热米饭”的加热原理:饭盒夹层中的水与生石灰接触,反应发出大量热。该反应的化学方程式为 。
(3)自来水厂生产自来水的过程中,常加入 ,用来吸附水中一些溶解性的杂质,除去臭味。
三、实验与探究题。
23、实验是科学探究的重要方式,请结合图示回答下列问题:
(1)实验一可用于实验室检验二氧化碳气体,烧杯中应盛放的试剂是______,通入二氧化碳气体后,现象是_______。
(2)实验二是向一定量的水中不断通入二氧化碳气体,利用pH传感器采集到的数据如下图所示,可推测出混合后溶液显_______(填“酸性”或“碱性”),t1时刻后,溶液pH几乎无变化,其原因是__________(填字母序号)。
A.二氧化碳难溶于水
B.二氧化碳与水不能发生化学反应
C.二氧化碳在水中已经达饱和状态
(3)实验三可用于探究二氧化碳与氢氧化钠溶液的反应,该反应的化学方程式是_______,反应过程中利用pH传感器采集到的数据如下图所示,可推测出反应后减少的物质是_______。
(4)综上所述,对于有明显现象的化学反应,可借助生成沉淀或________等现象(写一条即可)判断化学反应是否发生:对于没有明显现象的化学反应,可以从验证反应物的减少或验证_______等角度来判断化学反应是否发生。
四、计算题。
24、侯德榜是我国著名的化学家,由他发明的侯氏制碱法制得的纯碱中可能含有少量杂质氯化钠,现取仅含氯化钠杂质的纯碱样品11g,加入93.4g 稀盐酸中,恰好完全反应,得氯化钠溶液100g。请计算:
(1)该纯碱样品中 Na2CO3的质量为 g。
(2)反应后所得溶液的溶质质量分数 。
第八章 常见的酸、碱、盐同步练习附答案2023—2024学年科粤版(2012)化学九年级下册
一、选择题。
1、某同学测定了生活中常见物质的pH,部分数据如下,其中酸性最强的是( )
A.洁厕剂:1 B.白醋:3 C.牙膏:9 D.洗发水:10
【答案】A
2、关于酸和碱的描述正确的是( )
A.紫色石蕊溶液遇碱溶液变蓝色 B.生石灰和熟石灰都属于碱
C.酸就是有酸味的物质 D.碱就是有腐蚀性的物质
【答案】A
3、若将100g10%的氢氧化钠溶液和100g10%稀盐酸混合,下列叙述正确的是( )
A.混合后溶液的pH =7
B.混合前后溶液的温度不变
C.混合后溶液的质量为200g
D.混合后溶液中溶质的质量分数仍为10%
【答案】C
4、下列各组物质的溶液,不用其他试剂就能鉴别的是( )
A.KCl、Ba(NO3)2、AgNO3、HCl
B.MgSO4、H2SO4、BaCl2、NaOH
C.FeCl3、NaOH、K2SO4、Ba(NO3) 2
D.MgCl2、BaCl2、NaOH、H2SO4
【答案】B
5、下列属于钾肥的是( )
A.NH4Cl B.K2CO3 C.NH4H2PO4 D.Ca3 (PO4)2
【答案】B
6、下列物质的化学式、俗名及所属类别的对应关系正确的是( )
A.NaOH 烧碱 盐 B.CO2固体 干冰 氧化物
C.NaHCO3 小苏打 酸 D.Hg 水银 非金属
【答案】B
7、下列实验所示的图像中,其纵坐标随横坐标变化关系合理的是( )
A. 硝酸铵溶于水
B. 等量CaCO3与足量盐酸
C. 稀释一定量浓硫酸
D. 向盐酸中滴加NaOH
【答案】C
8、小李在学习酸碱指示剂与常见酸、碱溶液作用时,归纳成如右图所示的关系。图中A、B、C、D是两圆相交的部分,分别表示指示剂与酸、碱溶液作用时所显示出的颜色,则其中表示不正确的是( )
A.紫色 B.蓝色 C.红色 D.无色
【答案】A
9、在一定质量的NaOH溶液中逐滴加入稀盐酸,如图中能正确表示溶液的pH变化的是( )
(横坐标表示加入稀盐酸的质量,纵坐标表示溶液的pH)
A. B.
C. D.
【答案】B
10、一包不纯的氯化钾粉末,所含杂质可能是氯化钠、硝酸钾、氯化钙、硝酸铜、碳酸钠中的一种或几种。为确定其成分,某兴趣小组的同学们进行如下实验:
(1)取少量该粉末于烧杯中,加蒸馏水,充分搅拌,得无色澄清溶液。
(2)取上述无色溶液少许于试管中,滴加氯化钡溶液有白色沉淀生成。
(3)另称取149g该粉末于烧杯中,加入蒸馏水溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后生成28.7g白色沉淀。
根据上述实验判断,下列说法正确的是( )
A.杂质中可能含有硝酸钾、氯化钠
B.杂质中肯定不含硝酸钾、硝酸铜、碳酸钠
C.杂质中肯定含有碳酸钠,可能含有氯化钠
D.杂质中肯定含有氯化钠、碳酸钠,可能含有硝酸钾
【答案】D
11、下列化肥中,属于氮肥的是( )
A.氯化钾(KCl) B.碳酸钾(K2CO3)
C.尿素[CO(NH2)2] D.磷酸二氢钙[Ca(H2PO4)]
【答案】C
12、化学基本概念和原理对学习化学有重要的指导作用。下列说法中,错误的是( )
A.水通电发生分解反应,是破坏旧分子、形成新分子的过程
B.氧化物是指含有氧元素的化合物
C.化合物一定含有两种或两种以上元素
D.盐酸、硫酸有相似的化学性质,是因为它们的溶液中都存在H+
【答案】B
13、如图所示的四个图象,能正确反映对应变化关系的是( )
A. 向pH=1的溶液中加水
B. 向等质量的碳酸钙和碳酸钠(粉末)中分别加入过量的等浓度的盐酸,a曲线表示碳酸钠,b曲线表示碳酸钙
C. 一定温度时,向一定量饱和石灰水中加入氧化钙
D. 一定量的稀硫酸中插入铁丝
【答案】C
14、在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的和金属.有气体产生时,托盘天平指针慢慢向左偏转(如图所示);指针偏转到一定角度后,又慢慢向右偏转;反应结束,托盘天平指针指向右端.则托盘天平右端加入的金属可能是( )
A. B. C. D.
【答案】A
15、下列实验方案,不能达到实验目的的是( )
A.证明盐酸与NaOH溶液反应
B.证明分子不断运动
C.比较镁和铝的金属活动性强弱
D.检验氧气是否集满
【答案】B
16、2022虎年春晚舞蹈《只此青绿》还原了宋代名画《千里江山图》。该画所用颜料青色是石青所制,主要成分为Cu3(CO3)2(OH)2:绿色是石绿所制,主要成分为Cu2(OH)2CO3.下列有关于两种物质的主要成分说法正确的是( )
A.都属于碱 B.都由五种元素组成
C.都可以与盐酸反应 D.Cu元素的化合价不相同
【答案】C
二、填空题。
17、铅蓄电池在生产、生活中使用广泛,其构造如图所示,回答下列问题。
(1)铅蓄电池充电时是将电能转化为 ______ (填序号)。
A 机械能 B 热能 C 化学能
(2)铅蓄电池放电过程中,反应的化学方程式为:
,据此可知,铅蓄电池在放电时,溶液的pH不断 ______ (选填“增大”“减小”或“不变”)。
【答案】C 增大
18、某实验小组探究酸的化学性质,在做盐酸除铁锈的实验时发现:
(1)将带锈铁钉放入试管后加入稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为 ,待铁锈消失后又看到 现象。
(2)课后清洗仪器时,一同学发现试管中的黄色溶液变成浅绿色,表明此时的溶液已变为 溶液。
【答案】;有气泡产生;氯化亚铁
19、向盐酸中滴加氢氧化钠溶液时,当溶液的pH=5时,溶液显____性,溶液中的溶质是__________,(填化学式)当溶液的pH=7时,溶液显____性,溶液中的溶质是__________(填化学式),当溶液的pH=13时,溶液显____性,溶液中的溶质是_________(填化学式)。
【答案】酸 HCl和NaCl 中 NaCl 碱 NaCl和NaOH
20、Ba2+是有毒性的物质。
(1)对胃作X光造影时,BaSO4可用作钡餐而不造成中毒,这是因为________。
(2)若用BaCO3代替BaSO4,将导致中毒,这是因为________ 。
【答案】硫酸钡不溶解. 碳酸钡溶于胃酸
21、家用干粉灭火器,是利用压缩的二氧化碳吹干粉(主要含有磷酸二氢铵)来灭火的,灭火器的罐体有铝合金和铁质的,前者的使用年限约是后者的6倍。回答下列问题:
(1)二氧化碳可利用空气中含量最多的气体来代替,该气体是______(填化学式);
(2)磷酸二氢铵(NH4H2PO4)溶于水时与NH4NO3相似,会出现明显的______(填“升温”或“降温”)现象;
(3)NH4H2PO4在灭火时的作用之一是:它受热分解后在可燃物表面形成一层玻璃状的覆盖层。其灭火原理是______;
(4)为了变废为宝,报废灭火器中的NH4H2PO4可作为______(填写字母标号)使用。
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
(5)用化学知识解释,两种罐体的使用年限为什么不同?
______
______ 。
【答案】(1)N2 (2)降温 (3)隔绝空气(或隔绝氧气) (4)D
(5)合金的硬度大,耐腐蚀,而铁易生锈。铁在空气中容易生锈,铝在空气中能被氧气氧化成一层致密而坚硬的氧化物薄膜,对铝起保护作用
22、水是生命之源,也是工农业生产不可缺少的物质,合理利用和保护水资源是我们义不容辞的责任。
(1)利用如图所示的简易装置可把海水转化为淡水。下列说法错误的是 (填序号)。
a 小容器中的水为淡水
b 大容器中得到的溶液一定是氯化钠的饱和溶液
c 获得淡水的快慢与温度有关
(2)市售“自热米饭”的加热原理:饭盒夹层中的水与生石灰接触,反应发出大量热。该反应的化学方程式为 。
(3)自来水厂生产自来水的过程中,常加入 ,用来吸附水中一些溶解性的杂质,除去臭味。
【答案】b 活性炭
三、实验与探究题。
23、实验是科学探究的重要方式,请结合图示回答下列问题:
(1)实验一可用于实验室检验二氧化碳气体,烧杯中应盛放的试剂是______,通入二氧化碳气体后,现象是_______。
(2)实验二是向一定量的水中不断通入二氧化碳气体,利用pH传感器采集到的数据如下图所示,可推测出混合后溶液显_______(填“酸性”或“碱性”),t1时刻后,溶液pH几乎无变化,其原因是__________(填字母序号)。
A.二氧化碳难溶于水
B.二氧化碳与水不能发生化学反应
C.二氧化碳在水中已经达饱和状态
(3)实验三可用于探究二氧化碳与氢氧化钠溶液的反应,该反应的化学方程式是_______,反应过程中利用pH传感器采集到的数据如下图所示,可推测出反应后减少的物质是_______。
(4)综上所述,对于有明显现象的化学反应,可借助生成沉淀或________等现象(写一条即可)判断化学反应是否发生:对于没有明显现象的化学反应,可以从验证反应物的减少或验证_______等角度来判断化学反应是否发生。
【答案】(1) 澄清石灰水 澄清石灰水变浑浊 (2)酸性 C
(3) 氢氧化钠【NaOH】
(4) 气体(或颜色等合理即可) 生成物的生成
四、计算题。
24、侯德榜是我国著名的化学家,由他发明的侯氏制碱法制得的纯碱中可能含有少量杂质氯化钠,现取仅含氯化钠杂质的纯碱样品11g,加入93.4g 稀盐酸中,恰好完全反应,得氯化钠溶液100g。请计算:
(1)该纯碱样品中 Na2CO3的质量为 g。
(2)反应后所得溶液的溶质质量分数 。
【答案】(1)10.6 (2)12.1%。
【详解】(2)设生成的氯化钠质量为y,则
由(1)可知,样品中含有的氯化钠质量为
故反应后所得溶液的溶质质量分数为
答:反应后所得溶液的溶质质量分数为12.1%。
