第九单元金属课后题附答案2023—2024学年鲁教版化学九年级下册(含答案)
文档属性
| 名称 | 第九单元金属课后题附答案2023—2024学年鲁教版化学九年级下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 269.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-19 00:00:00 | ||
图片预览



文档简介
第九单元 金属课后题附答案2023—2024学年鲁教版化学九年级下册
一、选择题。
1、哈尔滨的太阳岛公园是中外游客向往的旅游胜地,下列叙述错误的是( )
A.欧式灯饰外框用的黄铜主要成分是铜和锡
B.紫丁香树的种植可以提高公园内空气质量
C.铺设宽阔的柏油路面所用的沥青是石油炼制的产品
D.大理石围栏主要成分是碳酸钙
2、某兴趣小组进行实验探究,向盛有硝酸亚铁和硝酸银混合液的烧杯中加入一定量的锌粉,反应停止后过滤,向滤渣中加入稀盐酸,有气泡产生。下列说法正确的是( )
A.滤液中一定含有Zn2+和Fe2+,一定没有Ag+
B.滤液中一定含有Zn2+,一定没有Fe2+和Ag+
C.滤渣中一定含有银和铁,可能含有锌
D.滤渣中一定含有银,可能含有锌和铁
3、下列物质中不能由金属单质和盐酸直接反应生成的是( )
A. B. C. D.AlCl3
4、日常生活中的一些铁制品经常会被锈蚀,下列做法中不能起防锈作用的是( )
①在铁制品表面镀锌 ②在铁制品表面涂油脂 ③在铁制品表面覆盖搪瓷 ④在铁器表面刷油漆
⑤自行车脏了用清水冲洗 ⑥用废酸液冲洗铁制污水管道 ⑦切完咸菜后,尽快将菜刀洗净擦干
⑧保留铁件表面的铁锈作保护层.
A.①③⑦ B.②④ C.⑤⑥⑧ D.①⑦
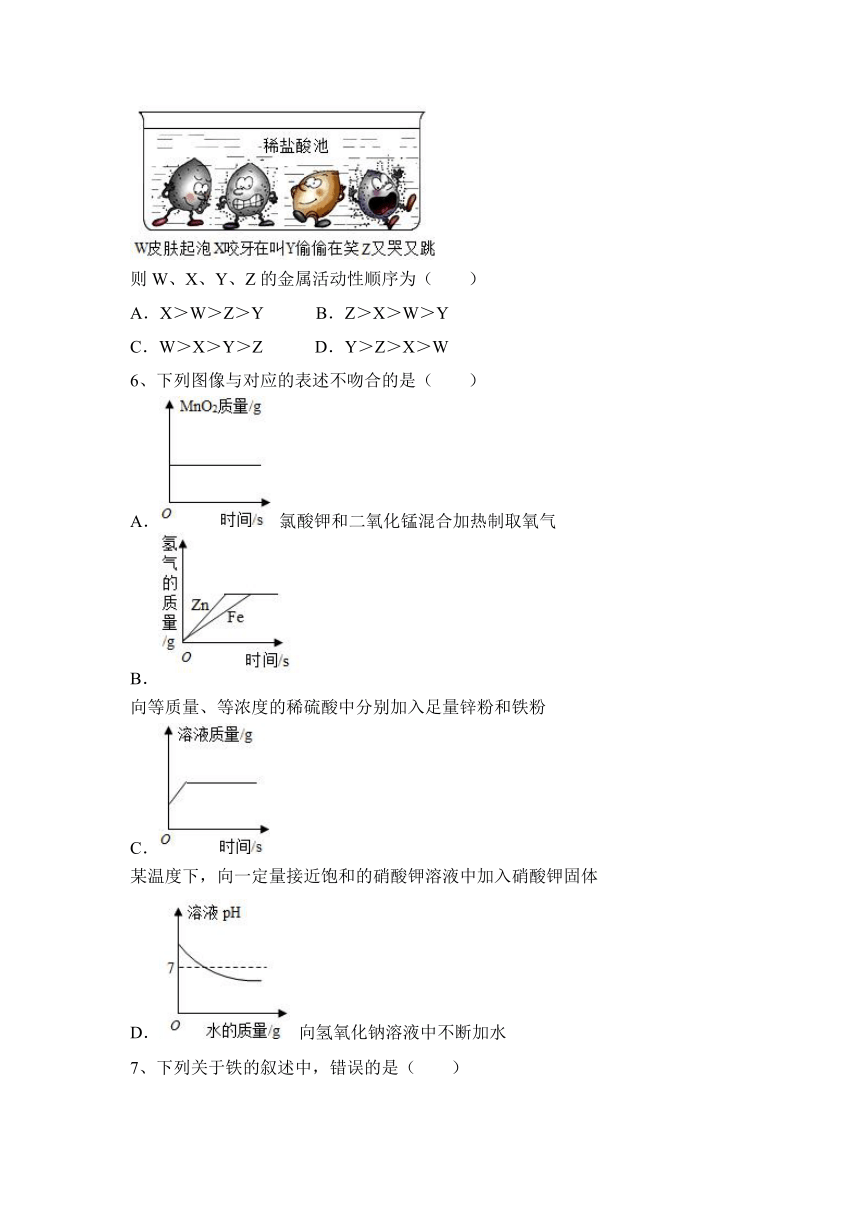
5、金属单质家族四兄弟W、X、Y、Z,不小心掉入稀盐酸池,神情如图所示:
则W、X、Y、Z的金属活动性顺序为( )
A.X>W>Z>Y B.Z>X>W>Y
C.W>X>Y>Z D.Y>Z>X>W
6、下列图像与对应的表述不吻合的是( )
A. 氯酸钾和二氧化锰混合加热制取氧气
B.
向等质量、等浓度的稀硫酸中分别加入足量锌粉和铁粉
C.
某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
D. 向氢氧化钠溶液中不断加水
7、下列关于铁的叙述中,错误的是( )
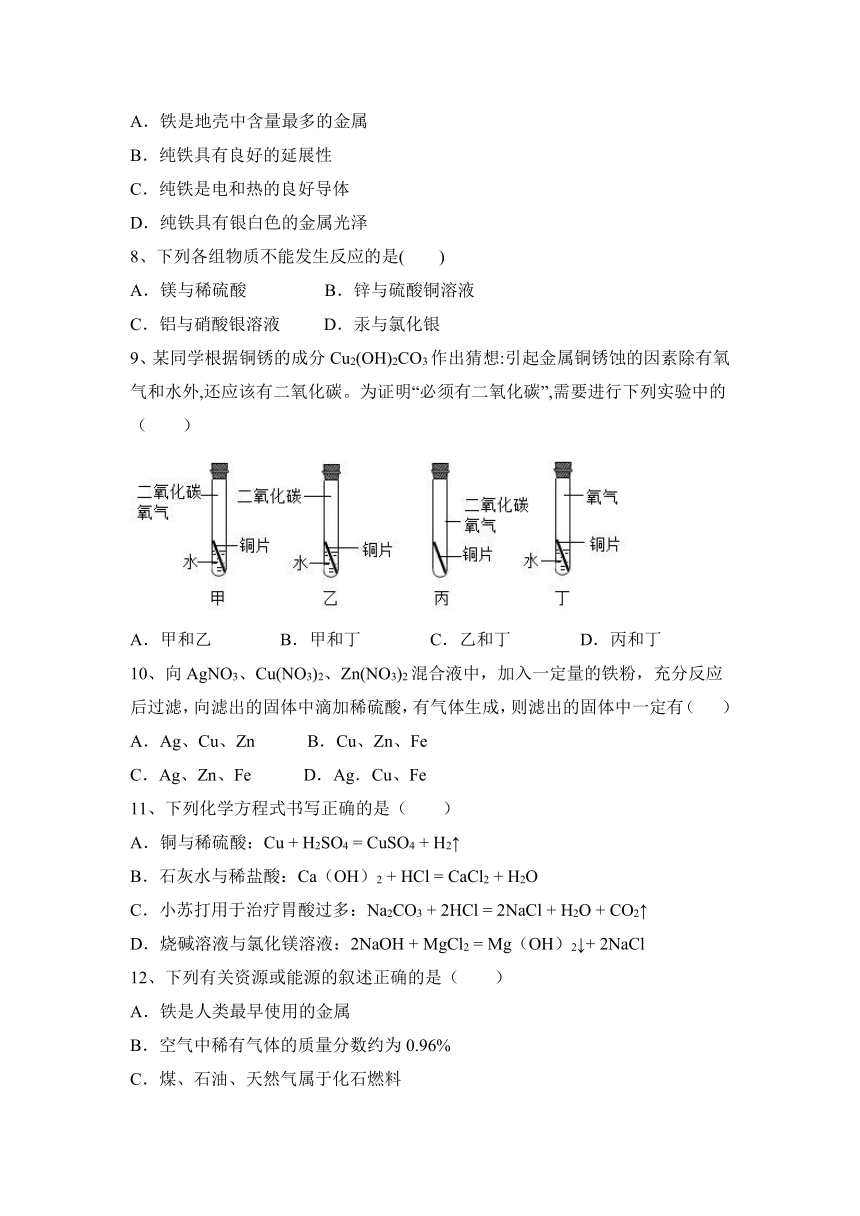
A.铁是地壳中含量最多的金属
B.纯铁具有良好的延展性
C.纯铁是电和热的良好导体
D.纯铁具有银白色的金属光泽
8、下列各组物质不能发生反应的是( )
A.镁与稀硫酸 B.锌与硫酸铜溶液
C.铝与硝酸银溶液 D.汞与氯化银
9、某同学根据铜锈的成分Cu2(OH)2CO3作出猜想:引起金属铜锈蚀的因素除有氧气和水外,还应该有二氧化碳。为证明“必须有二氧化碳”,需要进行下列实验中的( )
A.甲和乙 B.甲和丁 C.乙和丁 D.丙和丁
10、向AgNO3、Cu(NO3)2、Zn(NO3)2混合液中,加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体中一定有( )
A.Ag、Cu、Zn B.Cu、Zn、Fe
C.Ag、Zn、Fe D.Ag.Cu、Fe
11、下列化学方程式书写正确的是( )
A.铜与稀硫酸:Cu + H2SO4 = CuSO4 + H2↑
B.石灰水与稀盐酸:Ca(OH)2 + HCl = CaCl2 + H2O
C.小苏打用于治疗胃酸过多:Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
D.烧碱溶液与氯化镁溶液:2NaOH + MgCl2 = Mg(OH)2↓+ 2NaCl
12、下列有关资源或能源的叙述正确的是( )
A.铁是人类最早使用的金属
B.空气中稀有气体的质量分数约为0.96%
C.煤、石油、天然气属于化石燃料
D.地球上可利用的淡水资源约占全球水储量的2.53%
13、归纳推理是学习化学的一种重要的思维方法。下列归纳推理正确的是( )
A.蜡烛燃烧生成CO2和H2O,则蜡烛组成中一定含有碳、氢元素
B.铝表面会形成氧化铝保护层,则铁制品表面的铁锈也可起到保护作用
C.置换反应有单质生成,则有单质生成的反应一定是置换反应
D.催化剂在化学反应前后质量不变,则化学反应前后质量不变的物质一定是催化剂
14、(双选)如图所示为某化学兴趣小组的同学设计的观察铁制品锈蚀的实验装置。以下相关叙述正确的是( )
A.此实验设计必须在玻璃仪器中进行
B.一段时间后,塑料瓶会变瘪,说明铁生锈与空气有关
C.一段时间后,铁丝会由下到上出现锈蚀现象
D.一段时间后,水面处铁丝锈蚀严重,而水 上、水下部分生锈不明显
15、同学们为探究不同金属的活动性强弱,设计了如下的实验方案,下列方案中实验设计、现象、结论均正确的一组是( )
选项 实验设计 现 象 结论(金属的活动性)
A 将铝丝放入硫酸铜溶液中 无现象 Cu > Al
B 将铝丝放入硫酸镁溶液中 铝丝表面有固体析出 Al > Mg
C 分别将锌粉与铁丝放入相同浓度的稀盐酸中 锌粉产生气泡的速率比 铁丝快 Zn > Fe
D 分别将铁丝与铜丝放入相同浓度的稀盐酸中 铁丝表面产生气泡, 铜丝无现象 Fe > Cu
A.A B.B C.C D.D
16、已知12.4克Fe2O3和CuO的混合物与CO充分反应后,固体减少3.1克,则原混合物中Fe2O3和CuO的质量比是( )
A.3:2 B.3:1 C.2:1 D.1:1
二、填空题。
17、写出下列矿石主要成分的化学式。
(1)赤铁矿:________________;
(2)磁铁矿:________________;
(3)菱铁矿:________________;
(4)铝土矿:________________。
18、质监部门对市场上的粽叶进行专项检查时,发现有些颜色翠绿的粽叶是用硫酸铜溶液浸泡的,人吃了用这种粽叶包的粽子,严重影响身体健康;但硫酸铜在农业上可用于配制农药波尔多液.可见,合理利用化学物质可以造福于人类,反之则会给人类带来危害.请回答: 波尔多液由生石灰与硫酸铜溶液混合配制而成,有效成分为碱式硫酸铜,在配制过程中不能用铁制或铝制容器,请用化学方程式解释其原理________ 。
19、用所学的化学知识填空
(1)空气中能供给呼吸的气体是___________
(2)生活中防止铁质栅栏生锈的一种方法是___________
(3)冰箱中放入活性炭除异味,利用了活性炭的___________性
(4)关闭燃气开关灭火,运用的原理是___________
(5)保险丝(铅锑合金)比组成它的纯金属的熔点___________
20、(1)写出下列粒子符号。
①2个镁原子______;②2个钠离子______。
(2)写出相应的金属元素符号。
①熔点最低的金属元素是______;
②能在空气中形成致密氧化膜的金属元素是______;
③导电导热最好的金属元素是______。
21、金属材料与人类生活息息相关,请回答下列问题。
(1)下列厨房用品所使用的主要材料属于金属材料的是_______(填字母)。
A.陶瓷碗 B.木筷 C.橡胶手套 D.不锈钢炊具
(2)灯管后面的反光片为铝箔,铝块能制成铝箔是利用了铝的 性。
(3)工业上用赤铁矿石炼铁的化学方程式是 。
(4)向含有硫酸铜和硫酸锌的混合溶液中,加入过量的铁粉,充分反应后过滤、得到滤液和滤渣。写出上述反应的化学方程式 ,滤渣中含有的物质是 。
三、科学与探究题。
22、小金为探究铁制品锈蚀的条件,进行如下实验:
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好.药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器,收集20mLO2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形普内的铁丝其现象如表所示。
观察对象 现象
①干燥的普通铁丝 没有明显变化
②潮湿的普通铁丝 较多红褐色锈斑
③潮湿的纯铁丝 没有明显变化
(1)步骤1中,检查U形管内是否已充满O2的方法是:
。
(2)铁制品锈蚀的条件之一是需要 O2,在此实验中能支持此条件的证据是:
。
(3)通过对比实险现象,此实验还可得出铁制品锈蚀的条件是:
。
四、综合应用题。
23、金属及金属材料在生产、生活中应用广泛。
(1)下列生活用品中,主要利用金属导热性的是________(填序号)。
(2)银、铁、铜是日常生活中经常接触到的三种金属。对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是________。
①Fe、Ag、CuSO4溶液
②Cu、Ag、FeSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
(3)日常生活中,铁制品生锈是铁与__________和__________发生反应;用于铁栏杆外层防止其生锈的涂料中的“银粉”大多是金属________的粉末。
(4)明明在学习金属的化学性质时,做了如下探究实验:
向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B。向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有________;滤液B中一定没有的金属离子是________。
(5)钢铁是使用最多的金属。工业上常用赤铁矿石炼铁,某炼铁厂每天消耗含氧化铁80%的赤铁矿500 t,该厂每天最多能炼出含杂质3%的生铁多少吨________。?(结果精确到0.1 t)
五、计算题。
24、将一氧化碳通入盛有氧化铁的试管内,加热反应一段时间后,停止加热,继续通入一氧化碳至试管冷却,此时,试管内残留固体的质量为,计算反应生成铁的质量。
第九单元 金属课后题附答案2023—2024学年鲁教版化学九年级下册
一、选择题。
1、哈尔滨的太阳岛公园是中外游客向往的旅游胜地,下列叙述错误的是( )
A.欧式灯饰外框用的黄铜主要成分是铜和锡
B.紫丁香树的种植可以提高公园内空气质量
C.铺设宽阔的柏油路面所用的沥青是石油炼制的产品
D.大理石围栏主要成分是碳酸钙
【答案】A
2、某兴趣小组进行实验探究,向盛有硝酸亚铁和硝酸银混合液的烧杯中加入一定量的锌粉,反应停止后过滤,向滤渣中加入稀盐酸,有气泡产生。下列说法正确的是( )
A.滤液中一定含有Zn2+和Fe2+,一定没有Ag+
B.滤液中一定含有Zn2+,一定没有Fe2+和Ag+
C.滤渣中一定含有银和铁,可能含有锌
D.滤渣中一定含有银,可能含有锌和铁
【答案】C
3、下列物质中不能由金属单质和盐酸直接反应生成的是( )
A. B. C. D.AlCl3
【答案】A
4、日常生活中的一些铁制品经常会被锈蚀,下列做法中不能起防锈作用的是( )
①在铁制品表面镀锌 ②在铁制品表面涂油脂 ③在铁制品表面覆盖搪瓷 ④在铁器表面刷油漆
⑤自行车脏了用清水冲洗 ⑥用废酸液冲洗铁制污水管道 ⑦切完咸菜后,尽快将菜刀洗净擦干
⑧保留铁件表面的铁锈作保护层.
A.①③⑦ B.②④ C.⑤⑥⑧ D.①⑦
【答案】C
5、金属单质家族四兄弟W、X、Y、Z,不小心掉入稀盐酸池,神情如图所示:
则W、X、Y、Z的金属活动性顺序为( )
A.X>W>Z>Y B.Z>X>W>Y
C.W>X>Y>Z D.Y>Z>X>W
【答案】B
6、下列图像与对应的表述不吻合的是( )
A. 氯酸钾和二氧化锰混合加热制取氧气
B.
向等质量、等浓度的稀硫酸中分别加入足量锌粉和铁粉
C.
某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
D. 向氢氧化钠溶液中不断加水
【答案】D
7、下列关于铁的叙述中,错误的是( )
A.铁是地壳中含量最多的金属
B.纯铁具有良好的延展性
C.纯铁是电和热的良好导体
D.纯铁具有银白色的金属光泽
【答案】A
8、下列各组物质不能发生反应的是( )
A.镁与稀硫酸 B.锌与硫酸铜溶液
C.铝与硝酸银溶液 D.汞与氯化银
【答案】D
9、某同学根据铜锈的成分Cu2(OH)2CO3作出猜想:引起金属铜锈蚀的因素除有氧气和水外,还应该有二氧化碳。为证明“必须有二氧化碳”,需要进行下列实验中的( )
A.甲和乙 B.甲和丁 C.乙和丁 D.丙和丁
【答案】B
10、向AgNO3、Cu(NO3)2、Zn(NO3)2混合液中,加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体中一定有( )
A.Ag、Cu、Zn B.Cu、Zn、Fe
C.Ag、Zn、Fe D.Ag.Cu、Fe
【答案】D
11、下列化学方程式书写正确的是( )
A.铜与稀硫酸:Cu + H2SO4 = CuSO4 + H2↑
B.石灰水与稀盐酸:Ca(OH)2 + HCl = CaCl2 + H2O
C.小苏打用于治疗胃酸过多:Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
D.烧碱溶液与氯化镁溶液:2NaOH + MgCl2 = Mg(OH)2↓+ 2NaCl
【答案】D
12、下列有关资源或能源的叙述正确的是( )
A.铁是人类最早使用的金属
B.空气中稀有气体的质量分数约为0.96%
C.煤、石油、天然气属于化石燃料
D.地球上可利用的淡水资源约占全球水储量的2.53%
【答案】C
13、归纳推理是学习化学的一种重要的思维方法。下列归纳推理正确的是( )
A.蜡烛燃烧生成CO2和H2O,则蜡烛组成中一定含有碳、氢元素
B.铝表面会形成氧化铝保护层,则铁制品表面的铁锈也可起到保护作用
C.置换反应有单质生成,则有单质生成的反应一定是置换反应
D.催化剂在化学反应前后质量不变,则化学反应前后质量不变的物质一定是催化剂
【答案】A
14、(双选)如图所示为某化学兴趣小组的同学设计的观察铁制品锈蚀的实验装置。以下相关叙述正确的是( )
A.此实验设计必须在玻璃仪器中进行
B.一段时间后,塑料瓶会变瘪,说明铁生锈与空气有关
C.一段时间后,铁丝会由下到上出现锈蚀现象
D.一段时间后,水面处铁丝锈蚀严重,而水 上、水下部分生锈不明显
【答案】BD
15、同学们为探究不同金属的活动性强弱,设计了如下的实验方案,下列方案中实验设计、现象、结论均正确的一组是( )
选项 实验设计 现 象 结论(金属的活动性)
A 将铝丝放入硫酸铜溶液中 无现象 Cu > Al
B 将铝丝放入硫酸镁溶液中 铝丝表面有固体析出 Al > Mg
C 分别将锌粉与铁丝放入相同浓度的稀盐酸中 锌粉产生气泡的速率比 铁丝快 Zn > Fe
D 分别将铁丝与铜丝放入相同浓度的稀盐酸中 铁丝表面产生气泡, 铜丝无现象 Fe > Cu
A.A B.B C.C D.D
【答案】D
16、已知12.4克Fe2O3和CuO的混合物与CO充分反应后,固体减少3.1克,则原混合物中Fe2O3和CuO的质量比是( )
A.3:2 B.3:1 C.2:1 D.1:1
【答案】D
二、填空题。
17、写出下列矿石主要成分的化学式。
(1)赤铁矿:________________;
(2)磁铁矿:________________;
(3)菱铁矿:________________;
(4)铝土矿:________________。
【答案】(1)Fe2O3 (2)Fe3O4 (3)FeCO3 (4)Al2O3
18、质监部门对市场上的粽叶进行专项检查时,发现有些颜色翠绿的粽叶是用硫酸铜溶液浸泡的,人吃了用这种粽叶包的粽子,严重影响身体健康;但硫酸铜在农业上可用于配制农药波尔多液.可见,合理利用化学物质可以造福于人类,反之则会给人类带来危害.请回答: 波尔多液由生石灰与硫酸铜溶液混合配制而成,有效成分为碱式硫酸铜,在配制过程中不能用铁制或铝制容器,请用化学方程式解释其原理________ 。
【答案】Fe+CuSO 4=== FeSO 4 +Cu【2Al+3CuSO 4 =3Cu+Al 2(SO 4)3】
19、用所学的化学知识填空
(1)空气中能供给呼吸的气体是___________
(2)生活中防止铁质栅栏生锈的一种方法是___________
(3)冰箱中放入活性炭除异味,利用了活性炭的___________性
(4)关闭燃气开关灭火,运用的原理是___________
(5)保险丝(铅锑合金)比组成它的纯金属的熔点___________
【答案】(1)氧气 (2)刷漆 (3)吸附 (4)去除可燃物 (5)低
20、(1)写出下列粒子符号。
①2个镁原子______;②2个钠离子______。
(2)写出相应的金属元素符号。
①熔点最低的金属元素是______;
②能在空气中形成致密氧化膜的金属元素是______;
③导电导热最好的金属元素是______。
【答案】
21、金属材料与人类生活息息相关,请回答下列问题。
(1)下列厨房用品所使用的主要材料属于金属材料的是_______(填字母)。
A.陶瓷碗 B.木筷 C.橡胶手套 D.不锈钢炊具
(2)灯管后面的反光片为铝箔,铝块能制成铝箔是利用了铝的 性。
(3)工业上用赤铁矿石炼铁的化学方程式是 。
(4)向含有硫酸铜和硫酸锌的混合溶液中,加入过量的铁粉,充分反应后过滤、得到滤液和滤渣。写出上述反应的化学方程式 ,滤渣中含有的物质是 。
【答案】(1)D (2)延展 (3)Fe2O3+3CO2Fe+ 3CO2
(4) Fe+CuSO4= FeSO4+Cu Fe、Cu
三、科学与探究题。
22、小金为探究铁制品锈蚀的条件,进行如下实验:
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好.药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器,收集20mLO2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形普内的铁丝其现象如表所示。
观察对象 现象
①干燥的普通铁丝 没有明显变化
②潮湿的普通铁丝 较多红褐色锈斑
③潮湿的纯铁丝 没有明显变化
(1)步骤1中,检查U形管内是否已充满O2的方法是:
。
(2)铁制品锈蚀的条件之一是需要 O2,在此实验中能支持此条件的证据是:
。
(3)通过对比实险现象,此实验还可得出铁制品锈蚀的条件是:
。
【答案】(1)将带火星的木条放置在b管口,若木条复燃,则证明U形管内已经充满氧气;
(2) 观察到注射器活塞向左移动(或注射器内的氧气体积减少)
(3)水分和金属的内部结构
四、综合应用题。
23、金属及金属材料在生产、生活中应用广泛。
(1)下列生活用品中,主要利用金属导热性的是________(填序号)。
(2)银、铁、铜是日常生活中经常接触到的三种金属。对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是________。
①Fe、Ag、CuSO4溶液
②Cu、Ag、FeSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
(3)日常生活中,铁制品生锈是铁与__________和__________发生反应;用于铁栏杆外层防止其生锈的涂料中的“银粉”大多是金属________的粉末。
(4)明明在学习金属的化学性质时,做了如下探究实验:
向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B。向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有________;滤液B中一定没有的金属离子是________。
(5)钢铁是使用最多的金属。工业上常用赤铁矿石炼铁,某炼铁厂每天消耗含氧化铁80%的赤铁矿500 t,该厂每天最多能炼出含杂质3%的生铁多少吨________。?(结果精确到0.1 t)
【答案】(1)A (2)② (3)氧气 水蒸气 铝
(4)银、铜和铁 Cu2+和Ag+ (5)288.7 t。
五、计算题。
24、将一氧化碳通入盛有氧化铁的试管内,加热反应一段时间后,停止加热,继续通入一氧化碳至试管冷却,此时,试管内残留固体的质量为,计算反应生成铁的质量。
【答案】反应生成的铁的质量为5.6g。
一、选择题。
1、哈尔滨的太阳岛公园是中外游客向往的旅游胜地,下列叙述错误的是( )
A.欧式灯饰外框用的黄铜主要成分是铜和锡
B.紫丁香树的种植可以提高公园内空气质量
C.铺设宽阔的柏油路面所用的沥青是石油炼制的产品
D.大理石围栏主要成分是碳酸钙
2、某兴趣小组进行实验探究,向盛有硝酸亚铁和硝酸银混合液的烧杯中加入一定量的锌粉,反应停止后过滤,向滤渣中加入稀盐酸,有气泡产生。下列说法正确的是( )
A.滤液中一定含有Zn2+和Fe2+,一定没有Ag+
B.滤液中一定含有Zn2+,一定没有Fe2+和Ag+
C.滤渣中一定含有银和铁,可能含有锌
D.滤渣中一定含有银,可能含有锌和铁
3、下列物质中不能由金属单质和盐酸直接反应生成的是( )
A. B. C. D.AlCl3
4、日常生活中的一些铁制品经常会被锈蚀,下列做法中不能起防锈作用的是( )
①在铁制品表面镀锌 ②在铁制品表面涂油脂 ③在铁制品表面覆盖搪瓷 ④在铁器表面刷油漆
⑤自行车脏了用清水冲洗 ⑥用废酸液冲洗铁制污水管道 ⑦切完咸菜后,尽快将菜刀洗净擦干
⑧保留铁件表面的铁锈作保护层.
A.①③⑦ B.②④ C.⑤⑥⑧ D.①⑦
5、金属单质家族四兄弟W、X、Y、Z,不小心掉入稀盐酸池,神情如图所示:
则W、X、Y、Z的金属活动性顺序为( )
A.X>W>Z>Y B.Z>X>W>Y
C.W>X>Y>Z D.Y>Z>X>W
6、下列图像与对应的表述不吻合的是( )
A. 氯酸钾和二氧化锰混合加热制取氧气
B.
向等质量、等浓度的稀硫酸中分别加入足量锌粉和铁粉
C.
某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
D. 向氢氧化钠溶液中不断加水
7、下列关于铁的叙述中,错误的是( )
A.铁是地壳中含量最多的金属
B.纯铁具有良好的延展性
C.纯铁是电和热的良好导体
D.纯铁具有银白色的金属光泽
8、下列各组物质不能发生反应的是( )
A.镁与稀硫酸 B.锌与硫酸铜溶液
C.铝与硝酸银溶液 D.汞与氯化银
9、某同学根据铜锈的成分Cu2(OH)2CO3作出猜想:引起金属铜锈蚀的因素除有氧气和水外,还应该有二氧化碳。为证明“必须有二氧化碳”,需要进行下列实验中的( )
A.甲和乙 B.甲和丁 C.乙和丁 D.丙和丁
10、向AgNO3、Cu(NO3)2、Zn(NO3)2混合液中,加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体中一定有( )
A.Ag、Cu、Zn B.Cu、Zn、Fe
C.Ag、Zn、Fe D.Ag.Cu、Fe
11、下列化学方程式书写正确的是( )
A.铜与稀硫酸:Cu + H2SO4 = CuSO4 + H2↑
B.石灰水与稀盐酸:Ca(OH)2 + HCl = CaCl2 + H2O
C.小苏打用于治疗胃酸过多:Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
D.烧碱溶液与氯化镁溶液:2NaOH + MgCl2 = Mg(OH)2↓+ 2NaCl
12、下列有关资源或能源的叙述正确的是( )
A.铁是人类最早使用的金属
B.空气中稀有气体的质量分数约为0.96%
C.煤、石油、天然气属于化石燃料
D.地球上可利用的淡水资源约占全球水储量的2.53%
13、归纳推理是学习化学的一种重要的思维方法。下列归纳推理正确的是( )
A.蜡烛燃烧生成CO2和H2O,则蜡烛组成中一定含有碳、氢元素
B.铝表面会形成氧化铝保护层,则铁制品表面的铁锈也可起到保护作用
C.置换反应有单质生成,则有单质生成的反应一定是置换反应
D.催化剂在化学反应前后质量不变,则化学反应前后质量不变的物质一定是催化剂
14、(双选)如图所示为某化学兴趣小组的同学设计的观察铁制品锈蚀的实验装置。以下相关叙述正确的是( )
A.此实验设计必须在玻璃仪器中进行
B.一段时间后,塑料瓶会变瘪,说明铁生锈与空气有关
C.一段时间后,铁丝会由下到上出现锈蚀现象
D.一段时间后,水面处铁丝锈蚀严重,而水 上、水下部分生锈不明显
15、同学们为探究不同金属的活动性强弱,设计了如下的实验方案,下列方案中实验设计、现象、结论均正确的一组是( )
选项 实验设计 现 象 结论(金属的活动性)
A 将铝丝放入硫酸铜溶液中 无现象 Cu > Al
B 将铝丝放入硫酸镁溶液中 铝丝表面有固体析出 Al > Mg
C 分别将锌粉与铁丝放入相同浓度的稀盐酸中 锌粉产生气泡的速率比 铁丝快 Zn > Fe
D 分别将铁丝与铜丝放入相同浓度的稀盐酸中 铁丝表面产生气泡, 铜丝无现象 Fe > Cu
A.A B.B C.C D.D
16、已知12.4克Fe2O3和CuO的混合物与CO充分反应后,固体减少3.1克,则原混合物中Fe2O3和CuO的质量比是( )
A.3:2 B.3:1 C.2:1 D.1:1
二、填空题。
17、写出下列矿石主要成分的化学式。
(1)赤铁矿:________________;
(2)磁铁矿:________________;
(3)菱铁矿:________________;
(4)铝土矿:________________。
18、质监部门对市场上的粽叶进行专项检查时,发现有些颜色翠绿的粽叶是用硫酸铜溶液浸泡的,人吃了用这种粽叶包的粽子,严重影响身体健康;但硫酸铜在农业上可用于配制农药波尔多液.可见,合理利用化学物质可以造福于人类,反之则会给人类带来危害.请回答: 波尔多液由生石灰与硫酸铜溶液混合配制而成,有效成分为碱式硫酸铜,在配制过程中不能用铁制或铝制容器,请用化学方程式解释其原理________ 。
19、用所学的化学知识填空
(1)空气中能供给呼吸的气体是___________
(2)生活中防止铁质栅栏生锈的一种方法是___________
(3)冰箱中放入活性炭除异味,利用了活性炭的___________性
(4)关闭燃气开关灭火,运用的原理是___________
(5)保险丝(铅锑合金)比组成它的纯金属的熔点___________
20、(1)写出下列粒子符号。
①2个镁原子______;②2个钠离子______。
(2)写出相应的金属元素符号。
①熔点最低的金属元素是______;
②能在空气中形成致密氧化膜的金属元素是______;
③导电导热最好的金属元素是______。
21、金属材料与人类生活息息相关,请回答下列问题。
(1)下列厨房用品所使用的主要材料属于金属材料的是_______(填字母)。
A.陶瓷碗 B.木筷 C.橡胶手套 D.不锈钢炊具
(2)灯管后面的反光片为铝箔,铝块能制成铝箔是利用了铝的 性。
(3)工业上用赤铁矿石炼铁的化学方程式是 。
(4)向含有硫酸铜和硫酸锌的混合溶液中,加入过量的铁粉,充分反应后过滤、得到滤液和滤渣。写出上述反应的化学方程式 ,滤渣中含有的物质是 。
三、科学与探究题。
22、小金为探究铁制品锈蚀的条件,进行如下实验:
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好.药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器,收集20mLO2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形普内的铁丝其现象如表所示。
观察对象 现象
①干燥的普通铁丝 没有明显变化
②潮湿的普通铁丝 较多红褐色锈斑
③潮湿的纯铁丝 没有明显变化
(1)步骤1中,检查U形管内是否已充满O2的方法是:
。
(2)铁制品锈蚀的条件之一是需要 O2,在此实验中能支持此条件的证据是:
。
(3)通过对比实险现象,此实验还可得出铁制品锈蚀的条件是:
。
四、综合应用题。
23、金属及金属材料在生产、生活中应用广泛。
(1)下列生活用品中,主要利用金属导热性的是________(填序号)。
(2)银、铁、铜是日常生活中经常接触到的三种金属。对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是________。
①Fe、Ag、CuSO4溶液
②Cu、Ag、FeSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
(3)日常生活中,铁制品生锈是铁与__________和__________发生反应;用于铁栏杆外层防止其生锈的涂料中的“银粉”大多是金属________的粉末。
(4)明明在学习金属的化学性质时,做了如下探究实验:
向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B。向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有________;滤液B中一定没有的金属离子是________。
(5)钢铁是使用最多的金属。工业上常用赤铁矿石炼铁,某炼铁厂每天消耗含氧化铁80%的赤铁矿500 t,该厂每天最多能炼出含杂质3%的生铁多少吨________。?(结果精确到0.1 t)
五、计算题。
24、将一氧化碳通入盛有氧化铁的试管内,加热反应一段时间后,停止加热,继续通入一氧化碳至试管冷却,此时,试管内残留固体的质量为,计算反应生成铁的质量。
第九单元 金属课后题附答案2023—2024学年鲁教版化学九年级下册
一、选择题。
1、哈尔滨的太阳岛公园是中外游客向往的旅游胜地,下列叙述错误的是( )
A.欧式灯饰外框用的黄铜主要成分是铜和锡
B.紫丁香树的种植可以提高公园内空气质量
C.铺设宽阔的柏油路面所用的沥青是石油炼制的产品
D.大理石围栏主要成分是碳酸钙
【答案】A
2、某兴趣小组进行实验探究,向盛有硝酸亚铁和硝酸银混合液的烧杯中加入一定量的锌粉,反应停止后过滤,向滤渣中加入稀盐酸,有气泡产生。下列说法正确的是( )
A.滤液中一定含有Zn2+和Fe2+,一定没有Ag+
B.滤液中一定含有Zn2+,一定没有Fe2+和Ag+
C.滤渣中一定含有银和铁,可能含有锌
D.滤渣中一定含有银,可能含有锌和铁
【答案】C
3、下列物质中不能由金属单质和盐酸直接反应生成的是( )
A. B. C. D.AlCl3
【答案】A
4、日常生活中的一些铁制品经常会被锈蚀,下列做法中不能起防锈作用的是( )
①在铁制品表面镀锌 ②在铁制品表面涂油脂 ③在铁制品表面覆盖搪瓷 ④在铁器表面刷油漆
⑤自行车脏了用清水冲洗 ⑥用废酸液冲洗铁制污水管道 ⑦切完咸菜后,尽快将菜刀洗净擦干
⑧保留铁件表面的铁锈作保护层.
A.①③⑦ B.②④ C.⑤⑥⑧ D.①⑦
【答案】C
5、金属单质家族四兄弟W、X、Y、Z,不小心掉入稀盐酸池,神情如图所示:
则W、X、Y、Z的金属活动性顺序为( )
A.X>W>Z>Y B.Z>X>W>Y
C.W>X>Y>Z D.Y>Z>X>W
【答案】B
6、下列图像与对应的表述不吻合的是( )
A. 氯酸钾和二氧化锰混合加热制取氧气
B.
向等质量、等浓度的稀硫酸中分别加入足量锌粉和铁粉
C.
某温度下,向一定量接近饱和的硝酸钾溶液中加入硝酸钾固体
D. 向氢氧化钠溶液中不断加水
【答案】D
7、下列关于铁的叙述中,错误的是( )
A.铁是地壳中含量最多的金属
B.纯铁具有良好的延展性
C.纯铁是电和热的良好导体
D.纯铁具有银白色的金属光泽
【答案】A
8、下列各组物质不能发生反应的是( )
A.镁与稀硫酸 B.锌与硫酸铜溶液
C.铝与硝酸银溶液 D.汞与氯化银
【答案】D
9、某同学根据铜锈的成分Cu2(OH)2CO3作出猜想:引起金属铜锈蚀的因素除有氧气和水外,还应该有二氧化碳。为证明“必须有二氧化碳”,需要进行下列实验中的( )
A.甲和乙 B.甲和丁 C.乙和丁 D.丙和丁
【答案】B
10、向AgNO3、Cu(NO3)2、Zn(NO3)2混合液中,加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体中一定有( )
A.Ag、Cu、Zn B.Cu、Zn、Fe
C.Ag、Zn、Fe D.Ag.Cu、Fe
【答案】D
11、下列化学方程式书写正确的是( )
A.铜与稀硫酸:Cu + H2SO4 = CuSO4 + H2↑
B.石灰水与稀盐酸:Ca(OH)2 + HCl = CaCl2 + H2O
C.小苏打用于治疗胃酸过多:Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
D.烧碱溶液与氯化镁溶液:2NaOH + MgCl2 = Mg(OH)2↓+ 2NaCl
【答案】D
12、下列有关资源或能源的叙述正确的是( )
A.铁是人类最早使用的金属
B.空气中稀有气体的质量分数约为0.96%
C.煤、石油、天然气属于化石燃料
D.地球上可利用的淡水资源约占全球水储量的2.53%
【答案】C
13、归纳推理是学习化学的一种重要的思维方法。下列归纳推理正确的是( )
A.蜡烛燃烧生成CO2和H2O,则蜡烛组成中一定含有碳、氢元素
B.铝表面会形成氧化铝保护层,则铁制品表面的铁锈也可起到保护作用
C.置换反应有单质生成,则有单质生成的反应一定是置换反应
D.催化剂在化学反应前后质量不变,则化学反应前后质量不变的物质一定是催化剂
【答案】A
14、(双选)如图所示为某化学兴趣小组的同学设计的观察铁制品锈蚀的实验装置。以下相关叙述正确的是( )
A.此实验设计必须在玻璃仪器中进行
B.一段时间后,塑料瓶会变瘪,说明铁生锈与空气有关
C.一段时间后,铁丝会由下到上出现锈蚀现象
D.一段时间后,水面处铁丝锈蚀严重,而水 上、水下部分生锈不明显
【答案】BD
15、同学们为探究不同金属的活动性强弱,设计了如下的实验方案,下列方案中实验设计、现象、结论均正确的一组是( )
选项 实验设计 现 象 结论(金属的活动性)
A 将铝丝放入硫酸铜溶液中 无现象 Cu > Al
B 将铝丝放入硫酸镁溶液中 铝丝表面有固体析出 Al > Mg
C 分别将锌粉与铁丝放入相同浓度的稀盐酸中 锌粉产生气泡的速率比 铁丝快 Zn > Fe
D 分别将铁丝与铜丝放入相同浓度的稀盐酸中 铁丝表面产生气泡, 铜丝无现象 Fe > Cu
A.A B.B C.C D.D
【答案】D
16、已知12.4克Fe2O3和CuO的混合物与CO充分反应后,固体减少3.1克,则原混合物中Fe2O3和CuO的质量比是( )
A.3:2 B.3:1 C.2:1 D.1:1
【答案】D
二、填空题。
17、写出下列矿石主要成分的化学式。
(1)赤铁矿:________________;
(2)磁铁矿:________________;
(3)菱铁矿:________________;
(4)铝土矿:________________。
【答案】(1)Fe2O3 (2)Fe3O4 (3)FeCO3 (4)Al2O3
18、质监部门对市场上的粽叶进行专项检查时,发现有些颜色翠绿的粽叶是用硫酸铜溶液浸泡的,人吃了用这种粽叶包的粽子,严重影响身体健康;但硫酸铜在农业上可用于配制农药波尔多液.可见,合理利用化学物质可以造福于人类,反之则会给人类带来危害.请回答: 波尔多液由生石灰与硫酸铜溶液混合配制而成,有效成分为碱式硫酸铜,在配制过程中不能用铁制或铝制容器,请用化学方程式解释其原理________ 。
【答案】Fe+CuSO 4=== FeSO 4 +Cu【2Al+3CuSO 4 =3Cu+Al 2(SO 4)3】
19、用所学的化学知识填空
(1)空气中能供给呼吸的气体是___________
(2)生活中防止铁质栅栏生锈的一种方法是___________
(3)冰箱中放入活性炭除异味,利用了活性炭的___________性
(4)关闭燃气开关灭火,运用的原理是___________
(5)保险丝(铅锑合金)比组成它的纯金属的熔点___________
【答案】(1)氧气 (2)刷漆 (3)吸附 (4)去除可燃物 (5)低
20、(1)写出下列粒子符号。
①2个镁原子______;②2个钠离子______。
(2)写出相应的金属元素符号。
①熔点最低的金属元素是______;
②能在空气中形成致密氧化膜的金属元素是______;
③导电导热最好的金属元素是______。
【答案】
21、金属材料与人类生活息息相关,请回答下列问题。
(1)下列厨房用品所使用的主要材料属于金属材料的是_______(填字母)。
A.陶瓷碗 B.木筷 C.橡胶手套 D.不锈钢炊具
(2)灯管后面的反光片为铝箔,铝块能制成铝箔是利用了铝的 性。
(3)工业上用赤铁矿石炼铁的化学方程式是 。
(4)向含有硫酸铜和硫酸锌的混合溶液中,加入过量的铁粉,充分反应后过滤、得到滤液和滤渣。写出上述反应的化学方程式 ,滤渣中含有的物质是 。
【答案】(1)D (2)延展 (3)Fe2O3+3CO2Fe+ 3CO2
(4) Fe+CuSO4= FeSO4+Cu Fe、Cu
三、科学与探究题。
22、小金为探究铁制品锈蚀的条件,进行如下实验:
步骤1:利用图甲所示装置,将干燥的O2从导管a通入U形管(装置气密性良好.药品如图所示);待U形管内充满O2后,在导管b处连接一活塞推至底部的注射器,收集20mLO2后在导管a处连接乳胶管并用止水夹夹紧,如图乙所示。
步骤2:一段时间后,观察U形普内的铁丝其现象如表所示。
观察对象 现象
①干燥的普通铁丝 没有明显变化
②潮湿的普通铁丝 较多红褐色锈斑
③潮湿的纯铁丝 没有明显变化
(1)步骤1中,检查U形管内是否已充满O2的方法是:
。
(2)铁制品锈蚀的条件之一是需要 O2,在此实验中能支持此条件的证据是:
。
(3)通过对比实险现象,此实验还可得出铁制品锈蚀的条件是:
。
【答案】(1)将带火星的木条放置在b管口,若木条复燃,则证明U形管内已经充满氧气;
(2) 观察到注射器活塞向左移动(或注射器内的氧气体积减少)
(3)水分和金属的内部结构
四、综合应用题。
23、金属及金属材料在生产、生活中应用广泛。
(1)下列生活用品中,主要利用金属导热性的是________(填序号)。
(2)银、铁、铜是日常生活中经常接触到的三种金属。对Ag、Fe、Cu三种金属活动性顺序的探究,下列所选试剂组不可行的是________。
①Fe、Ag、CuSO4溶液
②Cu、Ag、FeSO4溶液
③Cu、FeSO4溶液、AgNO3溶液
(3)日常生活中,铁制品生锈是铁与__________和__________发生反应;用于铁栏杆外层防止其生锈的涂料中的“银粉”大多是金属________的粉末。
(4)明明在学习金属的化学性质时,做了如下探究实验:
向硝酸银、硝酸铜、硝酸亚铁的混合溶液中加入一定质量的锌粉,反应停止后过滤,洗涤,得滤渣A和滤液B。向滤渣A中加入稀盐酸,有气泡冒出。则滤渣A中一定有________;滤液B中一定没有的金属离子是________。
(5)钢铁是使用最多的金属。工业上常用赤铁矿石炼铁,某炼铁厂每天消耗含氧化铁80%的赤铁矿500 t,该厂每天最多能炼出含杂质3%的生铁多少吨________。?(结果精确到0.1 t)
【答案】(1)A (2)② (3)氧气 水蒸气 铝
(4)银、铜和铁 Cu2+和Ag+ (5)288.7 t。
五、计算题。
24、将一氧化碳通入盛有氧化铁的试管内,加热反应一段时间后,停止加热,继续通入一氧化碳至试管冷却,此时,试管内残留固体的质量为,计算反应生成铁的质量。
【答案】反应生成的铁的质量为5.6g。
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
