化学人教版(2019)必修第一册2.1.2钠及其化合物(共20张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册2.1.2钠及其化合物(共20张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 14.3MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-20 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
生活中的“钠”些物质
——以Na2CO3与NaHCO3为例
人教版 高中化学必修1 第一册 第二章 第一节钠及其化合物
PART
1.1
生活探寻
生活里有它们
饼干
(NaHCO3)
蛋糕、面包(NaHCO3)
苏打水
(NaHCO3)
胃药
(NaHCO3)
食用苏打和小苏打
( Na2CO3 、NaHCO3)
肥皂
(Na2CO3)
PART
1.2
问题思考
如何鉴别苏打和小苏打?
PART
02
课前调研
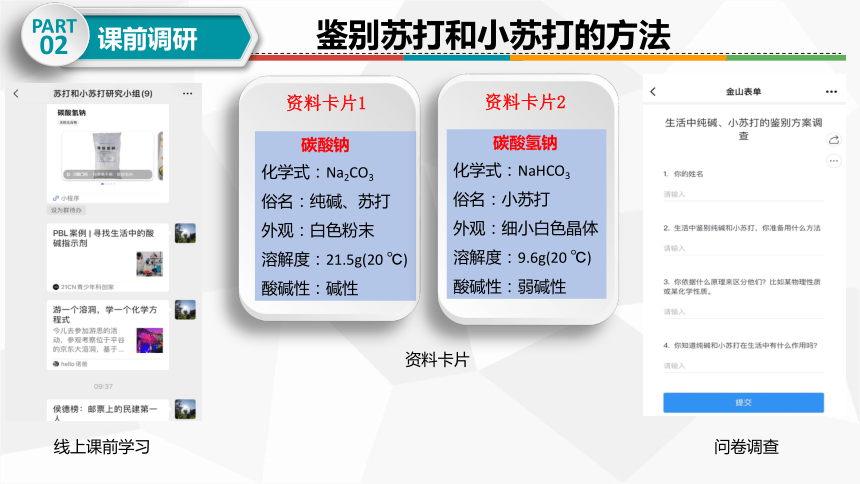
鉴别苏打和小苏打的方法
资料卡片1
碳酸钠
化学式:Na2CO3
俗名:纯碱、苏打
外观:白色粉末
溶解度:21.5g(20 ℃)
酸碱性:碱性
资料卡片2
碳酸氢钠
化学式:NaHCO3
俗名:小苏打
外观:细小白色晶体
溶解度:9.6g(20 ℃)
酸碱性:弱碱性
线上课前学习
资料卡片
问卷调查
PART
02
课前调研
统计汇总鉴别方法
PART
03
家庭实验分享 1
家庭实验探究两者的外观和溶解情况
观察外观:
溶解情况:
细小的晶体
粉末颗粒更大
加入几滴水后
碳酸钠固体
碳酸氢钠固体
溶解过程热成像视频
PART
03
家庭实验分享 2
家庭实验探究两者的酸碱性
资料1
花青素是一种水溶性天然食用色素,广泛存在于各种植物组织中。因其化学结构和颜色会随环境pH值的变化而发生明显变化,因此花青素被用于开发各种pH指示材料,以达到示警、指示的效果。
富含花青素
PART
03
家庭实验分享 3
家庭实验探究和食醋的反应
等体积的食醋
等体积的食醋
等质量碳酸钠和碳酸氢钠固体
向等体积碳酸钠和碳酸氢钠溶液中
PART
04
小组合作探究1
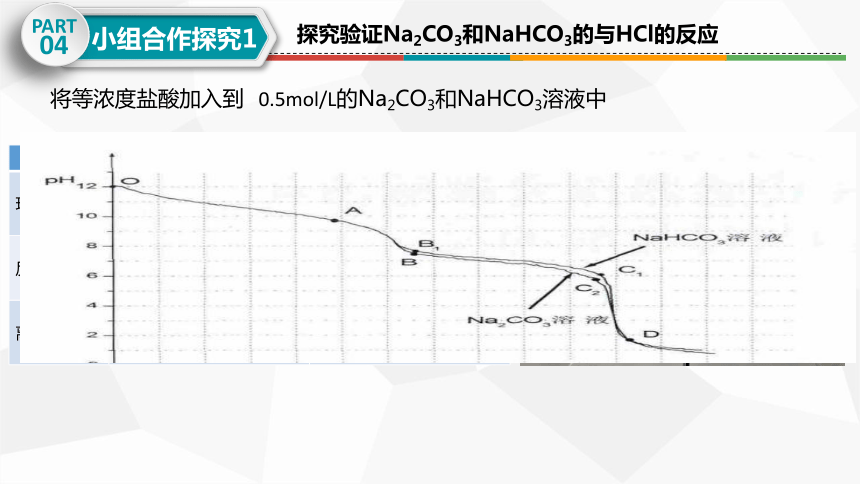
探究验证Na2CO3和NaHCO3的与HCl的反应
将等浓度盐酸加入到 0.5mol/L的Na2CO3和NaHCO3溶液中
Na2CO3 NaHCO3
现象描述
反应实质
离子方程式
PART
04
小组合作探究1
探究验证Na2CO3和NaHCO3的与HCl的反应
②将等浓度盐酸加入到 12ml 0.5mol/L的Na2CO3和NaHCO3溶液中
Na2CO3 NaHCO3
现象描述
反应实质
离子方程式
一开始无气泡或气泡较少,后产生气泡,溶液由红色逐渐变为无色
一开始产生气泡溶液由淡红色逐渐变为无色
NaHCO3+HCl=NaCl+CO2↑+H2O
Na2CO3+HCl= NaHCO3 + NaCl
NaHCO3+HCl=NaCl+CO2↑+H2O
微观解析:
PART
04
小组合作探究2
探究验证Na2CO3和NaHCO3的热稳定性
观察超市食品袋说明
碳酸氢钠标签
食品添加剂
膨松剂
碳酸氢钠分解
PART
04
小组合作探究2
探究验证Na2CO3和NaHCO3的热稳定性
该装置的缺点
要进行两次加热
没法同时比较两种物质的受热情况
实验装置改进
1.向上下两根试管中分别加入少量的碳酸钠和碳酸氢钠固体。
2.向U型管内倒入一定量的澄清石灰水至刚好没过导管口,向U型管内滴加几滴酚酞。
3.用外焰加热最下面那根试管底部,观察U型管内的现象。
文献查阅
两者受热分解温度
碳酸钠:
1203.74 ℃ -1227.69 ℃
碳酸氢钠:
50.9 ℃ -54.56 ℃
PART
04
小组合作探究3
探究Na2CO3和NaHCO3溶液与Ca(OH)2和CaCl2反应
分别向0.1mol/L的Na2CO3和NaHCO3溶液中滴加数滴0.1mol/L的CaCl2溶液和澄清石灰水
所加物质 项目 Na2CO3 NaHCO3 结论
0.1mol/L的CaCl2溶液 现象
方程式 离子方程式 澄清石灰水 现象
方程式 离子方程式
PART
05
讨论总结
鉴别苏打和小苏打的方法
性质 碳酸钠 碳酸氢钠
颜色状态 白色粉末 细小白色晶体
溶解情况 易溶(S:21.5g),溶于水放热 可溶(S:9.6g),溶于水吸热
水溶液酸碱性 都为碱性,相同浓度下碳酸钠的碱性大于碳酸氢钠 与酸反应 碳酸钠、碳酸氢钠加入盐酸中 Na2CO3+2HCl=NaCl+CO2↑+H2O (反应更慢) NaHCO3+HCl=NaCl+CO2↑+H2O (反应更剧烈)
盐酸加入碳酸钠、碳酸氢钠中 一开始无气泡,后产生气泡 Na2CO3+HCl= NaHCO3+ NaCl NaHCO3+HCl=NaCl+CO2↑+H2O 一开始就产生气泡 NaHCO3+HCl=NaCl+CO2↑+H2O
热稳定性 一般认为不分解 2NaHCO3=Na2CO3+CO2↑+H2O
与碱反应 与澄清石灰水反应变浑浊Na2CO3+Ca(OH)2=2NaOH+CaCO3↓ 与澄清石灰水反应变浑浊NaHCO3+Ca(OH)2=NaOH+CaCO3↓+H2O
与盐反应 Na2CO3+CaCl2=2NaCl+CaCO3↓ CaCl2和BaCl2反应产生沉淀 与CaCl2和BaCl2不反应
△
PART
06
问题再探
雪碧和碳酸钠的故事
Na2CO3+CO2 + H2O =2NaHCO3
向一瓶雪碧里加入足量的碳酸钠固体,用力摇动,另外一瓶不加任何东西,也用力摇动,观察两者现象。
PART
06
问题再探
碳酸钠和碳酸氢钠的互相转化
Na2CO3
NaHCO3
①CO2 + H2O
②加少量HCl
①固体加热
②NaOH溶液
①Na2CO3+CO2 + H2O =2NaHCO3
②Na2CO3+ HCl =NaHCO3+ NaCl
④
③
PART
07
学以致用
解释生活中的一些应用与现象
为什么食堂阿姨用碱粉(纯碱)洗盆碗?
为什么医生建议用小苏打来治疗胃酸过多?
1.为什么苏打水里装的不是苏打而是小苏打?
2.喝碱性水真的有益身体健康吗?
3.15打假真言
1.生命细胞代谢所有过程离不开水,所以要喝水,水是营养物质溶解的载体。
2.只要符合国家饮用水标准的水都是好水。
3.碱性水有益健康的说法只是一种营销手段,不能当真。
PART
08
课堂小结
总结本堂课
鉴别碳酸钠和碳酸氢钠
观察外观
食醋检验反应剧烈程度
与盐酸互滴现象
与澄清石灰水
热稳定性
课堂探究
家庭探究
紫甘蓝检验酸碱性
总结碳酸钠和碳酸氢钠的转化
验证碳酸钠和碳酸氢钠在生活中应用
与CaCl2反应
PART
09
课后任务
完成以下课后任务
观看《千分才子侯德榜》
侯氏制碱法原理
NaCl + NH3 +H2O = NaHCO3 ↓+ NH4Cl
2NaHCO3 = Na2CO3+CO2↑+H2O
给家人们做一份健康又多彩的“变色”的爱心紫薯粥
动动手
感谢您的聆听
敬请批评指正
生活中的“钠”些物质
——以Na2CO3与NaHCO3为例
人教版 高中化学必修1 第一册 第二章 第一节钠及其化合物
PART
1.1
生活探寻
生活里有它们
饼干
(NaHCO3)
蛋糕、面包(NaHCO3)
苏打水
(NaHCO3)
胃药
(NaHCO3)
食用苏打和小苏打
( Na2CO3 、NaHCO3)
肥皂
(Na2CO3)
PART
1.2
问题思考
如何鉴别苏打和小苏打?
PART
02
课前调研
鉴别苏打和小苏打的方法
资料卡片1
碳酸钠
化学式:Na2CO3
俗名:纯碱、苏打
外观:白色粉末
溶解度:21.5g(20 ℃)
酸碱性:碱性
资料卡片2
碳酸氢钠
化学式:NaHCO3
俗名:小苏打
外观:细小白色晶体
溶解度:9.6g(20 ℃)
酸碱性:弱碱性
线上课前学习
资料卡片
问卷调查
PART
02
课前调研
统计汇总鉴别方法
PART
03
家庭实验分享 1
家庭实验探究两者的外观和溶解情况
观察外观:
溶解情况:
细小的晶体
粉末颗粒更大
加入几滴水后
碳酸钠固体
碳酸氢钠固体
溶解过程热成像视频
PART
03
家庭实验分享 2
家庭实验探究两者的酸碱性
资料1
花青素是一种水溶性天然食用色素,广泛存在于各种植物组织中。因其化学结构和颜色会随环境pH值的变化而发生明显变化,因此花青素被用于开发各种pH指示材料,以达到示警、指示的效果。
富含花青素
PART
03
家庭实验分享 3
家庭实验探究和食醋的反应
等体积的食醋
等体积的食醋
等质量碳酸钠和碳酸氢钠固体
向等体积碳酸钠和碳酸氢钠溶液中
PART
04
小组合作探究1
探究验证Na2CO3和NaHCO3的与HCl的反应
将等浓度盐酸加入到 0.5mol/L的Na2CO3和NaHCO3溶液中
Na2CO3 NaHCO3
现象描述
反应实质
离子方程式
PART
04
小组合作探究1
探究验证Na2CO3和NaHCO3的与HCl的反应
②将等浓度盐酸加入到 12ml 0.5mol/L的Na2CO3和NaHCO3溶液中
Na2CO3 NaHCO3
现象描述
反应实质
离子方程式
一开始无气泡或气泡较少,后产生气泡,溶液由红色逐渐变为无色
一开始产生气泡溶液由淡红色逐渐变为无色
NaHCO3+HCl=NaCl+CO2↑+H2O
Na2CO3+HCl= NaHCO3 + NaCl
NaHCO3+HCl=NaCl+CO2↑+H2O
微观解析:
PART
04
小组合作探究2
探究验证Na2CO3和NaHCO3的热稳定性
观察超市食品袋说明
碳酸氢钠标签
食品添加剂
膨松剂
碳酸氢钠分解
PART
04
小组合作探究2
探究验证Na2CO3和NaHCO3的热稳定性
该装置的缺点
要进行两次加热
没法同时比较两种物质的受热情况
实验装置改进
1.向上下两根试管中分别加入少量的碳酸钠和碳酸氢钠固体。
2.向U型管内倒入一定量的澄清石灰水至刚好没过导管口,向U型管内滴加几滴酚酞。
3.用外焰加热最下面那根试管底部,观察U型管内的现象。
文献查阅
两者受热分解温度
碳酸钠:
1203.74 ℃ -1227.69 ℃
碳酸氢钠:
50.9 ℃ -54.56 ℃
PART
04
小组合作探究3
探究Na2CO3和NaHCO3溶液与Ca(OH)2和CaCl2反应
分别向0.1mol/L的Na2CO3和NaHCO3溶液中滴加数滴0.1mol/L的CaCl2溶液和澄清石灰水
所加物质 项目 Na2CO3 NaHCO3 结论
0.1mol/L的CaCl2溶液 现象
方程式 离子方程式 澄清石灰水 现象
方程式 离子方程式
PART
05
讨论总结
鉴别苏打和小苏打的方法
性质 碳酸钠 碳酸氢钠
颜色状态 白色粉末 细小白色晶体
溶解情况 易溶(S:21.5g),溶于水放热 可溶(S:9.6g),溶于水吸热
水溶液酸碱性 都为碱性,相同浓度下碳酸钠的碱性大于碳酸氢钠 与酸反应 碳酸钠、碳酸氢钠加入盐酸中 Na2CO3+2HCl=NaCl+CO2↑+H2O (反应更慢) NaHCO3+HCl=NaCl+CO2↑+H2O (反应更剧烈)
盐酸加入碳酸钠、碳酸氢钠中 一开始无气泡,后产生气泡 Na2CO3+HCl= NaHCO3+ NaCl NaHCO3+HCl=NaCl+CO2↑+H2O 一开始就产生气泡 NaHCO3+HCl=NaCl+CO2↑+H2O
热稳定性 一般认为不分解 2NaHCO3=Na2CO3+CO2↑+H2O
与碱反应 与澄清石灰水反应变浑浊Na2CO3+Ca(OH)2=2NaOH+CaCO3↓ 与澄清石灰水反应变浑浊NaHCO3+Ca(OH)2=NaOH+CaCO3↓+H2O
与盐反应 Na2CO3+CaCl2=2NaCl+CaCO3↓ CaCl2和BaCl2反应产生沉淀 与CaCl2和BaCl2不反应
△
PART
06
问题再探
雪碧和碳酸钠的故事
Na2CO3+CO2 + H2O =2NaHCO3
向一瓶雪碧里加入足量的碳酸钠固体,用力摇动,另外一瓶不加任何东西,也用力摇动,观察两者现象。
PART
06
问题再探
碳酸钠和碳酸氢钠的互相转化
Na2CO3
NaHCO3
①CO2 + H2O
②加少量HCl
①固体加热
②NaOH溶液
①Na2CO3+CO2 + H2O =2NaHCO3
②Na2CO3+ HCl =NaHCO3+ NaCl
④
③
PART
07
学以致用
解释生活中的一些应用与现象
为什么食堂阿姨用碱粉(纯碱)洗盆碗?
为什么医生建议用小苏打来治疗胃酸过多?
1.为什么苏打水里装的不是苏打而是小苏打?
2.喝碱性水真的有益身体健康吗?
3.15打假真言
1.生命细胞代谢所有过程离不开水,所以要喝水,水是营养物质溶解的载体。
2.只要符合国家饮用水标准的水都是好水。
3.碱性水有益健康的说法只是一种营销手段,不能当真。
PART
08
课堂小结
总结本堂课
鉴别碳酸钠和碳酸氢钠
观察外观
食醋检验反应剧烈程度
与盐酸互滴现象
与澄清石灰水
热稳定性
课堂探究
家庭探究
紫甘蓝检验酸碱性
总结碳酸钠和碳酸氢钠的转化
验证碳酸钠和碳酸氢钠在生活中应用
与CaCl2反应
PART
09
课后任务
完成以下课后任务
观看《千分才子侯德榜》
侯氏制碱法原理
NaCl + NH3 +H2O = NaHCO3 ↓+ NH4Cl
2NaHCO3 = Na2CO3+CO2↑+H2O
给家人们做一份健康又多彩的“变色”的爱心紫薯粥
动动手
感谢您的聆听
敬请批评指正
