第九单元金属练习题(含答案)-2023-2024学年九年级化学鲁教版下册
文档属性
| 名称 | 第九单元金属练习题(含答案)-2023-2024学年九年级化学鲁教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 516.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-20 00:00:00 | ||
图片预览



文档简介
第九单元金属练习题-2023-2024学年九年级化学鲁教版下册
一、选择题
1.卡塔尔世界杯中国元素无处不在。下列说法不正确的是( )
A.打造的卢塞尔体育场的主体钢结构材料属于合金
B.承建的阿尔卡萨光伏电站使用二氧化硅做电极材料
C.支持的比赛草坪灌溉及保养技术可充分利用淡水资源
D.提供的纯电动客车中LiFePO4电池绿色环保能量密度大
2.下列关于金属说法不正确的是( )
A.人类使用金属铜早于铁
B.铝较活泼,其耐腐蚀性比铁差
C.硫酸铜溶液不能盛放在铁桶中
D.合金拓宽了金属材料的应用范围
3.下列关于金属物品使用的描述中,正确的是( )
A.铁制车棚定期喷涂油漆
B.在铁桶中加入硫酸铜溶液和石灰水配制杀菌剂
C.常用自来水冲洗自行车可防止生锈
D.铝合金门窗变旧暗后用砂纸或钢丝球打磨
4.向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,反应过程中,测得混合物中溶液的质量与加入铁粉的质量关系如图所示。有关该反应过程中的下列说法正确的是( )
A.b点,溶液中的阳离子有Fe2+、Cu2+、Ag+
B.c点,向过滤后得到的固体中滴加稀盐酸,无气泡产生
C.d点,溶液中的溶质为Fe(NO3)2和Cu(NO3)2
D.e点,过滤后得到的固体中只含有2种物质
5.芯片的制造代表一个国家的科技水平,我国华为公司在5G及芯片设计开发方面走在了世界的前列。生产芯片的半导体材料主要是硅,工业上以石英砂(SiO2)为主要原料制取高纯硅,涉及反应:。下列说法不正确的是( )
A.该反应中最小微粒是:Si、O、C
B.SiO2发生了还原反应
C.X固体可用于人工降雨
D.SiO2中硅元素和氧元素质量比为7:8
6.小明结合化学知识,给家中厨房用品的使用写了下列建议。其中不可取的是( )
A.燃气灶火焰呈现黄色,锅底出现黑色时,可增大灶具进风口
B.炒菜时油锅中的油着火了,可用锅盖盖灭
C.家里冰箱有异味时,可以放活性炭除臭
D.用钢刷擦洗铝锅表面污垢
7.下列反应中属于置换反应的是( )
A.C+H2O CO+H2
B.2Na2O2+2CO2═2Na2CO2+O2
C.3CO+Fe2O3 2Fe+3CO2
D.2NaCl(熔融) 2Na+Cl2↑
8.化学是无处不在的。下列说法中不正确的是( )
A.石油、煤、天然气都是不可再生的化石燃料
B.小苏打可用于治疗胃酸过多或烘焙蛋糕
C.金制成金箔是利用了金具有良好的导电性
D.室内点煤炉,烟囱通畅可以防止煤气中毒
9.下列观点正确的是( )
A.钢与纯铁相比优点是硬度大、强度高、耐腐蚀、熔点低
B.物质的性质是决定物质用途的唯一因素,物质的用途反映物质的性质
C.浓硫酸与稀硫酸除浓度有差别外,物理和化学性质都相同
D.任何物质只要给予足够高的温度和充足的氧气,一定能够燃烧
10.铝能制成铝箔是因为铝具有( )
A.延展性 B.导电性 C.导热性 D.抗腐蚀性
11.推理是学习化学的重要方法,以下推理正确的是()
A.草原火灾可以用吹风机灭火,则牲畜草料库失火也可以用吹风机灭火
B.燃烧和缓慢氧化都会放出热量,所以粮食发酵过程中一定会放出热量
C.铁是金属,熔点较高,所以金属都是熔点较高的物质
D.催化剂在化学反应前后质量不变,则化学反应前后质量不变的物质就是催化剂
12.下列物质实验现象描述错误的是( )
A.打开浓盐酸的试剂瓶,瓶口冒“白雾”
B.铁丝放入硫酸铜溶液中表面会析出白色固体,溶液由蓝色变为无色
C.木炭在氧气中燃烧,发白光,放出热量,产生能使澄清石灰水变浑浊的气体
D.硫在空气中燃烧,发出淡蓝色火焰,放出热量,产生刺激性气味的气体
13.向一定质量的和的混合溶液中加入一定质量的锌粉,充分反应后过滤,得滤渣和滤液,向滤渣中加入稀盐酸,有气泡产生,根据实验现象分析判断下列说法中不正确的是( )
A.滤液中可能存在
B.化学反应前后滤渣质量一定减少
C.滤渣中一定含Cu和Fe,可能含Zn
D.滤液的颜色可能呈蓝色
14.如图所示的四个图像,能正确反映对应变化关系的是( )
A.向一定量的铜粉中加入硝酸银溶液
B.在密闭容器中用足量红磷测定空气中氧气的含量
C.加热一定量的高锰酸钾制氧气
D.等质量的锌、铁与足量的稀硫酸反应
二、非选择题
15.某金属加工厂生产过程中产生的废液,含有少量硝酸银和硝酸铜,该厂向废液中加入一定量的铁粉,一定会发生反应的化学方程式为 。反应停止后过滤,如果向滤液中加入少量的稀盐酸,无沉淀产生,说明滤液中一 定不含有 。向滤渣中加入稀盐酸,无气体放出,则滤出的固体中可能含有 。
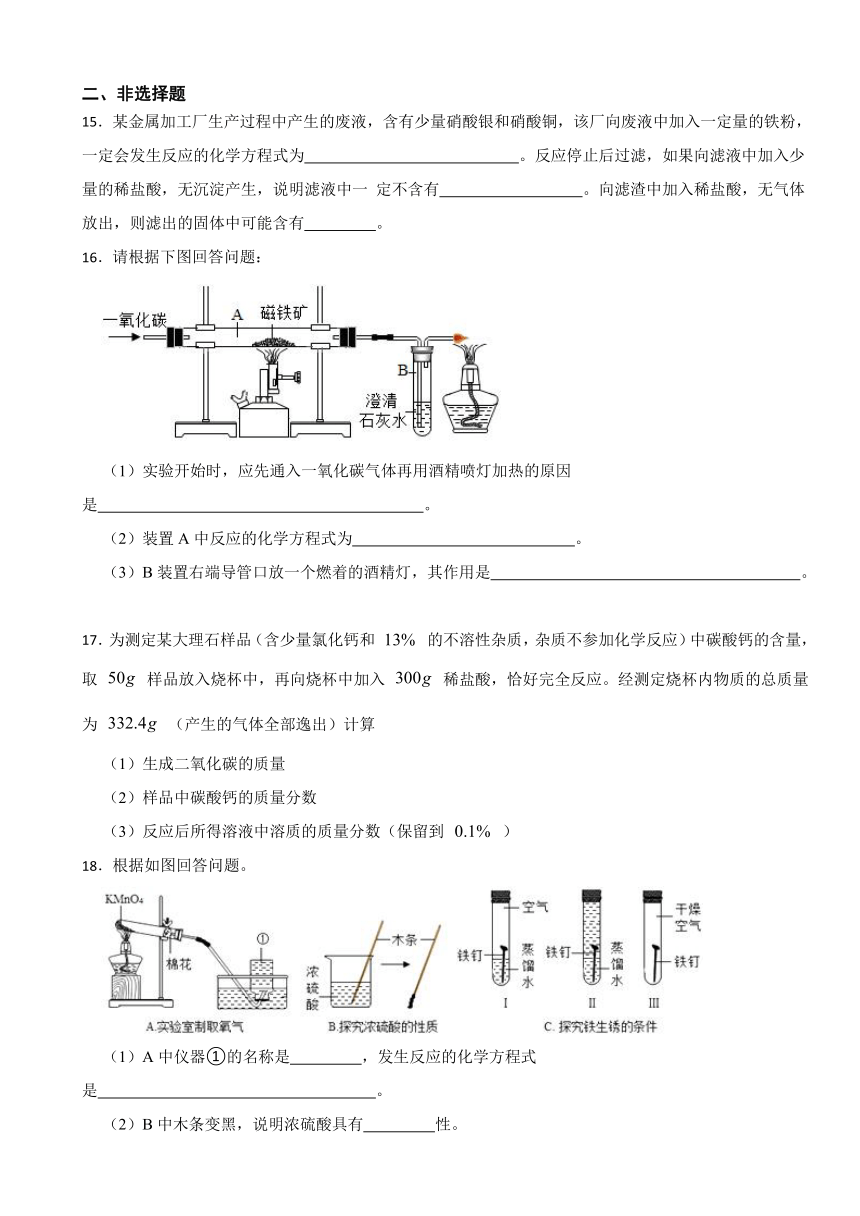
16.请根据下图回答问题:
(1)实验开始时,应先通入一氧化碳气体再用酒精喷灯加热的原因是 。
(2)装置A中反应的化学方程式为 。
(3)B装置右端导管口放一个燃着的酒精灯,其作用是 。
17.为测定某大理石样品(含少量氯化钙和 的不溶性杂质,杂质不参加化学反应)中碳酸钙的含量,取 样品放入烧杯中,再向烧杯中加入 稀盐酸,恰好完全反应。经测定烧杯内物质的总质量为 (产生的气体全部逸出)计算
(1)生成二氧化碳的质量
(2)样品中碳酸钙的质量分数
(3)反应后所得溶液中溶质的质量分数(保留到 )
18.根据如图回答问题。
(1)A中仪器①的名称是 ,发生反应的化学方程式是 。
(2)B中木条变黑,说明浓硫酸具有 性。
(3)C中会出现明显现象的试管是 (填序号),试管Ⅱ中的蒸馏水需要煮沸、迅速冷却后再使用,目的是 。
19.某化学兴趣小组对金属的性质做了如下探究,请你帮他们完成下面的内容。
(1)探究铁生锈的原因(如下图)(每支试管中均放有完全相同的洁净铁钉):
①一段时间后甲同学观察到: 试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与 共同作用的结果。
②为防止金属锈蚀,可以采取的措施有 (填一种)。
③在焊接铁制品前,常用稀盐酸清除其表面的锈,该反应的化学方程式是 。
(2)某同学分别向盛有形状、大小相同的铁片和锌片的试管中,倒入等质量、溶质质量分数相同的稀硫酸,以“ ”为依据来判断两种金属的活动性强弱。
(3)将一定质量的铁粉放入硫酸铜、硫酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是 ,所得滤液中一定含有的溶质是 (填化学式)。
20.材料是人类赖以生存和发展的物质基础。
(1)(一)C60可用作吸氢材料,其原理是C60与H2在一定条件下反应生成氢化物;该氢化物在80 ~ 215 ℃时,又会分解放出H2。
C60属于________(填字母序号)。
A.单质
B.化合物
C.混合物
(2)求算C60的相对分子质量的计算式为 。
(3)C60可用作吸氢材料是利用了其 (填“物理”或“化学”)性质。
(4)(二)铝是目前最经济实用的材料之一。
由铝制成的铝箔厚度仅为0.01 mm,广泛用于食品包装等。铝能制成铝箔,主要利用的铝的性质是 。
(5)铝箔表面有一层致密的氧化膜。用化学方程式表示 。
(6)某小组同学用铝箔做了如下实验:将铝箔在酒精灯上加热,发现铝箔逐渐变软,中间有液体被外面的固体包裹住。由此可以推测氧化铝的熔点比金属铝 (填“高”或“低”)。
21. 我国古代科技璀璨夺目,金属的冶炼与使用在当时已处于世界先进水平。
(1)日常生活中,适合制作电缆的金属是 (填标号)。
A.金 B. 铜 C. 汞 D. 钨
(2)明代《天工开物》描述了锡的冶炼方法,如图a。
①原料锡砂中的SnO2和木炭反应得到锡和二氧化碳,化学方程式为 。
②炼锡时混入少许铅形成合金,产物更易熔化流出,原因是 。
(3)图b为古代炼锌工艺原理示意图。炉甘石成分是ZnCO3,高温易分解生成ZnO。
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是 。
②已知锌的沸点为907℃。泥罐下部温度可达1200℃,上部约为600℃,该工艺从反应混合物中收集液态锌的方法属于 (填标号)。
A.结晶 B.蒸发 C.蒸馏 D.升华
③必须冷却后才能取锌,是为了防止发生反应: (写化学方程式)。
(4)湿法冶金利用置换反应。向Cu(NO3)2、AgNO3混合液中加入Fe粉,充分反应后过滤。若滤渣中有两种金属,则滤液中一定不含的金属阳离子是 。
答案解析部分
1.【答案】B
2.【答案】B
3.【答案】A
4.【答案】B
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】C
9.【答案】A
10.【答案】A
11.【答案】B
12.【答案】B
13.【答案】D
14.【答案】D
15.【答案】;AgNO3或硝酸银;铜或Cu
16.【答案】(1)排出装置内的空气,防止加热时发生爆炸
(2)
(3)进行尾气处理,防止一氧化碳污染空气
17.【答案】(1)17.6g
(2)80%
(3)14.7%
18.【答案】(1)集气瓶;2KMnO4 K2MnO4+MnO2+O2↑
(2)脱水
(3)Ⅰ;除尽水中的氧气
19.【答案】(1)A;氧气和水;在铁制品表面刷漆;Fe2O3+6HCl═2FeCl3+3H2O
(2)金属表面产生气泡的快慢(或剧烈程度)
(3)Cu;ZnSO4、FeSO4
20.【答案】(1)A
(2)12×60
(3)化学
(4)延展性
(5)4Al+3O2 = 2Al2O3
(6)高
21.【答案】(1)B
(2);形成合金熔点降低
(3)作还原剂;C;
(4)银离子或Ag
一、选择题
1.卡塔尔世界杯中国元素无处不在。下列说法不正确的是( )
A.打造的卢塞尔体育场的主体钢结构材料属于合金
B.承建的阿尔卡萨光伏电站使用二氧化硅做电极材料
C.支持的比赛草坪灌溉及保养技术可充分利用淡水资源
D.提供的纯电动客车中LiFePO4电池绿色环保能量密度大
2.下列关于金属说法不正确的是( )
A.人类使用金属铜早于铁
B.铝较活泼,其耐腐蚀性比铁差
C.硫酸铜溶液不能盛放在铁桶中
D.合金拓宽了金属材料的应用范围
3.下列关于金属物品使用的描述中,正确的是( )
A.铁制车棚定期喷涂油漆
B.在铁桶中加入硫酸铜溶液和石灰水配制杀菌剂
C.常用自来水冲洗自行车可防止生锈
D.铝合金门窗变旧暗后用砂纸或钢丝球打磨
4.向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入铁粉,反应过程中,测得混合物中溶液的质量与加入铁粉的质量关系如图所示。有关该反应过程中的下列说法正确的是( )
A.b点,溶液中的阳离子有Fe2+、Cu2+、Ag+
B.c点,向过滤后得到的固体中滴加稀盐酸,无气泡产生
C.d点,溶液中的溶质为Fe(NO3)2和Cu(NO3)2
D.e点,过滤后得到的固体中只含有2种物质
5.芯片的制造代表一个国家的科技水平,我国华为公司在5G及芯片设计开发方面走在了世界的前列。生产芯片的半导体材料主要是硅,工业上以石英砂(SiO2)为主要原料制取高纯硅,涉及反应:。下列说法不正确的是( )
A.该反应中最小微粒是:Si、O、C
B.SiO2发生了还原反应
C.X固体可用于人工降雨
D.SiO2中硅元素和氧元素质量比为7:8
6.小明结合化学知识,给家中厨房用品的使用写了下列建议。其中不可取的是( )
A.燃气灶火焰呈现黄色,锅底出现黑色时,可增大灶具进风口
B.炒菜时油锅中的油着火了,可用锅盖盖灭
C.家里冰箱有异味时,可以放活性炭除臭
D.用钢刷擦洗铝锅表面污垢
7.下列反应中属于置换反应的是( )
A.C+H2O CO+H2
B.2Na2O2+2CO2═2Na2CO2+O2
C.3CO+Fe2O3 2Fe+3CO2
D.2NaCl(熔融) 2Na+Cl2↑
8.化学是无处不在的。下列说法中不正确的是( )
A.石油、煤、天然气都是不可再生的化石燃料
B.小苏打可用于治疗胃酸过多或烘焙蛋糕
C.金制成金箔是利用了金具有良好的导电性
D.室内点煤炉,烟囱通畅可以防止煤气中毒
9.下列观点正确的是( )
A.钢与纯铁相比优点是硬度大、强度高、耐腐蚀、熔点低
B.物质的性质是决定物质用途的唯一因素,物质的用途反映物质的性质
C.浓硫酸与稀硫酸除浓度有差别外,物理和化学性质都相同
D.任何物质只要给予足够高的温度和充足的氧气,一定能够燃烧
10.铝能制成铝箔是因为铝具有( )
A.延展性 B.导电性 C.导热性 D.抗腐蚀性
11.推理是学习化学的重要方法,以下推理正确的是()
A.草原火灾可以用吹风机灭火,则牲畜草料库失火也可以用吹风机灭火
B.燃烧和缓慢氧化都会放出热量,所以粮食发酵过程中一定会放出热量
C.铁是金属,熔点较高,所以金属都是熔点较高的物质
D.催化剂在化学反应前后质量不变,则化学反应前后质量不变的物质就是催化剂
12.下列物质实验现象描述错误的是( )
A.打开浓盐酸的试剂瓶,瓶口冒“白雾”
B.铁丝放入硫酸铜溶液中表面会析出白色固体,溶液由蓝色变为无色
C.木炭在氧气中燃烧,发白光,放出热量,产生能使澄清石灰水变浑浊的气体
D.硫在空气中燃烧,发出淡蓝色火焰,放出热量,产生刺激性气味的气体
13.向一定质量的和的混合溶液中加入一定质量的锌粉,充分反应后过滤,得滤渣和滤液,向滤渣中加入稀盐酸,有气泡产生,根据实验现象分析判断下列说法中不正确的是( )
A.滤液中可能存在
B.化学反应前后滤渣质量一定减少
C.滤渣中一定含Cu和Fe,可能含Zn
D.滤液的颜色可能呈蓝色
14.如图所示的四个图像,能正确反映对应变化关系的是( )
A.向一定量的铜粉中加入硝酸银溶液
B.在密闭容器中用足量红磷测定空气中氧气的含量
C.加热一定量的高锰酸钾制氧气
D.等质量的锌、铁与足量的稀硫酸反应
二、非选择题
15.某金属加工厂生产过程中产生的废液,含有少量硝酸银和硝酸铜,该厂向废液中加入一定量的铁粉,一定会发生反应的化学方程式为 。反应停止后过滤,如果向滤液中加入少量的稀盐酸,无沉淀产生,说明滤液中一 定不含有 。向滤渣中加入稀盐酸,无气体放出,则滤出的固体中可能含有 。
16.请根据下图回答问题:
(1)实验开始时,应先通入一氧化碳气体再用酒精喷灯加热的原因是 。
(2)装置A中反应的化学方程式为 。
(3)B装置右端导管口放一个燃着的酒精灯,其作用是 。
17.为测定某大理石样品(含少量氯化钙和 的不溶性杂质,杂质不参加化学反应)中碳酸钙的含量,取 样品放入烧杯中,再向烧杯中加入 稀盐酸,恰好完全反应。经测定烧杯内物质的总质量为 (产生的气体全部逸出)计算
(1)生成二氧化碳的质量
(2)样品中碳酸钙的质量分数
(3)反应后所得溶液中溶质的质量分数(保留到 )
18.根据如图回答问题。
(1)A中仪器①的名称是 ,发生反应的化学方程式是 。
(2)B中木条变黑,说明浓硫酸具有 性。
(3)C中会出现明显现象的试管是 (填序号),试管Ⅱ中的蒸馏水需要煮沸、迅速冷却后再使用,目的是 。
19.某化学兴趣小组对金属的性质做了如下探究,请你帮他们完成下面的内容。
(1)探究铁生锈的原因(如下图)(每支试管中均放有完全相同的洁净铁钉):
①一段时间后甲同学观察到: 试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与 共同作用的结果。
②为防止金属锈蚀,可以采取的措施有 (填一种)。
③在焊接铁制品前,常用稀盐酸清除其表面的锈,该反应的化学方程式是 。
(2)某同学分别向盛有形状、大小相同的铁片和锌片的试管中,倒入等质量、溶质质量分数相同的稀硫酸,以“ ”为依据来判断两种金属的活动性强弱。
(3)将一定质量的铁粉放入硫酸铜、硫酸锌的混合溶液中,充分反应后过滤,所得固体中一定含有的物质是 ,所得滤液中一定含有的溶质是 (填化学式)。
20.材料是人类赖以生存和发展的物质基础。
(1)(一)C60可用作吸氢材料,其原理是C60与H2在一定条件下反应生成氢化物;该氢化物在80 ~ 215 ℃时,又会分解放出H2。
C60属于________(填字母序号)。
A.单质
B.化合物
C.混合物
(2)求算C60的相对分子质量的计算式为 。
(3)C60可用作吸氢材料是利用了其 (填“物理”或“化学”)性质。
(4)(二)铝是目前最经济实用的材料之一。
由铝制成的铝箔厚度仅为0.01 mm,广泛用于食品包装等。铝能制成铝箔,主要利用的铝的性质是 。
(5)铝箔表面有一层致密的氧化膜。用化学方程式表示 。
(6)某小组同学用铝箔做了如下实验:将铝箔在酒精灯上加热,发现铝箔逐渐变软,中间有液体被外面的固体包裹住。由此可以推测氧化铝的熔点比金属铝 (填“高”或“低”)。
21. 我国古代科技璀璨夺目,金属的冶炼与使用在当时已处于世界先进水平。
(1)日常生活中,适合制作电缆的金属是 (填标号)。
A.金 B. 铜 C. 汞 D. 钨
(2)明代《天工开物》描述了锡的冶炼方法,如图a。
①原料锡砂中的SnO2和木炭反应得到锡和二氧化碳,化学方程式为 。
②炼锡时混入少许铅形成合金,产物更易熔化流出,原因是 。
(3)图b为古代炼锌工艺原理示意图。炉甘石成分是ZnCO3,高温易分解生成ZnO。
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是 。
②已知锌的沸点为907℃。泥罐下部温度可达1200℃,上部约为600℃,该工艺从反应混合物中收集液态锌的方法属于 (填标号)。
A.结晶 B.蒸发 C.蒸馏 D.升华
③必须冷却后才能取锌,是为了防止发生反应: (写化学方程式)。
(4)湿法冶金利用置换反应。向Cu(NO3)2、AgNO3混合液中加入Fe粉,充分反应后过滤。若滤渣中有两种金属,则滤液中一定不含的金属阳离子是 。
答案解析部分
1.【答案】B
2.【答案】B
3.【答案】A
4.【答案】B
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】C
9.【答案】A
10.【答案】A
11.【答案】B
12.【答案】B
13.【答案】D
14.【答案】D
15.【答案】;AgNO3或硝酸银;铜或Cu
16.【答案】(1)排出装置内的空气,防止加热时发生爆炸
(2)
(3)进行尾气处理,防止一氧化碳污染空气
17.【答案】(1)17.6g
(2)80%
(3)14.7%
18.【答案】(1)集气瓶;2KMnO4 K2MnO4+MnO2+O2↑
(2)脱水
(3)Ⅰ;除尽水中的氧气
19.【答案】(1)A;氧气和水;在铁制品表面刷漆;Fe2O3+6HCl═2FeCl3+3H2O
(2)金属表面产生气泡的快慢(或剧烈程度)
(3)Cu;ZnSO4、FeSO4
20.【答案】(1)A
(2)12×60
(3)化学
(4)延展性
(5)4Al+3O2 = 2Al2O3
(6)高
21.【答案】(1)B
(2);形成合金熔点降低
(3)作还原剂;C;
(4)银离子或Ag
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
