第八单元金属和金属材料基础练习题(含答案)-2023-2024学年九年级化学人教版下册
文档属性
| 名称 | 第八单元金属和金属材料基础练习题(含答案)-2023-2024学年九年级化学人教版下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 158.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-20 00:00:00 | ||
图片预览



文档简介
第八单元 金属和金属材料 基础练习题(含答案)2023—2024学年人教版化学人教九年级下册
一、选择题。
1、下列关于“金属之最”的说法中正确的是( )
A.硬度最高的金属是铁 B.目前,世界年产量最高的金属是铝
C.导电性最好的金属是钨 D.熔点最低的金属是汞
2、合金由于其优良的性能在生产生活中得到了广泛的使用。下列关于合金及纯金属的各项比较及应用中,不正确的是( )
A.强度:硬铝>铝 硬铝可用于制作汽车、飞机和火箭
B.抗腐蚀能力:不锈钢>纯铁 不锈钢用于制造医疗器械
C.硬度:纯铁>生铁 用生铁制作机器底座
D.熔点:纯锡>武德合金 用武德合金制作保险丝
3、下图是某原子的结构示意图。下列关于该原子的说法不正确的是( )
A. 属于金属元素原子 B. 最外层电子数为7
C. 容易得到电子 D. 有3个电子层
4、黄金是一种贵重金属,它不仅被视为美好和富有的象征,而且还以其特有的价值造福于人类。常言道:“真金不怕火炼”主要是指( )
A.熔点高 B.延展性好 C.有金属光泽 D.化学性质稳定
5、为了探究镁、锌、铜三种金属的活动性强弱,将形状、大小相同的三种金属分别放入装有X溶液的试管中,通过观察现象即能得出实验结论。则X溶液是( )
A.稀硫酸 B.硝酸银溶液
C.氯化铜溶液 D.氯化镁溶液
6、向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入m g Zn,充分反应后过滤,将滤渣洗涤、干燥后再称量,得到的质量为m g。据此,下列说法错误的是( )
A. 取反应后的滤液观察,滤液可能呈蓝色
B. 取反应后的滤液滴加稀盐酸,有白色沉淀产生
C. 取滤渣滴加稀硫酸,可能有气泡产生
D. 滤渣中的物质至少有两种
7、下列关于金属的说法中不正确的是( )
A.大多数金属在自然界中以化合物的形式存在
B.钢和生铁均属于铁的合金
C.应该大力开发金属矿物资源以满足人类生产和生活的需要
D.人类最早使用的金属是铜,常见的铜矿有黄铜矿和辉铜矿等
8、下列有关金属资源的利用与保护的说法不合理的是( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
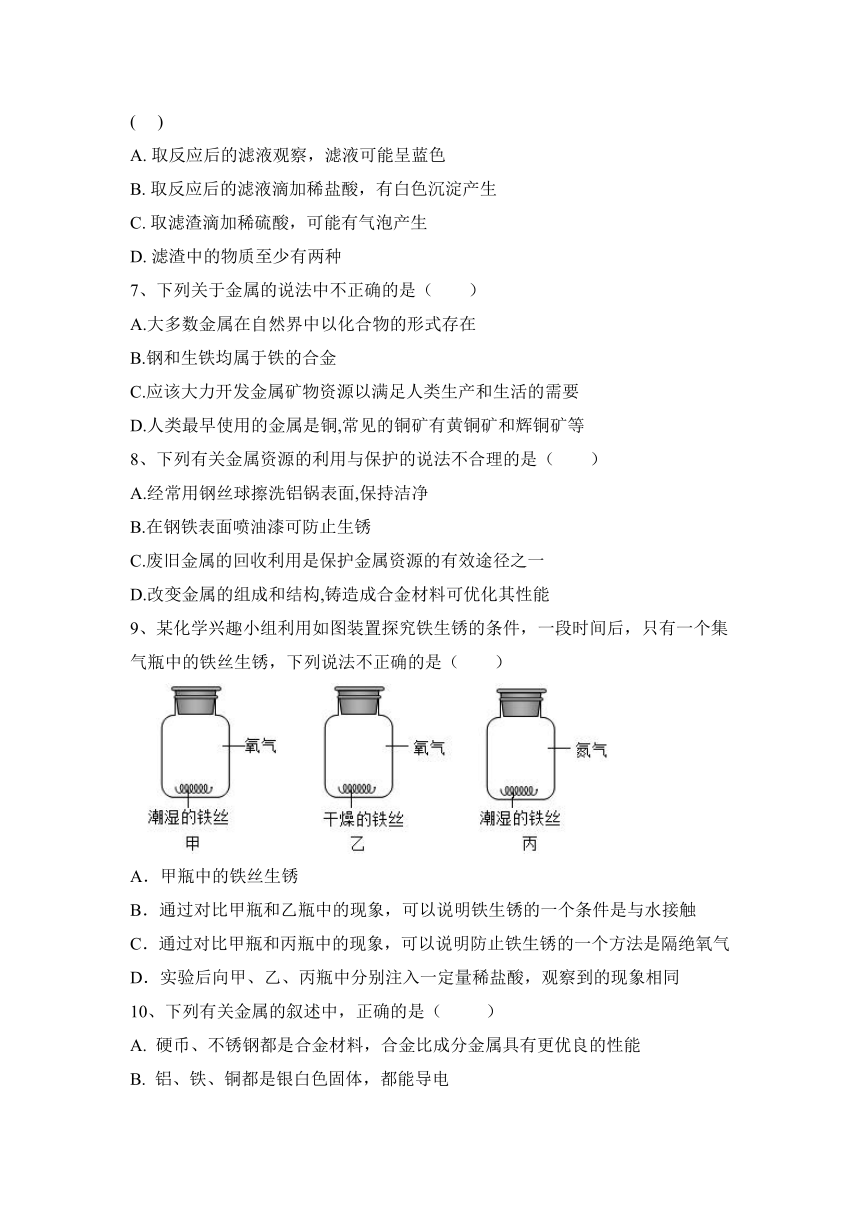
9、某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法不正确的是( )
A.甲瓶中的铁丝生锈
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比甲瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向甲、乙、丙瓶中分别注入一定量稀盐酸,观察到的现象相同
10、下列有关金属的叙述中,正确的是( )
A. 硬币、不锈钢都是合金材料,合金比成分金属具有更优良的性能
B. 铝、铁、铜都是银白色固体,都能导电
C. 镁、铝都是活泼金属,相同质量时与足量的盐酸反应放出氢气的体积相同
D. 铁在空气中燃烧,冒出浓烈的黑烟,放出热量,生成黑色粉末
11、将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
A.反应结束后镁一定有剩余
B.反应消耗盐酸的总质量一定相等
C.0~t1时段,产生氢气的质量镁比铁大
D.0~t2时段,参加反应的镁的质量与铁相等
12、合金在生活中的应用非常广泛,下列关于合金的说法正确的是( )
A. 合金不属于金属材料 B. 合金的硬度一般比组成金属小
C. 生铁的含铁量比钢高 D. 合金不一定是金属和金属熔合而成的
13、现有三种金属X、Y、Z,它们之间能发生如下反应:Y+X(NO3)2=X+Y(NO3)2, X + ZCl2=Z+ XCl2.问X、Y、Z三种金属的活动性由强到弱的排列顺序是( )
A. Z>Y=X B. X<Y<Z C. Y>X>Z D. X>Z>Y
14、下列有关金属材料的说法错误的是( )
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
15、下列叙述属于铁的物理性质的是( )
A.铁在氧气中燃烧时火花四溅 B.铁在1 535 ℃时变为铁水
C.铁投入盐酸中,有气泡冒出 D.铁投入硫酸铜溶液有铜析出
16、有一镁的合金2.4 g,在合金中加入100 g一定质量分数的稀盐酸后,金属与稀盐酸恰好完全反应,产生氢气的质量为m,下列说法错误的是( )
A.若是镁铝合金,则m>0.2 g
B.若是镁锌合金,则m<0.2 g
C.若是镁铜合金,则稀盐酸溶质的质量分数小于7.3%
D.若是镁铁合金,m=0.16 g,则合金中铁的质量分数是5
二、填空题。
17、合金比起组成它们的纯金属,其强度和硬度更_____,熔点更______, ___________性能更好。
18、现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末。欲确定R的成分,请你一起完成:
(1)请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置。
(2)取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是___________________________。
(3)待不再产生气泡时,再进行__________(填写一种实验操作方法),得到溶液和铜。然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是______。
(4)写出金属R与稀硫酸反应的化学方程式____________________________。
该反应的基本类型属于______(填“化合”、“分解”、“置换”或“复分解”)反应。
19、铝、铁、铜是人类广泛使用的三种金属,与我们的生活息息相关。
(1)用铜块制成铜片、铜丝利用了铜的________性.钢铁制品容易发生锈蚀,在其表面涂油漆的防锈原理是________ 。
(2)钢铁是用量最大、用途最广的含________量不同的铁合金。
(3)将纯铝和铝合金相互刻划,纯铝上留下明显划痕.请你解释其中的原因________ 。
20、金属材料在生产、生活中应用广泛。
(1)由于金属铜具有良好的________,常用于制作导线。
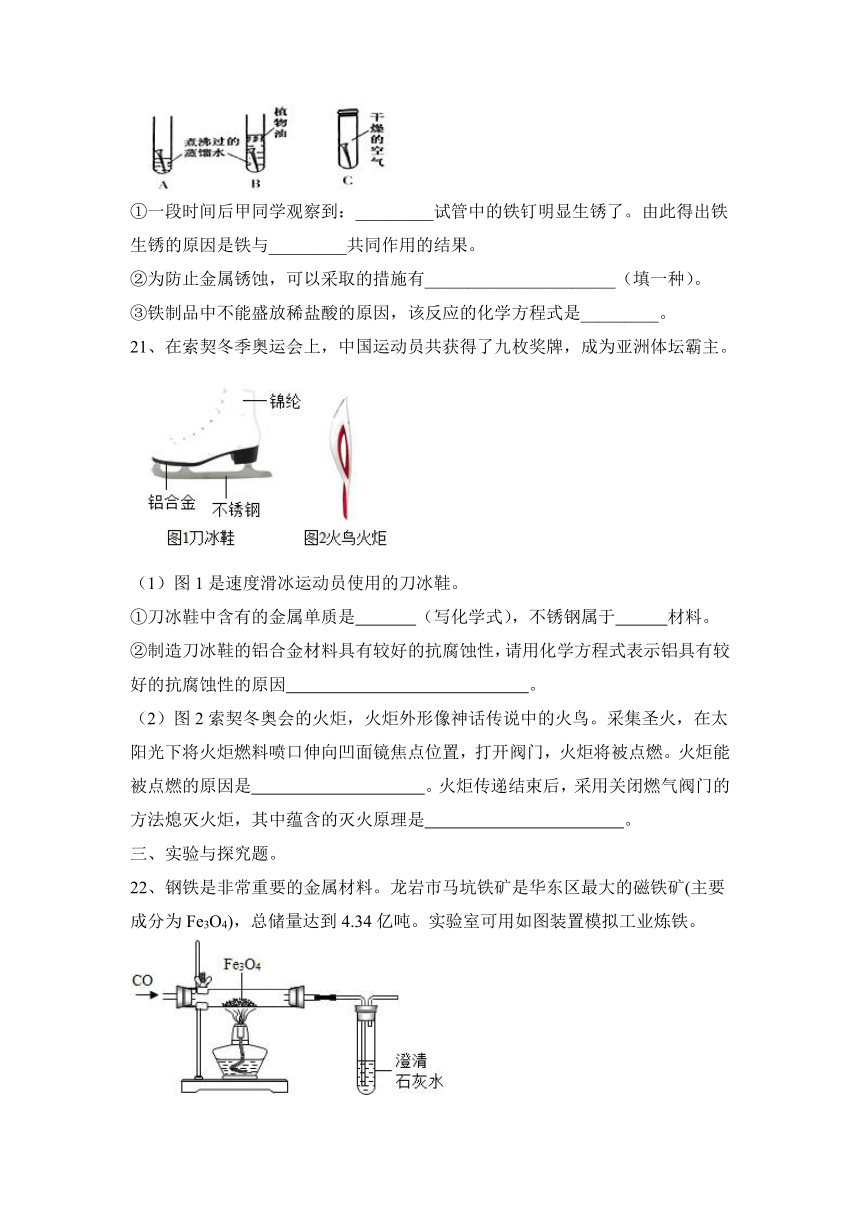
(2)现有如下实验装置(每支试管中均放有完全相同的洁净铁钉):
①一段时间后甲同学观察到:_________试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与_________共同作用的结果。
②为防止金属锈蚀,可以采取的措施有______________________(填一种)。
③铁制品中不能盛放稀盐酸的原因,该反应的化学方程式是_________。
21、在索契冬季奥运会上,中国运动员共获得了九枚奖牌,成为亚洲体坛霸主。
(1)图1是速度滑冰运动员使用的刀冰鞋。
①刀冰鞋中含有的金属单质是 (写化学式),不锈钢属于 材料。
②制造刀冰鞋的铝合金材料具有较好的抗腐蚀性,请用化学方程式表示铝具有较好的抗腐蚀性的原因 。
(2)图2索契冬奥会的火炬,火炬外形像神话传说中的火鸟。采集圣火,在太阳光下将火炬燃料喷口伸向凹面镜焦点位置,打开阀门,火炬将被点燃。火炬能被点燃的原因是 。火炬传递结束后,采用关闭燃气阀门的方法熄灭火炬,其中蕴含的灭火原理是 。
三、实验与探究题。
22、钢铁是非常重要的金属材料。龙岩市马坑铁矿是华东区最大的磁铁矿(主要成分为Fe3O4),总储量达到4.34亿吨。实验室可用如图装置模拟工业炼铁。
(1)写出CO与Fe3O4反应的化学方程式 ___________ 。
(2)实验过程中,常在装置图末端的导气管口放一盏燃着的酒精灯(灯焰处于导管口),这样做的目的是___________。
(3)为检验反应后有铁生成,进行如下实验:将反应后的固体取少量放入稀盐酸中,观察到有气泡冒出。写出该反应的化学方程式:___________。
(4)工业炼铁时还需要石灰石等原料,我市也有着丰富的石灰石资源。请写出石灰石的另一种用途___________。
23、如图所示是一氧化碳还原氧化铁的实验。
(1)硬质玻璃管中观察到的现象是 ,发生反应的化学方程式为 。
(2)试管中澄清石灰水的作用是 。
(3)该实验进行尾气处理的方法体现了CO具有的化学性质是 。
24、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
(1)一段时间后,可观察到实验Ⅱ中现象是 ;反应的化学方程式是 。
(2)甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱。你认为他依据的实验现象是__ 。
(3)乙和丙两位同学认为上述三个实验不能够得出四种金属活动性顺序,原因是 ;并在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的。
他们的实验:X是金属Fe,Y是__ __(写出化学式)溶液。
四、计算题。
25、我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 第二次 第三次
连续加入盐酸的体积/mL 10 10 10
生成氢气的质量/g 0.08 0.08 0.04
(1)从上表数据分析,小华用10 g合金粉末总共收集到氢气________g。
(2)求该合金中铜的质量分数。
第八单元 金属和金属材料 基础练习题(含答案)2023—2024学年人教版化学人教九年级下册
一、选择题。
1、下列关于“金属之最”的说法中正确的是( )
A.硬度最高的金属是铁 B.目前,世界年产量最高的金属是铝
C.导电性最好的金属是钨 D.熔点最低的金属是汞
【答案】D
2、合金由于其优良的性能在生产生活中得到了广泛的使用。下列关于合金及纯金属的各项比较及应用中,不正确的是( )
A.强度:硬铝>铝 硬铝可用于制作汽车、飞机和火箭
B.抗腐蚀能力:不锈钢>纯铁 不锈钢用于制造医疗器械
C.硬度:纯铁>生铁 用生铁制作机器底座
D.熔点:纯锡>武德合金 用武德合金制作保险丝
【答案】C
3、下图是某原子的结构示意图。下列关于该原子的说法不正确的是( )
A. 属于金属元素原子 B. 最外层电子数为7
C. 容易得到电子 D. 有3个电子层
【答案】A
4、黄金是一种贵重金属,它不仅被视为美好和富有的象征,而且还以其特有的价值造福于人类。常言道:“真金不怕火炼”主要是指( )
A.熔点高 B.延展性好 C.有金属光泽 D.化学性质稳定
【答案】D
5、为了探究镁、锌、铜三种金属的活动性强弱,将形状、大小相同的三种金属分别放入装有X溶液的试管中,通过观察现象即能得出实验结论。则X溶液是( )
A.稀硫酸 B.硝酸银溶液
C.氯化铜溶液 D.氯化镁溶液
【答案】A
6、向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入m g Zn,充分反应后过滤,将滤渣洗涤、干燥后再称量,得到的质量为m g。据此,下列说法错误的是( )
A. 取反应后的滤液观察,滤液可能呈蓝色
B. 取反应后的滤液滴加稀盐酸,有白色沉淀产生
C. 取滤渣滴加稀硫酸,可能有气泡产生
D. 滤渣中的物质至少有两种
【答案】B
7、下列关于金属的说法中不正确的是( )
A.大多数金属在自然界中以化合物的形式存在
B.钢和生铁均属于铁的合金
C.应该大力开发金属矿物资源以满足人类生产和生活的需要
D.人类最早使用的金属是铜,常见的铜矿有黄铜矿和辉铜矿等
【答案】C
8、下列有关金属资源的利用与保护的说法不合理的是( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
【答案】A
9、某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法不正确的是( )
A.甲瓶中的铁丝生锈
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比甲瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向甲、乙、丙瓶中分别注入一定量稀盐酸,观察到的现象相同
【答案】D
10、下列有关金属的叙述中,正确的是( )
A. 硬币、不锈钢都是合金材料,合金比成分金属具有更优良的性能
B. 铝、铁、铜都是银白色固体,都能导电
C. 镁、铝都是活泼金属,相同质量时与足量的盐酸反应放出氢气的体积相同
D. 铁在空气中燃烧,冒出浓烈的黑烟,放出热量,生成黑色粉末
【答案】A
11、将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
A.反应结束后镁一定有剩余
B.反应消耗盐酸的总质量一定相等
C.0~t1时段,产生氢气的质量镁比铁大
D.0~t2时段,参加反应的镁的质量与铁相等
【答案】D
12、合金在生活中的应用非常广泛,下列关于合金的说法正确的是( )
A. 合金不属于金属材料 B. 合金的硬度一般比组成金属小
C. 生铁的含铁量比钢高 D. 合金不一定是金属和金属熔合而成的
【答案】D
13、现有三种金属X、Y、Z,它们之间能发生如下反应:Y+X(NO3)2=X+Y(NO3)2, X + ZCl2=Z+ XCl2.问X、Y、Z三种金属的活动性由强到弱的排列顺序是( )
A. Z>Y=X B. X<Y<Z C. Y>X>Z D. X>Z>Y
【答案】C
14、下列有关金属材料的说法错误的是( )
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
【答案】C
15、下列叙述属于铁的物理性质的是( )
A.铁在氧气中燃烧时火花四溅 B.铁在1 535 ℃时变为铁水
C.铁投入盐酸中,有气泡冒出 D.铁投入硫酸铜溶液有铜析出
【答案】B
16、有一镁的合金2.4 g,在合金中加入100 g一定质量分数的稀盐酸后,金属与稀盐酸恰好完全反应,产生氢气的质量为m,下列说法错误的是( )
A.若是镁铝合金,则m>0.2 g
B.若是镁锌合金,则m<0.2 g
C.若是镁铜合金,则稀盐酸溶质的质量分数小于7.3%
D.若是镁铁合金,m=0.16 g,则合金中铁的质量分数是5
【答案】D
二、填空题。
17、合金比起组成它们的纯金属,其强度和硬度更_____,熔点更______, ___________性能更好。
【答案】高 低 抗腐蚀
18、现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末。欲确定R的成分,请你一起完成:
(1)请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置。
(2)取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是___________________________。
(3)待不再产生气泡时,再进行__________(填写一种实验操作方法),得到溶液和铜。然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是______。
(4)写出金属R与稀硫酸反应的化学方程式____________________________。
该反应的基本类型属于______(填“化合”、“分解”、“置换”或“复分解”)反应。
【答案】(1)
(2)银(或Ag) (3)过滤 铁(或Fe)
(4)Fe+H2SO4 ==== FeSO4+H2↑ 置换
19、铝、铁、铜是人类广泛使用的三种金属,与我们的生活息息相关。
(1)用铜块制成铜片、铜丝利用了铜的________性.钢铁制品容易发生锈蚀,在其表面涂油漆的防锈原理是________ 。
(2)钢铁是用量最大、用途最广的含________量不同的铁合金。
(3)将纯铝和铝合金相互刻划,纯铝上留下明显划痕.请你解释其中的原因________ 。
【答案】(1)延展;隔绝水和氧气 (2)碳
(3)铝合金的硬度比纯铝大
20、金属材料在生产、生活中应用广泛。
(1)由于金属铜具有良好的________,常用于制作导线。
(2)现有如下实验装置(每支试管中均放有完全相同的洁净铁钉):
①一段时间后甲同学观察到:_________试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与_________共同作用的结果。
②为防止金属锈蚀,可以采取的措施有______________________(填一种)。
③铁制品中不能盛放稀盐酸的原因,该反应的化学方程式是_________。
【答案】导电性 A 水和氧气 在铁制品表面刷漆
Fe+2HCl═FeCl2+H2↑
21、在索契冬季奥运会上,中国运动员共获得了九枚奖牌,成为亚洲体坛霸主。
(1)图1是速度滑冰运动员使用的刀冰鞋。
①刀冰鞋中含有的金属单质是 (写化学式),不锈钢属于 材料。
②制造刀冰鞋的铝合金材料具有较好的抗腐蚀性,请用化学方程式表示铝具有较好的抗腐蚀性的原因 。
(2)图2索契冬奥会的火炬,火炬外形像神话传说中的火鸟。采集圣火,在太阳光下将火炬燃料喷口伸向凹面镜焦点位置,打开阀门,火炬将被点燃。火炬能被点燃的原因是 。火炬传递结束后,采用关闭燃气阀门的方法熄灭火炬,其中蕴含的灭火原理是 。
【答案】Fe或Al 金属 4Al+3O2==2Al2O3
(2)温度达到着火点 隔离可燃物
三、实验与探究题。
22、钢铁是非常重要的金属材料。龙岩市马坑铁矿是华东区最大的磁铁矿(主要成分为Fe3O4),总储量达到4.34亿吨。实验室可用如图装置模拟工业炼铁。
(1)写出CO与Fe3O4反应的化学方程式 ___________ 。
(2)实验过程中,常在装置图末端的导气管口放一盏燃着的酒精灯(灯焰处于导管口),这样做的目的是___________。
(3)为检验反应后有铁生成,进行如下实验:将反应后的固体取少量放入稀盐酸中,观察到有气泡冒出。写出该反应的化学方程式:___________。
(4)工业炼铁时还需要石灰石等原料,我市也有着丰富的石灰石资源。请写出石灰石的另一种用途___________。
【答案】
除去尾气中的CO 生产生石灰
23、如图所示是一氧化碳还原氧化铁的实验。
(1)硬质玻璃管中观察到的现象是 ,发生反应的化学方程式为 。
(2)试管中澄清石灰水的作用是 。
(3)该实验进行尾气处理的方法体现了CO具有的化学性质是 。
【答案】(1)红色粉末逐渐变成黑色 3CO+Fe2O3 2Fe+3CO2
(2)检验产物是否生成二氧化碳 (3)可燃性
24、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
(1)一段时间后,可观察到实验Ⅱ中现象是 ;反应的化学方程式是 。
(2)甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱。你认为他依据的实验现象是__ 。
(3)乙和丙两位同学认为上述三个实验不能够得出四种金属活动性顺序,原因是 ;并在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的。
他们的实验:X是金属Fe,Y是__ __(写出化学式)溶液。
【答案】铜片表面有银白色固体析出,溶液由无色变为蓝色 Cu+2AgNO3===2Ag+Cu(NO3)2 锌与稀盐酸反应的程度要比铁的剧烈
无法比较铁与铜的活动性强弱 CuSO4[或CuCl2、Cu(NO3)2等]
四、计算题。
25、我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 第二次 第三次
连续加入盐酸的体积/mL 10 10 10
生成氢气的质量/g 0.08 0.08 0.04
(1)从上表数据分析,小华用10 g合金粉末总共收集到氢气________g。
(2)求该合金中铜的质量分数。
【答案】(1)0.2g (2)35%
一、选择题。
1、下列关于“金属之最”的说法中正确的是( )
A.硬度最高的金属是铁 B.目前,世界年产量最高的金属是铝
C.导电性最好的金属是钨 D.熔点最低的金属是汞
2、合金由于其优良的性能在生产生活中得到了广泛的使用。下列关于合金及纯金属的各项比较及应用中,不正确的是( )
A.强度:硬铝>铝 硬铝可用于制作汽车、飞机和火箭
B.抗腐蚀能力:不锈钢>纯铁 不锈钢用于制造医疗器械
C.硬度:纯铁>生铁 用生铁制作机器底座
D.熔点:纯锡>武德合金 用武德合金制作保险丝
3、下图是某原子的结构示意图。下列关于该原子的说法不正确的是( )
A. 属于金属元素原子 B. 最外层电子数为7
C. 容易得到电子 D. 有3个电子层
4、黄金是一种贵重金属,它不仅被视为美好和富有的象征,而且还以其特有的价值造福于人类。常言道:“真金不怕火炼”主要是指( )
A.熔点高 B.延展性好 C.有金属光泽 D.化学性质稳定
5、为了探究镁、锌、铜三种金属的活动性强弱,将形状、大小相同的三种金属分别放入装有X溶液的试管中,通过观察现象即能得出实验结论。则X溶液是( )
A.稀硫酸 B.硝酸银溶液
C.氯化铜溶液 D.氯化镁溶液
6、向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入m g Zn,充分反应后过滤,将滤渣洗涤、干燥后再称量,得到的质量为m g。据此,下列说法错误的是( )
A. 取反应后的滤液观察,滤液可能呈蓝色
B. 取反应后的滤液滴加稀盐酸,有白色沉淀产生
C. 取滤渣滴加稀硫酸,可能有气泡产生
D. 滤渣中的物质至少有两种
7、下列关于金属的说法中不正确的是( )
A.大多数金属在自然界中以化合物的形式存在
B.钢和生铁均属于铁的合金
C.应该大力开发金属矿物资源以满足人类生产和生活的需要
D.人类最早使用的金属是铜,常见的铜矿有黄铜矿和辉铜矿等
8、下列有关金属资源的利用与保护的说法不合理的是( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
9、某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法不正确的是( )
A.甲瓶中的铁丝生锈
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比甲瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向甲、乙、丙瓶中分别注入一定量稀盐酸,观察到的现象相同
10、下列有关金属的叙述中,正确的是( )
A. 硬币、不锈钢都是合金材料,合金比成分金属具有更优良的性能
B. 铝、铁、铜都是银白色固体,都能导电
C. 镁、铝都是活泼金属,相同质量时与足量的盐酸反应放出氢气的体积相同
D. 铁在空气中燃烧,冒出浓烈的黑烟,放出热量,生成黑色粉末
11、将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
A.反应结束后镁一定有剩余
B.反应消耗盐酸的总质量一定相等
C.0~t1时段,产生氢气的质量镁比铁大
D.0~t2时段,参加反应的镁的质量与铁相等
12、合金在生活中的应用非常广泛,下列关于合金的说法正确的是( )
A. 合金不属于金属材料 B. 合金的硬度一般比组成金属小
C. 生铁的含铁量比钢高 D. 合金不一定是金属和金属熔合而成的
13、现有三种金属X、Y、Z,它们之间能发生如下反应:Y+X(NO3)2=X+Y(NO3)2, X + ZCl2=Z+ XCl2.问X、Y、Z三种金属的活动性由强到弱的排列顺序是( )
A. Z>Y=X B. X<Y<Z C. Y>X>Z D. X>Z>Y
14、下列有关金属材料的说法错误的是( )
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
15、下列叙述属于铁的物理性质的是( )
A.铁在氧气中燃烧时火花四溅 B.铁在1 535 ℃时变为铁水
C.铁投入盐酸中,有气泡冒出 D.铁投入硫酸铜溶液有铜析出
16、有一镁的合金2.4 g,在合金中加入100 g一定质量分数的稀盐酸后,金属与稀盐酸恰好完全反应,产生氢气的质量为m,下列说法错误的是( )
A.若是镁铝合金,则m>0.2 g
B.若是镁锌合金,则m<0.2 g
C.若是镁铜合金,则稀盐酸溶质的质量分数小于7.3%
D.若是镁铁合金,m=0.16 g,则合金中铁的质量分数是5
二、填空题。
17、合金比起组成它们的纯金属,其强度和硬度更_____,熔点更______, ___________性能更好。
18、现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末。欲确定R的成分,请你一起完成:
(1)请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置。
(2)取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是___________________________。
(3)待不再产生气泡时,再进行__________(填写一种实验操作方法),得到溶液和铜。然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是______。
(4)写出金属R与稀硫酸反应的化学方程式____________________________。
该反应的基本类型属于______(填“化合”、“分解”、“置换”或“复分解”)反应。
19、铝、铁、铜是人类广泛使用的三种金属,与我们的生活息息相关。
(1)用铜块制成铜片、铜丝利用了铜的________性.钢铁制品容易发生锈蚀,在其表面涂油漆的防锈原理是________ 。
(2)钢铁是用量最大、用途最广的含________量不同的铁合金。
(3)将纯铝和铝合金相互刻划,纯铝上留下明显划痕.请你解释其中的原因________ 。
20、金属材料在生产、生活中应用广泛。
(1)由于金属铜具有良好的________,常用于制作导线。
(2)现有如下实验装置(每支试管中均放有完全相同的洁净铁钉):
①一段时间后甲同学观察到:_________试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与_________共同作用的结果。
②为防止金属锈蚀,可以采取的措施有______________________(填一种)。
③铁制品中不能盛放稀盐酸的原因,该反应的化学方程式是_________。
21、在索契冬季奥运会上,中国运动员共获得了九枚奖牌,成为亚洲体坛霸主。
(1)图1是速度滑冰运动员使用的刀冰鞋。
①刀冰鞋中含有的金属单质是 (写化学式),不锈钢属于 材料。
②制造刀冰鞋的铝合金材料具有较好的抗腐蚀性,请用化学方程式表示铝具有较好的抗腐蚀性的原因 。
(2)图2索契冬奥会的火炬,火炬外形像神话传说中的火鸟。采集圣火,在太阳光下将火炬燃料喷口伸向凹面镜焦点位置,打开阀门,火炬将被点燃。火炬能被点燃的原因是 。火炬传递结束后,采用关闭燃气阀门的方法熄灭火炬,其中蕴含的灭火原理是 。
三、实验与探究题。
22、钢铁是非常重要的金属材料。龙岩市马坑铁矿是华东区最大的磁铁矿(主要成分为Fe3O4),总储量达到4.34亿吨。实验室可用如图装置模拟工业炼铁。
(1)写出CO与Fe3O4反应的化学方程式 ___________ 。
(2)实验过程中,常在装置图末端的导气管口放一盏燃着的酒精灯(灯焰处于导管口),这样做的目的是___________。
(3)为检验反应后有铁生成,进行如下实验:将反应后的固体取少量放入稀盐酸中,观察到有气泡冒出。写出该反应的化学方程式:___________。
(4)工业炼铁时还需要石灰石等原料,我市也有着丰富的石灰石资源。请写出石灰石的另一种用途___________。
23、如图所示是一氧化碳还原氧化铁的实验。
(1)硬质玻璃管中观察到的现象是 ,发生反应的化学方程式为 。
(2)试管中澄清石灰水的作用是 。
(3)该实验进行尾气处理的方法体现了CO具有的化学性质是 。
24、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
(1)一段时间后,可观察到实验Ⅱ中现象是 ;反应的化学方程式是 。
(2)甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱。你认为他依据的实验现象是__ 。
(3)乙和丙两位同学认为上述三个实验不能够得出四种金属活动性顺序,原因是 ;并在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的。
他们的实验:X是金属Fe,Y是__ __(写出化学式)溶液。
四、计算题。
25、我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 第二次 第三次
连续加入盐酸的体积/mL 10 10 10
生成氢气的质量/g 0.08 0.08 0.04
(1)从上表数据分析,小华用10 g合金粉末总共收集到氢气________g。
(2)求该合金中铜的质量分数。
第八单元 金属和金属材料 基础练习题(含答案)2023—2024学年人教版化学人教九年级下册
一、选择题。
1、下列关于“金属之最”的说法中正确的是( )
A.硬度最高的金属是铁 B.目前,世界年产量最高的金属是铝
C.导电性最好的金属是钨 D.熔点最低的金属是汞
【答案】D
2、合金由于其优良的性能在生产生活中得到了广泛的使用。下列关于合金及纯金属的各项比较及应用中,不正确的是( )
A.强度:硬铝>铝 硬铝可用于制作汽车、飞机和火箭
B.抗腐蚀能力:不锈钢>纯铁 不锈钢用于制造医疗器械
C.硬度:纯铁>生铁 用生铁制作机器底座
D.熔点:纯锡>武德合金 用武德合金制作保险丝
【答案】C
3、下图是某原子的结构示意图。下列关于该原子的说法不正确的是( )
A. 属于金属元素原子 B. 最外层电子数为7
C. 容易得到电子 D. 有3个电子层
【答案】A
4、黄金是一种贵重金属,它不仅被视为美好和富有的象征,而且还以其特有的价值造福于人类。常言道:“真金不怕火炼”主要是指( )
A.熔点高 B.延展性好 C.有金属光泽 D.化学性质稳定
【答案】D
5、为了探究镁、锌、铜三种金属的活动性强弱,将形状、大小相同的三种金属分别放入装有X溶液的试管中,通过观察现象即能得出实验结论。则X溶液是( )
A.稀硫酸 B.硝酸银溶液
C.氯化铜溶液 D.氯化镁溶液
【答案】A
6、向一定质量的AgNO3和Cu(NO3)2的混合溶液中加入m g Zn,充分反应后过滤,将滤渣洗涤、干燥后再称量,得到的质量为m g。据此,下列说法错误的是( )
A. 取反应后的滤液观察,滤液可能呈蓝色
B. 取反应后的滤液滴加稀盐酸,有白色沉淀产生
C. 取滤渣滴加稀硫酸,可能有气泡产生
D. 滤渣中的物质至少有两种
【答案】B
7、下列关于金属的说法中不正确的是( )
A.大多数金属在自然界中以化合物的形式存在
B.钢和生铁均属于铁的合金
C.应该大力开发金属矿物资源以满足人类生产和生活的需要
D.人类最早使用的金属是铜,常见的铜矿有黄铜矿和辉铜矿等
【答案】C
8、下列有关金属资源的利用与保护的说法不合理的是( )
A.经常用钢丝球擦洗铝锅表面,保持洁净
B.在钢铁表面喷油漆可防止生锈
C.废旧金属的回收利用是保护金属资源的有效途径之一
D.改变金属的组成和结构,铸造成合金材料可优化其性能
【答案】A
9、某化学兴趣小组利用如图装置探究铁生锈的条件,一段时间后,只有一个集气瓶中的铁丝生锈,下列说法不正确的是( )
A.甲瓶中的铁丝生锈
B.通过对比甲瓶和乙瓶中的现象,可以说明铁生锈的一个条件是与水接触
C.通过对比甲瓶和丙瓶中的现象,可以说明防止铁生锈的一个方法是隔绝氧气
D.实验后向甲、乙、丙瓶中分别注入一定量稀盐酸,观察到的现象相同
【答案】D
10、下列有关金属的叙述中,正确的是( )
A. 硬币、不锈钢都是合金材料,合金比成分金属具有更优良的性能
B. 铝、铁、铜都是银白色固体,都能导电
C. 镁、铝都是活泼金属,相同质量时与足量的盐酸反应放出氢气的体积相同
D. 铁在空气中燃烧,冒出浓烈的黑烟,放出热量,生成黑色粉末
【答案】A
11、将等质量的镁和铁分别放入等质量、相同质量分数的稀盐酸中,产生氢气的质量与反应时间的关系如图所示,下列说法错误的是( )
A.反应结束后镁一定有剩余
B.反应消耗盐酸的总质量一定相等
C.0~t1时段,产生氢气的质量镁比铁大
D.0~t2时段,参加反应的镁的质量与铁相等
【答案】D
12、合金在生活中的应用非常广泛,下列关于合金的说法正确的是( )
A. 合金不属于金属材料 B. 合金的硬度一般比组成金属小
C. 生铁的含铁量比钢高 D. 合金不一定是金属和金属熔合而成的
【答案】D
13、现有三种金属X、Y、Z,它们之间能发生如下反应:Y+X(NO3)2=X+Y(NO3)2, X + ZCl2=Z+ XCl2.问X、Y、Z三种金属的活动性由强到弱的排列顺序是( )
A. Z>Y=X B. X<Y<Z C. Y>X>Z D. X>Z>Y
【答案】C
14、下列有关金属材料的说法错误的是( )
A.在潮湿的空气中铁易生锈
B.金属的回收利用是保护金属资源的有效途径之一
C.铝和金都有很好的抗腐蚀性,是因为二者的化学性质都很稳定
D.高炉炼铁的原理是在高温条件下,用一氧化碳把铁从铁矿石里还原出来
【答案】C
15、下列叙述属于铁的物理性质的是( )
A.铁在氧气中燃烧时火花四溅 B.铁在1 535 ℃时变为铁水
C.铁投入盐酸中,有气泡冒出 D.铁投入硫酸铜溶液有铜析出
【答案】B
16、有一镁的合金2.4 g,在合金中加入100 g一定质量分数的稀盐酸后,金属与稀盐酸恰好完全反应,产生氢气的质量为m,下列说法错误的是( )
A.若是镁铝合金,则m>0.2 g
B.若是镁锌合金,则m<0.2 g
C.若是镁铜合金,则稀盐酸溶质的质量分数小于7.3%
D.若是镁铁合金,m=0.16 g,则合金中铁的质量分数是5
【答案】D
二、填空题。
17、合金比起组成它们的纯金属,其强度和硬度更_____,熔点更______, ___________性能更好。
【答案】高 低 抗腐蚀
18、现有铜与另一种金属R(可能是银、镁、铁中的一种)的混合粉末。欲确定R的成分,请你一起完成:
(1)请将银、镁、铁三种金属的元素符号填写在下列金属活动性顺序表中的相应位置。
(2)取少量的金属粉末于试管中,逐滴加入稀硫酸,有气泡产生,则R不可能是___________________________。
(3)待不再产生气泡时,再进行__________(填写一种实验操作方法),得到溶液和铜。然后往溶液中加入洁净的锌片,锌片表面有金属析出,则R是______。
(4)写出金属R与稀硫酸反应的化学方程式____________________________。
该反应的基本类型属于______(填“化合”、“分解”、“置换”或“复分解”)反应。
【答案】(1)
(2)银(或Ag) (3)过滤 铁(或Fe)
(4)Fe+H2SO4 ==== FeSO4+H2↑ 置换
19、铝、铁、铜是人类广泛使用的三种金属,与我们的生活息息相关。
(1)用铜块制成铜片、铜丝利用了铜的________性.钢铁制品容易发生锈蚀,在其表面涂油漆的防锈原理是________ 。
(2)钢铁是用量最大、用途最广的含________量不同的铁合金。
(3)将纯铝和铝合金相互刻划,纯铝上留下明显划痕.请你解释其中的原因________ 。
【答案】(1)延展;隔绝水和氧气 (2)碳
(3)铝合金的硬度比纯铝大
20、金属材料在生产、生活中应用广泛。
(1)由于金属铜具有良好的________,常用于制作导线。
(2)现有如下实验装置(每支试管中均放有完全相同的洁净铁钉):
①一段时间后甲同学观察到:_________试管中的铁钉明显生锈了。由此得出铁生锈的原因是铁与_________共同作用的结果。
②为防止金属锈蚀,可以采取的措施有______________________(填一种)。
③铁制品中不能盛放稀盐酸的原因,该反应的化学方程式是_________。
【答案】导电性 A 水和氧气 在铁制品表面刷漆
Fe+2HCl═FeCl2+H2↑
21、在索契冬季奥运会上,中国运动员共获得了九枚奖牌,成为亚洲体坛霸主。
(1)图1是速度滑冰运动员使用的刀冰鞋。
①刀冰鞋中含有的金属单质是 (写化学式),不锈钢属于 材料。
②制造刀冰鞋的铝合金材料具有较好的抗腐蚀性,请用化学方程式表示铝具有较好的抗腐蚀性的原因 。
(2)图2索契冬奥会的火炬,火炬外形像神话传说中的火鸟。采集圣火,在太阳光下将火炬燃料喷口伸向凹面镜焦点位置,打开阀门,火炬将被点燃。火炬能被点燃的原因是 。火炬传递结束后,采用关闭燃气阀门的方法熄灭火炬,其中蕴含的灭火原理是 。
【答案】Fe或Al 金属 4Al+3O2==2Al2O3
(2)温度达到着火点 隔离可燃物
三、实验与探究题。
22、钢铁是非常重要的金属材料。龙岩市马坑铁矿是华东区最大的磁铁矿(主要成分为Fe3O4),总储量达到4.34亿吨。实验室可用如图装置模拟工业炼铁。
(1)写出CO与Fe3O4反应的化学方程式 ___________ 。
(2)实验过程中,常在装置图末端的导气管口放一盏燃着的酒精灯(灯焰处于导管口),这样做的目的是___________。
(3)为检验反应后有铁生成,进行如下实验:将反应后的固体取少量放入稀盐酸中,观察到有气泡冒出。写出该反应的化学方程式:___________。
(4)工业炼铁时还需要石灰石等原料,我市也有着丰富的石灰石资源。请写出石灰石的另一种用途___________。
【答案】
除去尾气中的CO 生产生石灰
23、如图所示是一氧化碳还原氧化铁的实验。
(1)硬质玻璃管中观察到的现象是 ,发生反应的化学方程式为 。
(2)试管中澄清石灰水的作用是 。
(3)该实验进行尾气处理的方法体现了CO具有的化学性质是 。
【答案】(1)红色粉末逐渐变成黑色 3CO+Fe2O3 2Fe+3CO2
(2)检验产物是否生成二氧化碳 (3)可燃性
24、在探究铁、铜、锌、银的金属活动性顺序时,某小组做了如下三个实验:(所用金属的形状与大小和稀盐酸的用量均相同)
(1)一段时间后,可观察到实验Ⅱ中现象是 ;反应的化学方程式是 。
(2)甲同学认为:通过实验Ⅰ和Ⅲ可比较出锌和铁的金属活动性强弱。你认为他依据的实验现象是__ 。
(3)乙和丙两位同学认为上述三个实验不能够得出四种金属活动性顺序,原因是 ;并在上述实验的基础上,补充了一个实验(如图所示),实现了探究目的。
他们的实验:X是金属Fe,Y是__ __(写出化学式)溶液。
【答案】铜片表面有银白色固体析出,溶液由无色变为蓝色 Cu+2AgNO3===2Ag+Cu(NO3)2 锌与稀盐酸反应的程度要比铁的剧烈
无法比较铁与铜的活动性强弱 CuSO4[或CuCl2、Cu(NO3)2等]
四、计算题。
25、我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn),它可用来制造电器零件及日用品。小华利用一瓶稀盐酸和相关的仪器,测定黄铜样品的组成(不考虑黄铜中的其他杂质)。将30mL稀盐酸分三次加入到10g黄铜样品粉末中,每次充分反应后,测定生成氢气的质量,实验数据见下表:
第一次 第二次 第三次
连续加入盐酸的体积/mL 10 10 10
生成氢气的质量/g 0.08 0.08 0.04
(1)从上表数据分析,小华用10 g合金粉末总共收集到氢气________g。
(2)求该合金中铜的质量分数。
【答案】(1)0.2g (2)35%
同课章节目录
