河南省许昌市2023-2024学年高二上学期2月期末教学质量检测化学试题(含答案)
文档属性
| 名称 | 河南省许昌市2023-2024学年高二上学期2月期末教学质量检测化学试题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 751.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-24 00:00:00 | ||
图片预览


文档简介
许昌市2023-2024学年高二上学期2月期末教学质量检测
化学
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并认真核准准考证号条形码上的以上信息,将条形码粘贴在答题卡上的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作答;字体工整,笔迹清楚。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列溶液因盐的水解而呈酸性的是( )
A. B. C. D.溶液
2.相同条件下,质量相等的两份与足量的充分反应,分别生成液态水(反应①)和水蒸气(反应②)。下列说法正确的是( )
A.反应①放出的热量多 B.反应②放出的热量多
C.反应①、②放出的热量一样多 D.无法比较反应①、②放出的热量
3.采取下列措施对增大化学反应速率有明显效果的是( )
A.少量钠与水反应时,增加水的量
B.铝与稀硫酸反应制时,改用浓硫酸
C.与溶液反应时,增大压强
D.大理石块与盐酸反应制时,改为用粉末状大理石
4.下列说法中,正确的是( )
A.自发进行的反应一定不是吸热反应
B.冰在室温下自动熔化成水,这是熵增的过程
C.化学反应热只是由反应过程中化学键的断裂和生成来决定的
D.孤立体系中进行的化学反应,反应混合物温度一定会发生明显变化
5.下列物质溶解于水时,电离出的阳离子能使水的电离平衡向右移动的是( )
A. B. C. D.
6.下列有关电解的叙述中错误的是( )
A.与电源正极相连的是阳极 B.与电源负极相连的是阴极
C.在阴极上发生氧化反应 D.阴离子向阳极方向移动
7.下列关于物质性质的比较,不正确的是( )
A.金属性强弱: B.原子半径大小:
C.酸性强弱: D.碱性强弱:
8.下列各组元素中,原子半径依次减小、元素第一电离能逐渐增大的是( )
A.K、Na、Li B.C、N、O C.Cl、S、P D.Al、Mg、Na
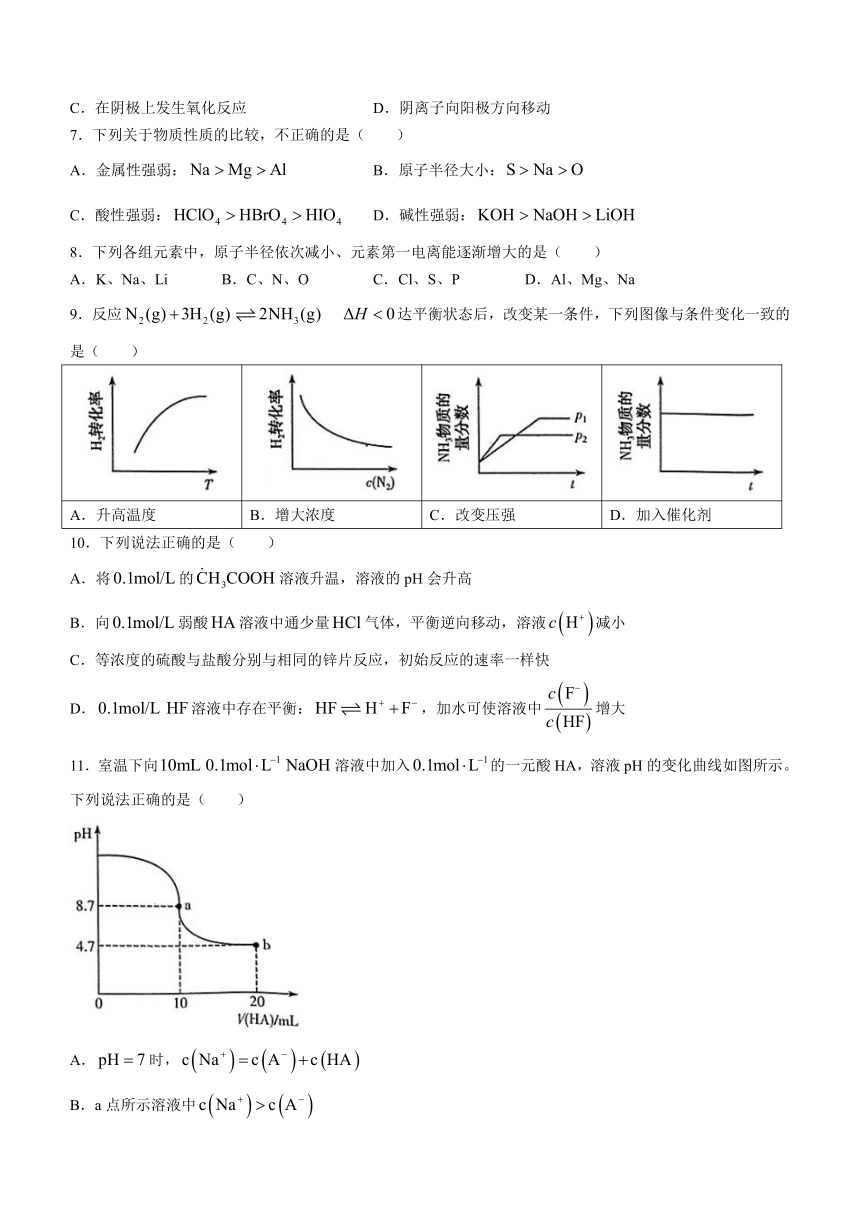
9.反应 达平衡状态后,改变某一条件,下列图像与条件变化一致的是( )
A.升高温度 B.增大浓度 C.改变压强 D.加入催化剂
10.下列说法正确的是( )
A.将的溶液升温,溶液的pH会升高
B.向弱酸溶液中通少量气体,平衡逆向移动,溶液减小
C.等浓度的硫酸与盐酸分别与相同的锌片反应,初始反应的速率一样快
D.溶液中存在平衡:,加水可使溶液中增大
11.室温下向溶液中加入的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )
A.时,
B.a点所示溶液中
C.b点所示溶液中
D.a、b两点所示溶液中水的电离程度:
12.W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y的最外层电子数与其K层电子数相等,是形成酸雨的物质之一。下列说法正确的是( )
A.原子半径: B.简单氢化物的沸点:
C.Y与X可形成离子化合物 D.Z的最高价含氧酸是弱酸
13.某化学小组通过手持技术探究铁钉在4种溶液中的吸氧腐蚀情况,相关数据如表所示。
实验装置 实验编号 浸泡液 pH 氧气体积分数随时间的变化
① 5
② 5
③ 7
④ 7
已知铁在负极被氧化的过程由3个步骤构成:
①;②;
③。
下列说法错误的是( )
A.铁钉吸氧腐蚀的负极总反应式为
B.上述实验的正极反应式均为
C.由实验可知,铁钉在中性溶液中比在弱酸性溶液更难被腐蚀
D.和相比浸泡液存在带相同电荷数的,使铁钉更难腐蚀
14.在密闭容器中充有与,在催化剂作用下反应生成甲醇。的平衡转化率()与温度(T)、压强(p)的关系如图所示。下列说法正确的是( )
A.反应达到a点平衡状态所需时间小于c点
B.a点对应反应状态的平衡常数为4
C.a、b两点对应平衡状态的容器体积相同
D.a、c两点平衡体系中,甲醇的体积分数相同
二、非选择题:本题共4小题,共58分。
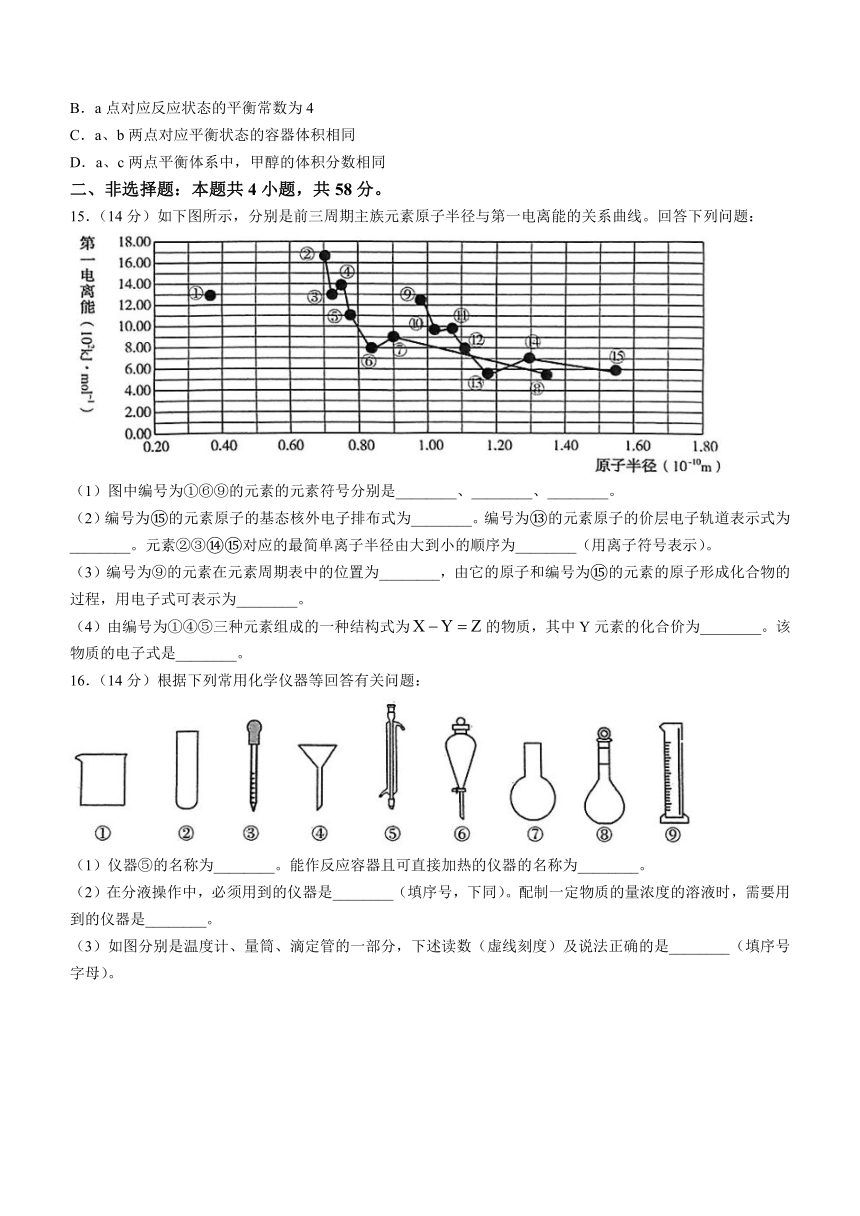
15.(14分)如下图所示,分别是前三周期主族元素原子半径与第一电离能的关系曲线。回答下列问题:
(1)图中编号为①⑥⑨的元素的元素符号分别是________、________、________。
(2)编号为 的元素原子的基态核外电子排布式为________。编号为 的元素原子的价层电子轨道表示式为________。元素②③ 对应的最简单离子半径由大到小的顺序为________(用离子符号表示)。
(3)编号为⑨的元素在元素周期表中的位置为________,由它的原子和编号为 的元素的原子形成化合物的过程,用电子式可表示为________。
(4)由编号为①④⑤三种元素组成的一种结构式为的物质,其中Y元素的化合价为________。该物质的电子式是________。
16.(14分)根据下列常用化学仪器等回答有关问题:
(1)仪器⑤的名称为________。能作反应容器且可直接加热的仪器的名称为________。
(2)在分液操作中,必须用到的仪器是________(填序号,下同)。配制一定物质的量浓度的溶液时,需要用到的仪器是________。
(3)如图分别是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是________(填序号字母)。
A.①是量筒,读数为 B.②是量筒,读数为
C.③是滴定管,读数为 D.②是温度计,读数为2.5℃
(4)某实验小组用酸碱滴定法测定某食用白醋的醋酸含量(),回答下列问题:
①部分准备与滴定
a.待测液的准备:将10mL食用白醋稀释至100mL,用________(填仪器名称)量取稀释后的溶液20.00mL于锥形瓶中。量取时如果直接用用蒸馏水洗净的该仪器量取白醋,会导致该测定实验最终结果________(填“偏高”或“偏低”或“不受影响”)。
b.标准溶液的准备:用碱式滴定管盛装适量的标准溶液。
c.滴定:向盛有白醋样品的锥形瓶中加入2滴________指示剂,把锥形瓶放在碱式滴定管的下方,瓶下垫一张白纸,小心地滴入碱。边滴边摇动锥形瓶(接近终点时,改为滴加半滴碱),直到因加入半滴碱后,溶液颜色从________,且30s不褪色,表示已经到达滴定终点。实验中滴加“半滴碱”的操作方法是:使滴定管的尖嘴处悬挂一滴不滴落的碱液,用________。
②重复上述操作三次。四次测定数据如下表:
序号 1 2 3 4
标准溶液体积/mL 20.05 20.00 16.40 19.95
计算得出白醋的总酸量为________。
17.(15分)二氧化氯()是高效、广谱、快速、安全的杀菌消毒剂,被认为是“第四代消毒剂”。电解法是目前最为热门的生产的方法之一。直接电解氯酸钠()溶液自动催化循环制备高纯的实验装置示意图如图所示。
回答下列问题(不考虑放电。):
(1)亚氯酸根离子()中氯元素的化合价为________价。在水中的电离方程式为________________。
(2)已知铅酸蓄电池的工作原理为
①电解氯酸钠溶液时,M电极上发生________(填“氧化”或“还原”)反应。
②电解氯酸钠溶液时,若以铅酸蓄电池作为电源,则R应与________(填“Pb”或“”)电极相连,N电极上的电极反应式为________________。
(3)亚氯酸盐具有较强氧化性。可以用与和溶液反应制备,制备时的化学方程式为________。反应每消耗2.24L标准状况下的气体,可生成气体物质的质量为________。
若要除去水中超标的亚氯酸盐,下列物质最适宜的是________(填标号)。
A.明矾 B.氯化钾 C.盐酸 D.硫酸亚铁
(4)由图示信息等,可以判断下列说法错误的是________(填标号)。
A.氯酸钠与硫酸溶液反应可以产生 B.促进了,转化成为
C.电解进行时,M极的电势高于N极 D.电解时,穿过质子交换膜移向M极
18.(15分)甲烷和二氧化碳是两种主要的温室气体,工业上利用甲烷和二氧化碳催化重整为合成气,实现节能减排。重整过程中主要发生如下反应:
Ⅰ. ;
Ⅱ. 。
回答下列问题:
(1)根据反应Ⅰ、Ⅱ,下列能提高平衡转化率的是________(填字母)。
A.恒温恒容下增加的用量 B.恒温恒压下通入惰性气体
C.升高温度 D.加入更高效催化剂
(2)研究表明,反应Ⅰ的一种反应机理(ads指吸附在催化剂表面的中间物种)如下:
ⅰ.;
ⅱ.;
ⅲ.……
ⅳ.,。
则反应ⅱ的方程式为________________。
(3)甲烷和二氧化碳催化重整反应体系中,催化剂失活主要是由于催化剂的表面积炭所致。
催化剂表面积炭主要来自裂解: 和的歧化:。
①歧化反应的________。
②研究表明,催化剂所用助剂碱性越强,抗积炭能力越强。用下列物质作助剂的催化剂抗积炭能力最强的是________(填字母)。
A. B. C. D.
(4)在恒压、反应物起始物质的量比条件下,发生上述反应Ⅰ、Ⅱ,和的平衡转化率随温度变化的曲线如图所示。
①表示的平衡转化率随温度变化的曲线是________(填“曲线A”或“曲线B”)。
②恒压、800K、初始条件下,要使转化率的值从X点提高到Y点,需要改变的条件可能是________________(答出1点即可)。
③已知图中940K时曲线A、B对应物质的平衡转化率分别为80%和60%,则平衡体系中的物质的量分数为此温度下,反应Ⅱ的平衡常数________。
高二化学参考答案
说明:方程式出现化学式错误无分,配平占1分,其它不占分;简答题答出要点即可。
1-5AADBC 6-10 CBADD 11-14BCDD
15.(没标明分值的空,均为1分,共14分)
(1)H B Cl (2)
(3)第三(或3)周期,VIIA族(2分) (2分)
(4)(2分) (2分)
16.(没标明分值的空,均为1分,共14分)
(1)冷凝管(或直形冷凝管) 试管
(2)①⑥(全对1分,见错没分) ①③⑧⑨(共2分,答对3个得1分,见错没分)
(3)B
(4)①a.酸式滴定管 偏低 c.酚酞 无色变成浅红色
用锥形瓶内壁将其靠下来,并用蒸馏水将其冲入锥形瓶内(2分) ②6.0(2分)
17.(没标明分值的空,均为1分,共15分)
(1) (2分)
(2)①还原 ②Pb (2分)
(3)(2分) 1.6g(2分) D(2分)
(4)C(2分)
18.(没标明分值的空,均为2分,共15分)
(1)BC(对1个1分,见错没分)
(2)
(3)① ②A(1分)
(4)①曲线A ②将生成物移出体系(或增大的量) 43.75% 1.4
化学
注意事项:
1.答题前,先将自己的姓名、准考证号、考场号、座位号填写在试卷和答题卡上,并认真核准准考证号条形码上的以上信息,将条形码粘贴在答题卡上的指定位置。
2.请按题号顺序在答题卡上各题目的答题区域内作答,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3.选择题用2B铅笔在答题卡上把所选答案的标号涂黑;非选择题用黑色签字笔在答题卡上作答;字体工整,笔迹清楚。
可能用到的相对原子质量:H 1 C 12 N 14 O 16
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.下列溶液因盐的水解而呈酸性的是( )
A. B. C. D.溶液
2.相同条件下,质量相等的两份与足量的充分反应,分别生成液态水(反应①)和水蒸气(反应②)。下列说法正确的是( )
A.反应①放出的热量多 B.反应②放出的热量多
C.反应①、②放出的热量一样多 D.无法比较反应①、②放出的热量
3.采取下列措施对增大化学反应速率有明显效果的是( )
A.少量钠与水反应时,增加水的量
B.铝与稀硫酸反应制时,改用浓硫酸
C.与溶液反应时,增大压强
D.大理石块与盐酸反应制时,改为用粉末状大理石
4.下列说法中,正确的是( )
A.自发进行的反应一定不是吸热反应
B.冰在室温下自动熔化成水,这是熵增的过程
C.化学反应热只是由反应过程中化学键的断裂和生成来决定的
D.孤立体系中进行的化学反应,反应混合物温度一定会发生明显变化
5.下列物质溶解于水时,电离出的阳离子能使水的电离平衡向右移动的是( )
A. B. C. D.
6.下列有关电解的叙述中错误的是( )
A.与电源正极相连的是阳极 B.与电源负极相连的是阴极
C.在阴极上发生氧化反应 D.阴离子向阳极方向移动
7.下列关于物质性质的比较,不正确的是( )
A.金属性强弱: B.原子半径大小:
C.酸性强弱: D.碱性强弱:
8.下列各组元素中,原子半径依次减小、元素第一电离能逐渐增大的是( )
A.K、Na、Li B.C、N、O C.Cl、S、P D.Al、Mg、Na
9.反应 达平衡状态后,改变某一条件,下列图像与条件变化一致的是( )
A.升高温度 B.增大浓度 C.改变压强 D.加入催化剂
10.下列说法正确的是( )
A.将的溶液升温,溶液的pH会升高
B.向弱酸溶液中通少量气体,平衡逆向移动,溶液减小
C.等浓度的硫酸与盐酸分别与相同的锌片反应,初始反应的速率一样快
D.溶液中存在平衡:,加水可使溶液中增大
11.室温下向溶液中加入的一元酸HA,溶液pH的变化曲线如图所示。下列说法正确的是( )
A.时,
B.a点所示溶液中
C.b点所示溶液中
D.a、b两点所示溶液中水的电离程度:
12.W、X、Y、Z为短周期主族元素,原子序数依次增大,最外层电子数之和为19。Y的最外层电子数与其K层电子数相等,是形成酸雨的物质之一。下列说法正确的是( )
A.原子半径: B.简单氢化物的沸点:
C.Y与X可形成离子化合物 D.Z的最高价含氧酸是弱酸
13.某化学小组通过手持技术探究铁钉在4种溶液中的吸氧腐蚀情况,相关数据如表所示。
实验装置 实验编号 浸泡液 pH 氧气体积分数随时间的变化
① 5
② 5
③ 7
④ 7
已知铁在负极被氧化的过程由3个步骤构成:
①;②;
③。
下列说法错误的是( )
A.铁钉吸氧腐蚀的负极总反应式为
B.上述实验的正极反应式均为
C.由实验可知,铁钉在中性溶液中比在弱酸性溶液更难被腐蚀
D.和相比浸泡液存在带相同电荷数的,使铁钉更难腐蚀
14.在密闭容器中充有与,在催化剂作用下反应生成甲醇。的平衡转化率()与温度(T)、压强(p)的关系如图所示。下列说法正确的是( )
A.反应达到a点平衡状态所需时间小于c点
B.a点对应反应状态的平衡常数为4
C.a、b两点对应平衡状态的容器体积相同
D.a、c两点平衡体系中,甲醇的体积分数相同
二、非选择题:本题共4小题,共58分。
15.(14分)如下图所示,分别是前三周期主族元素原子半径与第一电离能的关系曲线。回答下列问题:
(1)图中编号为①⑥⑨的元素的元素符号分别是________、________、________。
(2)编号为 的元素原子的基态核外电子排布式为________。编号为 的元素原子的价层电子轨道表示式为________。元素②③ 对应的最简单离子半径由大到小的顺序为________(用离子符号表示)。
(3)编号为⑨的元素在元素周期表中的位置为________,由它的原子和编号为 的元素的原子形成化合物的过程,用电子式可表示为________。
(4)由编号为①④⑤三种元素组成的一种结构式为的物质,其中Y元素的化合价为________。该物质的电子式是________。
16.(14分)根据下列常用化学仪器等回答有关问题:
(1)仪器⑤的名称为________。能作反应容器且可直接加热的仪器的名称为________。
(2)在分液操作中,必须用到的仪器是________(填序号,下同)。配制一定物质的量浓度的溶液时,需要用到的仪器是________。
(3)如图分别是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是________(填序号字母)。
A.①是量筒,读数为 B.②是量筒,读数为
C.③是滴定管,读数为 D.②是温度计,读数为2.5℃
(4)某实验小组用酸碱滴定法测定某食用白醋的醋酸含量(),回答下列问题:
①部分准备与滴定
a.待测液的准备:将10mL食用白醋稀释至100mL,用________(填仪器名称)量取稀释后的溶液20.00mL于锥形瓶中。量取时如果直接用用蒸馏水洗净的该仪器量取白醋,会导致该测定实验最终结果________(填“偏高”或“偏低”或“不受影响”)。
b.标准溶液的准备:用碱式滴定管盛装适量的标准溶液。
c.滴定:向盛有白醋样品的锥形瓶中加入2滴________指示剂,把锥形瓶放在碱式滴定管的下方,瓶下垫一张白纸,小心地滴入碱。边滴边摇动锥形瓶(接近终点时,改为滴加半滴碱),直到因加入半滴碱后,溶液颜色从________,且30s不褪色,表示已经到达滴定终点。实验中滴加“半滴碱”的操作方法是:使滴定管的尖嘴处悬挂一滴不滴落的碱液,用________。
②重复上述操作三次。四次测定数据如下表:
序号 1 2 3 4
标准溶液体积/mL 20.05 20.00 16.40 19.95
计算得出白醋的总酸量为________。
17.(15分)二氧化氯()是高效、广谱、快速、安全的杀菌消毒剂,被认为是“第四代消毒剂”。电解法是目前最为热门的生产的方法之一。直接电解氯酸钠()溶液自动催化循环制备高纯的实验装置示意图如图所示。
回答下列问题(不考虑放电。):
(1)亚氯酸根离子()中氯元素的化合价为________价。在水中的电离方程式为________________。
(2)已知铅酸蓄电池的工作原理为
①电解氯酸钠溶液时,M电极上发生________(填“氧化”或“还原”)反应。
②电解氯酸钠溶液时,若以铅酸蓄电池作为电源,则R应与________(填“Pb”或“”)电极相连,N电极上的电极反应式为________________。
(3)亚氯酸盐具有较强氧化性。可以用与和溶液反应制备,制备时的化学方程式为________。反应每消耗2.24L标准状况下的气体,可生成气体物质的质量为________。
若要除去水中超标的亚氯酸盐,下列物质最适宜的是________(填标号)。
A.明矾 B.氯化钾 C.盐酸 D.硫酸亚铁
(4)由图示信息等,可以判断下列说法错误的是________(填标号)。
A.氯酸钠与硫酸溶液反应可以产生 B.促进了,转化成为
C.电解进行时,M极的电势高于N极 D.电解时,穿过质子交换膜移向M极
18.(15分)甲烷和二氧化碳是两种主要的温室气体,工业上利用甲烷和二氧化碳催化重整为合成气,实现节能减排。重整过程中主要发生如下反应:
Ⅰ. ;
Ⅱ. 。
回答下列问题:
(1)根据反应Ⅰ、Ⅱ,下列能提高平衡转化率的是________(填字母)。
A.恒温恒容下增加的用量 B.恒温恒压下通入惰性气体
C.升高温度 D.加入更高效催化剂
(2)研究表明,反应Ⅰ的一种反应机理(ads指吸附在催化剂表面的中间物种)如下:
ⅰ.;
ⅱ.;
ⅲ.……
ⅳ.,。
则反应ⅱ的方程式为________________。
(3)甲烷和二氧化碳催化重整反应体系中,催化剂失活主要是由于催化剂的表面积炭所致。
催化剂表面积炭主要来自裂解: 和的歧化:。
①歧化反应的________。
②研究表明,催化剂所用助剂碱性越强,抗积炭能力越强。用下列物质作助剂的催化剂抗积炭能力最强的是________(填字母)。
A. B. C. D.
(4)在恒压、反应物起始物质的量比条件下,发生上述反应Ⅰ、Ⅱ,和的平衡转化率随温度变化的曲线如图所示。
①表示的平衡转化率随温度变化的曲线是________(填“曲线A”或“曲线B”)。
②恒压、800K、初始条件下,要使转化率的值从X点提高到Y点,需要改变的条件可能是________________(答出1点即可)。
③已知图中940K时曲线A、B对应物质的平衡转化率分别为80%和60%,则平衡体系中的物质的量分数为此温度下,反应Ⅱ的平衡常数________。
高二化学参考答案
说明:方程式出现化学式错误无分,配平占1分,其它不占分;简答题答出要点即可。
1-5AADBC 6-10 CBADD 11-14BCDD
15.(没标明分值的空,均为1分,共14分)
(1)H B Cl (2)
(3)第三(或3)周期,VIIA族(2分) (2分)
(4)(2分) (2分)
16.(没标明分值的空,均为1分,共14分)
(1)冷凝管(或直形冷凝管) 试管
(2)①⑥(全对1分,见错没分) ①③⑧⑨(共2分,答对3个得1分,见错没分)
(3)B
(4)①a.酸式滴定管 偏低 c.酚酞 无色变成浅红色
用锥形瓶内壁将其靠下来,并用蒸馏水将其冲入锥形瓶内(2分) ②6.0(2分)
17.(没标明分值的空,均为1分,共15分)
(1) (2分)
(2)①还原 ②Pb (2分)
(3)(2分) 1.6g(2分) D(2分)
(4)C(2分)
18.(没标明分值的空,均为2分,共15分)
(1)BC(对1个1分,见错没分)
(2)
(3)① ②A(1分)
(4)①曲线A ②将生成物移出体系(或增大的量) 43.75% 1.4
同课章节目录
