9.2溶解度同步练习人教版化学九年级下册(含答案)
文档属性
| 名称 | 9.2溶解度同步练习人教版化学九年级下册(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 474.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-26 00:00:00 | ||
图片预览



文档简介
9.2溶解度同步练习人教版化学九年级下册
学校:___________姓名:___________班级:___________考号:___________
一、多选题
1.1956年中国首次人工合成结晶牛胰岛素,说法正确的是
A.晶体都带有结晶水
B.晶体具有规则的几何形状
C.形成晶体的过程称为蒸发
D.从不饱和溶液中析出晶体,一般需要消耗能量
2.如图表示a、b两种固体物质的溶解度曲线,下列叙述正确的是
A.a的溶解度大于b的溶解度
B.a、b均为易溶物质
C.在t℃a、b两种物质的饱和溶液中溶质质量分数相等
D.a、b两种物质的溶解度受温度影响变化较小
3.将不再冒出气泡的汽水瓶(敞口)置于温水中,瓶内出现较多气泡。分析正确的是
A.瓶内压强减少导致溶解度减小
B.温度升高导致气体溶解度增大
C.出现大量气泡后溶液为饱和溶液
D.出现大量气泡后溶液中气体溶质质量分数变小
4.下表是氯化钠和硝酸钾在不同温度时的溶解度。以下说法正确的是(_____)
温度/℃ 10 20 30 40 50 60
溶解 度/g NaCl 35.8 36.0 36.3 36.6 37.0 37.3
KNO3 20.9 31.6 45.8 63.9 85.5 110
A.20℃时将20g KNO3加入到50g水中,能得到65.8g溶液
B.KNO3的溶解度比NaCl的溶解度大
C.60℃时将210g KNO3饱和溶液降温至20℃,溶液质量变为131.6g
D.20℃时将40g NaCl加入到100g水中,再升温至60℃可形成不饱和溶液
5.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
A.t1℃时,甲和乙的饱和溶液的溶质质量分数相等
B.t1℃时,120g甲的饱和溶液中含有20g甲
C.将甲、乙饱和溶液从t2℃降温至t1℃,析出晶体的质量:甲>乙
D.甲中混有少量杂质乙,可采用蒸发结晶的方式提纯甲
二、选择题
6.如表是不同温度时硝酸钾的溶解度,有关说法正确的是
温度/℃ 0 20 40 60 80 100
溶解度/克 13.3 31.6 63.9 110 169 246
A.20℃时,100g水中溶解的硝酸钾越多溶解度就越大
B.40℃时,100g硝酸钾饱和溶液中含有硝酸钾63.9克
C.100℃的水能溶解的硝酸钾一定比80℃的水能溶解的硝酸钾多
D.0℃的硝酸钾饱和溶液一定比60℃的硝酸钾饱和溶液的溶质质量分数小
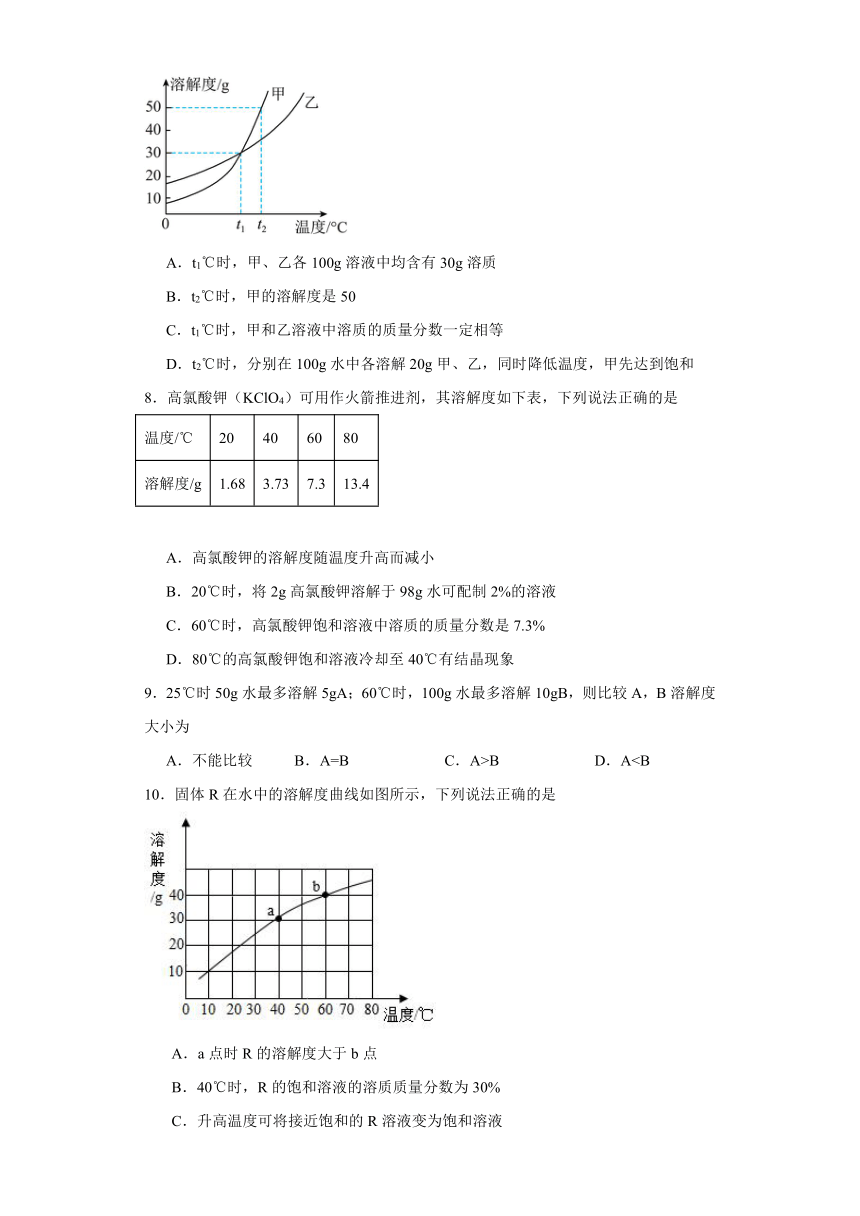
7.如图,是甲、乙两物质的溶解度曲线,下列叙述中正确的是
A.t1℃时,甲、乙各100g溶液中均含有30g溶质
B.t2℃时,甲的溶解度是50
C.t1℃时,甲和乙溶液中溶质的质量分数一定相等
D.t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
8.高氯酸钾(KClO4)可用作火箭推进剂,其溶解度如下表,下列说法正确的是
温度/℃ 20 40 60 80
溶解度/g 1.68 3.73 7.3 13.4
A.高氯酸钾的溶解度随温度升高而减小
B.20℃时,将2g高氯酸钾溶解于98g水可配制2%的溶液
C.60℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%
D.80℃的高氯酸钾饱和溶液冷却至40℃有结晶现象
9.25℃时50g水最多溶解5gA;60℃时,100g水最多溶解10gB,则比较A,B溶解度大小为
A.不能比较 B.A=B C.A>B D.A10.固体R在水中的溶解度曲线如图所示,下列说法正确的是
A.a点时R的溶解度大于b点
B.40℃时,R的饱和溶液的溶质质量分数为30%
C.升高温度可将接近饱和的R溶液变为饱和溶液
D.60℃时,向50g水中加入20gR,充分搅拌后形成饱和溶液
11.右图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是
A.甲的溶解度大于乙的溶解度
B.35℃时100g甲的溶液中含甲的质量60g
C.10℃时甲、乙两物质的溶解度相等
D.甲中混有少量乙时可用蒸发结晶的方法提纯甲
12.如图是 a b c三种固体物质(均不含结晶水)的溶解度曲线,下列说法不正确的是
A.在 t1℃时,a c两种物质的溶解度相等
B.若 a物质中混有少量 b物质,最好采用降温结晶的方法提纯 a
C.将 t2℃时,a b c的饱和溶液降温至 t1℃,所得溶液的溶质质量分 数:b>a>c
D.t2℃时,将 a b c三种物质的饱和溶液分别降温至 t1℃,析出晶体的质量 a一定大于 b,而 c无晶体析出
13.实验室中区分下列各组物质的两种方法都正确的是
选项 需区分的物质 方法一 方法二
A 蒸馏水和食盐水 品尝 蒸干
B 铁粉和木炭粉 观察颜色 加入硫酸铜溶液,观察
C 饱和溶液和饱和石灰水 升温,观察 加入少量硝酸钾,观察
D 18K金和黄铜 在空气中灼烧 滴加稀盐酸
A.A B.B C.C D.D
14.关于溶液的叙述正确的是
A.溶液中各部分的性质不同 B.凡是均一稳定的液体都是溶液
C.饱和溶液一定是浓溶液 D.医用生理盐水是溶液
15.如图为甲、乙两种固体(不含结晶水)在水中的溶解度曲线,下列说法正确的是
A.甲物质的溶解度大于乙
B.除去甲中少量的乙,用蒸发结晶的方法
C.t1℃时,甲、乙的饱和溶液溶质质量分数都是 25%
D.t2℃时,等质量的甲和乙的饱和溶液中,溶剂质量甲<乙
三、综合应用题
16.溶液是生产生活中常见的物质,依据相关信息回答问题。资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如下表所示:
温度/℃ 10 20 30 40 50 60 70
溶解度/g 21 32 46 64 86 110 138
(1)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。
①(填字母序号) 中盛的一定是饱和溶液。
②使B烧杯的溶液升温至50℃时,溶液的质量为 g。
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是 (填字母序号)。
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(2)某校化学课外小组用硫酸亚铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体,主要的操作流程如图:
请回答下列问题:
①上述操作过程中用到的玻璃仪器有:①烧杯;②玻璃棒;③酒精灯;④温度计;⑤ ;
②流程中生成气体B的反应的化学方程式是: 。
17.(1)小明取串场河的河水,按下列流程进行实验,制取蒸馏水。请回答下列问题:
①滤液中有难闻的异味,可添加 除去,
②生活中常用 来比较所取水样与制得的蒸馏水的硬度。
③经过净化后的水,在生活中通过 方法,降低水的硬度并杀菌;
④消毒剂为高铁酸钾(K2FeO4)。高铁酸钾中铁元素的化合价为 。
(2)如图是A、B、C三种物质的溶解度曲线,请回答:
①在t2℃时,将30gA物质充分溶解在盛有50g水的烧杯中,所得溶液的质量为 g;若将烧杯内物质降温至t1℃(不考虑水蒸发),溶液中变化的是 (填字母序号)。
a 溶剂的质量 b 溶液的质量 c 溶质的质量分数
②当A物质中混有少量B、C两种物质时,采用 的方法可以提纯A.
③将t2℃的A、B、C三种物质的饱和溶液分别降温到t1℃时,所得溶液的溶质质量分数由大到小的顺序是 。
(3)实验室用质量分数为 6%的氯化钠溶液(密度为1.04g/cm3)配制 50g 质量分数为3%的氯化钠溶液。
①经计算,所需 6%的氯化钠的体积为 mL;加水 克
②若量取水时,采取仰视读数,其它操作均正确,则配制得到的稀溶液中溶质质量分数 3% (填“>”“<”或“ = ”)。
③向该49g20%的稀硫酸中,加入7.3g已部分氧化的锌粉,恰好完全反应。则所得溶液中溶质的质量为 (填字母序号)
A 15.5g B 16.1g C 18.1g
18.小明取酸性锌锰干电池进行探究,他发现电池内部结构如图1所示。
【查阅资料】(1)锌皮为金属锌(含有少量的铁)
(2)黑色糊状填充物由炭黑、MnO2、ZnC12和NH4Cl等组成
(3)有关数据见下表
温度/℃ 0 20 40 60 80 100
溶解度/g NH4Cl 29.3 37.2 45.8 55.3 65.6 77.3
ZnCl2 343 395 452 488 541 614
【实验探究一】小明取适量黑色糊状填充物,按图2所示实验流程进行探究。(1)溶液A中溶质主要有 (填化学式),操作Ⅱ中采用冷却热饱和溶液的方法实现两者分离的依据是 。
(2)欲从固体M 中得到较纯的MnO2,操作Ⅲ可采用的简便方法是 。
【实验探究二】小明取电池外壳锌皮,用砂纸打磨干净,剪成小块,进行实验。
(1)取一块锌皮放入盛有适量稀盐酸的烧杯中,有ZnCl2生成。
① 实验中可观察到的现象是 ;
② 下列各组物质混合后,也能生成ZnCl2的有 (填字母序号)。
A.ZnO与稀盐酸 B.ZnSO4溶液与BaC12溶液
C.ZnCO3与NaCl溶液 D.Zn(NO3)2溶液与NH4Cl溶液
(2)另取一块锌皮放入盛有一定量CuSO4溶液的烧杯中,充分反应后得到溶液E和固体F。当溶液E中只含一种溶质时,该溶质是 (填化学式);当固体F中只含一种物质时,溶液E中最少含有 种溶质。
③若将6.5g锌皮与足量稀硫酸完全反应,则生成氢气的质量 0.2g(选填“<”、“>”或“=”)。
参考答案:
1.BD
2.BC
3.CD
4.AC
5.AB
6.D
7.D
8.D
9.A
10.D
11.C
12.D
13.C
14.D
15.D
16. ABC 186 acd 漏斗 Fe+H2SO4=FeSO4+H2↑
17. 活性炭 肥皂水 煮沸 +6 70 bc 降温结晶 B>A>C 24 25 < B
18. NH4Cl、ZnCl2 两者的溶解度受温度变化的影响不同; 灼烧(在空气中充分燃烧); 固体溶解,有大量气泡产生;; A、B ZnSO4; 2; >。
学校:___________姓名:___________班级:___________考号:___________
一、多选题
1.1956年中国首次人工合成结晶牛胰岛素,说法正确的是
A.晶体都带有结晶水
B.晶体具有规则的几何形状
C.形成晶体的过程称为蒸发
D.从不饱和溶液中析出晶体,一般需要消耗能量
2.如图表示a、b两种固体物质的溶解度曲线,下列叙述正确的是
A.a的溶解度大于b的溶解度
B.a、b均为易溶物质
C.在t℃a、b两种物质的饱和溶液中溶质质量分数相等
D.a、b两种物质的溶解度受温度影响变化较小
3.将不再冒出气泡的汽水瓶(敞口)置于温水中,瓶内出现较多气泡。分析正确的是
A.瓶内压强减少导致溶解度减小
B.温度升高导致气体溶解度增大
C.出现大量气泡后溶液为饱和溶液
D.出现大量气泡后溶液中气体溶质质量分数变小
4.下表是氯化钠和硝酸钾在不同温度时的溶解度。以下说法正确的是(_____)
温度/℃ 10 20 30 40 50 60
溶解 度/g NaCl 35.8 36.0 36.3 36.6 37.0 37.3
KNO3 20.9 31.6 45.8 63.9 85.5 110
A.20℃时将20g KNO3加入到50g水中,能得到65.8g溶液
B.KNO3的溶解度比NaCl的溶解度大
C.60℃时将210g KNO3饱和溶液降温至20℃,溶液质量变为131.6g
D.20℃时将40g NaCl加入到100g水中,再升温至60℃可形成不饱和溶液
5.如图是甲、乙两种固体物质的溶解度曲线,下列说法正确的是
A.t1℃时,甲和乙的饱和溶液的溶质质量分数相等
B.t1℃时,120g甲的饱和溶液中含有20g甲
C.将甲、乙饱和溶液从t2℃降温至t1℃,析出晶体的质量:甲>乙
D.甲中混有少量杂质乙,可采用蒸发结晶的方式提纯甲
二、选择题
6.如表是不同温度时硝酸钾的溶解度,有关说法正确的是
温度/℃ 0 20 40 60 80 100
溶解度/克 13.3 31.6 63.9 110 169 246
A.20℃时,100g水中溶解的硝酸钾越多溶解度就越大
B.40℃时,100g硝酸钾饱和溶液中含有硝酸钾63.9克
C.100℃的水能溶解的硝酸钾一定比80℃的水能溶解的硝酸钾多
D.0℃的硝酸钾饱和溶液一定比60℃的硝酸钾饱和溶液的溶质质量分数小
7.如图,是甲、乙两物质的溶解度曲线,下列叙述中正确的是
A.t1℃时,甲、乙各100g溶液中均含有30g溶质
B.t2℃时,甲的溶解度是50
C.t1℃时,甲和乙溶液中溶质的质量分数一定相等
D.t2℃时,分别在100g水中各溶解20g甲、乙,同时降低温度,甲先达到饱和
8.高氯酸钾(KClO4)可用作火箭推进剂,其溶解度如下表,下列说法正确的是
温度/℃ 20 40 60 80
溶解度/g 1.68 3.73 7.3 13.4
A.高氯酸钾的溶解度随温度升高而减小
B.20℃时,将2g高氯酸钾溶解于98g水可配制2%的溶液
C.60℃时,高氯酸钾饱和溶液中溶质的质量分数是7.3%
D.80℃的高氯酸钾饱和溶液冷却至40℃有结晶现象
9.25℃时50g水最多溶解5gA;60℃时,100g水最多溶解10gB,则比较A,B溶解度大小为
A.不能比较 B.A=B C.A>B D.A
A.a点时R的溶解度大于b点
B.40℃时,R的饱和溶液的溶质质量分数为30%
C.升高温度可将接近饱和的R溶液变为饱和溶液
D.60℃时,向50g水中加入20gR,充分搅拌后形成饱和溶液
11.右图表示的是甲、乙两种固体物质的溶解度曲线,下列叙述正确的是
A.甲的溶解度大于乙的溶解度
B.35℃时100g甲的溶液中含甲的质量60g
C.10℃时甲、乙两物质的溶解度相等
D.甲中混有少量乙时可用蒸发结晶的方法提纯甲
12.如图是 a b c三种固体物质(均不含结晶水)的溶解度曲线,下列说法不正确的是
A.在 t1℃时,a c两种物质的溶解度相等
B.若 a物质中混有少量 b物质,最好采用降温结晶的方法提纯 a
C.将 t2℃时,a b c的饱和溶液降温至 t1℃,所得溶液的溶质质量分 数:b>a>c
D.t2℃时,将 a b c三种物质的饱和溶液分别降温至 t1℃,析出晶体的质量 a一定大于 b,而 c无晶体析出
13.实验室中区分下列各组物质的两种方法都正确的是
选项 需区分的物质 方法一 方法二
A 蒸馏水和食盐水 品尝 蒸干
B 铁粉和木炭粉 观察颜色 加入硫酸铜溶液,观察
C 饱和溶液和饱和石灰水 升温,观察 加入少量硝酸钾,观察
D 18K金和黄铜 在空气中灼烧 滴加稀盐酸
A.A B.B C.C D.D
14.关于溶液的叙述正确的是
A.溶液中各部分的性质不同 B.凡是均一稳定的液体都是溶液
C.饱和溶液一定是浓溶液 D.医用生理盐水是溶液
15.如图为甲、乙两种固体(不含结晶水)在水中的溶解度曲线,下列说法正确的是
A.甲物质的溶解度大于乙
B.除去甲中少量的乙,用蒸发结晶的方法
C.t1℃时,甲、乙的饱和溶液溶质质量分数都是 25%
D.t2℃时,等质量的甲和乙的饱和溶液中,溶剂质量甲<乙
三、综合应用题
16.溶液是生产生活中常见的物质,依据相关信息回答问题。资料:硝酸钾的溶解度数据(部分数据已做取整数处理)如下表所示:
温度/℃ 10 20 30 40 50 60 70
溶解度/g 21 32 46 64 86 110 138
(1)A、B、C、D四个烧杯中分别盛有100g水,在40℃时,向四个烧杯中分别加入110g、86g、64g、32g硝酸钾,充分溶解,如图所示。
①(填字母序号) 中盛的一定是饱和溶液。
②使B烧杯的溶液升温至50℃时,溶液的质量为 g。
③采用一种方法使A中的固体恰好溶解。对于最终四个烧杯中的溶液,下列说法正确的是 (填字母序号)。
a.溶剂质量可能相等
b.溶质质量可能相等
c.溶质质量分数可能有相等的
d.烧杯A中的溶液质量分数可能最大
(2)某校化学课外小组用硫酸亚铁废液(含少量硫酸铜和稀硫酸),制备硫酸亚铁晶体,主要的操作流程如图:
请回答下列问题:
①上述操作过程中用到的玻璃仪器有:①烧杯;②玻璃棒;③酒精灯;④温度计;⑤ ;
②流程中生成气体B的反应的化学方程式是: 。
17.(1)小明取串场河的河水,按下列流程进行实验,制取蒸馏水。请回答下列问题:
①滤液中有难闻的异味,可添加 除去,
②生活中常用 来比较所取水样与制得的蒸馏水的硬度。
③经过净化后的水,在生活中通过 方法,降低水的硬度并杀菌;
④消毒剂为高铁酸钾(K2FeO4)。高铁酸钾中铁元素的化合价为 。
(2)如图是A、B、C三种物质的溶解度曲线,请回答:
①在t2℃时,将30gA物质充分溶解在盛有50g水的烧杯中,所得溶液的质量为 g;若将烧杯内物质降温至t1℃(不考虑水蒸发),溶液中变化的是 (填字母序号)。
a 溶剂的质量 b 溶液的质量 c 溶质的质量分数
②当A物质中混有少量B、C两种物质时,采用 的方法可以提纯A.
③将t2℃的A、B、C三种物质的饱和溶液分别降温到t1℃时,所得溶液的溶质质量分数由大到小的顺序是 。
(3)实验室用质量分数为 6%的氯化钠溶液(密度为1.04g/cm3)配制 50g 质量分数为3%的氯化钠溶液。
①经计算,所需 6%的氯化钠的体积为 mL;加水 克
②若量取水时,采取仰视读数,其它操作均正确,则配制得到的稀溶液中溶质质量分数 3% (填“>”“<”或“ = ”)。
③向该49g20%的稀硫酸中,加入7.3g已部分氧化的锌粉,恰好完全反应。则所得溶液中溶质的质量为 (填字母序号)
A 15.5g B 16.1g C 18.1g
18.小明取酸性锌锰干电池进行探究,他发现电池内部结构如图1所示。
【查阅资料】(1)锌皮为金属锌(含有少量的铁)
(2)黑色糊状填充物由炭黑、MnO2、ZnC12和NH4Cl等组成
(3)有关数据见下表
温度/℃ 0 20 40 60 80 100
溶解度/g NH4Cl 29.3 37.2 45.8 55.3 65.6 77.3
ZnCl2 343 395 452 488 541 614
【实验探究一】小明取适量黑色糊状填充物,按图2所示实验流程进行探究。(1)溶液A中溶质主要有 (填化学式),操作Ⅱ中采用冷却热饱和溶液的方法实现两者分离的依据是 。
(2)欲从固体M 中得到较纯的MnO2,操作Ⅲ可采用的简便方法是 。
【实验探究二】小明取电池外壳锌皮,用砂纸打磨干净,剪成小块,进行实验。
(1)取一块锌皮放入盛有适量稀盐酸的烧杯中,有ZnCl2生成。
① 实验中可观察到的现象是 ;
② 下列各组物质混合后,也能生成ZnCl2的有 (填字母序号)。
A.ZnO与稀盐酸 B.ZnSO4溶液与BaC12溶液
C.ZnCO3与NaCl溶液 D.Zn(NO3)2溶液与NH4Cl溶液
(2)另取一块锌皮放入盛有一定量CuSO4溶液的烧杯中,充分反应后得到溶液E和固体F。当溶液E中只含一种溶质时,该溶质是 (填化学式);当固体F中只含一种物质时,溶液E中最少含有 种溶质。
③若将6.5g锌皮与足量稀硫酸完全反应,则生成氢气的质量 0.2g(选填“<”、“>”或“=”)。
参考答案:
1.BD
2.BC
3.CD
4.AC
5.AB
6.D
7.D
8.D
9.A
10.D
11.C
12.D
13.C
14.D
15.D
16. ABC 186 acd 漏斗 Fe+H2SO4=FeSO4+H2↑
17. 活性炭 肥皂水 煮沸 +6 70 bc 降温结晶 B>A>C 24 25 < B
18. NH4Cl、ZnCl2 两者的溶解度受温度变化的影响不同; 灼烧(在空气中充分燃烧); 固体溶解,有大量气泡产生;; A、B ZnSO4; 2; >。
同课章节目录
