8.2常见的酸和碱同步练习(含答案) 科粤版(2012)化学九年级下册
文档属性
| 名称 | 8.2常见的酸和碱同步练习(含答案) 科粤版(2012)化学九年级下册 |
|
|
| 格式 | docx | ||
| 文件大小 | 462.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-27 00:00:00 | ||
图片预览



文档简介
8.2常见的酸和碱同步练习科粤版(2012)化学九年级下册
学校:___________姓名:___________班级:___________考号:___________
一、多选题
1.下列实验操作不正确的是
A.稀释浓硫酸时,将水沿器壁慢慢倒入浓硫酸中并用玻璃棒不断地搅拌
B.比较蜡烛火焰各层温度时,用火柴梗迅速竖放蜡烛火焰中,约1~2s后取出观察
C.用量筒量取液体时先倾倒,再改用胶头滴管滴加至刻度线处
D.点燃氢气前应先验纯
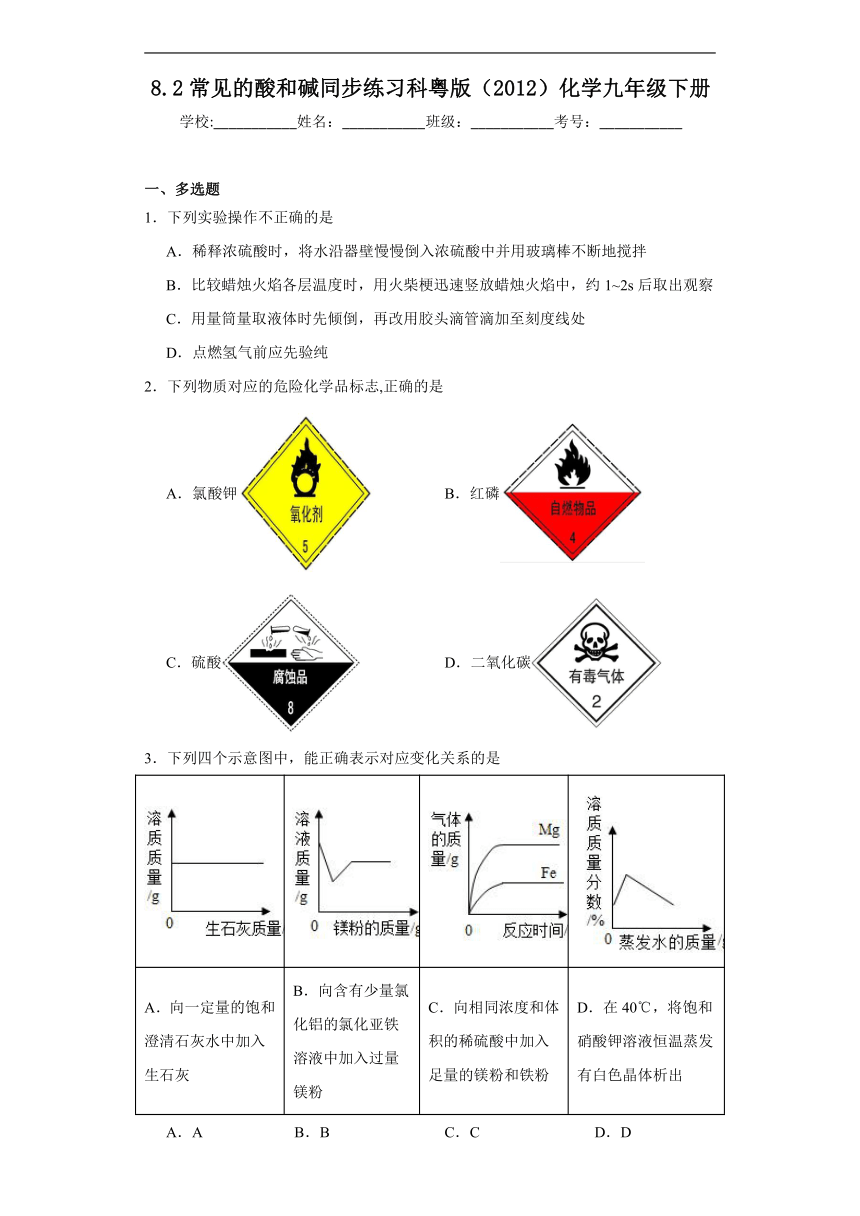
2.下列物质对应的危险化学品标志,正确的是
A.氯酸钾 B.红磷
C.硫酸 D.二氧化碳
3.下列四个示意图中,能正确表示对应变化关系的是
A.向一定量的饱和澄清石灰水中加入生石灰 B.向含有少量氯化铝的氯化亚铁溶液中加入过量镁粉 C.向相同浓度和体积的稀硫酸中加入足量的镁粉和铁粉 D.在40℃,将饱和硝酸钾溶液恒温蒸发有白色晶体析出
A.A B.B C.C D.D
4.下列物质露置于空气中,一段时间后,质量增加的是
A.浓硫酸 B.双氧水 C.浓盐酸 D.烧碱
5.如图所示,向试管中依次加入约3mL饱和硫酸铜溶液和约2mL浓硫酸,静止片刻后,可观察到的现象是
A.玻璃管中左液面上升,右液面下降
B.试管中的液体明显分为两层,上层呈蓝色,下层无色
C.有蓝色晶体析出
D.有白色固体沉降到试管底部
二、选择题
6.下列说法不正确的是
A.硝酸钠溶液能够导电是由于其水溶液中含有大量自由移动的电子
B.盐酸和稀硫酸的化学性质相似是由于溶液中所含的阳离子全部是H+
C.过氧化氢和水的化学性质不同是因为构成它们的分子种类不同
D.金刚石和石墨的物理性质差异较大是因为它们的碳原子排列方式不同
7.有如图所示的装置,小试管中装有一定量的水,开始时,U形管中a、b两液面处于同一水平线,向其中加入下列哪种物质进行溶解时,会造成U形管中的液面出现b低a高的情况( )
A.氯化钠 B.氢氧化钠 C.氧化钙 D.硝酸铵
8.推理是学习化学的科学方法。下列推理正确的是( )
A.铁在潮湿的空气中容易被锈蚀,所以金属在潮湿的空气中都容易被锈蚀
B.酸溶液的pH<7,常温下测得某溶液的pH=3,所以该溶液一定是酸性的
C.有机物中都含有碳元素,所以含有碳元素的化合物都是有机物
D.铵态氮肥与熟石灰混合使用可以明显提高肥效
9.在烧杯中加入10mLNaOH溶液,滴入几滴酚酞溶液,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液恰好由红色变成无色为止,则所得溶液的pH为
A.0 B.3 C.7 D.10
10.善于思考,学以致用。下列操作的相关解释错误的是
选项 A B C D
操作 在冰箱中放活性炭包除味 将铅笔芯粉末撒进生锈的锁芯中开锁 野外用氧化钙和水煮鸡蛋 温室大棚充入适量CO2作气肥
解释 活性炭有吸附性 石墨具有还原性 二者反应放热 CO2参与光合作用
A.A B.B C.C D.D
11.正确的实验操作是进行科学探究的重要保障。下列实验操作中,正确的是
A.测定某溶液的PH时,先用水将PH试纸润湿
B.稀释浓硫酸时,将水注入盛有浓硫酸的烧杯中
C.称量氢氧化钠固体时,应将其放在烧杯中称量
D.浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,涂上3%-5%的碳酸钠溶液
12.下列实验中能达到相应实验目的的是
选项 实验目的 实验方案
A 鉴别食盐和蔗糖 尝味道
B 鉴别生石灰和石灰石 加水
C 除去CO2中含有的少量CO 点燃
D 除去氯化钾固体中的氯酸钾 加入少量二氧化锰固体,加热
A.A B.B C.C D.D
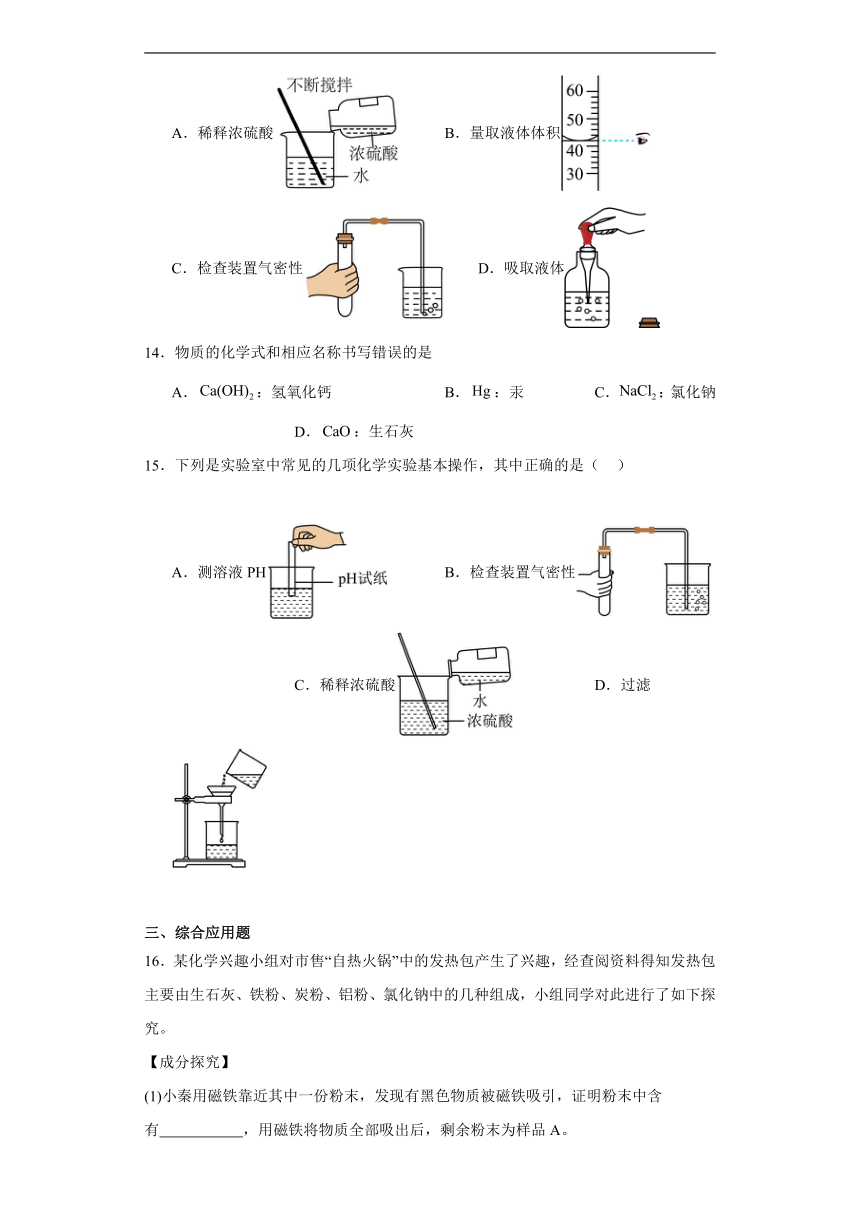
13.下图所示实验操作错误的是
A.稀释浓硫酸 B.量取液体体积
C.检查装置气密性 D.吸取液体
14.物质的化学式和相应名称书写错误的是
A.:氢氧化钙 B.:汞 C.:氯化钠 D.:生石灰
15.下列是实验室中常见的几项化学实验基本操作,其中正确的是( )
A.测溶液PH B.检查装置气密性 C.稀释浓硫酸 D.过滤
三、综合应用题
16.某化学兴趣小组对市售“自热火锅”中的发热包产生了兴趣,经查阅资料得知发热包主要由生石灰、铁粉、炭粉、铝粉、氯化钠中的几种组成,小组同学对此进行了如下探究。
【成分探究】
(1)小秦用磁铁靠近其中一份粉末,发现有黑色物质被磁铁吸引,证明粉末中含有 ,用磁铁将物质全部吸出后,剩余粉末为样品A。
(2)小秦取一定量样品A于烧杯中,加水充分溶解,静置后,取适量上层清液滴入几滴酚酞溶液,溶液变为 色,证明原粉末中含有生石灰。
(3)除上述物质外,样品A中还可能存在铝粉、氯化钠、炭粉中的至少两种物质,小秦对固体的组成提出下列猜想:
猜想一:铝粉、氯化钠和炭粉 猜想二:铝粉、氯化钠
猜想三:铝粉、炭粉 猜想四: 。
【实验验证】
小明另取一定量的样品A于烧杯中,加入足量的水,搅拌,静置,观察到固体部分溶解,烧杯底部有黑色不溶物B.向不溶物B中加入足量的稀盐酸,产生气泡,但黑色固体仍未完全溶解,剩余固体为不溶物C。
【实验结论】
(4)固体不溶物C是 。
(5)稀盐酸和不溶物B中的物质反应的化学方程式是 。
(6)经过分析,猜想 (填“一”“二”“三”或“四”)成立。
17.铜及铜的化合物在生产、生活中有着广泛的应用。铜生锈会生成碱式碳酸铜,而工业上所制得的碱式碳酸铜种类较多,其组成表示为:。
为了测定某种产品的组成,某兴趣小组准确称量了25.8 g的样品,设计了如图所示装置并进行实验:
【资料卡片】① 碱石灰可吸收水和二氧化碳
②加热至 200℃时会分解得到氧化铜、二氧化碳和水。
实验数据记录如下表,请完成下列问题:
B中溶液质量/g C中溶液质量/g D中固体质量/g
反应前 100.0 100.0 100.0
反应后 105.4 104.4 100.0
(1)实验前应该先 ,再鼓入一段时间氮气后称量B、C、D的质量。
(2)停止鼓入氮气,调控温电加热200℃持续加热,观察到装置B中 时表明碱式碳酸铜已经完全分解。
(3)写出装置C中发生反应的化学方程式 。
(4)装置D的作用是 。
(5)该碱式碳酸铜的化学式是 。
18.研究性学习课题:探究实验室中久置的NaOH的变质程度
[研究方案]先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量。从而进一步确定样品中NaOH的变质程度。
[解决问题]实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示。
填写下表:(计算结果保留小数点后面一位)
Na2CO3的质量/g
变质NaOH的质量/g
NaOH的变质程度(用质量分数表示)
[继续探究]计算实验过程中与NaOH反应消耗盐酸的质量 。[发现问题]根据“与NaOH反应消耗盐酸的质量”,对照图像,你发现了什么问题?
参考答案:
1.
2.AC
3.B
4.AD
5.BD
6.A
7.D
8.B
9.C
10.B
11.C
12.B
13.D
14.C
15.B
16.(1)铁粉
(2)红
(3)氯化钠、炭粉
(4)炭粉
(5)
(6)一
17.(1)检查装置气密性
(2)不再有气泡产生
(3)
(4)防止空气中的二氧化碳和水蒸气进入实验装置,影响实验结果
(5)
18. 5.3 4 33.3% 50g 氢氧化钠溶液完全反应后,继续滴加HCl并非立即产生二氧化碳气体
学校:___________姓名:___________班级:___________考号:___________
一、多选题
1.下列实验操作不正确的是
A.稀释浓硫酸时,将水沿器壁慢慢倒入浓硫酸中并用玻璃棒不断地搅拌
B.比较蜡烛火焰各层温度时,用火柴梗迅速竖放蜡烛火焰中,约1~2s后取出观察
C.用量筒量取液体时先倾倒,再改用胶头滴管滴加至刻度线处
D.点燃氢气前应先验纯
2.下列物质对应的危险化学品标志,正确的是
A.氯酸钾 B.红磷
C.硫酸 D.二氧化碳
3.下列四个示意图中,能正确表示对应变化关系的是
A.向一定量的饱和澄清石灰水中加入生石灰 B.向含有少量氯化铝的氯化亚铁溶液中加入过量镁粉 C.向相同浓度和体积的稀硫酸中加入足量的镁粉和铁粉 D.在40℃,将饱和硝酸钾溶液恒温蒸发有白色晶体析出
A.A B.B C.C D.D
4.下列物质露置于空气中,一段时间后,质量增加的是
A.浓硫酸 B.双氧水 C.浓盐酸 D.烧碱
5.如图所示,向试管中依次加入约3mL饱和硫酸铜溶液和约2mL浓硫酸,静止片刻后,可观察到的现象是
A.玻璃管中左液面上升,右液面下降
B.试管中的液体明显分为两层,上层呈蓝色,下层无色
C.有蓝色晶体析出
D.有白色固体沉降到试管底部
二、选择题
6.下列说法不正确的是
A.硝酸钠溶液能够导电是由于其水溶液中含有大量自由移动的电子
B.盐酸和稀硫酸的化学性质相似是由于溶液中所含的阳离子全部是H+
C.过氧化氢和水的化学性质不同是因为构成它们的分子种类不同
D.金刚石和石墨的物理性质差异较大是因为它们的碳原子排列方式不同
7.有如图所示的装置,小试管中装有一定量的水,开始时,U形管中a、b两液面处于同一水平线,向其中加入下列哪种物质进行溶解时,会造成U形管中的液面出现b低a高的情况( )
A.氯化钠 B.氢氧化钠 C.氧化钙 D.硝酸铵
8.推理是学习化学的科学方法。下列推理正确的是( )
A.铁在潮湿的空气中容易被锈蚀,所以金属在潮湿的空气中都容易被锈蚀
B.酸溶液的pH<7,常温下测得某溶液的pH=3,所以该溶液一定是酸性的
C.有机物中都含有碳元素,所以含有碳元素的化合物都是有机物
D.铵态氮肥与熟石灰混合使用可以明显提高肥效
9.在烧杯中加入10mLNaOH溶液,滴入几滴酚酞溶液,再用滴管慢慢滴入稀盐酸,并不断搅拌溶液,至溶液恰好由红色变成无色为止,则所得溶液的pH为
A.0 B.3 C.7 D.10
10.善于思考,学以致用。下列操作的相关解释错误的是
选项 A B C D
操作 在冰箱中放活性炭包除味 将铅笔芯粉末撒进生锈的锁芯中开锁 野外用氧化钙和水煮鸡蛋 温室大棚充入适量CO2作气肥
解释 活性炭有吸附性 石墨具有还原性 二者反应放热 CO2参与光合作用
A.A B.B C.C D.D
11.正确的实验操作是进行科学探究的重要保障。下列实验操作中,正确的是
A.测定某溶液的PH时,先用水将PH试纸润湿
B.稀释浓硫酸时,将水注入盛有浓硫酸的烧杯中
C.称量氢氧化钠固体时,应将其放在烧杯中称量
D.浓硫酸不慎沾到皮肤上,应立即用大量水冲洗,涂上3%-5%的碳酸钠溶液
12.下列实验中能达到相应实验目的的是
选项 实验目的 实验方案
A 鉴别食盐和蔗糖 尝味道
B 鉴别生石灰和石灰石 加水
C 除去CO2中含有的少量CO 点燃
D 除去氯化钾固体中的氯酸钾 加入少量二氧化锰固体,加热
A.A B.B C.C D.D
13.下图所示实验操作错误的是
A.稀释浓硫酸 B.量取液体体积
C.检查装置气密性 D.吸取液体
14.物质的化学式和相应名称书写错误的是
A.:氢氧化钙 B.:汞 C.:氯化钠 D.:生石灰
15.下列是实验室中常见的几项化学实验基本操作,其中正确的是( )
A.测溶液PH B.检查装置气密性 C.稀释浓硫酸 D.过滤
三、综合应用题
16.某化学兴趣小组对市售“自热火锅”中的发热包产生了兴趣,经查阅资料得知发热包主要由生石灰、铁粉、炭粉、铝粉、氯化钠中的几种组成,小组同学对此进行了如下探究。
【成分探究】
(1)小秦用磁铁靠近其中一份粉末,发现有黑色物质被磁铁吸引,证明粉末中含有 ,用磁铁将物质全部吸出后,剩余粉末为样品A。
(2)小秦取一定量样品A于烧杯中,加水充分溶解,静置后,取适量上层清液滴入几滴酚酞溶液,溶液变为 色,证明原粉末中含有生石灰。
(3)除上述物质外,样品A中还可能存在铝粉、氯化钠、炭粉中的至少两种物质,小秦对固体的组成提出下列猜想:
猜想一:铝粉、氯化钠和炭粉 猜想二:铝粉、氯化钠
猜想三:铝粉、炭粉 猜想四: 。
【实验验证】
小明另取一定量的样品A于烧杯中,加入足量的水,搅拌,静置,观察到固体部分溶解,烧杯底部有黑色不溶物B.向不溶物B中加入足量的稀盐酸,产生气泡,但黑色固体仍未完全溶解,剩余固体为不溶物C。
【实验结论】
(4)固体不溶物C是 。
(5)稀盐酸和不溶物B中的物质反应的化学方程式是 。
(6)经过分析,猜想 (填“一”“二”“三”或“四”)成立。
17.铜及铜的化合物在生产、生活中有着广泛的应用。铜生锈会生成碱式碳酸铜,而工业上所制得的碱式碳酸铜种类较多,其组成表示为:。
为了测定某种产品的组成,某兴趣小组准确称量了25.8 g的样品,设计了如图所示装置并进行实验:
【资料卡片】① 碱石灰可吸收水和二氧化碳
②加热至 200℃时会分解得到氧化铜、二氧化碳和水。
实验数据记录如下表,请完成下列问题:
B中溶液质量/g C中溶液质量/g D中固体质量/g
反应前 100.0 100.0 100.0
反应后 105.4 104.4 100.0
(1)实验前应该先 ,再鼓入一段时间氮气后称量B、C、D的质量。
(2)停止鼓入氮气,调控温电加热200℃持续加热,观察到装置B中 时表明碱式碳酸铜已经完全分解。
(3)写出装置C中发生反应的化学方程式 。
(4)装置D的作用是 。
(5)该碱式碳酸铜的化学式是 。
18.研究性学习课题:探究实验室中久置的NaOH的变质程度
[研究方案]先称取13.3g的NaOH样品(杂质为Na2CO3),配成溶液,然后向溶液中逐滴加入质量分数为14.6%的稀盐酸,根据生成CO2的质量测定Na2CO3的质量。从而进一步确定样品中NaOH的变质程度。
[解决问题]实验测得加入稀盐酸的质量与产生CO2气体的质量关系如图所示。
填写下表:(计算结果保留小数点后面一位)
Na2CO3的质量/g
变质NaOH的质量/g
NaOH的变质程度(用质量分数表示)
[继续探究]计算实验过程中与NaOH反应消耗盐酸的质量 。[发现问题]根据“与NaOH反应消耗盐酸的质量”,对照图像,你发现了什么问题?
参考答案:
1.
2.AC
3.B
4.AD
5.BD
6.A
7.D
8.B
9.C
10.B
11.C
12.B
13.D
14.C
15.B
16.(1)铁粉
(2)红
(3)氯化钠、炭粉
(4)炭粉
(5)
(6)一
17.(1)检查装置气密性
(2)不再有气泡产生
(3)
(4)防止空气中的二氧化碳和水蒸气进入实验装置,影响实验结果
(5)
18. 5.3 4 33.3% 50g 氢氧化钠溶液完全反应后,继续滴加HCl并非立即产生二氧化碳气体
