8.5化学肥料同步练习(含答案) 科粤版(2012)化学九年级下册
文档属性
| 名称 | 8.5化学肥料同步练习(含答案) 科粤版(2012)化学九年级下册 |

|
|
| 格式 | docx | ||
| 文件大小 | 359.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2024-02-27 00:00:00 | ||
图片预览



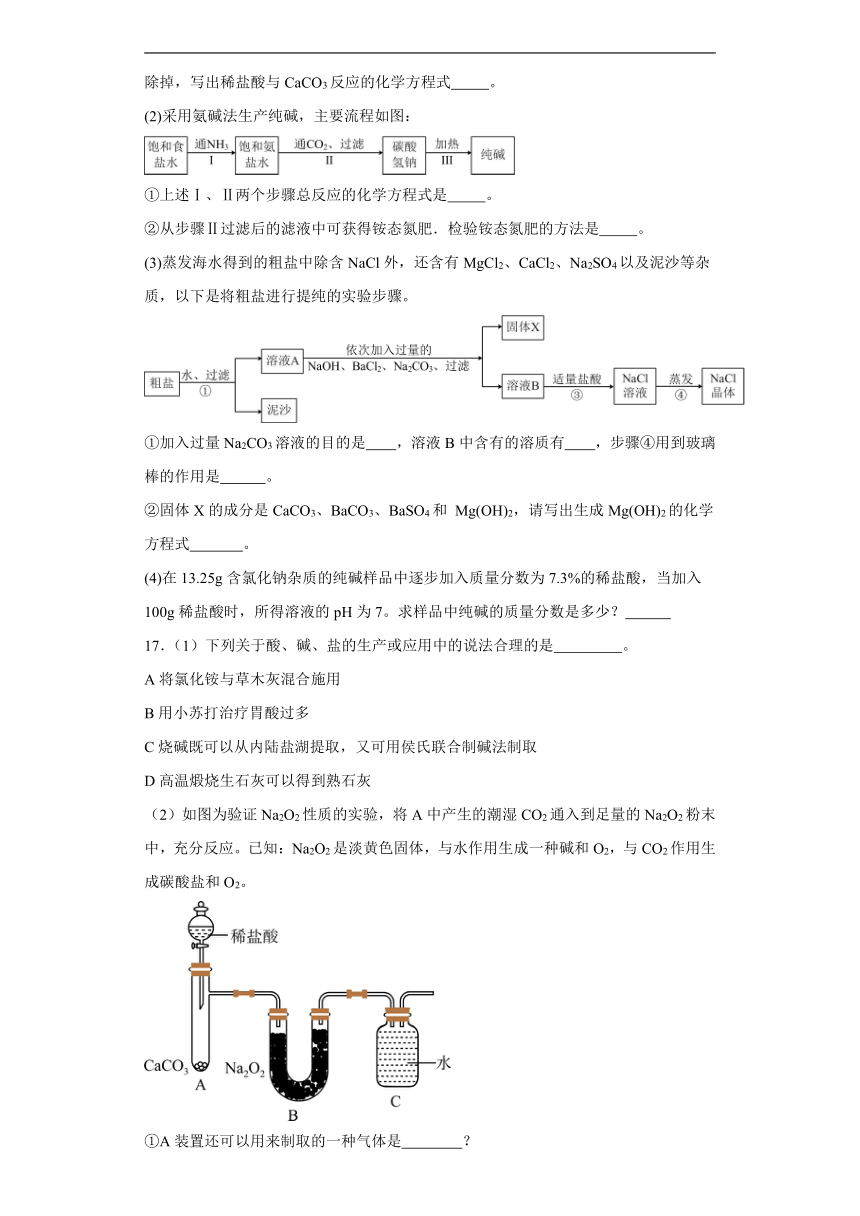
文档简介
8.5化学肥料同步练习科粤版(2012)化学九年级下册
学校:___________姓名:___________班级:___________考号:___________
一、多选题
1.由下列实验操作及现象所得到的结论正确的是( )
实验操作及现象 结论
A 将黄铜片(铜锌合金)与铜片相互刻画,铜片上有刻痕 黄铜片的硬度比铜片大
B 分别在放有少量锌片、铜片的试管中加入稀盐酸,观察到锌片上有气泡产生,铜片上没有气泡产生 锌的金属活动性比铜强
C 在镁条与盐酸反应后的溶液中滴加几滴氢氧化钠溶液,无白色沉淀 氯化镁与氢氧化钠不反应
D 取硝酸钠固体少量,加入少量熟石灰粉末,混合、研磨,未能闻到气味 氮肥与碱作用都无氨气放出
A.A B.B C.C D.D
2.下列实验方案正确的是
选项 实验内容 操作方法
A 鉴别氮气和氧气 分别闻气体的气味
B 鉴别硫酸铵和硝酸铵 取样,分别加入少量熟石灰粉末,研磨
C 硬水软化成软水 将硬水进行蒸馏
D 检验铝粉中是否含有铁粉 取样,用磁铁接近样品
A.A B.B C.C D.D
3.下列说法正确的是
A.镁原子和镁离子化学性质不同,是因为最外层电子数不同
B.用燃着的木条鉴别O2、CO2和空气三瓶无色气体
C.长期使用硫酸铵会使土壤呈酸性,应将硫酸铵与熟石灰混合使用
D.氯化钠溶液可以导电因为溶液中存在自由移动的Na+和Cl-
4.在给定条件下,下列转化可以通过一步反应实现的是
A.FeFe2O3 B.CO2→H2O
C.NH4HCO3NH3 D.CuO→Cu(OH)2
5.下列实验操作中能达到实验目的的是( )
选项 实验目的 实验方案
A 除去CuSO4溶液中的硫酸 加入过量铁粉,过滤
B 除去CO中的CO2 通入过量氢氧化钠溶液中,再通过浓硫酸
C 分离氧化铁粉末和碳粉的混合物 加入过量稀硫酸,过滤
D 鉴别(NH4)2SO4固体和K2SO4固体 分别加入熟石灰研磨,闻气味
A.A B.B C.C D.D
二、选择题
6.下列实验现象描述正确的是( )
A.将干燥的紫色小花(石蕊浸泡)放到二氧化碳气体中,小花由紫色变成红色
B.铁锈与稀盐酸反应后,溶液由无色变成了浅绿色
C.硫酸铵和熟石灰混合研磨,能闻到刺激性气味
D.打开盛有浓盐酸的瓶盖,瓶口出现白烟
7.下列与化学有关的知识内容完全正确的一组是
A ①食品包装填充氧气--防止变质、变形 ②食品包装放入生石灰--防止受潮 B ①Cl-得到一个电子----形成氯原子 ②墙内开花墙外香--分子不断运动
C ①H2、CH4均是可燃气体--点燃前须检验纯度 ②有腐蚀性的药液溅入眼睛内--要立即用水冲洗,切不可用手揉搓。 D ①减少汽车尾气污染-- --严禁生产使用汽车 ②鉴别硝酸铵和硫酸铵——加熟石灰研磨,闻气味
A.A B.B C.C D.D
8.下列归纳总结完全正确的一组是
A.化学之最 ①熔点最低的金属是汞 ②地壳中含量最高的金属元素是铁 ③天然存在的最硬的物质是金刚石 B. 化学与生活 ①衣服上的油污:可用汽油乳化后洗去 ②水壶上的水垢:可加食盐水浸泡除去 ③冰箱中的异味:可放活性炭吸附
C. 化学与工农业 ①用焦炭和铁矿石炼铁 ②用石油产品生产合成纤维 ③农作物施用化肥、农药,越多越好 D.物质保存方法及解释 ①浓盐酸密封保存:防止挥发 ②白磷在冷水中保存:隔绝空气防止自燃 ③氢氧化钠密封保存:防止潮解、变质
A.A B.B C.C D.D
9.分类是一种常用的学习方法。下列分类正确的是
A.原子构成:铁、金刚石、冰 B.单质:水、氧气、红磷
C.合金:不锈钢、黄铜、生铁 D.复合肥料:硝酸钾、磷酸二氢铵、钙镁磷肥
10.雷电能自然固氮并最终形成氮肥,下列属于含氮复合肥料的是( )
A.KNO3 B.Ca(NO3)2 C.NH4NO3 D.NaNO3
11.合理施用化肥,可增加作物产量。下列属于磷肥的是
A.KCl B.Ca3(PO4)2 C.KNO3 D.NH3·H2O
12.下列化肥分别与熟石灰混合研磨后,能闻到刺激性气味的是( )
A.碳酸氢铵 B.氯化钾 C.过磷酸钙 D.尿素
13.今年我市部分地区的小麦得了“软骨病”,出现倒伏现象,为预防这种现象的发生,应提前施用的化肥是
A.NH4H2PO4 B.CO(NH2)2 C.K2CO3 D.NH4HCO3
14.荔枝快成熟的时候特别需要磷肥和氮肥,下列符合条件的一种化肥是
A.NH4NO3 B.KCl C.NH4H2PO3 D.KNO3
15.“春分麦起身,水肥要紧跟”,大概意思是说,春分后冬小麦处于起身期,肥料和水分需要上、冬小麦起身期需要的氮肥比较多,因此需要适量施用的化肥是
A.KH2PO4 B.K2SO4 C.CO(NH2)2 D.Ca3(PO4)2
三、综合应用题
16.酸、碱、盐是中学化学学习和研究的重要内容。
(1)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是CaCO3和Mg(OH)2]可用稀盐酸除掉,写出稀盐酸与CaCO3反应的化学方程式 。
(2)采用氨碱法生产纯碱,主要流程如图:
①上述Ⅰ、Ⅱ两个步骤总反应的化学方程式是 。
②从步骤Ⅱ过滤后的滤液中可获得铵态氮肥.检验铵态氮肥的方法是 。
(3)蒸发海水得到的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
①加入过量Na2CO3溶液的目的是 ,溶液B中含有的溶质有 ,步骤④用到玻璃棒的作用是 。
②固体X的成分是CaCO3、BaCO3、BaSO4和 Mg(OH)2,请写出生成Mg(OH)2的化学方程式 。
(4)在13.25g含氯化钠杂质的纯碱样品中逐步加入质量分数为7.3%的稀盐酸,当加入100g稀盐酸时,所得溶液的pH为7。求样品中纯碱的质量分数是多少?
17.(1)下列关于酸、碱、盐的生产或应用中的说法合理的是 。
A将氯化铵与草木灰混合施用
B用小苏打治疗胃酸过多
C烧碱既可以从内陆盐湖提取,又可用侯氏联合制碱法制取
D高温煅烧生石灰可以得到熟石灰
(2)如图为验证Na2O2性质的实验,将A中产生的潮湿CO2通入到足量的Na2O2粉末中,充分反应。已知:Na2O2是淡黄色固体,与水作用生成一种碱和O2,与CO2作用生成碳酸盐和O2。
①A装置还可以用来制取的一种气体是 ?
②B中发生反应的化学方程式 (只写1个)。
③若由C装置收集反应后的气体,请把C装置中的导管补画完整 。
(3)同学用含有CO2的CO来模拟炼铁实并检验气体产物和收集尾气,他设计了如图所示的微型实验装置(夹持设备已略去)。
①装置A的作用是什么 ?
②写出B处玻璃管中发生反应的化学方程 。
③实验结束后,D中有部分溶液进入E处量筒中,请设计实验方案,确定该溶液中含有哪些溶质 ?(写出实验步骤、现象和结论)
(4)某小组按下图实验进行操作,计算E装置中Na2CO3的质量分数 。
18.回答下列问题。
(1)从硝酸钾、少量氯化钠和不溶性杂质(泥沙)的混合物中得到硝酸钾的流程如图:
温度/℃ 0 20 40 60 80
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4
KNO3 13.3 31.6 63.9 110 169
①操作a的名称是 。
②操作a用到的玻璃仪器有 。
③滤液2的溶质是 。
(2)A~D为初中化学常见物质,A、D为金属,在常温下通过如图所示转化可获取硝酸钾。回答下列问题。
①若D为银白色贵重金属,则反应Ⅰ的化学方程式是 ,基本反应类型是 。
②一步实现反应Ⅱ,能否加入氯化钾?判断并说明理由。 。
③硝酸钾可作化肥,能供给作物两种养分,属于 肥料。
参考答案:
1.AB
2.CD
3.ABD
4.BC
5.BD
6.C
7.C
8.D
9.C
10.A
11.B
12.A
13.C
14.C
15.C
16.(1)
(2)
与熟石灰混合研磨,闻气味
(3) 除去氯化钙和过量的氯化钡 氯化钠、氢氧化钠、碳酸钠 搅拌,防止局部温度过高,造成液滴飞溅
(4)解:设样品中纯碱的质量分数是x
x=80%
答:样品中纯碱的质量分数是80%
17. B H2 吸收二氧化碳气体 取少量溶液于试管中,滴加足量氯化钡(或氯化钙)溶液,静置,再向上层清液中滴加酚酞溶液,若无沉淀产生,溶液变红,说明溶质为氢氧化钠;若有白色沉淀产生,溶液变红,说明溶质为碳酸钠和氢氧化钠;若有白色沉淀产生,溶液不变红,说明溶质为碳酸钠 21.2%
18.(1) 降温结晶 烧杯 氯化钠、硝酸钾
(2) (合理即可) 置换反应 氯化钾与硝酸铜相互交换成分后不会生成沉淀、气体或水,两者不反应 复合
学校:___________姓名:___________班级:___________考号:___________
一、多选题
1.由下列实验操作及现象所得到的结论正确的是( )
实验操作及现象 结论
A 将黄铜片(铜锌合金)与铜片相互刻画,铜片上有刻痕 黄铜片的硬度比铜片大
B 分别在放有少量锌片、铜片的试管中加入稀盐酸,观察到锌片上有气泡产生,铜片上没有气泡产生 锌的金属活动性比铜强
C 在镁条与盐酸反应后的溶液中滴加几滴氢氧化钠溶液,无白色沉淀 氯化镁与氢氧化钠不反应
D 取硝酸钠固体少量,加入少量熟石灰粉末,混合、研磨,未能闻到气味 氮肥与碱作用都无氨气放出
A.A B.B C.C D.D
2.下列实验方案正确的是
选项 实验内容 操作方法
A 鉴别氮气和氧气 分别闻气体的气味
B 鉴别硫酸铵和硝酸铵 取样,分别加入少量熟石灰粉末,研磨
C 硬水软化成软水 将硬水进行蒸馏
D 检验铝粉中是否含有铁粉 取样,用磁铁接近样品
A.A B.B C.C D.D
3.下列说法正确的是
A.镁原子和镁离子化学性质不同,是因为最外层电子数不同
B.用燃着的木条鉴别O2、CO2和空气三瓶无色气体
C.长期使用硫酸铵会使土壤呈酸性,应将硫酸铵与熟石灰混合使用
D.氯化钠溶液可以导电因为溶液中存在自由移动的Na+和Cl-
4.在给定条件下,下列转化可以通过一步反应实现的是
A.FeFe2O3 B.CO2→H2O
C.NH4HCO3NH3 D.CuO→Cu(OH)2
5.下列实验操作中能达到实验目的的是( )
选项 实验目的 实验方案
A 除去CuSO4溶液中的硫酸 加入过量铁粉,过滤
B 除去CO中的CO2 通入过量氢氧化钠溶液中,再通过浓硫酸
C 分离氧化铁粉末和碳粉的混合物 加入过量稀硫酸,过滤
D 鉴别(NH4)2SO4固体和K2SO4固体 分别加入熟石灰研磨,闻气味
A.A B.B C.C D.D
二、选择题
6.下列实验现象描述正确的是( )
A.将干燥的紫色小花(石蕊浸泡)放到二氧化碳气体中,小花由紫色变成红色
B.铁锈与稀盐酸反应后,溶液由无色变成了浅绿色
C.硫酸铵和熟石灰混合研磨,能闻到刺激性气味
D.打开盛有浓盐酸的瓶盖,瓶口出现白烟
7.下列与化学有关的知识内容完全正确的一组是
A ①食品包装填充氧气--防止变质、变形 ②食品包装放入生石灰--防止受潮 B ①Cl-得到一个电子----形成氯原子 ②墙内开花墙外香--分子不断运动
C ①H2、CH4均是可燃气体--点燃前须检验纯度 ②有腐蚀性的药液溅入眼睛内--要立即用水冲洗,切不可用手揉搓。 D ①减少汽车尾气污染-- --严禁生产使用汽车 ②鉴别硝酸铵和硫酸铵——加熟石灰研磨,闻气味
A.A B.B C.C D.D
8.下列归纳总结完全正确的一组是
A.化学之最 ①熔点最低的金属是汞 ②地壳中含量最高的金属元素是铁 ③天然存在的最硬的物质是金刚石 B. 化学与生活 ①衣服上的油污:可用汽油乳化后洗去 ②水壶上的水垢:可加食盐水浸泡除去 ③冰箱中的异味:可放活性炭吸附
C. 化学与工农业 ①用焦炭和铁矿石炼铁 ②用石油产品生产合成纤维 ③农作物施用化肥、农药,越多越好 D.物质保存方法及解释 ①浓盐酸密封保存:防止挥发 ②白磷在冷水中保存:隔绝空气防止自燃 ③氢氧化钠密封保存:防止潮解、变质
A.A B.B C.C D.D
9.分类是一种常用的学习方法。下列分类正确的是
A.原子构成:铁、金刚石、冰 B.单质:水、氧气、红磷
C.合金:不锈钢、黄铜、生铁 D.复合肥料:硝酸钾、磷酸二氢铵、钙镁磷肥
10.雷电能自然固氮并最终形成氮肥,下列属于含氮复合肥料的是( )
A.KNO3 B.Ca(NO3)2 C.NH4NO3 D.NaNO3
11.合理施用化肥,可增加作物产量。下列属于磷肥的是
A.KCl B.Ca3(PO4)2 C.KNO3 D.NH3·H2O
12.下列化肥分别与熟石灰混合研磨后,能闻到刺激性气味的是( )
A.碳酸氢铵 B.氯化钾 C.过磷酸钙 D.尿素
13.今年我市部分地区的小麦得了“软骨病”,出现倒伏现象,为预防这种现象的发生,应提前施用的化肥是
A.NH4H2PO4 B.CO(NH2)2 C.K2CO3 D.NH4HCO3
14.荔枝快成熟的时候特别需要磷肥和氮肥,下列符合条件的一种化肥是
A.NH4NO3 B.KCl C.NH4H2PO3 D.KNO3
15.“春分麦起身,水肥要紧跟”,大概意思是说,春分后冬小麦处于起身期,肥料和水分需要上、冬小麦起身期需要的氮肥比较多,因此需要适量施用的化肥是
A.KH2PO4 B.K2SO4 C.CO(NH2)2 D.Ca3(PO4)2
三、综合应用题
16.酸、碱、盐是中学化学学习和研究的重要内容。
(1)热水瓶用久后,瓶胆内壁常附着一层水垢[主要成分是CaCO3和Mg(OH)2]可用稀盐酸除掉,写出稀盐酸与CaCO3反应的化学方程式 。
(2)采用氨碱法生产纯碱,主要流程如图:
①上述Ⅰ、Ⅱ两个步骤总反应的化学方程式是 。
②从步骤Ⅱ过滤后的滤液中可获得铵态氮肥.检验铵态氮肥的方法是 。
(3)蒸发海水得到的粗盐中除含NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质,以下是将粗盐进行提纯的实验步骤。
①加入过量Na2CO3溶液的目的是 ,溶液B中含有的溶质有 ,步骤④用到玻璃棒的作用是 。
②固体X的成分是CaCO3、BaCO3、BaSO4和 Mg(OH)2,请写出生成Mg(OH)2的化学方程式 。
(4)在13.25g含氯化钠杂质的纯碱样品中逐步加入质量分数为7.3%的稀盐酸,当加入100g稀盐酸时,所得溶液的pH为7。求样品中纯碱的质量分数是多少?
17.(1)下列关于酸、碱、盐的生产或应用中的说法合理的是 。
A将氯化铵与草木灰混合施用
B用小苏打治疗胃酸过多
C烧碱既可以从内陆盐湖提取,又可用侯氏联合制碱法制取
D高温煅烧生石灰可以得到熟石灰
(2)如图为验证Na2O2性质的实验,将A中产生的潮湿CO2通入到足量的Na2O2粉末中,充分反应。已知:Na2O2是淡黄色固体,与水作用生成一种碱和O2,与CO2作用生成碳酸盐和O2。
①A装置还可以用来制取的一种气体是 ?
②B中发生反应的化学方程式 (只写1个)。
③若由C装置收集反应后的气体,请把C装置中的导管补画完整 。
(3)同学用含有CO2的CO来模拟炼铁实并检验气体产物和收集尾气,他设计了如图所示的微型实验装置(夹持设备已略去)。
①装置A的作用是什么 ?
②写出B处玻璃管中发生反应的化学方程 。
③实验结束后,D中有部分溶液进入E处量筒中,请设计实验方案,确定该溶液中含有哪些溶质 ?(写出实验步骤、现象和结论)
(4)某小组按下图实验进行操作,计算E装置中Na2CO3的质量分数 。
18.回答下列问题。
(1)从硝酸钾、少量氯化钠和不溶性杂质(泥沙)的混合物中得到硝酸钾的流程如图:
温度/℃ 0 20 40 60 80
溶解度/g NaCl 35.7 36.0 36.6 37.3 38.4
KNO3 13.3 31.6 63.9 110 169
①操作a的名称是 。
②操作a用到的玻璃仪器有 。
③滤液2的溶质是 。
(2)A~D为初中化学常见物质,A、D为金属,在常温下通过如图所示转化可获取硝酸钾。回答下列问题。
①若D为银白色贵重金属,则反应Ⅰ的化学方程式是 ,基本反应类型是 。
②一步实现反应Ⅱ,能否加入氯化钾?判断并说明理由。 。
③硝酸钾可作化肥,能供给作物两种养分,属于 肥料。
参考答案:
1.AB
2.CD
3.ABD
4.BC
5.BD
6.C
7.C
8.D
9.C
10.A
11.B
12.A
13.C
14.C
15.C
16.(1)
(2)
与熟石灰混合研磨,闻气味
(3) 除去氯化钙和过量的氯化钡 氯化钠、氢氧化钠、碳酸钠 搅拌,防止局部温度过高,造成液滴飞溅
(4)解:设样品中纯碱的质量分数是x
x=80%
答:样品中纯碱的质量分数是80%
17. B H2 吸收二氧化碳气体 取少量溶液于试管中,滴加足量氯化钡(或氯化钙)溶液,静置,再向上层清液中滴加酚酞溶液,若无沉淀产生,溶液变红,说明溶质为氢氧化钠;若有白色沉淀产生,溶液变红,说明溶质为碳酸钠和氢氧化钠;若有白色沉淀产生,溶液不变红,说明溶质为碳酸钠 21.2%
18.(1) 降温结晶 烧杯 氯化钠、硝酸钾
(2) (合理即可) 置换反应 氯化钾与硝酸铜相互交换成分后不会生成沉淀、气体或水,两者不反应 复合
